上肢深静脉血栓形成的诊治进展
2018-10-29综述栾景源审校
王 谦 综述 栾景源 李 选* 审校
(北京大学国际医院介入血管外科,北京 102206)
上肢深静脉血栓形成(deep venous thrombosis,DVT)是指血液在上肢深静脉内异常凝结引起的静脉回流障碍性疾病,常见于锁骨下静脉、腋静脉及肱静脉。上肢DVT约占所有DVT的4%~10%[1,2],并非罕见,但可供学习查阅的文献有限。本文针对上肢DVT的诊治进展进行综述。
1 病因及危险因素
上肢DVT的主要原因是静脉壁损伤、血流缓慢和血液凝血功能异常,分为原发性和继发性。
1.1 原发性上肢DVT
原发性上肢DVT是指病史中没有明显的诱发因素,无确切的原因,约占上肢DVT的20%~33%[3]。原发性上肢DVT主要分为特发性(无诱发因素)上肢DVT和Paget-Schroetter综合征两类。特发性上肢DVT没有潜在的解剖原因或是特定的诱发因素。Paget-Schroetter综合征多伴有胸廓出口综合征,60%~80%的患者与上肢过度活动有关[4]。锁骨下静脉走行于锁骨及第一前肋骨之间,在上肢活动过程中,该间隙变窄,压迫锁骨下静脉[5],反复运动导致内皮损伤,最终诱发血栓形成。
1.2 继发性上肢DVT
继发性上肢DVT是指能找到诱发上肢DVT的原因,约占所有上肢DVT的66%~80%[6],静脉内导管和恶性肿瘤是最常见原因。继发性上肢DVT中93%有静脉内导管[7],导管诱发上肢DVT常与导管直径,材料(聚乙烯、聚氯乙烯>硅、聚氨酯),尖端位置,导管感染,静脉管径等因素相关[8~10]。Adelborg等[11]随访1087例上肢DVT,其中232例(21.3%)患有癌症。
2 临床表现
上肢DVT的临床表现多样。手臂水肿最多见,最高达96.7%[12],30%~50%的患者表现为某种形式的肢体疼痛,15%表现为红斑,5%无任何症状[4]。也可见青紫、颈静脉怒张[13]、低热等症状。有时在上肢近端或上胸壁皮下可见突出的浅静脉(Urschel征,图1[14])。无症状上肢DVT常会以肺栓塞等并发症为首发症状。
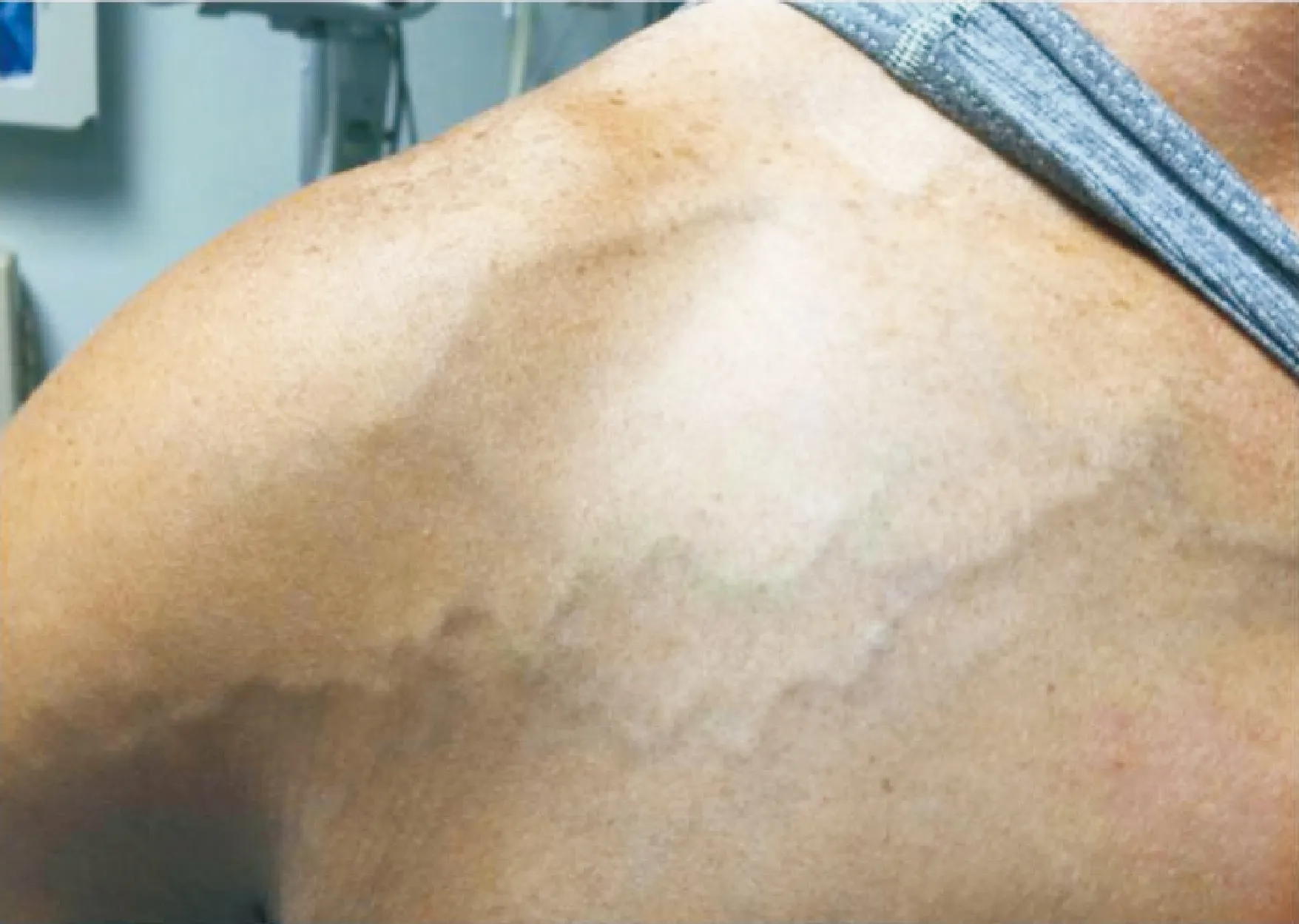
图1 Urschel征:上肢近端或上胸壁皮下可见突出的浅静脉[14]
蓝色炎性疼痛症(phlegmasia cerulea dolens,PCD)是较严重的临床表现,也是外周静脉血栓的一种特殊类型,常表现为严重水肿、剧烈疼痛、青紫色皮肤。经典的PCD常见于下肢DVT,称为疼痛性股青肿。在上肢DVT中少见,占2%~5%[15]。Greenberg等[16]总结38例上肢PCD,认为上肢PCD发生时,静脉内压力增高、间质压力增高(液体外渗到间质内)、低血容量和随后减少的毛细血管血流,这些因素可致动脉灌注不足,引起肢体缺血[17]。若不及时治疗,上肢PCD可迅速发展为静脉性坏疽,致使截肢和死亡风险增加[18]。
3 诊断
对于上肢DVT的诊断,无论是否有典型临床表现,均需进一步辅助检查,明确诊断,以免误诊和漏诊。
3.1 临床风险评估
用于诊断下肢DVT的Wells评分已被广泛认同,但上肢DVT还没有被广泛认同的评分。2008年,Constans等[19]提出上肢DVT的风险评分,见表1。

表1 Constans评分表[19]
3.2 辅助检查
3.2.1 血D-二聚体(D-dimer) D-dimer是纤维蛋白复合物溶解时产生的降解产物。Merminod等[20]认为其可能具有较高的阴性预测价值,并可作为除外上肢DVT的诊断方法,但一直没有足够的证据支持这一点。Sartori等[21]报道D-dimer诊断上肢DVT的敏感性和特异性分别为92%和60%,阴性预测值为98%。
其他情况如手术后、妊娠时D-dimer也会增高,并且会随着年龄的增长而增高,因此在高龄人群中D-dimer的特异性会更低。对于50岁以上人群,将D-dimer检测的正常值上限定为患者年龄×10 μg/L也许会增加特异性[22]。使用年龄校正后的D-dimer阈值联合风险评估,增加了诊断肺栓塞的阴性预测价值,在75岁以上老人中尤其显著[23]。van Es等[24]的研究显示,在疑似上肢DVT的诊断中,使用D-dimer固定阈值可使21%患者免于进一步行影像学检查和抗凝治疗,而采用年龄校正后的D-dimer阈值可使该比例提高到25%。越来越多有利的数据,使得D-dimer测定在临床疑似上肢DVT的诊断检查中,起到重要作用。
3.2.2 彩色多普勒超声检查 超声具有非侵入性、廉价和不受辐射的特点,成为诊断上肢DVT的首选方法。超声的灵敏性和特异性报道不一,Di Nisio等[25]的研究显示其具有较高的灵敏性(97%)和特异性(96%)。超声有其局限性,对于有症状且超声检查无明确阳性结果时,通常建议行血管造影等影像学检查进一步明确诊断。
3.2.3 静脉造影 静脉造影目前被广泛认为是诊断上肢DVT的“金标准”。在超声结果不确定,且临床高度怀疑上肢DVT时,可以行静脉造影。缺点是有创、造影剂过敏及肾毒性、有辐射等。
3.2.4 CT静脉成像或磁共振静脉成像 可用于静脉血栓的诊断,对解剖异常或胸廓出口梗阻的诊断具有优势[26]。
3.2.5 磁共振直接血栓成像(magnetic resonance direct thrombus imaging,MRDTI) 通过识别新鲜血栓中的血红蛋白来对血栓进行辨别。Theia研究[27]正在评价MRDTI在临床怀疑下肢DVT复发中的应用,但目前未见大型试验评价其在诊断上肢DVT中的应用价值。将MRDTI用于诊断上肢DVT还在探索阶段,Dronkers等[28]报道3例已明确诊断上肢DVT者进行MRDTI检查,全部得出阳性结果。MRDTI因无辐射和造影剂过敏等风险[29],有望成为诊断上肢DVT的一种新选择。
3.3 诊断策略及流程
ARMOUR试验中,将Constans评分表中1分及以下归为“上肢DVT低可能性”,2分及以上归为“上肢DVT高可能性”,并提出一套诊断流程,称为ARMOUR策略[30](图2)。
4 治疗
4.1 抗凝治疗
无论原发性还是继发性上肢DVT,是否抗凝治疗一直存在争议。目前尚缺乏大宗的随机对照试验数据,治疗建议主要来源于研究下肢DVT试验中的间接证据、小型的观察性研究及对上肢DVT自然病程的理解。对于腋静脉及其近心端静脉的急性上肢DVT,美国胸科医师学会(American College Of Chest Physicians,ACCP)建议仅抗凝治疗[31]。
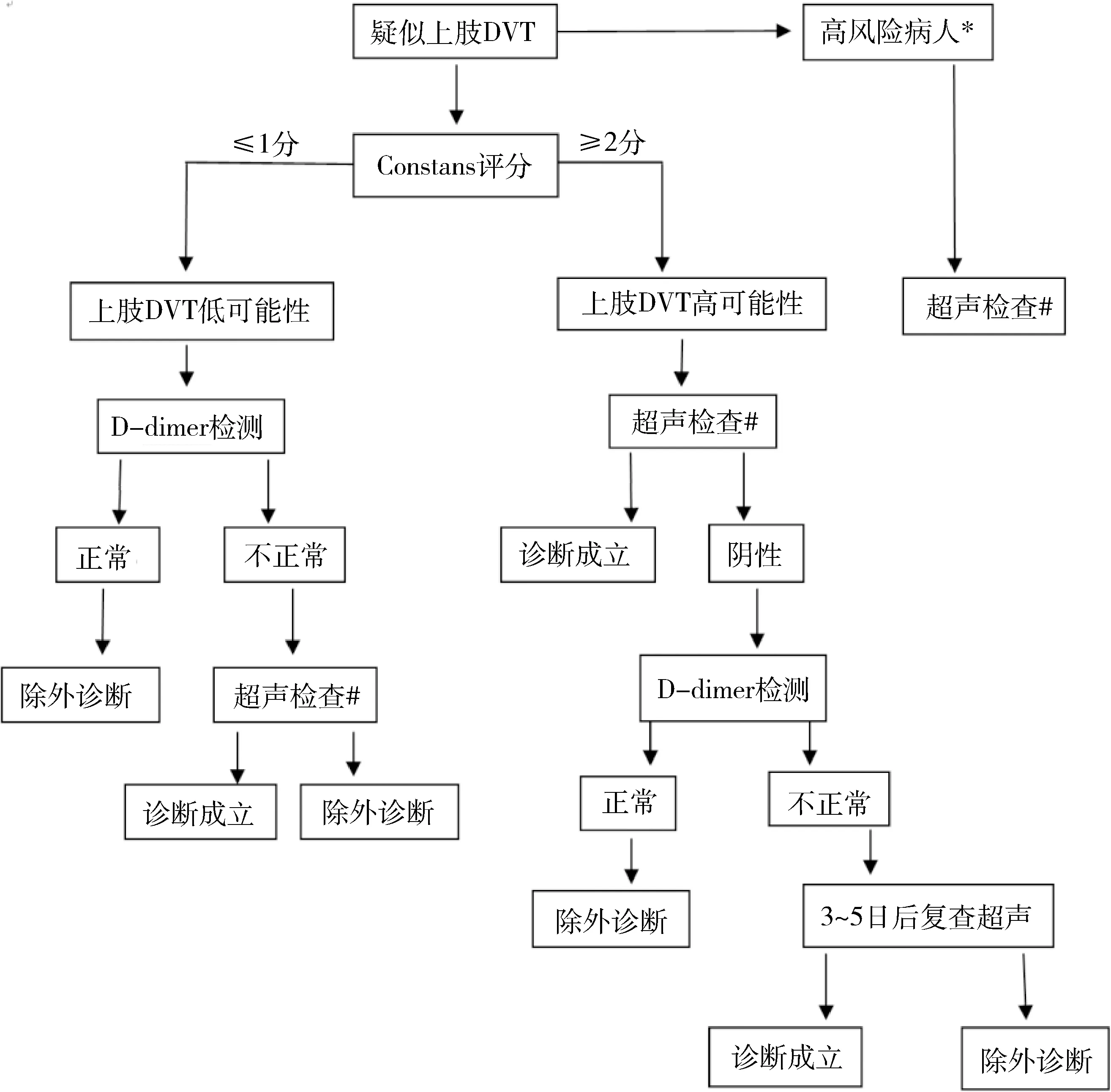
*高风险病人包括中心静脉导管、起搏器、活动期肿瘤、年龄>75岁#当超声检查结果为不确定时,3~5天后应复查超声,若结果仍是不确定,需要行CT静脉成像检查图2 AMOUR策略[30]
4.1.1 抗凝药物的选择 ACCP9[32]建议首选低分子肝素和磺达肝葵钠,其次为普通肝素静脉输注、普通肝素皮下注射,但ACCP10中未提及。基于EINSTEIN试验的结果,利伐沙班被正式批准用于静脉血栓栓塞症的治疗[33,34]。在下肢DVT非肿瘤患者的治疗中,建议直接口服抗凝药(direct oral anticoagulant,DOAC)优于维生素K拮抗剂[31]。但DOAC用于上肢DVT还在尝试阶段。Montiel等[35]使用瑞典国家抗凝登记处(AuriculA)的数据回顾性评估55例因上肢DVT接受DOAC治疗者,治疗期间复发率2%(1/55),停止治疗后复发率4%(2/55),无死亡,无严重出血,非严重出血发生率2%(1/55)。Davies等[36]的研究表明,利伐沙班对上肢DVT的治疗显示出了一定的疗效,然而需要重视治疗过程中的出血事件和致命肺栓塞。在利伐沙班被推荐使用前,需要进一步的研究来证实其安全性。另外,无论是否为静脉导管继发的上肢DVT,暂时没有理由采取不同的抗凝方式[37]。
4.1.2 抗凝期限 2012年英国血液学标准委员会(BCSH)[38]提出2B级证据:上肢DVT肝素抗凝至少5天,随后过渡华法林,使用华法林的期限暂没有非常明确的数据,3~6个月似乎具有安全性和较低的复发率。ACCP9[32]建议:累及腋静脉及其近心端上肢静脉的血栓,建议抗凝至少3个月。
4.2 溶栓治疗
溶栓的目的是早期恢复静脉通畅,降低血栓形成后综合征(post-thrombotic syndrome,PTS)的风险[39]。溶栓分为系统性溶栓和导管接触性溶栓(catheter directed thrombolysis,CDT)。目前溶栓治疗的药物、方式、并发症等研究多集中于下肢DVT[40~42]。Mahmoud等[43]报道CDT治疗24例上肢DVT,将闭塞静脉再通和新鲜血栓清除作为溶栓即时成功的衡量标准,手术成功率为91.7%(22/24),溶栓中位时间21.1 h,无术中并发症发生;1年二期通畅率为91.7%(22/24),1年复发率为0。因为溶栓的出血风险较大,而且没有大规模的临床试验证实溶栓确实能降低上肢PTS发生率,所以ACCP10[31]建议上肢DVT单纯抗凝即可,但同时提到以下情况可以选择溶栓治疗:①满足如下条件者将有可能从溶栓中获益,包括严重的症状,血栓涉及大部分腋静脉、锁骨下静脉,症状<14天,一般状况良好,预期寿命>1年,低出血风险;②有条件行CDT;③病人高度重视PTS的预防;④病人可接受复杂的起始治疗、高成本以及溶栓治疗出血的风险。
4.3 药物-机械血栓清除(pharmacomechanical thrombectomy,PMT)
PMT是指用一系列导管装置通过抽吸、研磨、切碎等方法清除血栓,并可联合药物溶栓。Mahmoud等[43]报道PMT治疗19例上肢DVT,将闭塞静脉的再通和新鲜血栓的清除作为溶栓即时成功的衡量标准,PMT手术成功率为100%(19/19),溶栓中位时间0.33 h,无术中并发症;1年二期通畅率为94.7%(18/19),1年复发率为0。Kärkkäinen等[44]报道,采取PMT治疗21例上肢DVT,血栓清除成功率达95.5%(21/22),因此认为PMT在早期清除血栓方面是有效的。
4.4 超声辅助经导管直接溶栓(ultrasound-accelerated catheter-directed thrombolysis,UACDT)
超声的能量可以打碎血栓,或在低强度超声波下分裂纤维蛋白链而不打碎血栓,局部联合使用溶栓药物,能强化药物渗透血栓内部。Ozcinar等[45]报道UACDT治疗16例上肢DVT,血栓完全清除率68.8%(11/16),部分清除率18.8%(3/16),出血发生率25%(4/16,包括2例消化道出血,2例穿刺点出血)。关于UACDT,期待未来有更多大样本的数据。
4.5 上腔静脉滤器置入
上肢DVT有抗凝禁忌、抗凝治疗引起并发症等情况下,可考虑置入上腔静脉滤器[46],但这些均是低级别证据,或许可以借鉴下腔静脉滤器置入相关意见:对于单纯抗凝治疗的DVT,不推荐常规应用下腔静脉滤器,对于抗凝治疗有禁忌或有并发症,或在充分抗凝治疗的情况下仍发生肺栓塞者,建议置入下腔静脉滤器[47];应严格掌握滤器置入适应证[48]。上腔静脉滤器置入的常见并发症有上腔静脉穿孔、上腔静脉血栓形成、气胸以及心脏压塞等。急性心脏压塞较多见,但Dalvie等[49]报道1例上腔静脉滤器取出16日后延迟出现心脏压塞。PREPIC试验[50]显示,8年内腔静脉滤器减少了肺栓塞的发生,但是增加了下肢DVT的复发,并且没有提高生存率。上腔静脉滤器置入后是否会增加上肢DVT的远期复发率,目前还没有明确的数据。
4.6 手术切开取栓
目前上肢DVT切开取栓较少报道。当发生PCD且不适宜溶栓时,可采取手术切开取栓[51]。快速行静脉切开取栓好处在于可以立即缓解静脉和间质内高压[18]。
5 小结
上肢DVT并非罕见,但文献较少,关于DVT治疗方面的研究多集中在下肢。我们将Constans评分、ARMOUR策略引入中文文献,并集中呈现了治疗方面的高级别证据及进展。关于MRDTI及UACDT的应用,上腔静脉滤器的长期随访等,期待将来有更多数据可供参考。
