高分辨率CBCT对人工耳蜗植入术后耳蜗内电极评估价值研究
2018-10-17方军杰胡宝华王建锋丁忠祥孙微干放邬亦椒郑建军
方军杰 胡宝华 王建锋 丁忠祥 孙微 干放 邬亦椒 郑建军
听力障碍患者的治疗与听力康复是临床关注的焦点。人工耳蜗植入(cochlear implantation,CI)技术与耳蜗装置的不断改进为重度及极重度感音神经性耳聋患者聆听世界提供了机会。但不同患者在CI术后听觉和言语康复情况差别较大,这与患者的耳蜗、听神经的自身条件、不同人工耳蜗的性能、手术植入技术及听力和言语的康复治疗等因素有关[1],这也与耳蜗电极植入的空间位置、电极的深度及有无电极折叠、电极滑脱等一些术后并发症有关。影像学检查有助于了解CI术后植入电极的相关情况。随着人工耳蜗电极设备的不断升级换代,观察内容从单纯评估耳蜗内电极向探讨电极位置与相关功能关系上延伸,为了能精确观察耳蜗内电极的形状、部位和数目,对影像学检测设备提出了更高的要求[2]。本研究通过对比分析高分辨率锥形束CT(CBCT)与64排螺旋CT对耳蜗内电极的显示与测量数据,探讨高分辨率CBCT对于CI术后耳蜗内电极的评估价值,现报道如下。
1 对象和方法
1.1 对象 选取2015年7月至2017年2月宁波市第二医院收治的因双耳极重度感音神经性耳聋行CI术患者16例,术前影像学评估与临床听力学检查均无CI术禁忌证。其中男9例,女7例;年龄2~42岁,平均16岁。8例患者植入COCHLEAR公司Nucleus CI512第五代人工耳蜗,线圈宽度32.0mm,电极矩阵长度19.0mm,22电极,材质为钛合金;8例患者植入NUROTRON公司CS-10A人工耳蜗,线圈宽度32.0mm,电极矩阵长度20.5mm,24电极,材质为钛合金。16例患者均为单侧植入。
1.2 检查方法 患者CI术后4~7d内行高分辨率CBCT检查和64排螺旋CT植入侧扫描。CBCT设备为PaX-Uni3D高分辨率CBCT机,管电压89kV,管电流4.0mA;植入侧颞骨扫描,患者站立位或坐位,头部固定。多排螺旋CT设备为德国西门子SOMATOM Definition 64排双源CT机,植入侧颞骨局部扫描,管电压120 kV,管电流45mA,螺距0.562mm,层厚0.625mm。对于无法配合检查的幼儿患者,检查前采用自然睡眠和人工药物催眠(口服水合氯醛)的方法来帮助婴幼儿入睡。CBCT检查采用儿童专用座椅,头部软枕固定,在监护人陪同下,进行检查。
1.3 重建方法 64排螺旋CT数据导入重建后台,选择骨函数图像,调节窗宽3 900、窗位1 865,使人工耳蜗高密度电极影与内耳骨质结构分界清晰;沿耳蜗蜗轴方向,做垂直于蜗轴和平行于蜗轴方向的三维重建,拆薄层厚为0.5mm,层间距为0mm;冠状位行MIP重建,层厚5.0mm,层间距3.0mm。曲面重建:选择Curved工具,在HD MIP图像上采用自动追踪电极中心行曲面重建(图1)。高分辨率CBCT重建方法与64排螺旋CT三维重建方式相同,层面上为了保持和MDCT的对比,尽量选择相同层面,曲面重建应用专门曲面重建及测量软件(图2)。
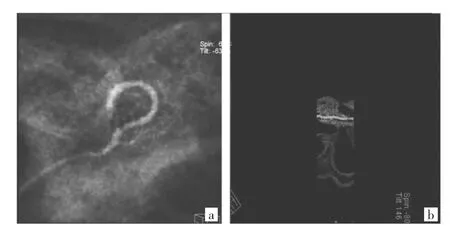
图1 64排螺旋CT图像重建(a:植入电极全景影像,周围有少许金属伪影;b:植入电极展开后图像,显示电极在耳蜗内走行,可测量电极深度)

图2 高分辨率CBCT图像重建(a:人工耳蜗重建后,显示电极在耳蜗内形态,清晰计数耳蜗电极;b:曲面重建展开后可以直接测量耳蜗内电极深度)
1.4 测量方法 电极计数采用3种表示方式,清晰计数,即电极和相邻电极边缘清晰;模糊计数,即电极边缘部分模糊,和相邻电极边界尚能分辨;未能计数,即电极边界模糊,和相邻电极不能区分。耳蜗内电极深度的测量方法,采用直接法和间接法2种方式。直接法:在HD MIP图像上自动追踪电极中心行曲面重建,展开电极,测得圆窗膜至耳蜗内人工耳蜗第一个电极的长度。间接法:已知人工耳蜗电极矩阵长度(Nucleus CI512为19.0mm,NUROTRON CS-10A为20.5mm),测得最后一个电极距离圆窗膜的距离,即总矩阵长度±最后一个电极距离耳蜗圆窗膜距离(图3)。电极位置的判断:耳蜗螺旋有三层结构,64排螺旋CT薄层重建及高分辨CBCT薄层重建后,可以显示前庭阶、鼓阶,主要辨认电极与耳蜗螺旋板的相对位置(图4)。测量及判断由2位副主任以上职称医师进行,两者意见不一致时,讨论或请教高一级医师解决。

图3 CBCT耳蜗内电极深度的测量(a:直接法;b:间接法)
1.5 观察指标 比较高分辨率CBCT与64排螺旋CT对CI术后耳蜗内电极的显示情况(计数、位置)及电极植入深度的测量结果。

图4 高分辨率CBCT重建后耳蜗内电极位置的判断(a:耳蜗内垂直于电极各层面图像,观察电极位置,蜗管内结构清晰,可显示位于下方的鼓阶;b:对比相对空间位置,显示电极位于下方鼓阶)
1.6 统计学处理 应用SPSS 23.0统计软件;计量资料以表示,组间比较采用两独立样本t检验;计数资料比较采用χ2检验;P<0.05为差异有统计学意义。
2 结果
2.1 高分辨率CBCT与64排螺旋CT对CI术后耳蜗内电极的显示情况比较 15例植入后未发现明显并发症,1例患者在术后CBCT检查时发现电极有折断重叠(图5),后进行二次手术。64排螺旋CT清晰计数74个电极,平均(4.6±1.1)个/例;模糊计数 138个,平均(8.6±1.7)个/例;高分辨率CBCT清晰计数330个电极,平均(20.6±2.0)个/例;模糊计数为 34个,平均(2.1±1.6)个/例;16例患者CI术后耳蜗内电极计数情况比较详见表1。高分辨率CBCT与64排螺旋CT对CI术后耳蜗内电极计数的差异有统计学意义(P<0.05),高分辨率CBCT优于64排螺旋CT。高分辨率CBCT判断术后电极位于鼓阶12例,前庭阶2例,2例未能判断;多排螺旋CT判断术后电极位于鼓阶13例,前庭阶2例,1例未能判断;高分辨率CBCT与64排螺旋CT对CI术后耳蜗内电极位置判断的差异无统计学意义(P>0.05)。
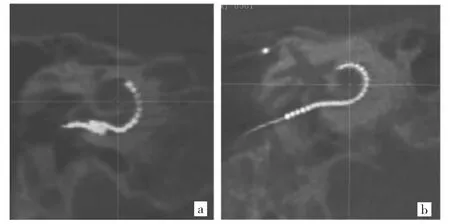
图5 高分辨率CBCT对CI术后耳蜗内电极的显示(a:人工耳蜗电极折断重叠,导致植入深度不够;b:植入电极深度明显不足,圆窗膜外尚留8个电极)

表1 16例患者CI术后耳蜗内电极计数情况比较(个)
2.2 高分辨率CBCT与64排螺旋CT对CI术后耳蜗内电极植入深度测量结果比较 两种植入电极阵列长度分别19.0、20.5mm,设计植入长度和手术实际植入深度并非一致。利用64排螺旋CT、高分辨率CBCT曲面重建和术中实际测得的电极植入深度比较见表2。

表2 16例患者CI术后耳蜗内电极植入深度4种方法测量结果比较(mm)
由表2可见,多排螺旋CT直接法测得CI术后耳蜗内电极植入深度>CBCT直接法>CBCT间接法,CBCT间接法测量的CI术后耳蜗内电极植入深度更加接近于术中实际测量值。而COCHLEAR公司Nucleus CI512人工耳蜗电极植入深度要深于NUROTRON公司的CS-10A人工耳蜗,两者比较有统计学差异(P<0.05)。
3 讨论
近30年来,CI的适应证已经被大大扩展,甚至可用于3个月大的婴幼儿,并且对有明显功能性残余听力的成人也有良好效果,尤其是有相当的低频率域内残余听力者[3]。如今CI在技术上虽已十分成熟,但仍存在一些问题,如植入位置异常、深度不够、电极折叠等,这些问题多数在术后开机调试时才能被发现,因此术后对耳蜗内电极的影像学评估意义重大。
目前在CI术后影像学评估方面,国内常用的检查方法有数字化X线摄片和多排螺旋CT扫描。数字化X线摄片早期应用较普遍,其优点是检查费用和扫描辐射剂量低,能查看电极整体形态,并能清晰计数电极,一定程度上能判断耳蜗内电极有无扭曲、打折,并能通过角度测量及曲率公式计算出植入耳蜗的深度[4]。但是X线检查的缺点是空间分辨率低,耳蜗内部细微结构与植入电极关系不能区分,并且受到投照角度的限制。多排螺旋CT不仅提升了空间分辨力,也大大降低了电极金属伪影,临床应用十分广泛,早先已有多名学者做了多排螺旋CT对CI术后耳蜗内电极影像评估的相关研究。Lane等[5-6]通过对比植入电极的尸体颞骨标本64排螺旋CT扫描图像及相对应的耳蜗切片图像,发现在合适平面上重建的三维图像可以分辨出电极在鼓阶或前庭阶的位置,这为CI术后耳蜗内电极的空间位置提供重要的技术手段。而耳蜗内电极植入的位置以及在耳蜗内电极植入的深度目前被认为是手术成功与否的关键因素[7]。
自从2002年Husstedt等[8]第一次报道利用CBCT技术显示CI术后电极和耳蜗轴的关系以来,CBCT已在临床广泛应用。CBCT具有金属伪影较少,辐射剂量极低,各向同性空间分辨率高等优点[9]。2014年,芬兰坦佩雷大学医学院Zhou等[10]设计了一个对照实验,利用高分辨CBCT采集系统测试CI术后耳蜗内定量标记电极阵列,并以微平板CT成像作为对照,发现CBCT可以作为临床应用识别电极阵列的检查手段。同时,有研究通过对比植入电极的人体颞骨标本的超微断层图像和CBCT扫描图像,肯定了高分辨CBCT在合适平面上重建的三维图像可以分辨出电极在鼓阶或前庭阶的位置[11],为确定CI术后耳蜗内电极的空间位置提供重要的技术手段。另有一项低剂量螺旋CT与CBCT在显示CI术后的对比研究,发现高分辨CBCT检查的辐射剂量要明显低于低剂量螺旋CT,而低剂量螺旋CT显示的耳蜗结构和整体图像质量与辐射剂量呈正相关;高分辨CBCT和低剂量多排螺旋CT都适合于术后CI成像[12]。因此,本研究采用低剂量CT局部扫描,一方面对CT图像质量影响有限,另一方面,可以有效控制辐射剂量。
本研究结果显示,高分辨率CBCT与64排螺旋CT对CI术后耳蜗内电极计数情况比较差异有统计学意义,高分辨率CBCT优于64排螺旋CT。而也有报道称,多排螺旋CT薄层扫描后,在植入电极显示上也非常清晰[6,12],但这类报道都基本研究的是12~16颗电极的人工耳蜗,由于电极间距较大,伪影相互影响相对较少。但在22~24颗电极的显示方面,多层螺旋CT只能清晰计数少数电极,CBCT存在明显优势。CBCT相对于多排螺旋CT,周围金属伪影明显减少,对于测量及显示单个电极方面更为准确。但CBCT更容易产生运动伪影,部分电极计数不清晰,多数是由于运动伪影影响。
本研究结果显示,高分辨率CBCT与64排螺旋CT对CI术后耳蜗内电极位置判断结果比较差异无统计学意义,两者均能较好地判断耳蜗内电极是位于鼓阶还是前庭阶。多排螺旋CT和高分辨率CBCT在判断电极植入位置时,需要观察电极在耳蜗管内的空间位置,最好能在一些层面上显示中间基底膜的大致位置,这样在判断上会更加的准确,这就需要高分辨率薄层重建。但在实际评估中,对于基底膜的显示较困难,而电极在耳蜗空间位置、前庭阶及骨螺旋板可清晰显示。
据文献报道,目前常用的影像评估电极植入深度的测量方法主要有:数字化X线图像上利用角度-长度公式及频率-长度公式测量电极深度[13];CT曲面重建自动跟踪法测量电极深度。本研究中,在多排螺旋CT上,利用影像工作站曲面重建的方法对植入电极行多平面三维重建,以电极进入圆窗膜位置为测量起点,直接测量人工耳蜗电极至耳蜗内最远端终点的距离,其整个测量方法类似于自动跟踪法,并且可以在一个平面上观察,即直接法测量。而同样,在高分辨率CBCT检查后,利用机器自带软件进行相同层面的重建,应用曲面重建软件进行植入电极长度的直接测量。根据曲面重建的成像原理,不难发现,测量展开后的电极深度,会有一定的测量点选择的人为误差,所以在已知电极矩阵长度时,可以采用间接法来减少这人为误差形成。间接法是电极矩阵长度±末位电极离圆窗膜长度,测得的平均深度要略小于直接法,并且更加接近于术中实际测得的电极植入深度。另外,Nucleus CI512电极为弯电极,在设计时植入深度较大,而在实际测量中,该弯电极的实际植入深度要明显比NUROTRON的CS-10A人工耳蜗直电极植入深度要深。可以看出,间接法更能减少测量误差,所以在能清晰判定最后一个电极位置时,利用高分辨率CBCT间接法测量将更加准确。
综上所述,相比64排螺旋CT,高分辨率CBCT不仅能显示CI术后耳蜗内电极位置,并能较准确测量耳蜗内电极植入深度及计数等指标,为需要调整电极位置或再次进行手术的患者提供较为准确的影像学评估资料,在临床上可以代替多排螺旋CT进行耳蜗内电极的影像学评估。
