[Cd(tinc)2·2(H2O)]n配合物的合成、结构及其与DNA的相互作用
2018-10-15高恩军
王 宁, 高恩军
(沈阳化工大学 辽宁省无机分子基化学重点实验室, 辽宁 沈阳 110142)
顺铂作为最早用于肿瘤治疗的金属配合物,因其抗癌谱广、作用强,已被广泛应用于临床治疗,然而其严重的消化道反应、肾毒性、骨髓抑制及神经毒性也给患者带来相应痛苦.因此具有抗肿瘤作用的新型金属配合物药物的发现与研究显得尤为重要.正常细胞发生癌变一般起因是DNA进行快速且无节制地复制,故配合物是否可与DNA发生相互作用可作为衡量配合物是否有潜在抗癌活性的依据,顺铂的作用机制即为其可抑制DNA的复制过程[1-2].
含氮羧酸配体具有丰富的配位模式,易形成结构稳定的功能型配合物.过渡金属配合物往往具有良好的生化活性,可以有效插入DNA分子阻止其复制[3].本文通过溶剂热法,选取含氮羧酸配体(1-三氮唑)异烟酸及过渡金属盐硝酸镉合成配合物[Cd(tinc)2·2(H2O)]n,利用X单晶衍射确定了该配合物的结构,借助荧光光谱法及分子对接研究了其与DNA的相互作用,发现该配合物与DNA有较强的结合能力.
1 实验部分
1.1 仪器与试剂
BRUKER SMART 1000 CCD面探X射线衍射仪,德国Bruker公司;Perkin-Elmer LS55荧光分光光度计,美国Pekin-Elmer公司.硝酸镉、2-(1-三氮唑)异烟酸、二甲基甲酰胺(DMF)等试剂均为分析纯,未经进一步纯化;实验用水为二次蒸馏水;溴化乙锭(EB)、鲱鱼精DNA(HS-DNA)为生化试剂,购置于国药集团.
1.2 配合物的合成
2-(1-三氮唑)异烟酸(0.005 g)与硝酸镉(0.015 g)溶解于装有3 mL DMF与H2O体积比为1∶2的溶剂的小瓶中,室温下充分搅拌后置于90 ℃烘箱中加热72 h,缓慢冷却至室温得无色片状晶体.经X单晶衍射确定所得晶体是结构为[Cd(tinc)2·2(H2O)]n的化合物.
1.3 荧光猝灭实验
利用荧光光谱法测定配合物与DNA的相互作用.在EB-DNA体系[c(DNA)/c(EB)=2.5,其中c(DNA)=2.5 μmol/L,c(EB)=1 μmol/L]中分别加入0~12 μmol/L的金属配合物,反应在Tris-HCl(pH=7.4)缓冲溶液中进行.实验结果以490 nm为激发波长,在520~760 nm波长区间记录每组溶液的荧光强度数值.
1.4 分子对接研究
分子对接研究使用分子对接软件YASARA完成.对接所需的配合物PDB格式文件由其CIF格式文件使用Mercury软件转换而来.DNA分子结构(PDB ID:2MG8)取自蛋白质数据库(protein data bank).
2 结果与讨论
2.1 配合物的结构
配合物[Cd(tinc)2·2(H2O)]n的结构如图1所示,镉原子分别与2个氮原子(分别来自2个tinc配体)、4个氧原子(其中2个分别来自2个tinc配体,2个来自水分子)以配位键连接.键长,λ/nm:Cd(1)—N(3)为0.228 4 nm,Cd(1)—O(2)为0.234 5 nm,Cd(1)—O(3)为0.230 2 nm.N(3)—Cd(1)—N(3),O(2)—Cd(1)—O(2),O(3)—Cd(1)—O(3)键角均为180°,即N(3)—Cd(1)—N(3),O(2)—Cd(1)—O(2),O(3)—Cd(1)—O(3)分别处于一条直线上,形成了一个以镉为中心呈中心对称的规则的八面体结构.
图2显示的配合物的一维链状结构是由中心Cd和N、O等原子以配位键连接而成.配合物的二维平面结构如图3所示,不同链状结构之间以氢键相连,为使配合物结构更加清晰,图中不必要的氢原子已被省去.
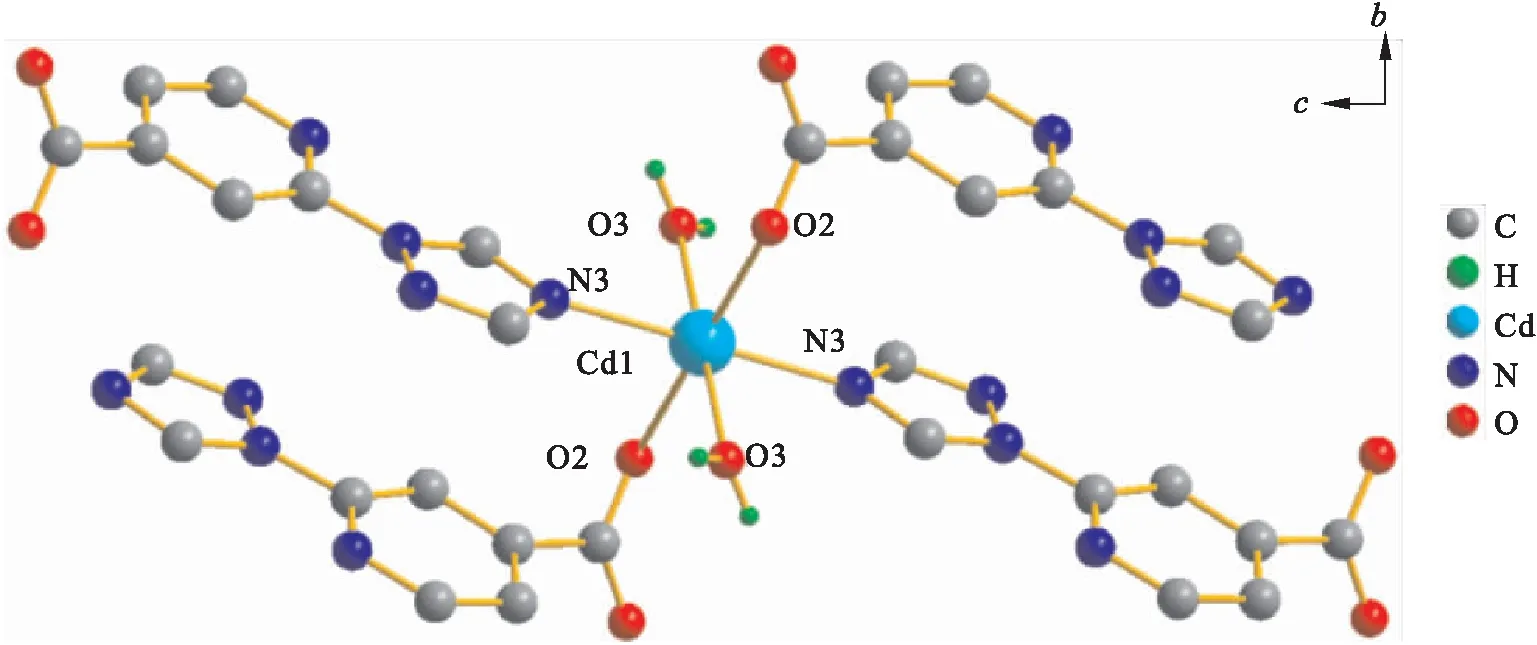
图1 配合物配位环境
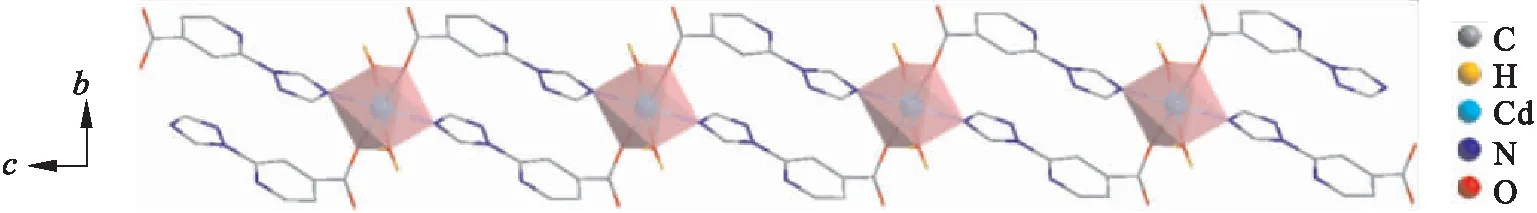
图2 配合物一维链状结构
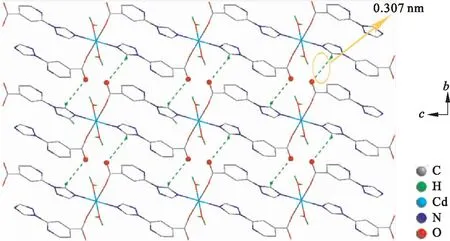
图3 配合物二维平面结构
2.2 配合物与HS-DNA作用的荧光光谱法研究
溴化乙锭(EtBr)是一种强的DNA嵌入剂,其本身荧光强度很弱,但可以插入DNA的碱基对中形成EtBr-DNA复合物而产生强荧光[4].通过配合物与EtBr-DNA反应后的荧光强度变化即是否发生荧光猝灭,可判断配合物是否与EtBr进行了竞争替换,从而判断配合物对DNA是否有插入作用[5].根据经典的Stern-Volmer方程:I0/I=1+Ksq·r,其中I0和I分别表示不存在及存在配合物时的荧光强度;r为配合物与HS-DNA的浓度比;Ksq为Stern-Volmer猝灭常数,可定量描述配合物与HS-DNA作用的强弱,Ksq值越大,表示配合物与HS-DNA作用强度越大,结合能力越强[6-8].配合物与EB-DNA[c(EtBr)=1×10-6mol/L,c(DNA)=5×10-6mol/L]体系作用的发射光谱如图4中所示.
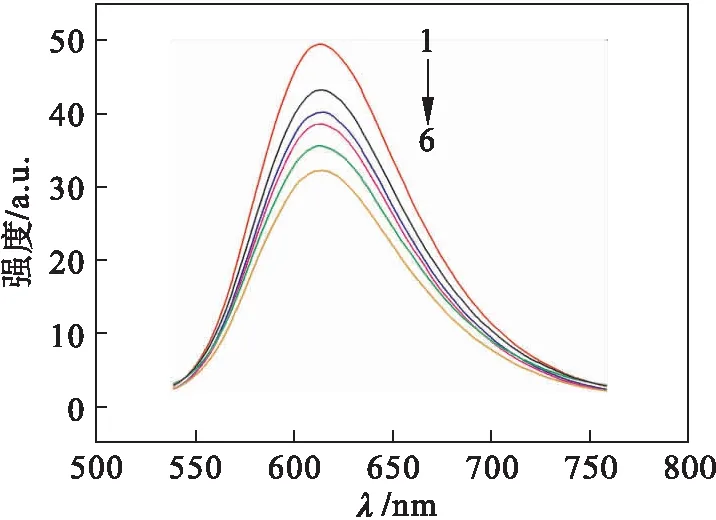
1.c(配合物)=0 mol·L-1
由图4可以看出:随配合物浓度的增大,荧光强度呈递降形势明显减弱,表明配合物与HS-DNA发生了插入作用,导致不同程度荧光猝灭的发生.由荧光猝灭曲线得Stern-Volmer猝灭常数Ksq值为0.200(图5),表明配合物与HS-DNA有较强的结合能力.
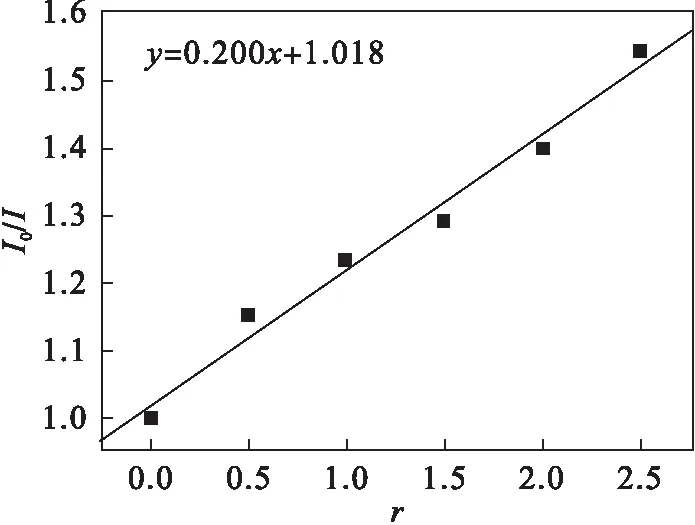
1.c(配合物)=0 mol·L-1
2.3 配合物的分子对接研究
分子对接是通过受体的特征以及受体和药物分子之间的相互作用方式来进行药物设计的方法,依据配体与受体作用的“锁-钥原理”,模拟小分子配体与生物大分子的相互作用[9-11].利用分子对接可进一步确认配合物与DNA的相互作用[12],对接结果如图6所示.其中球状模型部分为配合物分子,表面被范德华力覆盖的两条呈棍状模型的链状结构为DNA分子.对接研究结果显示配合物插入于DNA分子中并使其双链打开,进一步确定了配合物与DNA分子的相互作用模式为插入作用.
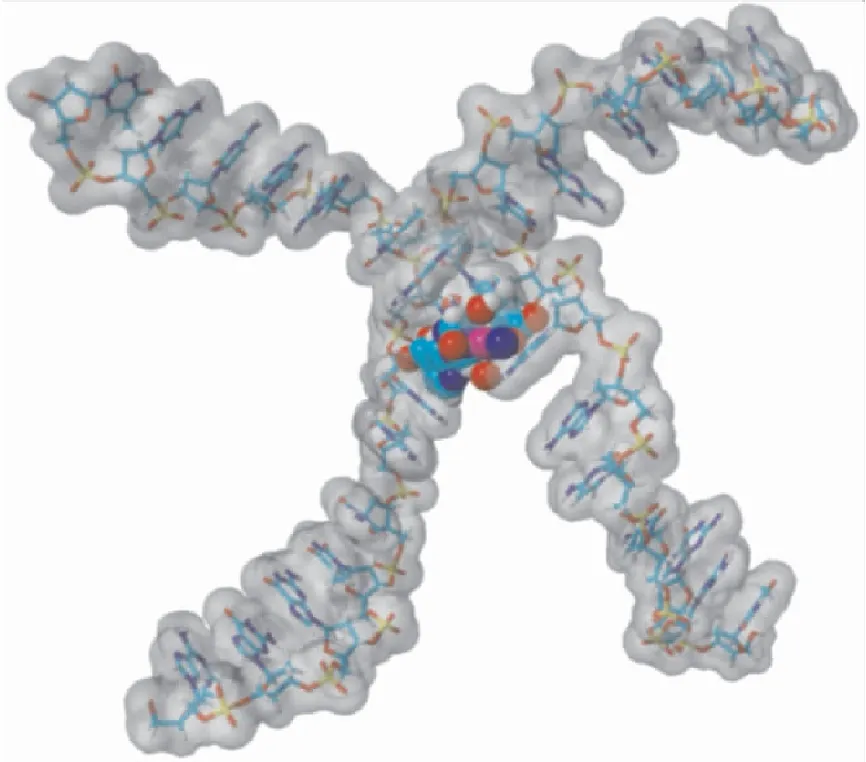
图6 配合物的DNA分子对接
3 结 论
(1) 用配体(1-三氮唑)异烟酸与金属镉盐采取溶剂热合成法合成了配合物[Cd(tinc)2·2(H2O)]n,通过X射线单晶衍射确定了该配合物为八面体构型,分别来自于2个配体的2个氮原子、2个氧原子以及2个水分子上的氧原子参与配位,形成了穿过金属原子Cd呈中心对称的规则的八面体结构.
(2) 利用配合物与EtBr的竞争实验确定了其与HS-DNA的作用方式为插入结合,并借助分子对接研究进一步验证了该配合物与DNA的作用模式,通过荧光猝灭常数计算(Ksq=0.200)表明配合物确与DNA有较强的亲和作用,可作为潜在的抗癌试剂进行进一步研究.
