不同改性方法 对蛋清粉致敏性与功能性的影响
2018-09-22宋启东涂宗财杨文华钟比真陆建伟
宋启东,涂宗财,2,*,王 辉,张 露,杨文华,钟比真,陆建伟
(1.南昌大学食品科学与技术国家重点实验室,江西南昌 330047; 2.江西师范大学生命科学学院,江西南昌 330022)
鸡蛋具有低廉的价格和很高的营养价值,已成为国民健康饮食的重要部分。因其具有优良的功能性而常作为原料、辅料、添加剂等应用于面类、肉类、休闲类食品的加工中[1]。但作为高蛋白食物,鸡蛋还是引起青少年和儿童过敏的主要过敏源,且大部分的鸡蛋过敏反应都是由蛋清中的蛋白所引起的[2-3]。所以,随着鸡蛋消耗量的持续增加和应用范围的不断推广,鸡蛋过敏率也有逐年递增的趋势,使得对鸡蛋(尤其是蛋清)致敏性的研究愈发得到重视[4]。

表1 鸡蛋过敏患者病史Table 1 Clinical history of egg allergy patients’ sera
目前,对鸡蛋改性的研究仍集中在功能性质上,而关于降低致敏性的改性研究较少,且主要是对蛋清中纯蛋白的研究。热处理是一种简单的降低食物过敏的方法,蛋白加热变性后原始的三级结构被破坏,使许多天然抗原被修饰。Shin等[5]发现热处理后卵类黏蛋白致敏性增加,卵清蛋白致敏性减少,溶菌酶和卵转铁蛋白的致敏性完全消失;Sicherer等[6]发现蛋清蛋白煮沸60 min后致敏性显著降低,95 ℃加热15 min后,卵清蛋白和卵类黏蛋白的IgE结合能力降低,但热处理会破坏蛋白结构,形成无规则卷曲的聚合体,降低溶解性。超声波作为新兴“冷处理”技术具有耗能少,效率高等优点,既可以提高蛋白的功能特性,还能很大程度的保留食品的天然品质和营养价值,且易与其他方法联合,具有很好的协同性[7]。糖基化是少数可直接应用于食品加工的化学方法之一。An等[8]发现随着卵清蛋白与羧甲基纤维素糖基化程度的加深,其复合物的乳化性、泡沫稳定性、蛋白热变性温度均显著增强。Seo等[9]发现溶菌酶与半乳糖、低聚半乳糖、半乳聚糖通过糖基化反应不仅可以提高溶解性、热稳定性和乳化稳定性,还能有效降低致敏性。复合改性是通过两种以上的方法协同改性蛋白,通过复合改性尤其是物理-化学复合改性,不仅可以互补单一处理方法的不足,还能更好的保持食品风味和营养,更高效的提高功能性质和脱敏效果。
本文拟采用热处理、糖基化、超声、超声预处理结合糖基化等方法改性实际生产和生活中常用的蛋清粉,通过对比研究不同改性方法对蛋清粉致敏性和功能性的影响,选出既可以高效降低致敏性又可以有效保留甚至提高其功能性的加工方法,以期为低致敏蛋制品的研发提供更有实际价值的参考。
1 材料与方法
1.1 材料与仪器
蛋清粉 郑州奥冉化工;人血清(一抗) 美国PlasmaLab International公司;酶标板 美国Corning公司;胃蛋白酶(≥250 U/mg)、羊抗人血清(二抗)、胰酶 美国Sigma公司;大豆油 益海嘉里集团;脱脂奶粉 雀巢公司;邻苯二甲醛(OPA) 美国Sigma公司;其他试剂 均为常用分析纯。
JY98-IIIDN型超声波细胞破碎仪 宁波新芝生物科技股份有限公司;HF2000型酶标仪 北京华安麦科;电热鼓风干燥箱 上海恒科学仪器有限公司;Leader-A1型超纯水仪 上海领德仪器有限公司;冷冻干燥机 北京亚泰科隆仪器技术有限公司;IKA T18型分散机 艾卡仪器设备有限公司。
1.2 实验方法
1.2.1 样品处理 蛋清粉用pH8.0磷酸盐缓冲液(PBS)稀释到10 mg/mL,离心后取上清液(U0)100 mL,再分别进行如下操作:
加热处理(C1):冻干处理后,在75%相对湿度条件下,70 ℃加热4 h;
糖基化(C2):按蛋清粉:糖质量比1∶8加入葡萄糖,冻干后在75%相对湿度条件下,70 ℃反应4 h;
超声(C3):冰水浴中600 W超声15 min,再冻干处理;
超声预处理结合糖基化(C4):冰水浴中600 W超声15 min,再按蛋清粉∶糖质量比1∶8加入葡萄糖,冻干后在75%相对湿度条件下70 ℃反应4 h;
模拟体外消化[10](C5):按C4处理后,加超纯水复溶至10 mg/mL,用1 mol/L HCl将pH调至2.0,37 ℃预热10 min,按酶∶底物质量比1∶50加入胃蛋白酶,37 ℃酶解3 h。用1 mol/L NaOH将pH调至7.5终止反应,37 ℃预热10 min,按酶∶底物质量比1∶50添加胰酶,37 ℃,3 h,煮沸10 min,冻干。
1.2.2 自由氨基含量测定 参考Nielsen等[11]的方法。将样品用pH8.0的PBS稀释成40 mg/mL,取10 μL样品或不同浓度(0~0.8 mg/mL)赖氨酸与200 μL OPA试剂避光反应2 min,340 nm测吸光值,通过标曲得到样品自由氨基含量。
1.2.3 过敏原性测定 通过间接ELISA进行测定。每孔加入100 μL 100 μg/mL样品(或原样),4 ℃包被过夜,洗板,拍干;加250 μL 5%脱脂奶粉进行封闭,37 ℃,1 h,洗板,拍干;加100 μL人血清,37 ℃,1 h,洗板,拍干;加100 μL二抗,37 ℃,1 h,洗板,拍干;加100 μL显色液,37 ℃,15 min;加100 μL H2SO4,450 nm测吸光值。
式中:A0:一抗为患者血清所测得的未处理样品吸光度与一抗为未对鸡蛋过敏的人血清所测得的未处理样品吸光度的差值;A1:一抗为患者血清所测得的处理后样品吸光度与一抗为未对鸡蛋过敏的人血清所测得的处理后样品吸光度的差值。
1.2.4 溶解性测定 用PBS将样品稀释为2 mg/mL并与考马斯亮蓝染液按体积比1∶5混合,静置5 min,595 nm测吸光值。以牛血清蛋白标品(0~100 μg/mL)的浓度为横坐标,吸光值为纵坐标作标曲,根据标曲计算得出可溶性蛋白含量[12]。
1.2.5 乳化性及其稳定性的测定 参考Zhao等[13]的方法加以调整。将样品用PBS稀释成4 mg/mL,按样品:大豆油质量比3∶1加入大豆油,11000 r/min均质2 min,迅速从底部吸取乳液与0.1% SDS,按1∶50体积比混匀后在500 nm测吸光值;10 min后重新从底部吸取乳液与0.1% SDS,按体积比1∶50混匀后在500 nm处测定吸光值。
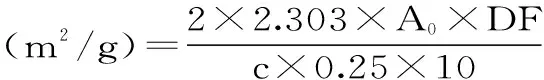

式中:DF为稀释因子(50);c为样品初始浓度(4 mg/mL);t为稳定时间(10 min);A0为0 min时吸光值;A10为10 min后吸光值。
1.2.6 抗氧化活性测定
1.2.6.1 还原力测定 将样品(25 mg/mL)、PBS(0.2 mol/L,pH6.6)、K3[Fe(CN)6](1%)等体积混合,50 ℃反应20 min,冰水浴冷却,取300 μL混合液与100 μL三氯乙酸(10%)混合,离心5 min后取200 μL上清液与40 μL三氯化铁(0.1%)50 ℃反应10 min,700 nm测定吸光值[14]。
1.2.6.2 亚铁离子螯合能力测定 将样品(25 mg/mL)、FeCl2(2 mmol/L)、菲洛嗪溶液(5 mmol/L)按体积比1∶1∶2依次加入,静置10 min,562 nm测吸光值[14]。
式中:A0为PBS替代样品测得的吸光值;A1为样品测得的吸光值。
1.2.6.3 DPPH·清除力测定 将样品(25 mg/mL)和DPPH(0.1 mmol/L溶于乙醇)按体积比1∶1混合,反应20 min,517 nm测定吸光值[15]。
式中:A0为PBS替代样品测得的吸光值;A1为样品测得的吸光值。
1.2.6.4 ABTS+·清除力测定 将ABTS(7 mmol/L)与过硫酸钾(2.45 mmol/L)等体积混匀,室温暗反应16 h,将混合液用PBS稀释至在734 nm的吸光值为0.70±0.02,将稀释后的工作液避光0.5 h,取100 μL 25 mg/mL的样品与3.9 mL工作液混合,避光反应10 min后在734 nm测定吸光值[15]。

式中:A0为PBS替代样品测得的吸光值;A1为样品测得的吸光值。
1.2.7 数据统计与分析 Origin 9.0作图,SPSS 17.0分析显著性(p<0.05),平行实验至少三次。
2 结果与分析
2.1 自由氨基含量分析
自由氨基含量可以很好的反映蛋白结构变化和糖基化程度。由图1可知,与原样(U0)相比,热处理和超声改性的样品自由氨基含量显著(p<0.05)增加。这可能是因为热处理使蛋白解离,二、三级结构改变,导致大量的氨基产生和暴露[16];而超声主要通过空化作用提供特殊物理环境,舒展蛋白的空间结构,但不能有效改变蛋白低级结构产生氨基,所以自由氨基含量低于热处理[17];糖基化改性后,样品发生羰胺缩合使自由氨基含量显著(p<0.05)降低,而且糖基化形成的糖蛋白还可以维持蛋白结构稳定,减少因结构改变导致的氨基暴露[18];复合改性后自由氨基含量进一步降低,说明尽管超声使蛋白结构展开,暴露了部分内部氨基,但也减小了空间位阻[19]促进了糖基化反应的进行,这也说明相比于超声,自由氨基含量主要受糖基化影响;将复合处理的样品进行体外消化后,蛋白通过酶解使肽键断裂,次级结构被破坏,大量氨基产生和暴露,自由氨基含量显著(p<0.05)升高。

图1 改性方法对蛋清粉自由氨基的影响Fig.1 Effect of different modification methods on the free aminos of egg white powder注:不同小写字母表示不同改性方法之间 差异显著(p<0.05);图2~图5同。
2.2 过敏原性分析
不同患者IgE水平和IgE识别的过敏表位不同,如卵白蛋白的某些线性表位会被长期鸡蛋过敏患者识别,但不会被短期患者识别[20]。热处理主要破坏蛋白的空间结构,而蛋清蛋白的过敏表位以线性表位为主[21],并且热处理在破坏构象表位的同时,也可能产生新的构象表位,暴露更多的线性表位,所以致敏性总体上是增加的,最高增加了12.77%(P2)。超声使蛋白结构舒展,更多的线性表位暴露甚至增加新的构象表位[22],而热处理能一定程度的解离蛋白低级结构,还能使蛋白卷曲聚集[5],这可以一定程度的修饰过敏表位,所以超声处理后样品致敏性增加程度更大,为20.84%(P2)。糖基化既可以通过外接糖分子阻塞线性表位,又可以改变蛋白结构修饰构象表位,使致敏性显著(p<0.05)降低[23],最大降低了29.08%(P4)。复合改性后,超声使蛋白结构展开,更多的过敏表位暴露在蛋白表面,但也减小了空间位阻并暴露出了更多的结合位点促进糖基化反应进行,抗原表位得到更全面的修饰,致敏性进一步降低,为43.9%(P4);模拟体外消化后样品的致敏性更大程度的降低,这是因为酶解可以使肽键大量断裂,更多的线性表位得到修饰,但酶解不能针对性的打断线性表位并且可能形成新的表位[24],所以经体外消化后的致敏性降低程度不大,最高降低了52.76%(P2)。联系自由氨基含量的变化我们可以发现,消化可以高效酶解蛋白,破坏线性表位,但并不会破坏糖基化产物对蛋白致敏性的修饰。
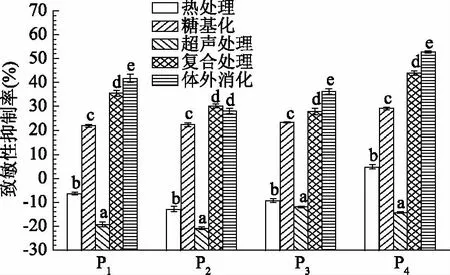
图2 改性方法对蛋清粉致敏性的影响Fig.2 Effects of different modification methods on the immunogenicity of egg white powder注:P1~P4为不同患者血清。
2.3 溶解性分析
溶解性是蛋白最关键的理化性质。热处理后蛋白溶解性降低,这主要是因为蛋白共价交联发生聚集,结构变化使疏水基团暴露导致表面疏水性增加[25];超声可使蛋白结构舒展,大量的疏水基团暴露[22]使溶解性也发生降低,但不会影响蛋白的聚集状态所以溶解性高于热处理;糖基化通过大量接入亲水基团提高蛋白亲水性,使溶解性显著增加(p<0.05);相比于原样,复合改性后溶解性提高了0.06751 mg/mL,这是因为超声预处理会展开蛋白结构,尽管会暴露更多的疏水基团,但也促进了糖基化反应的进行,使蛋白结合更多的亲水基团,溶解性进一步增加;再经体外消化后,蛋白被酶解成多肽,增加了亲水基团与外部水环境的接触,溶解性进一步增加。

图3 改性方法对蛋清粉溶解性的影响Fig.3 Effect of different modification methods on the solubility of egg white powder
2.4 乳化性及其稳定性分析
蛋白的乳化性是食品加工的重要功能性质之一,主要与溶解性、表面疏水性、表面电荷、分子柔性有关[17]。热处理后样品的乳化性降低,乳化稳定性没有显著变化,这是因为热处理可以通过改变蛋白的粒径、二级结构和表面疏水性来影响乳化性能[25],蛋白经热处理后分子发生共价交联形成聚集体,大量基团被掩埋,最终导致乳化性降低[6];超声处理可以展开蛋白结构且不发生聚集,内部基团大量暴露,所以尽管溶解性降低,但分子柔性和表面疏水性的增加仍会使乳化性提高,而且超声可以降低粒径并使粒径更均一[26-27],利于蛋白在油-水界面稳定扩散,显著增加稳定性(p<0.05);糖基化通过外接亲水基团在蛋白表面形成大量的亲水层,蛋白可以提供更多的亲水和带电基团[28],并且糖基化分子更易在油-水界面快速迁移并在油滴表面形成保护膜[29],阻碍油滴重新聚集,使乳化性及其稳定性显著增加(p<0.05);复合改性既可以通过超声增加疏水性又可以通过糖基化增强亲水性,并且超声预处理展开蛋白结构可以促进更多的糖与未糖基化蛋白结合,溶解性、表面电荷、表面疏水基团的进一步增加[27,29],使乳化性和乳化稳定性分别提升了38.18 m2/g、8.174 min。

图4 改性方法对蛋清粉乳化性能的影响Fig.4 Effect of different modification methods on the emulsion of egg white powder
2.5 抗氧化活性分析
同种物质在不同评价体系中抗氧化能力不同,所以我们通过四种指标来评价样品抗氧化能力。蛋白抗氧化活性与其空间结构、芳香族和含硫氨基酸中亲水性残基有关[30]。由图5可知,经热处理和超声改性后,样品的还原力、亚铁离子螯合能力与未处理原样相比没有显著(p>0.05)差异,而对DPPH·和ABTS+·的清除能力略有降低,这说明只改变蛋白结构的物理手段不能有效增强蛋白的供电子能力,而且蛋白溶解性降低还会使电子供体减少导致抗氧化能力降低;糖基化后的样品抗氧化活性均有提升,这是因为糖基化产物的生成、降解、聚合(如还原酮类、杂环类化合物等中间产物)以及焦糖化反应均有助于提高蛋白的抗氧化活性[31-32],DPPH·、ABTS+·等可以接受这些产物中抗氧化基团的氢原子以达到稳定状态,而且蛋白溶解性

图5 改性方法对蛋清粉抗氧化活性的影响Fig.5 Effects of different modification methods on the antioxidant activity of egg white powder
的增加也促进了抗氧化基团与自由基的接触,抗氧化活性进一步增强;复合改性过程中,超声使结构充分展开,更多氨基的暴露加速了糖基化反应,进一步增加了抗氧化物质的生成,提供更多的电子稳定自由基中断氧化反应的进行,最终使还原力、亚铁离子螯合能力、DPPH·和ABTS+·清除能力分别提升了1.133、57.22%、54.92%、34.55%;再经体外消化后,蛋白断裂成低分子肽,暴露更多的酪氨酸、色氨酸等抗氧化残基,释放更多的具有抗氧化能力的生物活性肽[33],并且溶解性的进一步增强也使抗氧化产物更易与自由基结合,样品的抗氧化活性显著增强(p<0.05)。
3 结论
70 ℃热处理4 h总体上会使蛋清粉致敏性增加,最高增加了12.77%,同时溶解性、乳化性能、抗氧化活性均出现不同程度降低;600 W冰水浴超声15 min后蛋清粉的致敏性增加程度更大,为20.84%,而乳化性能略有升高,但溶解性、抗氧化活性均降低;70 ℃糖基化改性4 h后致敏性显著降低(p<0.05),最大降低了29.08%,并且溶解性、乳化性能、抗氧化活性均有提升;复合改性后样品的致敏性降低程度更大,为43.9%,功能性也得到更大改善,溶解性、乳化性、乳化稳定性、还原力、亚铁离子螯合能力、DPPH·和ABTS+·清除能力相比原样分别提高了0.06751 mg/mL、38.18 m2/g、8.174 min、1.133、57.22%、54.92%、34.55%;复合改性再经体外消化后,样品的致敏性进一步降低,同时溶解性和抗氧化活性均有更大程度的提升。以上研究表明热处理不适合蛋制品加工,超声改性只适于开发高乳化性蛋制品,而糖基化和复合改性既可以有效降低致敏性,还能提高功能性,所以可用于蛋制品加工。并且复合改性的作用效果更显著,且复合改性后再经消化仍能很好的保持甚至提高产品品质,所以复合改性是蛋制品加工生产的最佳方法。
