从沉钒废水中回收铝制备纳米氢氧化铝的研究
2018-09-12职红涛马楠楠段建榜
职红涛,马楠楠,冯 修,段建榜,张 翔
(郑州大学化工与能源学院,河南郑州450001)
纳米氢氧化铝是一种优良的无机阻燃剂,具有阻燃、消烟和填充功能;纳米氢氧化铝化学性质不活泼,在燃烧过程中不产生有毒气体、不造成二次污染,因此在橡胶制品、电线电缆、日用品及其他领域中广泛应用[1-4]。此外,纳米氢氧化铝的表面效应、体积效应和小尺寸效应使其在催化剂、免疫佐剂等方面也有利用[5-6]。沉钒废水所含的金属离子中Al3+含量较高,为使Al3+重复利用并避免沉钒废水直接排放造成环境污染,笔者主要研究从沉钒废水中回收铝制备纳米氢氧化铝[7-8]。
1 实验部分
1.1 实验原料
沉钒废水来自某钒矿。将沉钒废水预处理,处理后的废水中各离子含量见表1。
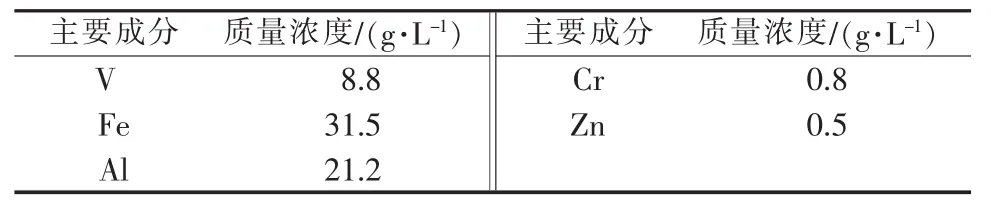
表1 预处理后的沉钒废水中主要成分及含量
1.2 实验方法
沉钒废水中铝、钒、亚铁离子含量较高,为分离这3种离子,加入氢氧化钠溶液使其生成氢氧化物沉淀,利用 Al(OH)3和 VO(OH)2可溶于强碱而 Fe(OH)2不溶于强碱的性质,调节溶液pH沉淀出Fe2+。然后加双氧水,将分离Fe2+后废水中的钒氧离子(VO2+)氧化为钒酸根(VO),利用VO在废水pH=5时不沉淀的性质,将废水中Al3+转化为Al(OH)3沉淀分离。将得到的Al(OH)3所附着的VO去除,进一步精制成纳米氢氧化铝。最后将纳米氢氧化铝做分散处理,以消除纳米粉体的团聚现象[9-10]。
2 结果与讨论
2.1 Fe2+的去除
取5份100mL废水,在常温下加入10 mol/L的氢氧化钠溶液,将废水中的铝、钒、亚铁离子转化为沉淀。继续滴加氢氧化钠溶液调节废水pH分别为10、11、12、13、13.5,搅拌 20 min,考察 pH 对铁沉淀率、铝和钒溶解量的影响,结果见图1。由图1可知,不同pH条件下沉钒废水中Fe(OH)2沉淀率均在99.4%以上,而 Al(OH)3和 VO(OH)2溶解量随 pH 增大而升高,并在pH达到13以后溶解量稳定,铝和钒的溶解量分别为90%、92%左右。因此溶液最佳pH为13。
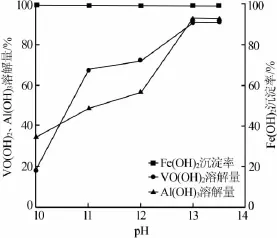
图1 pH对铁沉淀率、铝和钒溶解量的影响
2.2 VO的去除
加入双氧水将去除Fe2+后废水中的VO2+氧化为VO,然后用盐酸调节pH为5左右,氢氧化铝开始沉淀并有部分VO附着,将氢氧化铝胶体离心提取、烘干。对氢氧化铝进行精制,考察纳米氢氧化铝精制过程中氨水质量浓度、反应温度、反应时间对钒酸根去除的影响。
1)氨水质量浓度的影响。取6份3 g的氢氧化铝,加入到氨水质量浓度分别为 3、6、12、25、50、100 g/L的溶液中,反应温度为50℃,搅拌时间为60 min,考察氨水质量浓度对VO去除率的影响,结果见图2。从图2看出,在氨水质量浓度较低时,VO去除率随着氨水质量浓度的升高而迅速增大;在氨水质量浓度达到25 g/L后,VO去除率稳定在95%左右。这是因为,氨水溶液中会电离出OH-、NH等离子,这些离子起到电解质的作用并破坏氢氧化铝胶体,使胶体对VO的吸附作用减弱,而且NH与VO反应生成多聚钒酸盐溶于热水中。因此,氨水质量浓度选择25 g/L。
2)温度的影响。取7份3 g的氢氧化铝,加入到氨水质量浓度为25 g/L的溶液中,反应温度分别控制为 10、20、30、40、50、60、70 ℃,搅拌时间为 60 min,考察温度对VO去除率的影响,结果见图3。由图3可知,在50℃之前,VO去除率随温度的升高而增长迅速;当温度升高至50℃时,VO去除率达到94.2%;温度继续升高,VO去除率增长幅度较小。这是因为,温度升高不仅加快了体系的反应速度,而且破坏了氢氧化铝胶体。温度越高,胶体能量越大,胶体运动加剧,相互间碰撞机率增大,氢氧化铝胶核对VO的吸附力就会降低,则氢氧化铝的纯度提高。故反应温度选择50℃。
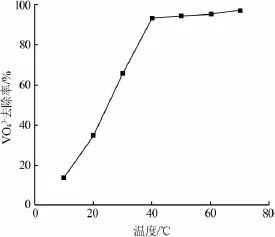
图3 温度对钒酸根去除率的影响
3)反应时间的影响。取7份3 g的氢氧化铝,加入到氨水质量浓度为25 g/L的溶液中,反应温度为50 ℃,控制搅拌时间分别为 10、12、20、25、30、35、40 min,考察搅拌时间对VO去除率的影响,结果见图4。由图4可知,在30 min前,VO去除率随着时间的增加而增长迅速;当反应时间为30 min时,VO43-去除率达到97.7%;继续增加反应时间,VO43-去除率增长幅度较小。因此,反应时间选择30 min。然后通过对氢氧化铝粉体进行分散处理消除其团聚现象后,最终得到纯度为97.3%的氢氧化铝。
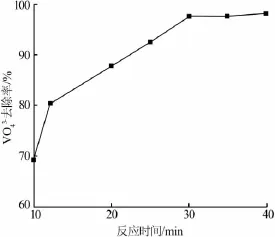
图4 反应时间对钒酸根去除率的影响
2.3 表征
1)IR分析。对制备的氢氧化铝进行红外光谱(IR,Varian800)分析,结果见图 5。 由图 5可知,3 440 cm-1处的吸收峰为吸附水和OH基变形振动的加和,1 520 cm-1处的吸收峰对应吸附水的变形振动,1 370 cm-1处的吸收峰对应OH基的面内弯曲振动,1 050 cm-1处的吸收峰对应OH基变形振动,621 cm-1处的吸收峰对应Al—O的伸缩振动,由此判定样品为氢氧化铝。
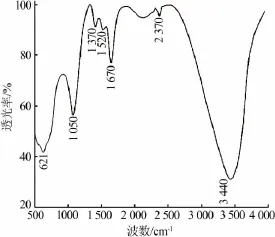
图5 氢氧化铝IR图
2)SEM分析。对制备的氢氧化铝进行扫描电子显微镜(SEM,JSM-6701)分析,结果见图6。由图6看出,氢氧化铝粒子呈球形,分布较均匀,平均粒径为40 nm左右,表明最终制备的样品为纳米级氢氧化铝。

图6 氢氧化铝SEM照片
3 结论
1)在常温下,向沉钒废水中加入氢氧化钠溶液,铝、钒、亚铁离子转化为氢氧化物沉淀。调节废水 pH=13,Fe(OH)2沉淀率为 99.4%,Al(OH)3和VO(OH)2溶解量达到90%以上,可沉淀分离Fe2+。
2)将双氧水加入除铁后的废水中将VO2+氧化为 VO。 调节废水 pH=5,VO不发生沉淀,Al(OH)3发生沉淀,将 Al(OH)3分离并烘干。
3)将 Al(OH)3加入氨水质量浓度为 25 g/L 的溶液中,控制反应温度为50℃、反应时间为30 min,可将Al(OH)3附着的 VO去除,得到纯度为 97.3%的氢氧化铝。通过IR及SEM分析确定,最终样品为直径为40 nm左右的纳米氢氧化铝。
