离子色谱法测定不同产地芡实中二氧化硫残留量
2018-09-01陈蓉陈伟顾炳仁
陈蓉,陈伟,顾炳仁
(1.苏州市药品检验检测研究中心,江苏 苏州 215104;2.苏州市中医医院,江苏 苏州 215009)
芡实为睡莲科植物芡EuryaleferoxSalisb的干燥成熟种仁,具有益肾固精,补脾止泻,除湿止带的功能,临床上用于遗精、尿频、脾虚久泻、带下[1]。芡实营养价值高,富含淀粉[2]、蛋白质[3]、多糖[4]等物质,除了是传统中药,如今也广泛应用于各种保健品和食品。由于营养性成分含量高,芡实在产地加工、贮藏过程中,为达到防霉、防虫的目的,常可能人为地引入硫磺熏蒸。
适量的熏蒸能达到杀菌防虫的目的,同时使中药材看起来更美观[5]。但过量的熏蒸易导致二氧化硫残留,既造成环境污染,又对人体产生潜在危害[6]。硫熏产生的二氧化硫,与药材中的水分、无机元素结合生成亚硫酸盐,亚硫酸盐是危害的源头,体内蓄积过量的亚硫酸盐严重影响到消化道和呼吸道黏膜,会加重哮喘患者的病情甚至导致死亡[7]。目前芡实的质量标准较为简单,《中国药典》检查项仅为水分、灰分、浸出物,而无有害物质控制项,对其进行二氧化硫残留量检查十分必要。
《中国药典》2015年版中规定了山药、牛膝、粉葛、甘遂、天冬、天麻、天花粉、白及、白芍、白术、党参等11味药材及其饮片中二氧化硫残留量不得过400 mg·kg-1;其他中药材及饮片二氧化硫残留量不得过150 mg·kg-1。《中国药典》2015年版四部附录通则2331二氧化硫残留量测定法,收录了酸碱滴定法、气相色谱法、离子色谱法三种方法[8]。酸碱滴定法操作简单,易普及,其原理为样品中亚硫酸盐在酸性条件下转化为二氧化硫,随氮气吹入吸收瓶,被过氧化氢吸收氧化为硫酸根离子,最后用氢氧化钠溶液滴定。但对于部分颜色较深的药材滴定终点判断不明显,易出现假阳性,该法也不适用于金银花、甘草、山楂等含有机酸的药材。气相色谱法虽然专属性强、灵敏度高,但需配备气密针形式的顶空进样装置,且样品前处理过程中需要蜡封,操作复杂,成本较高,不便于推广使用[9]。离子色谱法专属性较强、灵敏度高、稳定性好、前处理较简便,更适合大批量样品的检测[10-11]。本研究采用盐酸蒸馏法提取,过氧化氢吸收并氧化,离子色谱法测定硫酸根离子的含量,以期监测芡实药材中的二氧化硫残留量,保证用药和饮食安全。
1 仪器与试药
1.1仪器ICS-5000离子色谱仪,配备阴离子抑制器和电导检测器(美国Dionex公司);Dionex Inopac AS 11-HC阴离子分析柱(250 mm×4 mm),AG 11-HC保护柱(50 mm×4 mm);Sartorius CPA225D电子天平(d=0.1 mg,德国赛多利斯公司);Milli-Q超纯水机(美国Millipore公司);Thermo Biofuge primo R高速离心机(美国Thermo公司)。
1.2试药30%过氧化氢(国药集团化学试剂有限公司,优级纯);氢氧化钾(国药集团化学试剂有限公司,分析纯);亚硫酸钠(国药集团化学试剂有限公司,分析纯);盐酸(国药集团化学试剂有限公司,优级纯)。硫酸根标准溶液,标示量:1 000 mg·L-1,批号:13073,购自中国计量测试研究院。14批芡实药材分别来源于河北安国、广东肇庆、安徽芜湖、四川成都、江西武穴、福建莆田、四川中江、湖南益阳、山东菏泽、江苏苏州、江苏宝应、江苏金湖、江苏建湖、江苏浦口,经南京中医药大学吴启南教授鉴定为睡莲科植物芡EuryaleferoxSalisb的干燥成熟种仁,其中,福建莆田、江苏苏州、江苏宝应、江苏金湖、江苏建湖、江苏浦口为苏芡,其余产地为刺芡。
2 方法与结果
2.1色谱条件色谱柱:Dionex Inopac AS 11-HC阴离子分析柱(250 mm×4 mm);保护柱:AG 11-HC(50 mm×4 mm);柱温:30 ℃;洗脱液:20 mmol·L-1氢氧化钾溶液(在线淋洗液发生器);抑制器电流:60 mA;电导检测器温度:30 ℃;流速1.0 mL·min-1;进样量10 μL。
2.2溶液的制备
2.2.1对照品溶液的制备 取硫酸根标准溶液,加水稀释成制成200、100、50、20、5、1 mg·L-1的溶液,作为标准曲线系列溶液。
2.2.2供试品溶液的制备 取供试品粉末10 g,精密称定,置水蒸气蒸馏装置(参照《中国药典》2015年版四部通则2331第三法)的样品瓶中,加水50 mL,振匀;于100 mL量瓶中加入3%过氧化氢20 mL作为接收液,连接好水蒸气蒸馏装置,快速于样品瓶中加入盐酸5 mL,立即密封,进行水蒸气蒸馏。至接收瓶中液体接近100 mL时,停止蒸馏,取下接收瓶。用去离子水稀释至刻度,摇匀,离心,取上清液作为供试品溶液。
2.2.3空白溶液 空白溶液为不加供试品,自“加水50 mL”起,按“2.2.2”项下方法操作,即得。
2.2.4测定法 取对照品溶液、供试品溶液(广东肇庆)及空白溶液各10 μL,按“2.1”项下条件进行检测,结果表明待测离子与其他离子分离良好,空白不干扰硫酸根离子(二氧化硫)的测定[12],见图1。

注:A为对照品溶液,B为供试品溶液,C为空白溶液
图1离子色谱图
2.3系统适用性试验将“2.2.1”项下不同浓度的对照品溶液,按“2.1”项下条件进样10 μL,测定峰面积。分别以硫酸根离子浓度(mg·L-1)为横坐标,峰面积为纵坐标,绘制标准曲线,得回归方程
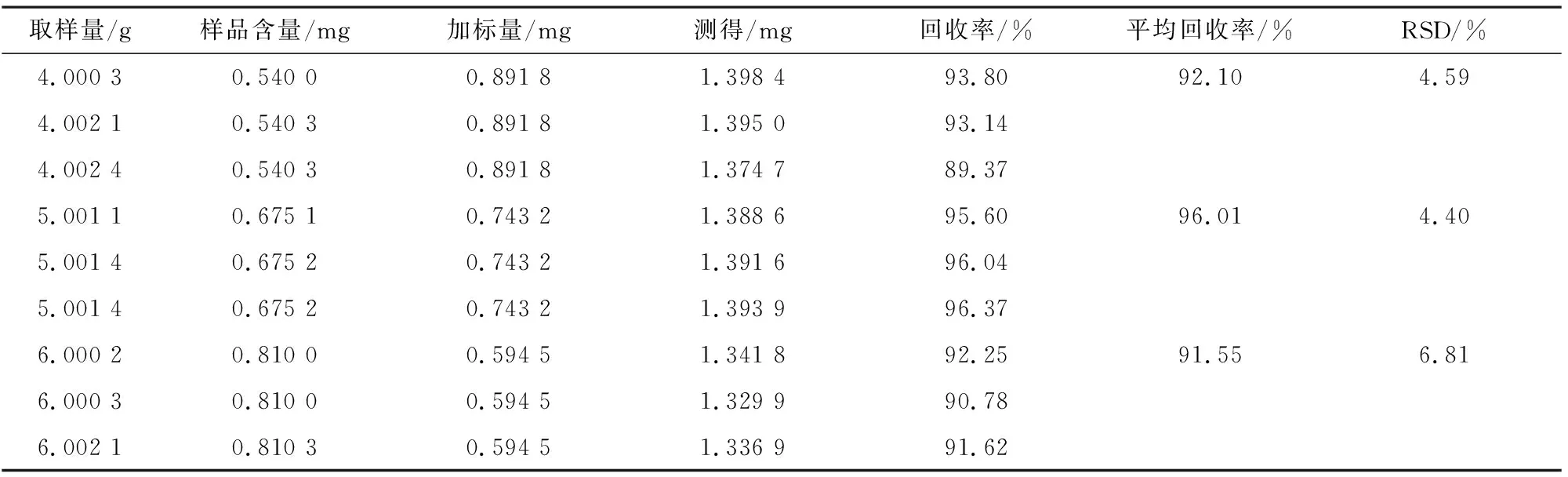
表1 回收率试验结果
(Y=0.679 1X-0.961 6,r=0.999 9),硫酸根离子在1.00~200.00 mg·L-1线性范围内呈现良好的线性关系。
2.4检出限和定量限根据峰高以信噪比S/N=3确定检出限为0.33 mg·L-1,S/N=10确定定量限为1.0 mg·L-1。
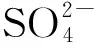
2.6稳定性试验取“2.2.2”项下广东肇庆的供试品溶液,按“2.1”项下条件分别于0、4、6、8、12、24 h进样,测定峰面积,其RSD为1.31%,说明样品在24 h内稳定。
2.7重复性试验精密称取广东肇庆样品6份,每份10 g,按“2.2.2”项下方法制备供试品溶液,按“2.1”项下条件测定峰面积,结果以二氧化硫/硫酸根离子=0.666 9计算二氧化硫残留量,平均含量为137.7 mg·kg-1,RSD为2.1%,说明方法重复性良好。
2.8加样回收率试验分别精密称取已测得含量的广东肇庆样品4、5、6 g,每个浓度各3份,分别精密加入亚硫酸钠溶液1.80、1.50、1.20 mL(亚硫酸钠标准溶液临用新配,并用碘量法[13]标定,以二氧化硫计,浓度为0.495 4 g·L-1),按“2.2.2”项下方法制备供试品溶液,按“2.1”项下条件测定峰面积,计算回收率,结果见表1。
2.9样品测定取14 批芡实样品各约10 g,精密称定,分别按“2.2.2”项下方法制备供试品溶液,按“2.1”项下条件测定峰面积,扣除空白溶液的响应值后,计算样品中二氧化硫残留量,结果见表2。
2.10聚类分析采用SPSS 18.0,以组间平均法,计算平方欧氏距离,对14个产地样品进行聚类分析,得到不同样品的聚类图。14个产地样品被聚为四类,结果见图2。
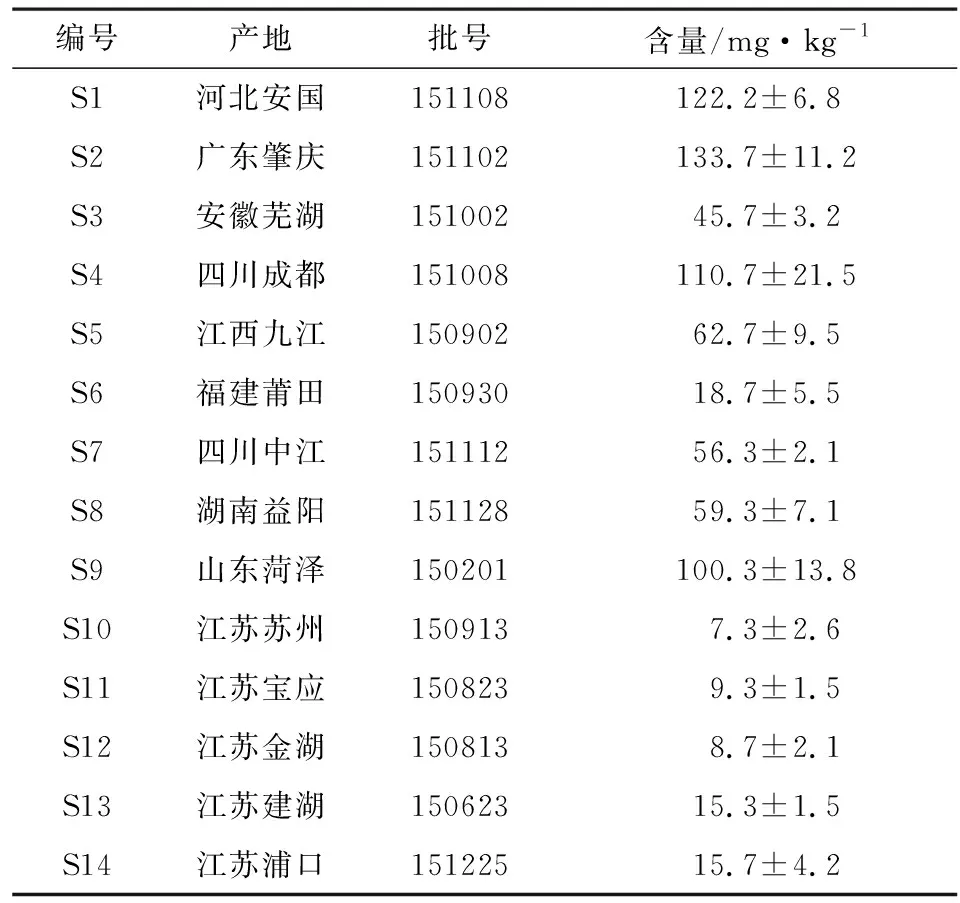
表2 芡实中二氧化硫残留量

图2 不同产地芡实二氧化硫残留量聚类结果
第一类包括6个产地(S6、S10、S11、S12、S13、S14),分别为江苏苏州、江苏宝应、江苏金湖、江苏建湖、江苏浦口、福建莆田,这一类产地芡实中二氧化硫残留量最低,不超过20 mg·kg-1。江苏和福建莆田芡实品种为果皮不带刺的苏芡,以食用为主,药用为辅[14]。其中江苏苏州的残留量最低,可能与苏州地区芡实主要作为时令水生蔬菜,以鲜品供食用有关,无需硫熏储存。
第二类包括4个产地(S3、S5、S7、S8),分别为安徽芜湖、江西九江、四川中江、湖南益阳,这些产地均在长江流域,水资源丰富地区,二氧化硫残留量均不超过70 mg·kg-1。
第三类包括2个产地(S4、S9),分别为四川成都、山东菏泽,这一类产地二氧化硫残留量均超过100 mg·kg-1,可能与成都气候湿润,硫熏为防霉变有关。
第四类包括2个产地(S1、S2),分别为河北安国、广东肇庆,这一类产地二氧化硫残留量均超过120 mg·kg-1,远高于其他产地,可能与河北安国是药材流通市场,硫熏能增强药材外观和贮存时间;广东肇庆是刺芡主产区,是药用芡实的主要来源,硫熏能增强产地加工的效果有关。
聚类结果显示,芡实药材中二氧化硫残留量有明显的产地差异,基本以苏芡量最少,长江流域次之,而刺芡中残留量最大,可能与产地气候、环境以及产品用途有关。故产地从一定程度上可以反应药材的硫熏情况。
3 讨论
各产地芡实药材均存在一定程度的二氧化硫残留,食用芡实较药用芡实安全性高,因此建议药材产地加工选用更为合理的熏制工艺,尽量减少二氧化硫在芡实中的残留,以保证药物安全。本研究采用的离子色谱法操作简便,精密度、稳定性、重复性较好,准确度较高,适合芡实中二氧化硫残留检测,可为芡实药材质量标准提高作一参考,也可为食品工业原料质控提供依据。
国际上对此已有相关限度要求。FAO/WHO及食品添加剂专家委员会(JECFA)认为:二氧化硫的成人摄入量每日不得超过0.7 mg·kg-1[15]。韩国食品医药品安全厅对中药材中二氧化硫的限量值规定为30 mg·kg-1[16]。国内外食品领域中的限量值多在30~100 mg·kg-1[17-18]。因此,根据试验结果及上述标准,并参考我国《食品添加剂使用卫生标准》,芡实中二氧化硫限量可暂定为150 mg·kg-1[19]。
此外需要注意的是,二氧化硫的残留量会随时间推移而变化,同时不同提取方法和测定手段得到的结果会有较大的差异[20],如滴定法人为因素影响大,准确度较低。离子色谱法相对灵敏度较高,蒸馏处理的样品较为洁净,但蒸馏速度太快,会导致结果偏差较大,因此实验条件应保证相对稳定。
