PEG-rhG-CSF对恶性肿瘤患者化疗间期生活质量的影响*
2018-08-29郭园园李玉梅周争光
汪 蕊,郭园园,李玉梅,刘 静,苏 方,杨 燕,周争光
(蚌埠医学院第一附属医院:1.肿瘤内科;2.泌尿外科,安徽蚌埠 233004)
近年来,恶性肿瘤的发病率和死亡率均逐年上升,已取代心血管疾病成为我国居民死亡原因的首位[1]。化疗作为不可切除或转移性晚期恶性肿瘤主要治疗方法之一,延长了恶性肿瘤患者的生存时间,提高了患者生活质量。在接受化疗的恶性肿瘤患者中,约80%会出现不同程度的骨髓抑制,重组人粒细胞集落刺激因子(recombinant human granulocyte colony- stimulating factor,rhG-CSF)是防治肿瘤化疗引起粒细胞减少的有效药物,但因其半衰期短,需重复注射给药,在改善骨髓造血状态同时也增加了患者痛苦[2]。随着长效聚乙二醇重组人粒细胞集落刺激因子(PEG-rhG-CSF)的问世,恶性肿瘤患者化疗期间的骨髓抑制不良反应发生率明显降低,生活质量也得到极大提高[3]。本研究回顾性分析了PEG-rhG-CSF在恶性肿瘤化疗间期的临床应用对恶性肿瘤患者化疗间期生活质量的影响,现将分析结果报道如下。
1 资料与方法
1.1一般资料 选取2016年6月至2017年11月在本科进行化疗治疗后发生Ⅲ~Ⅳ级中性粒细胞减少的恶性肿瘤患者76例。入选标准:(1)经组织病理学或细胞学确诊为恶性肿瘤;(2)接受化疗治疗后出现Ⅲ~Ⅳ级中性粒细胞减少;(3)年龄大于或等于18岁;(4)ECOG评分小于或等于2分;(5)无血液系统疾病;(6)化疗前中细胞(WBC)≥4.0×109/L、中性粒细胞绝对计数(ANC)≥2.0×109/L、血红蛋白(Hb)≥9.0 g/dL、血小板(PLT)≥80×109/L;(7)凝血功能正常;(8)心脏、肝、肾功能正常;(9)化疗间期进行了包含生活质量在内的出院随访。排除标准:(1)既往化疗中多次出现骨髓抑制;(2)难以控制的感染;(3)既往接受过PEG-rhG-CSF治疗;(4)严重心、肝、肾功能障碍;(5)既往接受过造血干细胞移植或器官移植;(6)既往接受过放疗治疗;(7)存在骨髓侵犯;(8)合并其他严重并发症;(9)怀孕或哺乳期女性。
1.2治疗方法 化疗结束后48 h血常规检查出现Ⅲ~Ⅳ级中性粒细胞减少,观察组给予PEG-rhG-CSF注射液3~6 mg[齐鲁制药有限公司,国药准字S20150013,规格1.35×108IU(3.0 mg)∶1.0 mL]皮下注射1次。对照组给予rhG-CSF注射液200 μg[齐鲁制药有限公司,国药准字S20033040,规格:200 μg∶1.2 mL]皮下注射,每日1次,直至血常规检查WBC≥4.0×109/L、ANC≥2.0×109/L。
1.3生活质量评估 在给药第7~14天,通过电话随访方式使用EORTC生命质量测定量表 QLQ-C30(V3.0)中文版对患者生活质量进行评估。量表评分标准:1~28条目,4个等级直接评价1~4分。29、30条目,7个等级,评1~7分。量表共包括5个功能领域(躯体、角色、情绪、认知和社会功能)、3个症状领域(疲倦、恶心呕吐和疼痛)、1个总体健康状况以及6个单一条目。每个领域得分(粗分RS,raw score)为该领域包括条目得分总和除以该领域条目数,即RS=(Q1+Q2+…+Qn)/n。为了方便比较各领域得分,采用极差化方法进行线性变换,将RS转换成0~100的标准化得分(standard score,SS)。量表中除29、30条目外均为逆向条目,得分越高,代表生活质量越差,而计分规则中规定,功能和总体健康领域得分越高表明功能状况和生活质量越好,症状领域计分越高说明生活质量越差,因此在功能领域计算时需要改变方向,具体的计算方式为:功能领域SS=[1-(RS-1)/R]×100;症状领域和总体健康状况领域SS=[(RS-1)/R]×100[4]。
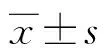
2 结 果
2.1两组一般资料比较 根据纳入标准,共收集了84例患者,其中观察组患者41例,对照组患者43例。因随访期内中性粒细胞减少未恢复至正常值、生活质量量表信息不完整等,观察组剔除5例,对照组剔除3例,最后选择观察组36例,对照组40例进行生活质量各领域评分比较。两组患者在年龄、性别、初始体力状态评分等方面差异无统计学意义(P>0.05),见表1。
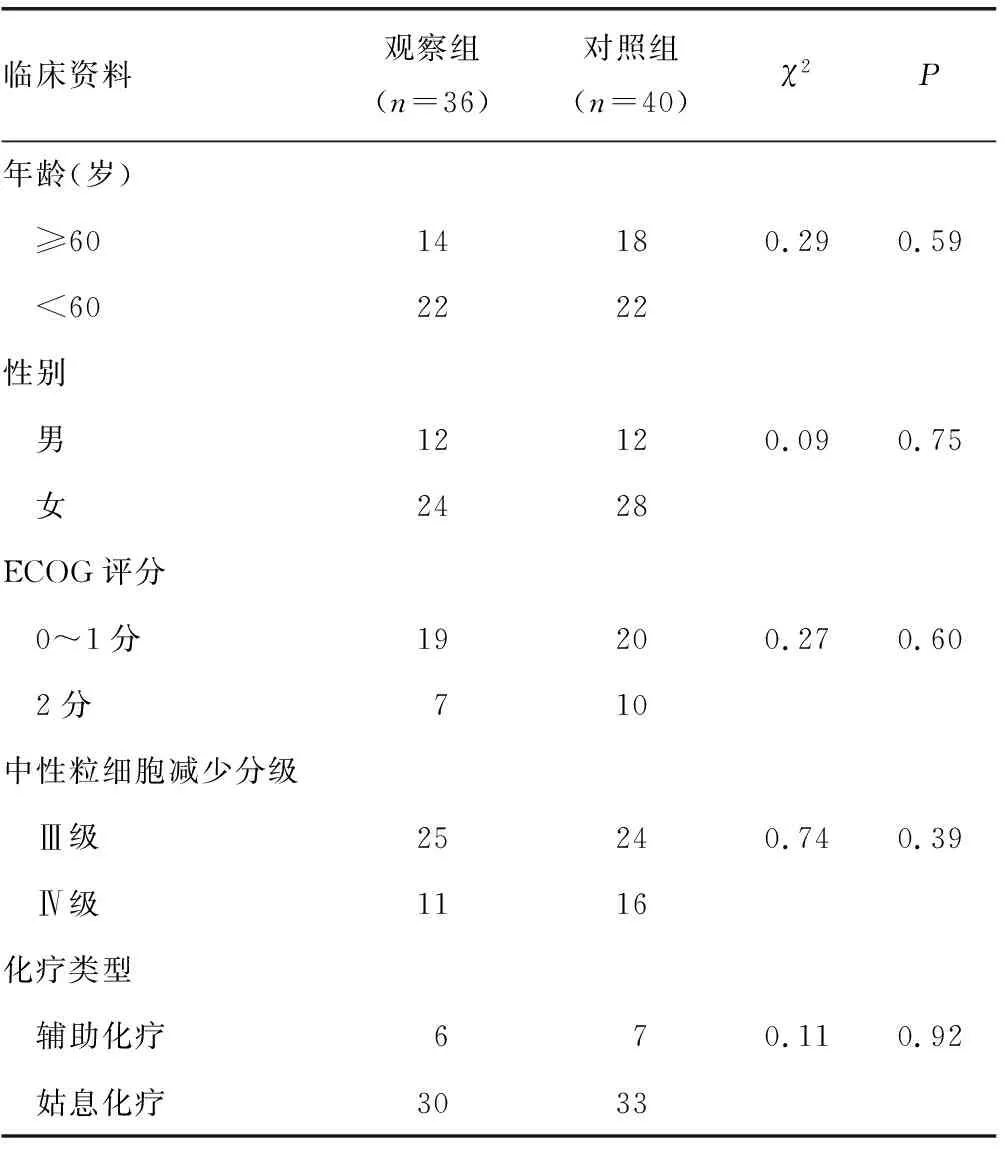
表1 两组患者一般资料比较
2.2两组功能领域比较 观察组患者治疗后第7~14天躯体、角色和情绪功能得分均明显高于对照组(P<0.01)。认知功能在观察组有提高趋势,但认知功能、社会功能差异均无统计学意义(P=0.125、0.634),见表2。
2.3两组症状领域比较 观察组患者治疗后第7~14天疲倦症状和疼痛症状显著低于对照组(P<0.05),而两组间恶心、呕吐症状差异无统计学意义(P>0.05),见表3。
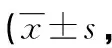
表2 两组功能领域得分比较分)
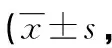
表3 两组症状领域得分比较分)
2.4两组单一条目比较 观察组治疗后第7~14天气促、便秘、腹泻和经济困难与对照组无明显差异(P>0.05);观察组患者失眠和食欲丧失症状轻于对照组(P<0.05),见表4。
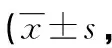
表4 两组单一条目得分比较分)
2.5两组总体健康状况比较 观察组治疗后第7~14天总体健康状况平均得分为(78.70±1.83)分,对照组为(66.25±1.74)分,观察组总体健康状况优于对照组(P<0.05)。
3 讨 论
骨髓抑制的发生是影响恶性肿瘤化疗执行率和疗效的主要原因之一,预防或有效治疗骨髓抑制不良反应是提高恶性肿瘤患者化疗疗效及生活质量的关键举措。rhG-CSF是通过基因重组技术生产的人粒细胞集落刺激因子,可治疗化疗引起的中性粒细胞减少及预防由此引起的感染,广泛应用于肿瘤各临床科室[5-6]。此外,还逐渐应用于骨髓移植术后治疗、骨髓增生异常综合征和干细胞动员等。因rhG-CSF在体内易被酶水解和肾脏清除,半衰期较短,需要反复多次注射,可引起皮肤过敏反应、骨骼肌疼痛、头痛、乏力和肾功能损害等不良反应[7]。为了解决rhG-CSF的不足,Amgen公司在1999年通过共价修饰技术生产的聚乙二醇(PEG)化的长效制剂PEG-rhG-CSF,降低体内的免疫原性,提高生物稳定性,减缓清除率,延长半衰期,减少注射次数,给患者带来了更大临床获益[8]。临床研究表明,PEG-rhG-CSF单次给药后,可持续有效的升高中性粒细胞绝对值,提高化疗耐受性,增强患者治疗信心,减少住院时间及多次给药带来的痛苦[9]。兰海涛等[10]研究表明,PEG-rhG-CSF与rhG-CSF在治疗因化疗引起的中性粒细胞减少患者中疗效相似,但PEG-rhG-CSF的便利性,显著改善了患者治疗的负面情绪,提高了生活质量。石远凯等[11]进行的多中心随机对照临床研究结果显示,PEG-rhG-CSF各项不良反应发生率同rhG-CSF类似,但程度较轻,耐受性更好,这为患者化疗间期的生活质量提供了保障。本研究发现,发生Ⅲ~Ⅳ级中性粒细胞减少的恶性肿瘤患者应用PEG-rhG-CSF第7~14天后,功能领域中躯体、角色和情绪均较对照组明显提高(P<0.05),认知和社会功能在长短效组中未见显著差异。症状领域中使用PEG-rhG-CSF的观察组疲倦和疼痛症状均低于传统对照组,恶心呕吐在两组之间差异不明显。单一条目中观察组失眠和食欲丧失症状轻于对照组,气促、便秘、腹泻和经济困难两组之间无统计学差异。观察组患者化疗间期总体健康状况优于对照组患者。可见,PEG-rhG-CSF可改善Ⅲ~Ⅳ级中性粒细胞减少的恶性肿瘤患者化疗间期相关领域的生活质量,考虑可能为PEG-rhG-CSF单次给药,减轻了患者局部多次注射疼痛症状,改善了患者对疾病产生的恐惧情绪,增强了治疗信心,继而影响了患者乏力、失眠、食欲丧失等症状以及躯体功能。尽管本研究为PEG-rhG-CSF的临床应用提供了一定的循证学依据,但因回顾性分析研究,样本量较少,两组比较时并未选择单一瘤种或是统一化疗方案,这势必影响研究结果的证据力度,因此有必要选择同一瘤种或相同化疗方案患者进行前瞻性随机对照临床研究进一步考察PEG-rhG-CSF对恶性肿瘤患者化疗间期生活质量的影响,以排除其他因素的干扰。
综上所述,PEG-rhG-CSF单次给药,更为便捷,还在一定程度上减轻了恶性肿瘤患者化疗间期治疗痛苦,改善了患者的治疗体验,提高了生活质量,是化疗后发生严重中性粒细胞减少患者的较好选择,具有良好的临床应用前景。
