超声造影时间-强度曲线评价射频消融治疗肝癌的应用价值
2018-08-28何燕莲余岳芬刘振华
何燕莲,余岳芬,刘振华
(海南省儋州市人民医院,海南 儋州 571799)
超声造影(CEUS)是通过造影剂的使用,在后散射回声增强的基础上,使得超声诊断的敏感性、特异性、分辨力都有明显提高的技术。目前评价肝癌射频消融术(RFA)疗效的主要影像学检查是增强CT(CECT)、磁共振成像(MRI),但在RFA后无法行床边即刻检查判断消融疗效。利用CEUS技术,可以客观获得肝内肿瘤及RFA治疗后病灶区域的微循环信息[1-2]。时间强度曲线(TIC)还可对获取的动态图像进行定量分析,精确反映感兴趣区内的微循环特征。本研究通过分析TIC在肝癌RFA治疗前和治疗后的情况,以判断消融治疗效果。
1 临床资料
1.1一般资料 收集2014年1月—2016年12月于海南省儋州市人民医院住院的肝癌患者85例,男60例,女25例;年龄41~82(58.74±10.26)岁;其中原发性肝癌(HCC)74例,转移性肝癌(MLC)11例,共108个病灶。108个病灶行RFA治疗1个月后,完全消融67个,部分消融或未消融41个。病例选择以无肝内血管、胆管主要分支及下腔静脉的侵犯为原则。患者RFA治疗前均行CEUS和/或增强CT、增强MRI及活检证实。
1.2方法
1.2.1主要仪器 使用日立HI Vision Preirus彩色多普勒超声诊断仪,探头频率为9~12 MHz,机械指数0.08。超声造影剂采用SonoVue(意大利Bracco公司),使用前加入生理盐水5 mL充分振摇制成微泡悬液。射频仪采用RITA MODEL1500型RFA系统(美国RITA公司),15G星形XL射频电极针(美国RITA公司)。
1.2.2超声检查 常规超声观察肝脏肿瘤的大小、形态、边界、位置、周边有无声晕、内部血流及阻力指数后行超声造影检查。注射造影剂记录观察病灶各个时相的灌注模式,并观察肿瘤全貌及相邻区域;在获得较完整的时相记录后快速扫查全肝观察有无异常廓清病灶,对可疑异常区需行2次注射造影。同时开启超声仪内置计时器,用超声图像工作站和内置光盘记录扫查。超声造影前患者均签署知情同意书,造影过程中嘱患者平静呼吸。造影结束后将造影动态图像导入SonoLiver CAP软件,在造影图像上勾画出感兴趣区,选择病灶区及参考区,优化图像,运动补偿后进行TIC分析,记录其上升时间(RT)、达峰时间(TTP)、平均通道时间(MTT)、峰值强度(PI)、峰值强度减半时间(DT/2)、内洗斜率(WIS)和曲线下面积(AUC)。
1.2.3射频消融及穿刺活检 RFA治疗前均行常规超声及CEUS检查。明确病灶的性质、数目及位置,确定病灶大小、范围,定好进针路线。局部麻醉后,超声引导置入冷循环射频针,每次治疗时间12 min。RFA治疗后5 min高回声消退,行CEUS检查,判定消融病灶疗效,实时观察肿瘤治疗区域造影剂灌注情况,若各期均无异常增强区,提示肿瘤完全灭活;若肿瘤内或边缘有增强区,提示肿瘤残留。RFA治疗1个月后行CEUS和TIC复查,与同期周围肝实质对比,判定消融病灶疗效。
1.2.4图像分析 由2位经验丰富的医师进行超声造影及图像分析,观察病灶的大小、形态、边界、强化方式、内部有无新生血管,图像导入超声造影TIC进行量化分析。
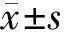
2 结 果
2.1超声造影TIC声像图 原发性肝癌动脉相病灶迅速增强,静脉相及延迟相回声消退,见图1。转移性肝癌造影呈多样表现,一般病灶周边在动脉相迅速增强,但与周围肝组织分界不如肝血管瘤清晰,见图2。
2.2原发性肝癌和转移性肝癌患者超声造影定量参数比较 原发性肝癌与转移性肝癌超声造影参数RT、TTP、MTT和DT/2比较差异均有统计学意义(P均<0.05),而PI、WIS和AUC比较差异均无统计学意义(P均>0.05)。见表1。
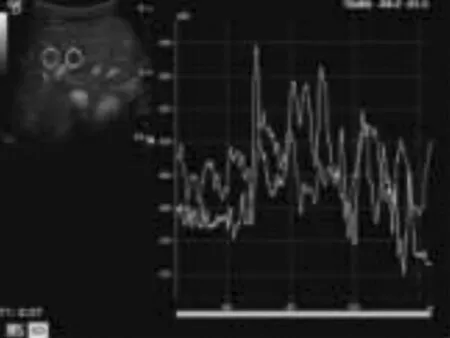
图1 原发性肝癌TIC
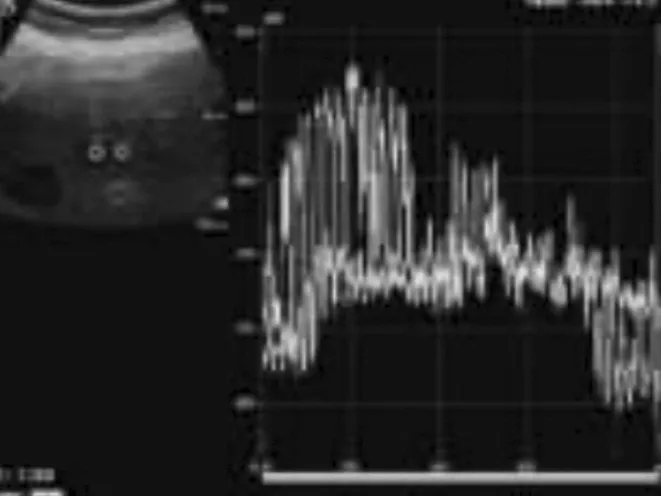
图2 转移性肝癌TIC

表1 原发性肝癌和转移性肝癌患者TIC参数比较
注:①与转移性肝癌比较,P<0.05。
2.3肝癌患者射频消融治疗前病灶和周围肝组织超声造影定量参数比较 肝癌患者治疗前病灶与肝组织超声造影参数RT、TTP和MTT比较差异均有
统计学意义(P均<0.05),而DT/2、PI、WIS和AUC比较差异均无统计学意义(P均>0.05)。见表2。
2.4肝癌患者射频消融治疗后病灶和周围肝组织超声造影定量参数比较 肝癌患者治疗后病灶与周围肝组织超声造影参数RT、TTP、MTT和WIS比较差异均有统计学意义(P均<0.05),而DT/2、PI和AUC比较差异均无统计学意义(P均>0.05)。见表3。

表2 肝癌患者射频消融治疗前病灶和周围肝组织TIC参数比较
注:①与周围肝组织比较,P<0.05。

表3 肝癌患者射频消融治疗后病灶和周围肝组织TIC参数比较
注:①与周围肝组织比较,P<0.05。
2.5超声造影和超声造影TIC评价肝癌治疗后的诊断效能 超声造影TIC检查的准确性优于超声造影,其灵敏度、特异度、阳性预测值及阴性预测值见表4。
表4 超声造影和超声造影TIC检查的准确性比较 %
3 讨 论
超声造影是指在常规超声检查的基础上,通过静脉注射造影剂来增强人体的血流信号,实时动态的观察组织微血管灌注信息,从而提高病变的检出率并对病变的良恶性进行鉴别的一项增强影像学检查手段。近年研究表明,CEUS可以大大提高肝癌的检出率,尤其对小病灶的检出率比增强CT还要高[3-4]。CEUS可准确识别荷瘤动脉血管,指导制定相应的治疗策略,消融荷瘤动脉血管或治疗前行肝动脉栓塞,以阻断或减少病灶内的血供,降低治疗后肿瘤的残留和复发[5]。对于肝硬化背景下的小肝癌、卫星灶以及高血供的转移灶,CEUS动脉期能够清晰显示病灶并引导电极精确穿刺进入病灶,完成消融治疗。超声造影TIC曲线在超声造影的基础上实时匹配相关成像技术,更为直观地显示肿瘤内血管的造影剂流速及流量随时间的变化,避免了肉眼观察的主观性,量化评价肿瘤内血管的丰富程度及灌注模式[6],可以较好地诊断肉眼无法鉴别的良、恶性占位病灶[7]。TIC通过定量计算上升时间、达峰时间、始增强度、峰值强度、峰值强度减半时间和曲线下面积等参数显示肿瘤的增强或消退速率,反映了肿瘤特有的血管形态所表现的血流动态。本研究结果显示,原发性肝癌动脉相病灶迅速增强,静脉相及延迟相回声消退,呈现出“快进快出”的影像学特征。转移性肝癌造影后呈多样表现,主要以早期环状增强为主,并向中心强化。原发性肝癌造影参数RT、TTP、MTT值明显低于转移性肝癌,而DT/2值明显高于转移性肝癌。提示原发性肝癌的峰值时间提前,消退时间慢于转移性肝癌。
超声引导下肝脏肿瘤射频消融术是目前治疗肿瘤的重要技术,有报道其对小肝癌治疗的生存期可与外科手术切除相媲美[8]。准确评价RFA的疗效,尽早发现肿瘤残留和复发并及时进行补充治疗是提高RFA疗效的关键。本研究中108个病灶行RFA治疗1个月后,完全消融组67个,部分消融组或未消融组41个。对肝癌患者进行TIC分析,发现RFA治疗前病灶造影参数RT、TTP和MTT值明显低于周围肝组织。RFA治疗后病灶造影参数TTP、MTT和RT值呈降低趋势且明显低于周围肝组织,而WIS值呈增高趋势且明显高于周围肝组织。在造影参数中MTT为造影剂通过ROI的平均时间,其值越小,表明造影剂消退的速度越快;WIS为单位时间内造影剂灌注强度,其值越大,表明造影剂灌注速度越快。提示TIC曲线参数RT、MTT、TTP和WIS比较可以分析RFA治疗后病灶与周围肝实质情况。叶艳艳等[9]研究表明肝癌病灶的灌注速度较快,增强时间较短,TIC上升陡直,斜率较大。比较CEUS和TIC在肝癌治疗后的诊断效能,发现TIC的准确性优于超声造影,其灵敏度、特异度、阳性预测值及阴性预测值分别为98.4%,84.8%,91.7%,98.2%,与Jaspers等[10]的研究基本一致。
综上所述,超声造影可以敏感而直观地显示肝肿瘤在不同时相内造影剂灌注的实时动态过程,在肝脏病变的诊断和肝癌RFA治疗中具有重要的作用。应用超声造影TIC技术可以较好地分析病变特征,使超声造影的分析过程更加真实、客观,避免以往超声造影诊断疾病的主观性,为肝癌的鉴别诊断和疗效评估提供可靠的依据。
