质谱中气相离子/离子反应的研究进展
2018-07-27叶似剑熊行创龚晓云刘大军
叶似剑,李 明,熊行创,江 游,龚晓云,刘大军,方 向
(1.长春理工大学化学与环境工程学院,吉林 长春 130000; 2.中国计量科学研究院,北京 100029)
近年来,质谱中的气相离子/离子反应被广泛应用于分析化学、有机化学等领域[1-2]。在质谱中,气相离子大多以单分子形式存在,反应效率较高;另外,还可以选择特定的离子进行反应,特异性强。根据质谱给出的质荷比信息可分辨产物和反应物的分子质量信息,并通过多种转换方式(如串联质谱等)分析化合物的结构。同时,气相离子/离子反应在探索有机化学反应机理、解析多肽结构等方面也发挥着重要作用。本工作拟对气相离子/离子反应的动力学、反应装置、反应类型及应用等方面进行综述。
1 离子/离子反应动力学理论研究
相较于离子/分子反应,离子/离子反应中带相反电荷的离子间库仑引力很大,作用范围更广。因此,两个离子形成的稳定运动轨道(一般为椭圆形)的横截面积更大,该面积的大小由反应离子的带电荷量、相对速度和相对质量决定[3]:
(1)
其中,Z1和Z2是反应离子所带单位电荷数,e是电子电量,ε0是真空介电常数,v是相对速度,μ是折算质量。一般情况下,两个离子间的距离很远而不足以发生化学反应,通过减小相对运动速度,可以拉近两个离子的距离,使其在相互吸引的电场中被捕获,从而发生离子/离子反应。有两种反应结果:1) 两者形成一个相对稳定的络合产物;2) 转移一个带电小粒子(质子或电子)。当发生质子或电子转移的距离大于发生物理碰撞(即形成较稳定的络合物)的距离时,后一种反应为主反应。以质子转移反应为例,一个质子能跃迁的最大距离rPT可用式(2)表示[4]:
(2)
其中,Z1和Z2分别是两个反应离子所带单位电荷数,ΔHPT是发生质子转移反应的焓变。可以看出,如果要得到相对稳定的络合产物,需选用带电荷数较少且横截面较大的反应物,反之则容易发生质子或电子转移反应。
2 主要反应装置
1991年Ogorzalek-Loo[5]首次研制了离子/离子反应装置,其结构示于图1。不同极性的离子被分别引入到一个60°的Y形毛细管中,并在此发生离子/离子反应,然后将反应产物导入四极杆质谱仪进行检测。这种Y型管式反应器可以完成一些简单的质子转移反应,包括降低电荷价态和电荷倒置的反应[6]。但是很难确定这种反应器的实验条件,因为在Y型管内的离子、溶剂蒸汽和空气状态会随着实验条件(如放电电流、针口间距和入口孔径大小等)的改变而改变。另外,四极杆质谱仪有限的质荷比检测范围也阻碍了对较大质荷比反应产物离子的检测。
1999年,Smith等[7]报道了一种用于降低生物大分子离子价态的离子/离子反应装置,其结构示于图2。它主要由电喷雾离子源(ESI)、电荷中和槽、正交飞行时间质量分析器3部分组成。电荷中和槽内的α-粒子源(210Po)产生的单电荷离子与ESI离子源产生的生物大分子离子发生离子/离子反应,可以有效降低生物大分子离子的电荷价态,从而简化生物大分子的质谱图解析。通过改变α-粒子源的表面积可以调节α-粒子的流出量,或是通过改变气体流速来增加或减少生物大分子离子在电荷中和槽内的通过时间,据此调控离子/离子反应效率。由于飞行时间质谱仪具有较宽的检测范围,离子/离子反应的应用范围也得到了相应的拓宽[8]。

图1 Y型管式反应器结构示意图[6]Fig.1 Schematic diagram of the Y-shaped capillary reactor
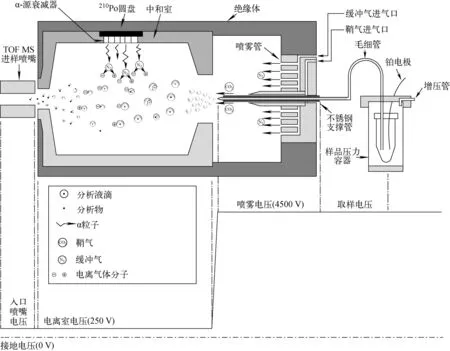
图2 降低生物大分子离子价态的离子/离子反应装置[7]Fig.2 Schematic diagram of the ion/ion reaction device used for charge reduction of biological macromolecule ions built
上述2种反应器的反应区域都是在高真空系统前的离子源附近,因此很难控制离子/离子反应的进度,而且四极杆质谱仪和飞行时间质谱仪不具备串联质谱功能,不能对反应产物做进一步分析。此后,开展的离子/离子反应研究主要集中于具有串联质谱功能的离子阱质谱仪[9]。离子阱属于动态质谱,与四极杆有很多相似之处,但离子阱不仅灵敏度较高,而且具有离子存储功能,可进行串联质谱分析,是研究气相离子/离子反应的理想选择。
2004年Hunt等[10]搭建了一套全新的基于线性离子阱的离子/离子反应装置:通过电喷雾离子源和化学电离源(CI)分别从前后端盖向离子阱内注入阳离子和阴离子;通过在线性离子阱两端盖上加一段射频电压,使线性离子阱可以同时存储不同极性的离子并完成反应,其反应步骤示意图示于图3。通过调节离子阱内三段杆的直流偏压值可灵活操控离子/离子反应完成一系列复杂的反应过程,包括离子注入、离子隔离、反应开始和反应终止等。该装置可以进行电子转移裂解反应(ETD),以及结合ETD与质子转移反应(PT)的多级串联质谱实验[11]。
美国McLuckey教授[12]通过对三重四极杆质谱仪进行改装,搭建了一种基于线性离子阱的气相离子/离子反应装置,其工作过程示于图4。当正离子进入仪器后,先在Q1筛选反应所需的离子并储存在Q2;在Q2两端加一段射频电压,这样Q2就被改装成线性离子阱来储存反应离子;随后经Q1筛选的负离子进入Q2发生离子/离子反应;最后反应产物被导入Q3进行质量分析。如果将Q3改为飞行时间检测器(TOF)就可以对反应产物进行高分辨分析,从而满足对生物大分子检测的要求[13]。
中国计量科学研究院与北京理工大学合作自主开发了一套可用于气相离子/离子反应的双极性质谱装置[14],其结构示于图5a。它由2套ESI离子源、2套离子光学系统、2组四极杆和1组线性离子阱组成。通过2套ESI离子源得到的正、负离子分别从两端注入中间的线性离子阱进行反应,利用2组四极杆的离子筛选功能选择性地传输正、负离子进入离子阱中反应。除交流电外,线性离子阱的2个弹射电极上还加了一段直流电压,电路图示于图5b。可见,正、负离子可分别从两个电极的狭缝弹出并被检测,实现了通过操控两种极性离子的分布控制和检测离子/离子反应的产物。

图3 在线性离子阱中进行离子/离子反应的步骤示意图[10]Fig.3 Schematic diagram of ion/ion reaction in a linear ion trap

图4 McLuckey实验室搭建的离子/离子反应装置结构图[12]Fig.4 Structure diagram of ion/ion reaction device built in McLuckey’s laboratory

注:a.装置结构图;b.线性离子阱的离子检测路径和电路连接关系图5 双极性质谱装置示意图[14]Fig.5 Schematic diagram of the dual-polarity MS apparatus[14]
3 气相离子/离子反应主要类型及应用
气相离子/离子反应可分为酸碱中和反应、氧化还原反应和共价键生成反应等3类。其中,酸碱中和反应可分为质子转移反应、金属离子转移反应和电荷倒置反应;而氧化还原反应常伴随着电子的转移,因此也称为电子转移反应。
3.1 质子转移反应
近年来,电喷雾离子化技术被广泛应用于蛋白和多肽等生物大分子的离子化,经电喷雾电离得到的蛋白质混合物离子往往带有多种电荷价态,如果直接进行质谱检测,效果并不理想。气相离子/离子的质子转移反应是一种去除多余电荷价态的有效手段,可以得到更加精确的结果。例如,Stephenson等[15]将pdA40~60阴离子与质子化苯并喹啉阳离子在离子阱中反应,得到了21个带单电荷的寡核苷酸阴离子。另一方面,一些多电荷蛋白离子的碰撞诱导解离(CID)碎裂离子也具有不同的电荷价态,通过质子转移反应可以简化离子电荷态。例如,Hogan等[16]将猪弹性蛋白酶离子的CID碎裂产物[M+19H]19+离子与全氟化碳阴离子反应,得到了单电荷猪弹性蛋白酶离子[M+H]+。
在离子阱中可以选取某一种电荷态离子,限制它的质子转移反应速度,而其他离子的反应不受影响,这样所选取的离子就像被“驻停”在离子阱中,而其他离子则继续进行质子转移反应,从而富集某一种电荷价态的离子,这一过程称之为“离子驻停”(ion parking)。这一技术有助于开展系列电荷价态的母离子的“自上而下”串联质谱研究[17]。
3.2 电子转移反应
1998年Zubarev等[18]发现多肽离子在捕获1个热电子后得到的碎裂离子与传统的CID所获得的离子不尽相同,这个过程被称为电子捕获裂解(ECD)。相比于CID,ECD可提供更丰富的序列信息,可优先断裂二硫键,也可以保护一些不稳定的翻译后修饰。2004年Coon等[10]发现了几种可以将电子转移给多肽阳离子的阴离子,并将这一过程称为电子转移裂解(ETD)。在此之后,ECD与ETD成为了碎裂多肽和蛋白质离子的重要手段,这种气相离子/离子反应已经被用于商业化仪器,为多肽、蛋白的多级质谱分析提供了新的裂解模式。作为传统CID的有效补充,ECD/ETD对糖肽类化合物裂解有着特殊的功效。使用CID时会破坏糖肽中的糖基部分,而ECD/ETD可以在保护糖基部分的情况下碎裂肽链,从而定位糖基化位点,为分析糖肽分子的结构提供了更好的碎裂方式[19]。
3.3 金属离子转移反应
在气相离子/离子反应中获得稳定产物是非常重要的,而金属离子转移反应是一种获得稳定产物的有效方式。金属离子转移反应是通过含金属(碱金属、碱土金属、过渡金属)复合物阴离子与多电荷多肽阳离子反应,使金属离子取代多肽阳离子上的质子,从而形成稳定产物[20],反应过程如下:
(M+Me+nH+2L)(n-1)+→
[M+Me+(n-2)H](n-1)++2HL
(3)
这里,M和Me分别代表待测物和金属离子,L代表单电荷配体阴离子。从式(3)可以看出,反应中既有金属离子转移到多肽阳离子中,也有质子转移到配体阴离子上,因此单电荷金属阳离子的转移伴随着两个质子转移。
研究含金属离子的生物分子有两个目的:一是了解金属离子在生物分子中的作用;二是将金属离子作为阳离子化游离基团用于串联质谱分析。含金属的多肽阳离子与质子化阳离子的质谱碎裂行为有明显区别,例如,通过多肽离子与AuCl4-阴离子反应,可将Au(Ⅰ)离子键入有二硫键的多肽阳离子,CID裂解后可以打开二硫键,而质子化的阳离子并没有这种特性[21]。
3.4 电荷倒置反应
上述3种反应都是降低多电荷分析物电荷态,而离子/离子反应也可用于单电荷分析物与多电荷反应物离子,导致分析物离子的电荷态转变,形成电荷倒置反应。例如,He等[22]利用电荷倒置反应提高单电荷离子的电荷价态,具体过程如下:先用去质子试剂(如羧基封端聚合物阴离子)将[M+H]+转换为[M-H]-,再用质子化试剂(如胺基封端聚合物阳离子)与[M-H]-反应,最终形成[M+2H]2+离子。
3.5 共价键生成反应
近年来,采用串联质谱技术对多肽进行结构表征的研究日渐增多,为了达到促进离子化、定量分析和结构分析等目的,通常需要将多肽分子在溶液中进行衍生化。离子/离子反应可以将气相离子与适当的有机离子反应生成共价键,达到对多肽进行结构表征的目的。相比传统的溶液衍生化法,气相反应具有更高的反应效率和选择性[2]。例如,Peng等[23]用酰亚胺与多肽羧基端反应生成酰胺键,从而延长多肽羧基端;Alice等[24]用高碘酸根阴离子氧化及裂解多肽离子内的二硫键来完成二硫键的定位。
4 气相离子/离子反应的最新研究进展
目前,气相离子/离子反应的研究主要集中在反应机理研究、仿真模拟计算和多肽蛋白阳离子与不同阴离子的共价键生成反应等方面。
荷兰Oomens等[25-26]发现多肽阳离子与荧蒽阴离子的ETD反应除了得到电荷价态降低的多肽阳离子外,还有中性的二氢荧蒽或氢分子以及中性荧蒽分子。通过红外光谱和理论计算发现,氢分子、中性荧蒽比二氢荧蒽更稳定,该研究首次揭示了不同结构阴离子反应物对反应结果的影响。
北京理工大学的徐伟等[27-31]通过GPU仿真模拟建立了气相离子/离子反应速度与反应离子的电子云密度和电荷价态的关系,发现提高离子反应速度,需要提高离子阱俘获电压、缓冲气压力,并得出不同极性的反应离子对,其质荷比越接近反应越容易进行的结论。该GPU仿真系统可实现百万级(106)离子相互作用的计算和仿真,离子轨迹仿真误差低于千分之一(100 ms内),仿真优化的线性离子阱具备单位分辨(FWHM)能力。
5 总结
质谱仪不仅是一种重要的分析仪器,同时也是研究化学反应的重要工具,在有机化学反应机理、多肽结构分析和气相离子化学等领域发挥着重要作用。气相离子/离子反应可以在质谱仪中高效快速地进行,通过转变分析离子的状态可以获得更多分析物的有效信息,也可以作为一种离子化技术把多电荷态离子解离成几种不同电荷态离子来得到目标离子更多的信息。可以预见,质谱中气相离子/离子反应将在化学、生物等领域发挥更大作用。
