考马斯亮蓝法测定归及乳膏中植物蛋白的含量*
2018-07-26陶平德常明泉郧西县人民医院药剂科湖北十堰44600湖北医药学院附属太和医院湖北十堰44000
潘 涛,陈 芳,陶平德,常明泉△(.郧西县人民医院药剂科,湖北 十堰44600;.湖北医药学院附属太和医院,湖北十堰44000)
归及乳膏是湖北医药学院附属太和医院与郧西县人民医院共同开发的中药软膏制剂,该乳膏以当归浸膏、白及溶胶为主药[1],加基质经乳化而成,具有清除皮肤自由基、软化角质、抗氧化、保湿润肤的功效,用于治疗皮肤皲裂[2-5]。前期作者以多糖为指标,对该乳膏的质量控制、体外释放度等内容进行过一些相关研究[6-8]。为了进一步明确其活性成分和药理作用,更好地控制归及乳膏质量,为开展后续研究奠定基础,作者采用考马斯亮蓝染色法对其中的植物蛋白含量进行测定。
1 材料与方法
1.1 材料
1.1.1 仪器 TU-1901型分光光度仪(北京普析通通用仪器有限责任公司),BCD-610W型冰箱(博西华家用电器有限公司,功率:1.07 kW),KM-410C型超声震荡仪(广州市科洁盟实验仪器有限公司,频率:40 kHZ),WGAUNI-10型超纯水器(北京普析通仪器有限责任公司,功率:300 W),FA-2004型电子分析天平(上海精密仪器有限公司,精度:0.000 1 g),MH-1000型电热套(北京科伟永兴仪器有限公司,功率:300 W),试管架(江苏新康医疗器械有限公司,规格:13 cm×50 cm),玻璃试管(10、20 mL)。
1.1.2 试药 归及乳膏(湖北医药学院附属太和医院生产,批号:20171712、20170723、20170809),牛血清蛋白标准品(中国食品药品检定研究院,批号:140619-201622,规格:23.5毫克/瓶),考马斯亮蓝G-250(成都艾科达化学试剂有限公司,批号:6401-58-1),无水乙醇(武汉市中天化工有限责任公司,批号:20161225),85%磷酸溶液(武汉市中天化工有限责任公司,批号:20161212),氯化钠(NaCl)(沈阳试剂厂,批号:2016010599,含量 95.00%~100.00%,基准试剂),纯化水(湖北医药学院附属太和医院生产)。
1.2 方法
1.2.1 溶液的制备 (1)0.15 mol/L Nacl溶液:精密称取0.438 7 g Nacl于50 mL容量瓶中,加纯化水溶解,定容,即得。(2)考马斯亮蓝溶液:精密称取考马斯亮蓝G-250 50 mg溶于25 mL乙醇中,加入85%磷酸溶液50 mL,混合,加纯化水稀释至 500 mL,即得。(3)标准蛋白溶液:精密称取牛血清蛋白标准品10 mg,置10 mL容量瓶中,加纯化水溶解,定容,即得1.0 mg/mL标准蛋白对照品储备液,置冰箱中低温保存(4℃),取该溶液0.2 mL于试管中,加0.15 mol/L Nacl溶液至2.0 mL,加入考马斯亮蓝溶液10.0 mL,混匀,在室温放置5 min,即得。(4)供试品溶液:精密称取归及乳膏0.25 g于烧杯中,加无水乙醇约20 mL,超声溶解,过滤至50 ml容量瓶中,用无水乙醇洗涤烧杯3次(每次约8 mL),集中滤液,用无水乙醇定容,取该溶液0.6 mL于试管中,加0.15 mol/L Nacl溶液至2.0 mL,加入考马斯亮蓝溶液10.0 mL,混匀,放置 5 min,即得。(5)空白溶液:精密吸取0.15 mol/L氯化钠溶液2 mL于试管中,加入考马斯亮蓝溶液10.0 mL混匀,在室温放置5 min,即得。
1.2.2 测定波长的选择 分别取“1.2.1”项下的标准蛋白溶液、供试品溶液和空白样品溶液,在分光光度仪上于500~700 nm波长处扫描,记录扫描图。
1.2.3 曲线方程的建立 分别精密吸取“1.2.1”项下浓度为 1.0 mg/mL 标准蛋白储备溶液 0.2、0.4、0.6、0.8、1.0 mL于10 mL试管中,每管加0.15 mol/L Nacl溶液至1.0 mL,混匀,各取0.1 mL于对应编号的新试管中,分别加入考马斯亮蓝溶液5.0 mL混匀,室温放置5 min,即得毎毫升含标准蛋白为 3.92、7.84、11.76、15.69、19.61µg的溶液,取各溶液分别在595 nm波长处测定吸收度,以浓度为横坐标(X),吸收度值为纵坐标(Y),绘制标准曲线。
1.2.4 精密度试验 取“1.2.1”项下的标准蛋白溶液,以相应试剂为空白,在595 nm波长处连续测定5次,记录吸光度值。
1.2.5 稳定性试验 取“1.2.1”项下的标准蛋白溶液在595 nm 波长处分别于0、1、3、6 h测定吸光度,记录吸光度值。
1.2.6 重复性试验 平行精密称取归及乳膏0.25 g于试管中,共5份,按“1.2.1”项下供试品溶液的方法制备样品溶液,以相应试剂为空白,在595 nm波长处测定吸光度,计算含量。
1.2.7 回收率试验 精密称取已测知含量的归及乳膏(批号:20170723)0.125 g共9份,毎3份为1组,分别按样品含量的80%、100%、120%加入标准蛋白溶液,按“1.2.1”项下供试品溶液制备方法制备溶液,以相应试剂为空白,在595 nm波长处测定吸光度,计算回收率。
1.2.8 含量测定 精密称取归及乳膏0.25 g(批号:20171712、20170723、20170809)于烧杯中,每个批号各3份,按“1.2.1”项下的方法制备供试品溶液,以相应试剂为空白,在分光光度仪上于595 nm处分别测定吸收度,计算含量。
2 结 果
2.1 测定波长的选择 标准蛋白溶液、供试品溶液均在595 nm处有最大吸收,空白样品溶液在此波长处无吸收,选择595 nm为测定波长,扫描图见图1。
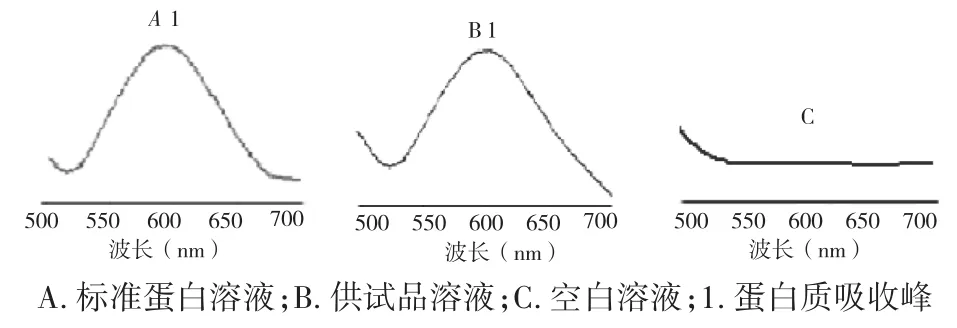
图1 紫外线扫描图
2.2 曲线方程的建立 得曲线方程为Y=0.036 0X−0.000 5,相关系数(r)=0.999 5,标准蛋白溶液在 3.92~19.61µg/mL范围内呈良好的线性关系。
2.3 精密度试验 相对标准偏差(RSD)为0.77%,表明仪器精密度良好。
2.4 稳定性试验RSD为1.89%,表明标准蛋白溶液在6 h内稳定。
2.5 重复性试验RSD为1.34%。
2.6 回收率试验 平均回收率为94.3%,RSD为1.91%。见表1。
2.7 含量测定 归及乳膏样品批号为20171712、20170723、20170809 的样品含量分别为 51.7、52.2、49.9 mg,RSD分别为 1.22%、1.47%、1.81%。
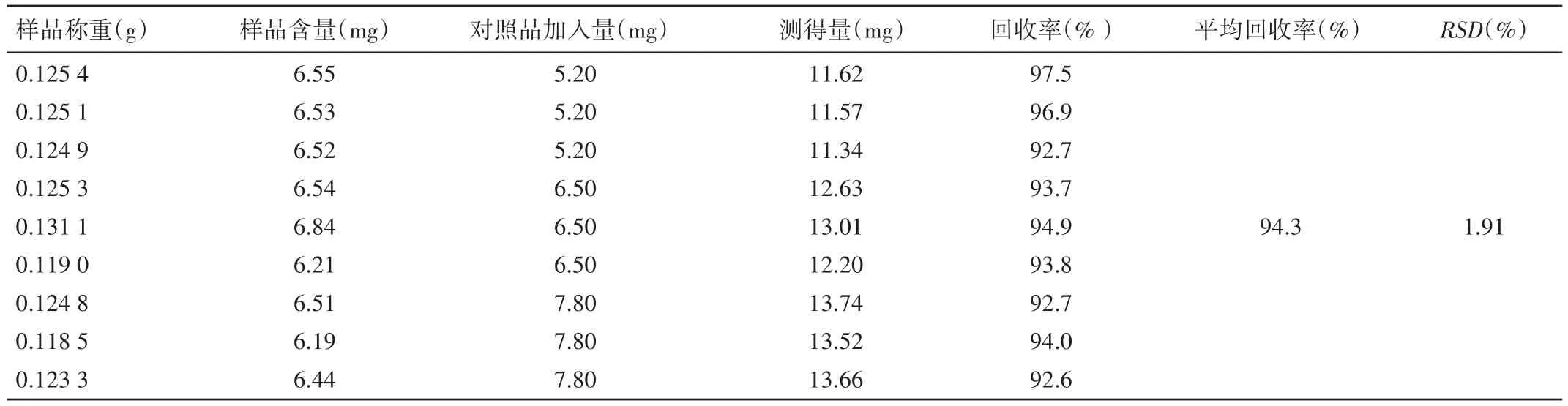
表1 归及乳膏中植物蛋白回收率试验(n=9)
3 讨 论
本研究中,考马斯亮蓝G-250在游离状态下呈红色,与蛋白质发生特异性结合后呈蓝色,在595 nm波长处有最大吸收值。在一定范围内,蛋白质与染色剂的结合量与测定波长的吸光度值成正比[8],因此采用考马斯亮蓝染色法测定归及乳膏中的植物蛋白含量。在制备供试品溶液时,曾使用纯化水、10%Nacl溶液、乙醇-氯仿(1∶1)混合液做乳膏的溶剂,超声处理,对液体分别应用离心、过滤等方法,但效果都不理想,而采用无水乙醇做溶剂,则溶解效果好、速度快,所制备的溶液澄清,检出效果良好。作者曾考虑到植物蛋白在酸、碱、丙酮、乙醇中会受到影响。是否因为植物蛋白表面有一层纤维膜,对氨基酸结构是否具有保护作用,后续将进行深入研究。
归及乳膏中的蛋白属于植物蛋白,成分比较复杂,不仅其含有多糖、植物蛋白,还含有植物色素等物质[9],植物色素可能也产生一定的光密度值,所以在配制样品时应使蛋白质浓度在0.1 mg/mL以内,必要时适当增加考马斯亮蓝染色液的用量,以保证与蛋白质染色反应完全,克服其他成分对蛋白质测定产生的影响[10]。酸碱对植物蛋白的测定会有一定影响,配制检测溶液时加入0.15 mol/L Nacl溶液稀释,可缓冲其影响。在测定试验前应把本研究所用器具用铬酸钾清洁液浸泡、用纯化水清洗干净,并避免使用石英吸收池,防止用具不洁对测定结果产生干扰,每次测定完毕用乙醇清洗比色皿,然后用纯化水清洗,以免考马斯亮蓝染色液在比色皿上存在残留。
