贝伐珠单抗联合化疗治疗转移性结直肠癌的疗效观察*
2018-07-23代怀杰许春蕾汤旭山姜雨唐勇
代怀杰,许春蕾,汤旭山,姜雨,唐勇
(830011乌鲁木齐 新疆医科大学附属医院肿瘤医院)
结直肠癌是我国常见的恶性肿瘤之一,其发病率男性为:16.9/10万,女性为:11.6/10万[1],位居恶性肿瘤发病率第3位,并显逐年上升趋势,且约有25%的大肠癌患者在初诊时就已经是晚期。尽管化疗方案的改进及分子靶向药物的联合应用,提高了患者的生存时间,但晚期结直肠癌的预后仍然很差,尤其是右半肠癌,且最新的回顾性研究结果提示不同位置的肠癌,其预后也存在差异。本文单中心回顾性分析2011年1月至2015年8月新疆医大肿瘤医院收治的晚期结直肠癌患者使用贝伐珠单抗的的近期、远期疗效、不良反应,进一步为贝伐珠单抗治疗转移性结直肠癌的临床治疗提供依据。
1 资料与方法
1.1 一般资料
收集2011年1月至2015年8月新疆医大肿瘤医院收治的晚期结直肠癌患者422例,根据研究目的将所有患者分为两组,其中观察组为81例,对照组为341例,两组患者一般资料无统计学差异(P>0.05),具有可比性,具体资料见表1。纳入标准:①入选对象首次就诊时均经过直肠指诊、盆腔CT或MRI扫描、纤维结肠镜检、活组织病理切片检查确诊并伴有远处器官转移;②研究对象均对化疗药物不过敏;③美国东部肿瘤协作组(ECOG)评分0~1分;④化疗均经患者同意并签知情同意书。排除标准:①使用贝伐珠单抗少于两个周期(3周方案)或少于三个周期(2周期方案);②治疗前合并严重的心、肺、脑血管疾病等。
1.2 治疗方法
观察组81例患者接受贝伐珠单抗联合化疗的治疗,对照组仅给予单纯化疗,两组化疗方案均以奥沙利铂(OXA)或伊立替康(CPT-11)联合氟尿嘧啶类化疗药物,其中观察组以奥沙利铂+卡培他滨(XELOX)化疗方案为41例,以奥沙利铂+亚叶酸钙+氟尿嘧啶(FOLFOX)化疗方案的为8例,以伊立替康+卡培他滨(XELIRI)化疗方案的为16例,以伊立替康+亚叶酸钙+氟尿嘧啶(FOLFIRI)化疗方案的为16例,对照组依次对应为156例、119例、33例、33例,以上所有方案剂量均为NCCN推荐剂量,其中XELOX方案中:奥沙利铂 130mg/m2,卡培他滨 1 000mg/m2bid d1~d14,q3w,FOLFOX方案中:奥沙利铂 85mg/m2+亚叶酸钙 200mg/m2+5-氟尿嘧啶400mg/m2d1+5-FU 2 400mg/m2微量泵静点46h,q2w,XELIRI方案中:伊立替康100mg/m2d1~d8/卡培他滨 1 000mg/m2bid d1~d14,q3w。FOLFIRI方案中:伊立替康180mg/m2+5-氟尿嘧啶(400mg/m2d1+5-FU 2 400mg/m2微量泵静点46h,q2w,贝伐珠单抗推荐剂量为:3周方案剂量为7.5mg/kg;2周方案剂量为5mg/kg。

表1 两组患者临床特征
1.3 疗效评价标准
按实体瘤疗效评价标准(RECIST1.1版)分为:完全缓解(CR):所有目标病灶消失,部分缓解(PR):基线病灶长径总和缩小≥30%,病情稳定(SD)基线病灶长径总和有缩小但未达到PR或者有增加但未达到PD,病情进展(PD)基线病灶长径总和增加≥20%或出现新病灶,客观缓解率(RR)%=CR+PR/总例数,临床获益率(CBR)%=(CR+PR+SD)/总例数。
1.4 患者随访
截止末次随访时间2017年3月31日,无进展生存时间(progression free survival,PFS)为患者确诊疾病至第一次进展时间,总生存时间(overall survival,OS)为患者确诊至死亡或末次随访时间。
1.5 统计学处理
相关数据结果用Spss20.0软件,两组间计量资料采用t检验;两组间计数资料的比较采用χ2检验,生存率的比较采用Kaplan-Meier法,P<0.05即表示差异具有统计学意义。
2 结 果
2.1 比较两组近期疗效
观察组中81例患者均采用贝伐珠单抗联合化疗,其中一线治疗(首次治疗时联合贝伐珠单抗)39例,二线治疗(一线治疗进展后再选择化疗联合贝伐珠单抗)42例,对照组341例均为一线治疗。观察组的客观缓解率为27.2%较对照组客观缓解率13.0%差异有统计学意义(P<0.01),观察组的总有效率82.7%较对照组57.2%差异有统计学意义(P<0.001)。详见表2~3。

表2 两组近期疗效
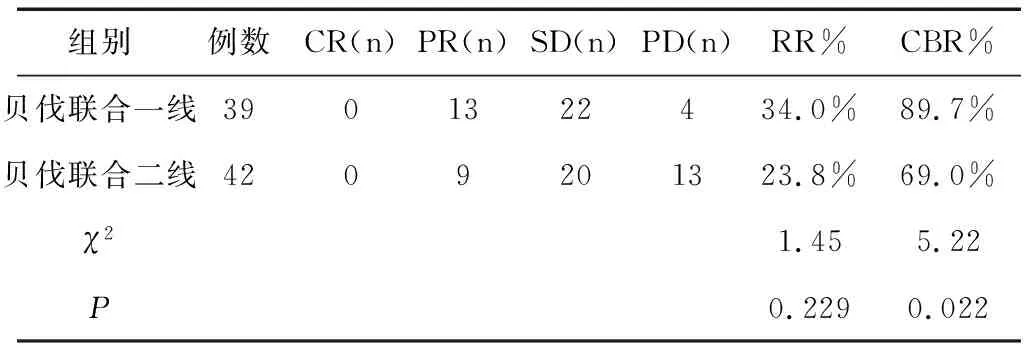
表3 贝伐联合一线、二线治疗的近期疗效

表4 两组不同部位肠癌的近期疗效
2.2 比较两组远期疗效
远期疗效包括PFS及OS,观察组与对照组中位PFS分别为8.5、4.9个月,差异具有统计学意义(χ2=59.3,P<0.001),两组中位OS分别为19.3、13.5月(χ2=26.5,P<0.001)。其中观察组中一线联合贝伐珠单抗与二线联合贝伐珠单抗的中位PFS分别为:10.3、6.8 个月(χ2=5.4,P=0.021),OS分别为23.1、16.2个月(χ2=13.8,P<0.001),贝伐珠单抗联合不同化疗方案(XELOX、FOLFOX、FOLFIRI、XELIRI)的中位OS分别为20.0、19.9、17.4、16.8个月(χ2=10.28,P=0.016),对照组分别对应中位OS为13.5、13.8、13.4、12.5个月(χ2=0.3,P=0.960)。观察组左半肠癌与右半肠癌的中位OS分别为20.8、15.0个月(χ2=9.6,P=0.002),对照组左半肠癌与右半肠癌的中位OS分别为14.9、11.8个月(χ2=25.9,P<0.001)。详见图1~4。
2.3 观察组不良反应。
本研究结果显示,观察组中化疗相关不良反应主要为骨髓抑制(白细胞减少、血小板较少)、消化道反应(恶性、呕吐)、神经系统毒性、手足综合征等,主要以0~Ⅱ级不良反应为主,Ⅲ~Ⅳ级相对较少,其中Ⅲ级毒性中,白细胞减少7例,血小板较少2例,手足综合征1例。贝伐珠单抗相关不良反应主要为高血压13例、蛋白尿8例、出血7例(表现为牙龈出血、鼻出血、月经量增多或延长)、皮疹5例等,其中高血压Ⅲ级毒性2例,经积极对症治疗后好转,详见表5。

图1a两组OS比较图1b两组PFS比较
图1观察组与对照组OS及PFS的比较

图2a OS比较图2b PFS比较
图2贝伐珠单抗联合一线、二线化疗的OS及PFS的比较

图3a观察组图3b对照组
图3观察组与对照组中不同肠癌位置的OS比较

图4a观察组图4b对照组
图4观察组与对照组不同化疗方案之间OS的比较

表5 贝伐珠单抗相关不良反应
注:以上化疗相关不良反应分级均根据WHO化疗毒副作用分级标准。
3 讨 论
随着人们生活水平的提高、饮食习惯的改变及环境因素影响等,结直肠癌的发病率显逐年上升趋势,新世纪以来,分子靶向药物的诞生引发抗癌理念的变革,为晚期结直肠癌(mCRC)提供了另一种新的有效治疗手段。贝伐珠单抗是一种抗血管内皮生长因子的单克隆抗体,它通过与VEGF 特异性性的结合,进而阻碍新生血管的形成[2-3],以达到延缓肿瘤生长的目的[4]。临床研究证实与常规化疗药物联用,可以明显改善这些患者的预后,目前,贝伐珠单抗已经被NCCN指南推荐为晚期结直肠癌一线用药。
在晚期结直肠癌患者的一线治疗中,贝伐珠单抗联合化疗用于晚期结直肠癌一线治疗可使患者生存获益。BRITE研究[5]、ARIES研究[6],以及BEAT研究[7]等均提示贝伐珠单抗用于一线治疗可以给患者带来生存获益,其中位 PFS在9.9至10.8个月之间,中位OS在 22.7至25.5个月之间。来至德国的一项多中心研究[8]也显示一线联合贝伐珠单抗,中位PFS达到10.6个月,中位OS在24.8至27.3个月之间。国内中山大学的一项回顾性分析[9]结果显示,一线联合贝伐珠单抗PFS 和OS 分别为10.6 个月和 24.2 个月,但不同化疗方案(以奥沙利铂为基础的化疗药物:FOLFOX、XELOX及以伊立替康为基础的化疗药:FOLFIRI、XELIRI)联合贝伐珠单抗之间的PFS和OS无明显差异。二线治疗上,E3200[10]、BE-BYP[11]研究显示疾病进展之后二线继续用贝伐珠单抗联合化疗仍然可以使患者获益。本研究中,贝伐珠单抗联合化疗其近期有效率、PFS及OS明显优于对单纯化疗,但观察组中PFS及OS分别为8.4个月和19.3个月,低于上述研究结果[5-9]。分析原因可能与入组时二线方案联合贝伐珠单抗的患者较多,并且二线方案化疗后的患者病情再次进展后,多数患者放弃治疗,或者因经济条件因素无法继续使用贝伐珠单抗而放弃治疗,导致中位OS较低,另外截止到末次随访时间,观察组中尚有10人生存,观察组一线治疗的PFS及OS分别为10.3个月和23.1个月,与上述结果类似,其中观察组中一线与二线的临床获益率为89.7%和69.0%,二线的PFS及OS高于对照组,患者一线进展后二线使用贝伐珠单抗仍然可以使患者获益,与上诉研究[10-11]结果一致,对于化疗方案之间,对照组无论何种化疗方案(XELOX、FOLFOX、FOLFIRI、XELIRI)之间的OS无明显差异,而观察组之间出现差异,观察组中奥沙利铂联合卡培他滨的方案中位OS达到20.0个月,分析研究数据提示观察组中一线使用XELOX方案的患者占半数以上,提示一线贝伐珠单抗联合XELOX方案化疗优于其他方案。
近年的一些研究逐渐显现出左右半结肠癌在生存方面的差异:左半结肠癌相对于右半结肠癌来说平均生存时间更长。Price等[12]的研究结果显晚期左半结肠癌预后优于右半结肠癌,左半肠癌的中位OS为20.3个月,右半肠癌中位OS为 9.6月(P<0.001);接受积极治疗(包括化疗及转移灶切除)的晚期结肠癌患者中,左半结肠癌的中位OS为29.4个月,右半结肠癌的中位OS为18.2个月;多因素回归分析显示原发肿瘤部位是独立的预后影响因素,原发于右半结肠的肿瘤预后比左侧大肠癌更差。同时研究也发现晚期左半结肠癌和直肠癌的预后相似,研究结果支持将直肠癌归为左半结肠癌的范畴。Boise等[13]、NCT00212615报道显示晚期直肠癌患者应用XELOX联合贝伐单抗的患者中,结果显示转移性结直肠癌患者接受一线XELOX方案联合贝伐珠单抗治疗,左半结肠癌中位PFS及中位OS均优于右半结肠癌。2016年ASCO年会上,CALGB/SWOG80405[14]研究分析显示左侧肿瘤和右侧肿瘤在中位OS分别为33.3个月和19.4个月。2016年ESM0大会上,CRYSTAL和FIRE-3[15]研究显示,对RAS野生型转移性结直肠癌患者肿瘤位置和预后、疗效预测的关系进行分析,研究结果显示,肿瘤位于结肠左侧的晚期肠癌患者,无进展生存,总生存和客观缓解率均显著优于右侧肠癌患者。国内的一些研究结果[16]也显示,结直肠癌单纯一线化疗中,回盲部组、升结肠+结肠肝曲组、横结肠+结肠脾曲组、降结肠+乙状结肠组、直肠组的有效率分别为21.3%、35.6%、14.3%、41.3%和32.6%,可见回盲部组和横结肠+结肠脾曲组的一线有效率最低,而降结肠+乙状结肠组有效率最高(P=0.028)。
大肠癌是两种不同疾病的概念是芬兰学者 Bufill等[17]首次提出的,由于大肠癌成瘤的分子生物学机制不同及胚胎起源不同,大肠癌应以结肠脾曲为界分为右半结肠癌与左半结肠癌。此后关于左、右半结肠癌的表观遗传学及肿瘤学生存结果的比较研究逐渐兴起,最新的研究结果[18]显示结肠癌发病部位可能是化疗方案选择的重要因素之一。然而,目前关于左右半结直肠癌位置关系的研究数据大多来自于非随机的的回顾性研究,因此左右半结肠癌位置差异在疾病发生、发展、诊治以及预后中的地位仍有待进一步深入研究。本研究中对照组中左、右半肠癌的临床获益率无统计学差异(P=0.13),而观察组中左半肠癌与右半肠癌的临床获益率有统计学差异(P=0.04),提示患者使用贝伐珠单抗后左半肠癌的近期疗效更优,两组左半肠癌患者的PFS及OS均优于右半肠癌患者,其中观察组中的左半肠癌与右半肠癌的OS为20.8和15.0个月,对照组中左半肠癌与右半肠癌OS分别为14.9和11.8个月,均显示无论何种化疗方案,左半肠癌患者有更长的生存获益。
贝伐珠单抗有关的常见副反应有蛋白尿、出血、高血压,严重副作用包括胃肠道穿孔、切口愈合异常、肾病综合征以及充血性心力衰竭等[19]。观察组出现的有关贝伐珠单抗的不良反应有高血压、蛋白尿及出血,但大多为1~2级,经积极对症处理后不影响后续治疗,患者总体耐受性好。
本文为回顾性研究,仍有很多不足之处,入组前病人基数不均衡,主要与患者就诊时的病情及患者可接受的治疗方案相关,入组对象主要是晚期结直肠癌的患者,贝伐珠单抗价格昂贵,并非每位晚期结直肠癌患者都能承受,而随着新的医改政策的实施,贝伐珠单抗纳入医保范围,将会使得更多的晚期结直肠癌患者获益,另外由于入组基线不平衡,即使对入组病人按入排标准纳入、转移病灶及原发病灶是否切除(包括转化治疗后手术切除的病人)等仍然可能影响患者的预后,由于观察组总体病例数较少,且多数为原始病灶或转移病灶不可切除的病人,致使转化治疗成果的病人较少,目前仍需进一步搜集相关数据。
综上所述,贝伐珠单抗联合化疗治疗晚期结直肠癌能提高患者的近期疗效,并使患者获得更长的生存时间,而转移后尽早使用、足疗程治疗是延长患者总生存的保障,而贝伐珠单抗联合何种化疗方案治疗不同部位肠癌的疗效更优,仍需进一步探讨。另外,随着左右半肠癌分子生物学机制的阐明,更新了结直肠癌的诊治理念,为结直肠肿瘤患者的“个体化”精准医疗提供进一步的支持。
作者声明:本文第一作者对于研究和撰写的论文出现的不端行为承担相应责任;
利益冲突:本文全部作者均认同文章无相关利益冲突;
学术不端:本文在初审、返修及出版前均通过中国知网(CNKI)科技期刊学术不端文献检测系统学术不端检测;
同行评议:经同行专家双盲外审,达到刊发要求。
