33例何首乌及其相关制剂致药物性肝损伤临床分析
2018-07-06王海珍李秀惠
王海珍 李秀惠
首都医科大学附属北京佑安医院肝病科 (北京, 100069)
何首乌亦曰马肝石[1]。近年来对何首乌肝毒性的报道呈上升趋势,动物实验也进一步证明何首乌中蒽醌类物质大黄素的药理毒性[2~4]。本研究回顾性分析2016年1月至2016年12月首都医科大学附属北京佑安医院收治的33例何首乌及其相关制剂致药物性肝损伤(DILI)患者的临床资料,探讨其临床特点,以期指导何首乌及其相关制剂的临床应用。
1 资料与方法
1.1 病例来源 2016年1月至2016年12月在我院住院诊断为DILI且发病前存在何首乌及其相关制剂应用史的33例患者。男13例,女20例;年龄17~86岁,平均(45.3±17.6)岁;应用何首乌单品6例,复方制剂及中成药27例;病程为急性25例,慢性8例。
1.2 诊断标准 采用中华中医药学会发布的《中草药相关肝损伤临床诊疗指南》[5~7]。具体诊断为:①肝功能异常前有中草药及其相关制剂应用史,生化指标:ALT≥5×ULN(正常值上限);或者ALP≥2×ULN;或者ALT≥3×ULN且TBiL≥2×ULN;②排除其他导致肝损伤的原因:病毒性、酒精、免疫、遗传代谢、胆管、血管等;③RUCAM评分[8]≥3分;④排除联合应用中明确肝毒性或相互作用引发药物肝毒性的西药;⑤能够获得并核实导致肝损伤的中草药及其相关制剂资料;⑥能够鉴定中草药基原,排除中草药混伪品以及有害物质污染;⑦检测出体内中草药特征代谢物;⑧发生中草药及其相关制剂再激发事件;⑨检测出中草药肝损伤的体内特异性生物标志物。疑似诊断:①+②+③;临床诊断:疑似诊断 +④+⑤(或⑥或⑦);确定诊断:疑似诊断+⑧,或者临床诊断+⑨。
1.3 纳入及排除标准 纳入标准:诊断为DILI的患者且发病前存在何首乌及其制剂应用史。排除标准:排除存在其他肝损伤相关性疾病的患者,如病毒性、酒精性、免疫性、胆管性等原因。
1.4 临床分型及评分标准 采用医学科学国际组织委员会药物性肝损伤的分型标准[9,10]。①肝细胞型:ALT>2ULN或ALT/ALP(R)≥5;②胆汁瘀积型:ALP>2ULN或R≤2;③混合型:ALT和ALP均>2ULN,R介于2~5之间。急性肝损伤:酶活性升高不超过6个月。慢性肝损伤:酶活性升高>6个月或再次出现肝损伤。RUCAM评分标准:①极可能相关:>8分;②很可能相关:6~8分;③可能相关:3~5分;④可能不相关:1~2分;⑤无关:≤0分。
1.5 研究方法 采用回顾性研究方法,收集患者性别、年龄、过敏史、既往史、用药史、临床症状、生化指标、肝组织病理表现及转归等临床资料,并对其进行肝细胞分型及RUCAM评分。
1.6 预后判断[11]①治愈:临床诊断及体征完全消失,血清生化指标恢复正常;②好转:症状及体征明显好转,血清生化指标<2ULN;③未愈:临床症状及体征无改善,血清生化学指标改善不明显或病情加重;④死亡。
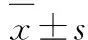
2 结果
2.1 分级诊断及治疗结果 应用中草药损伤相关指南的分级诊断结果:疑似诊断9例,临床诊断20例,明确诊断3例。治愈9例(27.27%),好转19例(57.28%),无效3例(9.09%),加重1例(3.03%),死亡1例(3.03%)。
2.2 主要基础疾病及用药史 27例(81.82%)患者发病前用药原因均为治疗其主要基础疾病,其中治疗脱发、白发9例(27.27%),心血管疾病及高血压各4例(12.12%),皮肤病、高脂血症、失眠、甲状腺功能异常、消化系统疾病各2例(6.06%),无基础病的患者6例(18.18%)。可追溯中成药及保健品药品名:治疗脱发白发的精乌胶囊、养血生发胶囊;治疗心血管疾病的心元胶囊、稳心胶囊、心荣胶囊;治疗高血压的天麻钩藤颗粒;治疗皮肤病的润燥止痒胶囊;治疗失眠的复方苁蓉益智颗粒、安神补脑液、百乐眠;治疗高血脂的降脂灵分散片及保健用药鸿茅药酒、三棵草等。 应用中药复方饮片的病例均无法收集到原中药配伍方。
2.3 临床症状 33例患者中多以出现黄疸相关症状前来就诊,以小便黄27例(81.82%),巩膜黄染21例(63.64%),厌油20例(60.61%),乏力17例(51.52%),恶心呕吐14例(42.42%),皮肤黄染例10例(30.30%),纳差9例(27.27%),腹胀腹痛8例(24.24%),皮肤瘙痒及皮疹7例(21.21%),灰白便3例(9.09%)。
2.4 生化指标及病理检测情况 33例患者肝功能不同程度升高,其中TBil升高27例(81.82%),Alb降低8例(24.24%),INR升高5例(15.15%)。对生化指标统计分析得出:ALT(905.81±841.89)U/L、AST(662.03±517.27)U/L、ALP(162.76±85.46)U/L、 GGT(195.92±159.27)U/L、TBil(164.62±145.33)umol/L、Alb(37.71±5.67)g/L,INR(1.1973±0.38)。33例患者有10例行肝组织活检术,均可见汇管区不同程度扩大及大量炎细胞浸润;病理结果:轻度小叶性肝炎1例(10.0%),轻~中度小叶性肝炎4例(40.0%),中度小叶性肝炎5例(50.0%)。
2.5 影响因素分析 见表1。
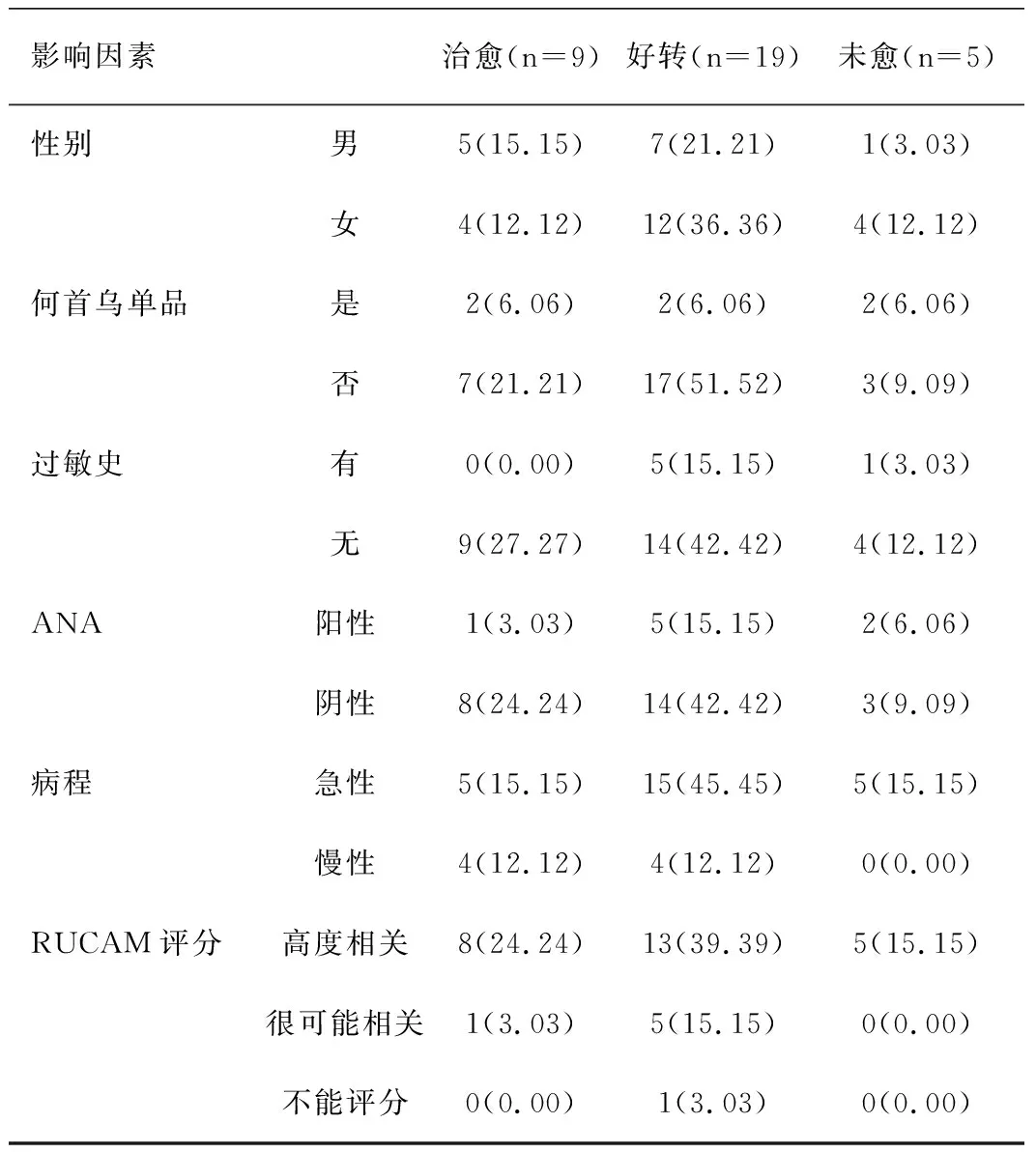
表1 影响因素与治疗结果的相关性 [n(%)]
2.6 相关生化指标与预后的相关性 见表2。
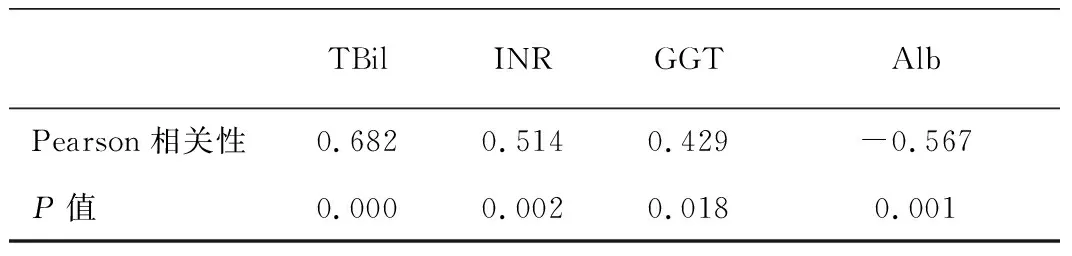
表2 生化指标与预后的相关性分析
3讨论
笔者发现何首乌及相关制剂的使用原因多以生发乌发、心血管疾病、皮肤病为主。何首乌单品与复方制剂对肝损伤后的转归没有明显差异,在研究中由于具体用药信息缺失,药物用法剂量不够完善,不排除其转归与药物用量及配伍相关。其次,大多数中成药成分复杂,加上伪劣药品的监管不严,使中药致肝损伤的风险居高不下。另外,对于很多添加中药的保健品[12],其安全性容易被大众忽视。这些无疑是DILI病例数量攀升的原因。
本研究的病例多为急性发作,以黄疸表现为主要就诊原因,肝损伤严重程度较明显,33例病例RUCAM评分均大于6分,表明何首乌相关DILI易被诊断;同文献相比,本研究中患者ALT、ALP、TBil的均值相对较高,TBil、INR、GGT、Alb与转归预后显著相关。有实验研究也提出:何首乌致肝损伤相关生化指标主要有血清 ALT、GGT及 CHE、TP、IgG[13、14]。
除外生化指标,也有研究推论何首乌肝毒性可能与特异体质显著相关[15]。因此,不除外何首乌较其他药物致肝损伤作用机理的严重性及特异性,还需要进一步研究支持。病理方面,既往有文献报道DILI的病理与自身免疫性肝病(AIH)不易区别,特别是高滴度的ANA阳性的病例,早期不易与AIH区分,部分DILI患者可出现自身免疫现象[16,17],本研究中病理结果主要表现为炎细胞浸润后导致的轻、中度肝炎表现,病理诊断明确,而本研究中有2例ANA阳性患者出现病情加重,占总ANA阳性患者的25%,占总未愈患者的40%,因此本研究不除外其预后与特异质体质的相关性。另外,DILI发病机制的研究分为药物对肝脏的直接打击及引起免疫介导失衡,免疫耐受打破、单克隆抗体所致免疫介导性疾病[18,19]是药物所致DILI重要肝损伤途径,为其损伤的特异体质的相关性提供证据。
何首乌具有双重性成分,降脂保肝是何首乌主要的药理作用,二苯乙烯苷为保肝降脂主要活性成分;蒽醌类成分为何首乌中具有毒性的成分[20]。因此,对何首乌的认识不能仅局限其肝毒性,在临床应用中需要将其药理作用及不良反应综合考虑,在减少药理毒性的同时发挥其最大的治疗效应。
[1] 李时珍.本草纲目[M].北京华文出版社,2009:158.
[2] 张斌,丁慎华,钱雪梅,等. 大剂量大黄素致大鼠肝损伤及其机制的初步研究[J]. 中国现代医学杂志,2015,25(1):18-21.
[3] 方红玫, 朱廷焱. 何首乌有效成分、毒性作用和相关研究进展[J]. 国 际药学研究杂志, 2010, 37(4): 283-286.
[4] 陶明宝,张乐,刘飞,等. 含蒽醌类成分中药的安全性研究进展[J]. 中药药理与临床,2016,32(6):238-243.
[5] 肖小河,李秀惠,朱云,等. 中草药相关肝损伤临床诊疗指南[J]. 中国中药杂志,2016,62(7):1165-1172.
[6] 朱云,王睿林,孙雪英,等. 《中草药相关肝损伤临床诊疗指南》指导临床诊断的回顾性分析[J]. 临床肝胆病杂志,2016,32(11):2159-2162.
[7] 何婷婷,宫嫚,白云峰,等. 2种药物性肝损伤诊断指南的应用分析[J]. 中国中药杂志,2016,62(16):3096-3099.
[8] Danan G,Benichou C .Causality assessment of adverse reactions to drugs: I. A novel method based on the conclusions of international consensus meetings: apphcation to drug-induced liver injuries[J]. Journal of Clinical Epidemiology , 1993,46(11):1323-1330.
[9] Benichou C. Criteria of drug-induced liver disorders Report of an international consensus meeting[J]. Journal of Hepatology , 1990,11(2):272-276。
[10] 陈成伟. 药物性肝损害诊断标准的评价[J]. 诊断学理论与实践,2009,8(27):121-124.
[11] 朱斌,章福彬,刘卫援,等. 药物性肝损害 88 例临床分析[J].实用肝脏病杂志,2008,11(6):396-397.
[12] ERNST E. Adulteration of Chinese herbal medicines with syn-thetic drugs: a systematic review[J]. J Intern Med,2002,52 (2) : 107 -113.
[13] 胡锡琴,李娅琳,王磊. 何首乌中鞣质对大鼠肝脏生化指标的影响[J].药物评价研究,2010,33(1):63-65.
[14] 胡锡琴,李敏,杨红莲,等. 何首乌中鞣质与二苯乙烯苷不同配比对大鼠肝功能指标的影响[J].上海中医药杂志,2011,45(4):56-59.
[15] 朱云,刘树红,王伽伯,等. 何首乌及其制剂导致药物性肝损伤的临床分析[J]. 中国中西医结合杂志,2015,35(12):1442-1447.
[16] 华静,徐芸,保洁,等. 加强对药物性肝损伤中自身抗体滴度的认识[J]. 世界华人消化杂志,2016,24(32):4404-4408.
[17] 姚云洁,刘鸿凌,朱冰,等. 441例药物性肝损伤患者临床和肝组织病理学特征分析[J]. 实用肝脏病杂志,2015,20(3):286-289.
[18] 陈鹰翔,常铠麟,赵思伟,等. 中药导致药物性肝损伤的作用机制的研究进展[J]. 黑龙江科技信息,2013,17(2):31-32.
[19] 赖荣陶,陈军,郭晓燕. 免疫介导的药物性肝损伤[J]. 肝脏,2016,18(5):396-397.
[20] 楼招欢,吕圭源,俞静静. 何首乌成分、药理及毒副作用相关的研究进展[J]. 浙江中医药大学学报,2014,38(4):495-500.
