仔猪大肠杆菌病、C型产气荚膜梭菌病二联灭活疫苗的研制与应用
2018-07-04刘泽文袁芳艳周丹娜段正赢杨克礼田永祥
刘泽文,袁芳艳,刘 威,周丹娜,段正赢,郭 锐,杨克礼,田永祥*,阮 征
(1.农业部畜禽细菌病防治制剂创制重点实验室/湖北省农业科学院畜牧兽医研究所,湖北武汉 430064;2.武汉市动物疫病预防控制中心,湖北武汉 430016)
仔猪大肠杆菌病(仔猪黄痢)和仔猪C型产气荚膜梭菌病(仔猪红痢)是新生仔猪最常见的两种肠道传染性疾病。仔猪黄痢是由某些血清型的大肠埃希菌引起,仔猪红痢是由C型产气荚膜梭菌引起的。仔猪红痢和仔猪黄痢在流行病学上具有很多共同特点,它们均属于肠道菌,发生于出生后1周内的新生仔猪,发病率和死亡率极高,而且发病急、死亡快,发病后药物治疗效果不佳,注射疫苗是预防和控制两种疾病发生的有效手段[1]。
本研究将大肠埃希菌C83549(K88)、C83644(K99)、C83710(987P)菌株和C型产气荚膜梭菌C59-2菌株分别接种适宜培养基,通过提取大肠埃希菌纤毛和C型产气荚膜梭菌外毒素,灭活和脱毒后加入冻干保护剂,冷冻干燥制成冻干灭活疫苗。经安全和效力试验表明,该疫苗对怀孕母猪具有良好的安全性,同时可以提高免疫母猪所产仔猪对仔猪大肠埃希菌和C型产气荚膜梭菌抵抗力,具有良好的免疫效果。
1 材料与方法
1.1 材料
1.1.1 制造与检验菌种 大肠埃希菌为C83549、C83644、C83710菌株,C型产气荚膜梭菌为C59-2株,均由中国兽医药品监察所鉴定、保管和供应。
1.1.2 主要培养基及血清 改良Minca汤培养基:取改良Minca汤粉15.4 g,另取甘油5 mL,加热溶解于1 000 mL超纯水中,调pH至7.2~7.4,115℃灭菌30 min。梭菌培养基:主要成分为大豆蛋白胨、水解酪蛋白、酵母浸膏和葡萄糖等。将各成分充分溶解于蒸馏水后,调节pH至8.5左右,115℃灭菌30 min。因子血清:大肠埃希菌K88、K99、987P因子血清,由中国兽医药品监察所提供。
1.2 方法
1.2.1 大肠埃希菌纤毛抗原的制备 分别按培养基总量的1%~3%接种大肠埃希菌C83549、C83644、C83710菌株种子液,温度为36℃~37℃培养6 h~9 h,取样纯检合格,同时纤毛因子血清平板凝集反应达“++++”即收获。按文献[2]提取大肠埃希菌的纤毛抗原。取样用反向间接血凝方法(RIHA)测定上清液中纤毛抗原效价,当K88、K99、987P纤毛抗原RIHA效价达1∶5 000以上时可以用于制苗。
1.2.2 C型产气荚膜梭菌毒素抗原的制备 按培养基总量的1%~5%接种C型产气荚膜梭菌种子液,35℃~37℃静置培养6 h~10 h,培养完成后取样,离心,测定上清毒素的含量,毒力应达到500小鼠致死剂量(MLD)/mL。按文献[3]进行灭活和脱毒。脱毒完成后,用脱毒后的抗原原液,尾静脉注射16 g~20 g小鼠2只,每只0.4 mL,观察24 h,小鼠全部健活后采用超滤方法对毒素抗原进行适当倍数的浓缩后用于配苗。
1.2.3 疫苗的制备 按每头份疫苗含一定含量的K88、K99、987P抗原和C型产气荚膜梭菌灭活毒素抗原混合,然后加入明胶蔗糖保护剂,充分搅拌混匀后,定量分装,冷冻真空干燥制备成二联冻干灭活疫苗。按此方法连续制备3批疫苗,批号分别为201101、201102和201103。
1.2.4 疫苗的性状检验 将3批疫苗随机取样,进行外观检验,观察疫苗颜色状态及加入疫苗稀释液后的溶解情况。
1.2.5 疫苗的无菌检验 将3批疫苗随机取样,按现行《中国兽药典》附录进行。
1.2.6 疫苗的安全试验
1.2.6.1 小鼠安全试验 每批疫苗随机抽取3瓶,用20%的铝胶生理盐水稀释成2 mL/头份,混合后,各皮下注射16 g~20 g小鼠5只,每只0.5 mL(含0.25头份)。连续观察7 d,统计小鼠的健活情况。
1.2.6.2 仔猪安全试验 按疫苗标签注明头份,用20%的铝胶生理盐水稀释成2 mL/头份。用21日龄~28日龄健康仔猪(大肠埃希菌K88、K99、987P纤毛抗体血凝效价不高于1∶16;C型产气荚膜梭菌毒素中和抗体阴性)5头,各肌肉注射疫苗4 mL,连续观察14日,记录试验猪临床反应状况。
1.2.6.3 怀孕母猪安全试验 按疫苗标签注明头份,用20%的铝胶生理盐水稀释成2 mL/头份。每批疫苗接种怀孕母猪5头,于产前40 d~45 d和15 d~20 d各免疫1次,每次每头肌肉注射疫苗2 mL,并设未接种对照母猪5头。每日观察猪的精神、食欲及有无流产状况等,连续观察至分娩时,记录母猪的不良反应及产仔情况。
1.2.7 疫苗的效力试验
1.2.7.1 疫苗大肠埃希菌纤毛抗原效价测定 用稀释液(含1.0 g/L BSA的PBS(0.01 mol/L,pH7.2))将疫苗稀释成2 mL/头份,用反向间接血凝试验[4]测定每头份疫苗中各纤毛抗原的含量。计算各纤毛抗原RP值(待检疫苗纤毛抗原RIHA单位/参照品纤毛抗原RIHA单位),当RP值≥1.0,疫苗大肠埃希菌纤毛抗原检验合格。
1.2.7.2 疫苗免疫家兔血清中和试验 用20%的铝胶生理盐水将疫苗稀释成2 mL/头份,然后再稀释2.5倍后,肌肉注射1.5 kg~2.0 kg的家兔5只,每只1 mL,免疫后21日采血并分离血清。将5只家兔的血清等量混合,取混合血清1 mL与等体积的C型产气荚膜梭菌毒素混合,置37℃水浴中和作用40 min后,静脉注射体重16 g~20 g昆明小鼠2只,每只0.2 mL;同时用同批小鼠2只,静脉注射1个小鼠MLD的C型产气荚膜梭菌毒素作为对照组。观察24 h,判定结果。如果对照小鼠应全部死亡,血清中和小鼠应全部健活,则判定疫苗梭菌部分检验合格。
1.2.7.3 疫苗免疫本动物的攻毒试验 分别用连续3批疫苗2次免疫怀孕母猪,同时设立不免疫对照组。母猪分娩后,对免疫组和对照组母猪所产并采食初乳18 h~24 h的仔猪分组后攻毒,分别口服发病剂量的大肠埃希菌C83549、C83644、C83710菌液和静脉注射1个致死剂量的C型产气荚膜梭菌毒素,另设不免疫对照组母猪所产仔猪为正常对照,攻毒后连续观察14 d,统计各试验组仔猪的发病和保护情况。
1.2.8 疫苗临床应用试验 将中间试生产的二联疫苗在6个仔猪黄痢和仔猪红痢发病较严重的猪场进行临床应用试验,共计免疫怀孕母猪600头,另300头母猪不免疫作为对照。经对免疫组和对照组10日龄仔猪进行统计,比较免疫组和对照组的窝平产仔数,确定疫苗的免疫效果。
2 结果
2.1 性状检验及无菌检验结果
3批疫苗均为类白色海绵状疏松团块,易与瓶壁脱落,加疫苗稀释液后迅速溶解;随机抽取5瓶进行无菌检验,结果均无菌生长。
2.2 疫苗安全试验结果
2.2.1 疫苗对小鼠安全试验结果 每批疫苗注射16 g~20 g小鼠5只,每只0.5 mL(含0.25头份),连续观察7 d,小鼠全部健活。
2.2.2 疫苗对断奶仔猪安全试验结果 每批疫苗注射仔猪4头,每头4 mL(含2头份),连续观察14 d,仔猪精神良好及食欲正常,注射部位无肿胀及局部炎症,疫苗对仔猪安全性良好。故3批疫苗均具有很好的安全性。
2.2.3 疫苗对怀孕母猪安全试验结果 每批疫苗2次接种怀孕母猪5头,接种后每天观察至分娩结束,母猪体温、精神和食欲正常,未发生流产状况;母猪产仔无弱仔、死胎,产仔数与对照母猪比较无明显差异。
2.3 效力检验结果
2.3.1 疫苗大肠埃希菌纤毛抗原效价测定结果 大肠埃希菌部分采用反向间接血凝试验测定每头份疫苗中各纤毛抗原的含量,与参照疫苗相比,均满足RP值≥1.0(表1)。
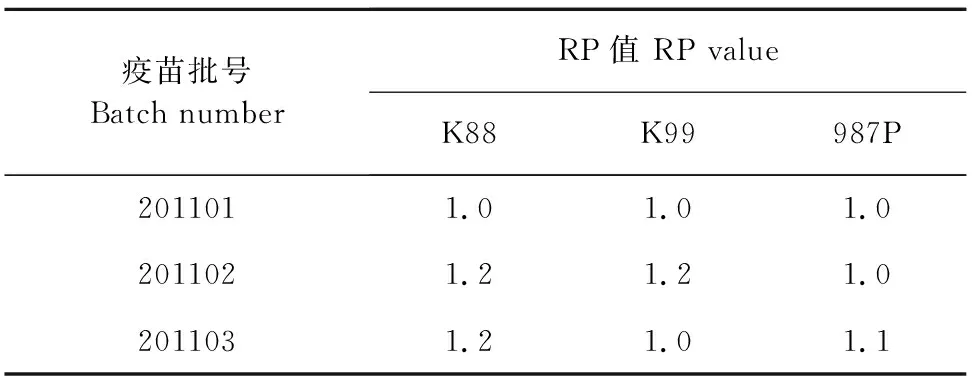
表1 疫苗大肠埃希菌纤毛抗原测定结果
2.3.2 疫苗免疫家兔血清中和试验结果 疫苗免疫家兔后采血、分离血清,用小鼠进行血清中和试验,结果对照小鼠全部死亡,血清中和小鼠全部健活,结果判为合格(表2)。

表2 疫苗梭菌部分效力检验结果
2.3.3 疫苗免疫本动物的攻毒试验结果
2.3.3.1 哺乳仔猪大肠埃希菌攻毒试验结果 分别用发病剂量的大肠埃希菌C83549、C83644、C83710对免疫组和对照组母猪所产并采食初乳18 h~24 h仔猪攻毒。大肠埃希菌攻毒对照组发病猪症状出现在攻毒后第2天~第3天,主要症状为拉黄褐色稀粪,精神沉郁,部分仔猪因脱水严重导致死亡,试验结果显示,201101批疫苗免疫组所产仔猪对大肠埃希菌C83549、C83644、C83710攻毒后的保护率分别为80%、100%和100%;201102批疫苗免疫组所产仔猪对大肠埃希菌C83549、C83644、C83710攻毒后的保护率分别为100%、80%和100%;201103批疫苗免疫组所产仔猪对大肠埃希菌C83549、C83644、C83710攻毒后的保护率分别为100%、100%和100%;对照组仔猪经大肠埃希菌C83549、C83644、C83710攻毒后的发病率均为100%(表3)。
2.3.3.2 哺乳仔猪C型产气荚膜梭菌攻毒试验结果 用仔猪最小致死剂量的C型产气荚膜梭菌C59-2毒素对免疫组和对照组母猪所产并采食初乳16 h~24 h仔猪攻毒。攻毒组死亡猪大多发生在攻毒后24 h内,表现为发病急,快速死亡。试验结果显示,201101、201102和201103批疫苗免疫组所产仔猪C型产气荚膜梭菌C59-2毒素攻毒后的保护率均为100%;对照组经C型产气荚膜梭菌C59-2毒素攻毒后全部死亡(5/5)(表4)。
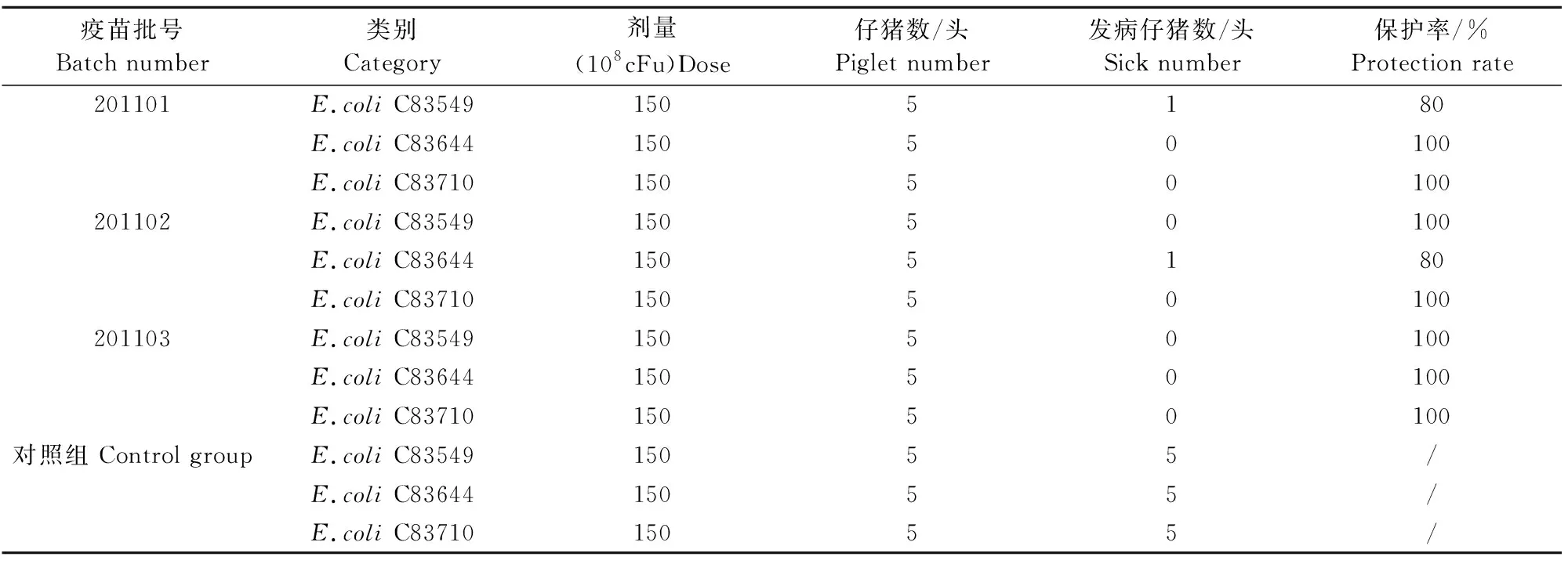
表3 免疫仔猪大肠埃希菌攻毒试验结果
2.4 二联疫苗临床应用结果
经对免疫组和对照组10日龄仔猪进行统计,免疫组母猪窝平成活仔猪数为9.47头,对照组母猪窝平成活仔猪数为7.94头,窝平仔猪成活数增加了1.53头(表5)。
3 讨论
仔猪大肠杆菌病和产气荚膜梭菌病是仔猪的两种常见腹泻病。仔猪大肠杆菌病是由某些血清型(如K88、K99和987P等)的大肠埃希菌引起,该菌主要通过纤毛吸附在新生仔猪小肠黏膜上繁殖并产生肠毒素致仔猪发病。产气荚膜梭菌可以引起仔猪[5]、鸡[6]、鹿[7]、羊[8]、牛[9]和家兔[10]等动物发病,其中仔猪红痢主要是由C型产气荚膜梭菌引起,其致病机理主要是在感染动物肠道里产生大量致死性外毒素引起发病死亡[11]。大肠埃希菌纤毛和C型产气荚膜梭菌外毒素均具有很好的免疫原性,能够刺激机体产生抗体,抵抗大肠埃希菌和C型产气荚膜梭菌的攻击[12]。本研究通过提取大肠埃希菌纤毛抗原和C型产气荚膜梭菌外毒素作为制苗抗原,能够避免细菌菌体对怀孕母猪引起的不良反应,提高疫苗安全性。
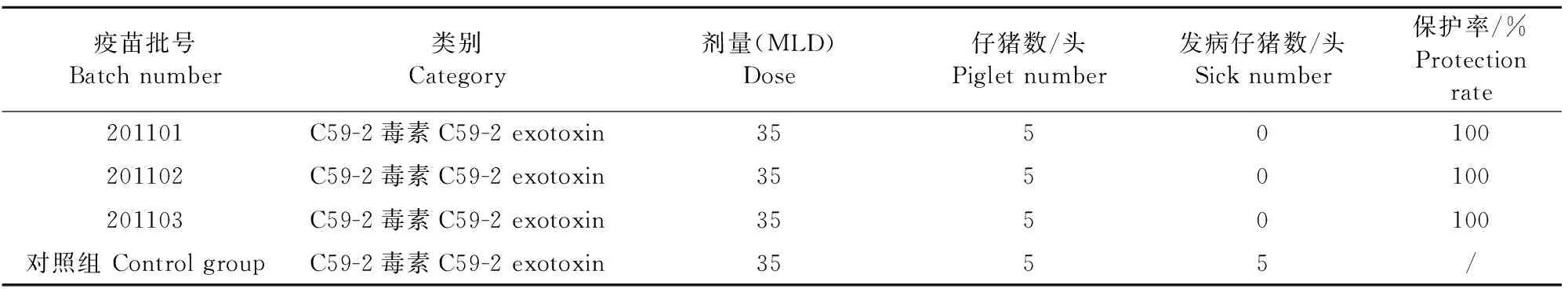
表4 免疫仔猪C型产气荚膜梭菌攻毒试验结果
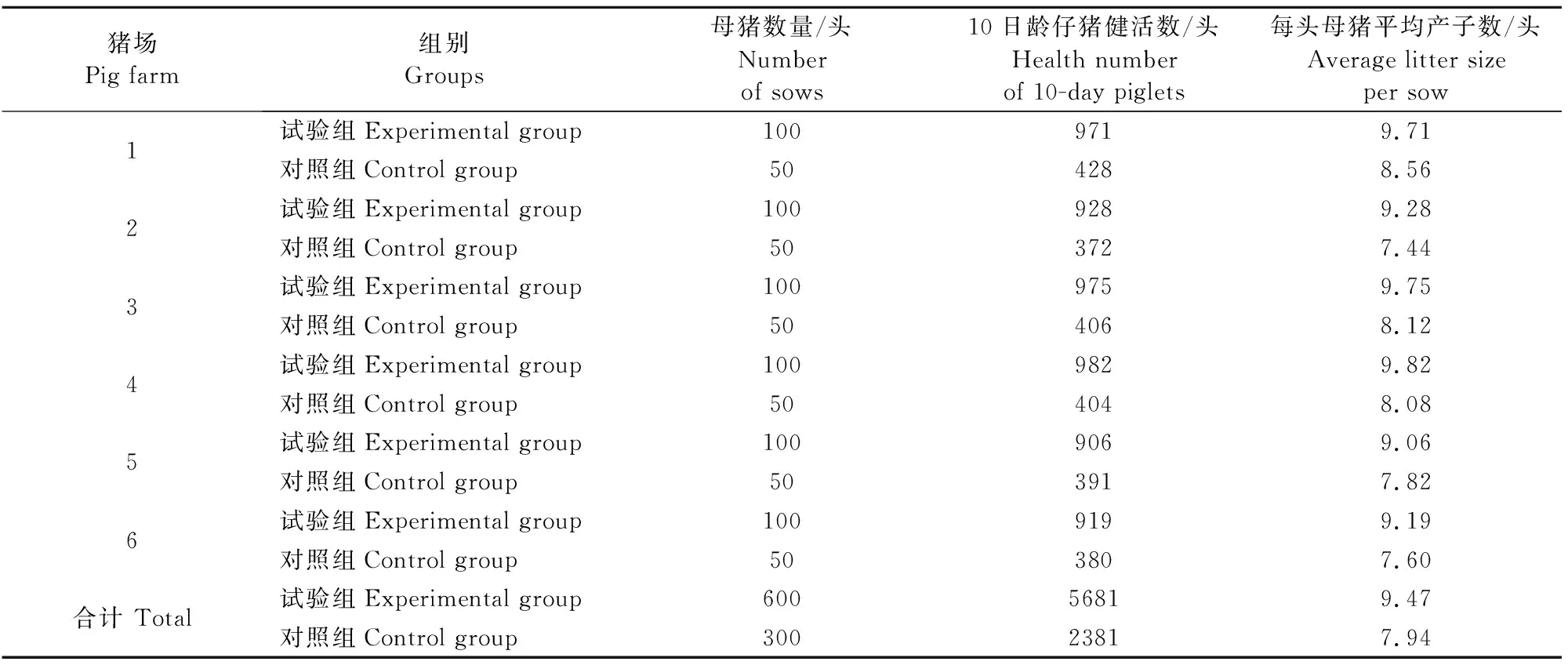
表5 二联疫苗临床免疫母猪产仔统计结果
目前我国已批准使用的这两种疾病的疫苗主要有仔猪大肠杆菌病三价灭活疫苗、仔猪大肠杆菌病K88、K99双价基因工程灭活疫苗及仔猪红痢灭活疫苗等,这些疫苗虽然在临床应用中效果较好,但在单联疫苗实际应用过程中,由于怀孕母猪需要多次注射,且注射剂量很大,给实际操作带来了极大的难度,也给怀孕母猪造成很大的应激反应。加之母猪怀孕期间还有其他种类疫苗如猪繁殖与呼吸综合征疫苗、细小病毒病疫苗等也要使用,会造成母猪在怀孕期间的免疫计划难以安排和执行。因此,研发此两种病的联苗可简化免疫程序,减轻母猪免疫压力,符合生产实践要求并具有临床应用价值。
佐剂是非特异性免疫增强剂,可以提升机体免疫系统对抗原或免疫原的免疫应答反应,目前用于灭活疫苗的佐剂主要有氢氧化铝胶佐剂、油乳佐剂、多糖佐剂、细胞因子佐剂以及纳米新型佐剂等[13]。本研究制备的疫苗是冻干疫苗,选用传统的氢氧化铝胶作为疫苗佐剂,不但有利于疫苗的稀释和均匀,而且价格较为便宜。
本研究通过提取大肠埃希菌纤毛抗原作为有效抗原,加入适当保护剂制备成冻干灭活疫苗,不仅可以保护疫苗中的有效抗原成分,延长疫苗的保存期,同时方便疫苗的运输和保存。根据兽用生物制品检验标准,我们对疫苗进行了物理性状检验和无菌检验,检验结果均能达到中华人民共和国兽药典[14]规定的质量标准。用该疫苗分别接种小鼠和断奶仔猪进行安全试验,结果小白鼠全部健活,断奶仔猪体温正常、精神良好及食欲正常,注射部位无肿胀及局部炎症,说明疫苗对小鼠和仔猪均具有很好的安全性。疫苗免疫怀孕母猪后,其所产仔猪对大肠埃希菌和C型产气荚膜梭菌攻毒保护率达到93%和100%,说明该疫苗对大肠埃希菌和C型产气荚膜梭菌具有良好的免疫原性,且保护率不低于国内的同类单苗,如浙江某生物技术有限公司生产的仔猪大肠杆菌病灭活疫苗保护率达93.05%,辽宁某生物制品厂生产的仔猪大肠埃希菌基因工程灭活苗的保护率为80.91%[15]。该疫苗在6个猪场进行了临床应用,经对免疫组和对照组母猪所产10日龄仔猪进行统计,结果显示,免疫组母猪窝平活仔数较对照组母猪窝平活仔数有较大提高,说明该疫苗免疫母猪后,其所产仔猪的成活率有较大提高,该疫苗有较好的免疫效果。
参考文献:
[1] Jeffrey J.Zimmerman,Locke A.Karriker,Alejandro Ramirez等主编.赵德明,张仲秋,周向梅等主译,猪病学[M].10版.北京:中国农业大学出版社,2014.
[2] 熊媛媛,黄 涛,郑 佳,等.大肠杆菌K88、K99、987P纤毛抗原提纯及抗血清制备[J].中国兽药杂志,2012,46(12):2-4.
[3] 刘泽文,邓均华,杨克礼,等.仔猪大肠埃希氏菌、C型产气荚膜梭菌的灭活及脱毒方法研究[J].安徽农业科学,2010,38(20):10702-10703.
[4] 刘泽文,田永祥,袁芳艳,等.仔猪大肠杆菌纤毛抗原反向间接血凝检测方法的建立与应用[J].华中农业大学学报,2017,36(3):69-73
[5] 刘泽文,袁芳艳,刘 威,等.猪C型产气荚膜梭菌的分离与鉴定[J].湖北农业科学,2016,55(23):6190-6191
[6] 胡 贺,覃宗华,王艳华,等.不同地区鸡源产气荚膜梭菌的毒素型鉴定和药敏试验[J].动物医学进展,2015,47(10)28-34
[7] 李自青,赵立峰,刘 宏,等.鹿产气荚膜梭菌二价灭活疫苗的制备和免疫效力试验[J].中国兽药杂志,2016,52(6)25-27
[8] 叶宝宏,冯 平,许信刚,等.羊源C型产气荚膜梭菌的分离鉴定、药敏试验及免疫治疗[J].西北农业学报,2016,25(7):960-965
[9] 王华欣,刘 宇,赵静虎,等.牛产气荚膜梭菌黑龙江分离株的分型鉴定[J].黑龙江八一农垦大学学报,2016,28(6):89-91.
[10] 王晓丽,马树芳,赵小勇,等.一例兔产气荚膜梭菌的分离与鉴定[J].中国养兔,2015,5:16-18.
[11] 李凡飞,张 云,李 强,等.C型产气荚膜梭菌致病机理研究进展[J].动物医学进展,2016,37(12):82-85.
[12] 韩学波,曾 瑾,王玉炯,等.C 型产气荚膜梭菌保护性抗原的免疫原性[J].中国生物制品学杂志,2008,21(3):201-203.
[13] 高 明,邵军军,常慧云,等.免疫佐剂研究进展[J].安徽农业科学,2016,43(34):204-206.
[14] 中国兽药典委员会编写,中华人民共和国兽药典(三部)[M].北京:中国农业出版社,2015.
[15] 陈晓锋,楼平儿,华坚青,等.两种仔猪大肠杆菌疫苗免疫效果试验[J].浙江畜牧兽医,2003,2:5.
