二维超声斑点追踪显像技术在心血管危险分层中的应用价值
2018-06-26石秀英米佳
石秀英,米佳
动脉粥样硬化性疾病,包括脑卒中、冠状动脉粥样硬化性心脏病(冠心病)等,是临床常见的威胁人类健康的主要疾病之一,准确预测患者心脑血管事件发生风险对于临床监护级别、治疗方式以及临床预后判断均有重要的临床价值[1,2]。超声二维斑点追踪成像技术(STI)是近些年发展而来的一种超声定量分析技术,可对同一位置的心肌运动轨迹进行不同帧频间的实时跟踪,从而准确、无创测量左心室旋转及扭转的角度[3]。与传统的组织多普勒技术相比较,斑点追踪技术克服了其角度依赖性,可实现对局部心肌功能的检测[4,5]。本研究探讨分析二维超声斑点追踪显像技术在心血管危险分层中的应用,报道如下:
1 资料与方法
1.1 研究对象选择2016年1月~2017年4月因胸痛就诊于陕西省延安大学附属医院心内科的157例患者作为研究对象,其中男性患者89例、女性患者68例,患者年龄24~88岁,平均年龄(52.18±15.92)岁。所有患者均行心脏及颈动脉超声,并收集高血压、糖尿病、吸烟史、心电图检查及生化指标等一般临床资料。排除标准:缺血性心肌病以外的心肌病、心律失常、肝肾功能不全、甲亢、先天性心脏病以及结缔组织病。
1.2 心血管危险分层Framingham危险评分(FRS)[6]是一个年龄、性别、高密度脂蛋白(HDL-C)、总胆固醇(TC)、收缩压(SBP)及吸烟史六个心血管疾病独立危险因素的综合评分,并根据患者综合评分情况进行分组。低危组:评分<12分,预测未来10年心血管事件风险<10%;中危组:评分12~15分,预测未来10年心血管事件风险10%~20%;高危组:评分>15分,预测未来10年心血管时间风险>20%。按照Framingham危险评分将患者分为低危组72例、中危组52例、高危组33例。
1.3 检查方法使用GE Vivid 7超声诊断仪以及M4S探头针对患者进行常规超声心动图检查,并检测患者左室收缩功能。使用12 L探头进行二维超声斑点追踪显像技术,检测时将探头置于患者颈动脉位置,获得患者经中动脉长轴二维图像,在总动脉分叉前1.5 cm处连续3个心动周期,采集频谱超声图像以及M型图像。采用Zoom模式针对M型图像进行颈动脉内中膜厚度(IMT)检查,若IMT>1.0 mm,则表示患者颈动脉内中膜增厚。然后选择12L探头模式,保证帧频为100~150帧/s间,从而获得指定位置的短轴动态图像,并储存备用。对上述获取的颈总动脉二维短轴动态图像采取用EchoPAC软件进行分析,从而获得患者颈动脉整体圆周应变(CS)。再测量患者右上肢动脉血压,进行三次检测后取平均值。使用肱动脉压差(PP)校正后获得CS/PP。
1.4 统计学分析采用统计学软件SPSS 22.0对本研究数据进行处理分析,计量资料采用(±s)表示,两组计量资料比较采用t检验,三组计量资料比较采用方差分析,计数资料采用百分率表示,两组计数资料比较采用χ2检验,三组计数资料比较采用秩和检验。采用ROC曲线分析各指标对高危型患者的预测价值,以P<0.05为差异有统计学意义。
2 结果
2.1 一般资料比较三组患者在性别、年龄、糖尿病等方面比较差异无统计学意义,P>0.05,随着心血管危险分层的升高,年龄升高(P<0.05),且随着患者心血管危险分层的升高,高血压、吸烟、高血脂比例明显升高(P<0.05)(表1)。

表1 三组患者临床资料比较
2.2 相关检测指标与心血管危险分层关系低危组CS、CS/PP及IMT分别为(7.03±1.79)%、0.19±0.12、(0.74±0.23)mm;中危组CS、CS/PP及IMT分别为(4.67±0.93)%、(0.11±0.07)(0.94±0.21)mm;高危组CS、CS/PP以及IMT分别为(3.15±0.77)%、0.06±0.11、(1.07±0.19)mm。不同心血管危险分层患者CS、CS/PP及IMT比较,差异有统计学意义,P<0.05。其中随着患者心血管危险分层危险程度的增加,CS、CS/PP水平降低(P<0.05),而IMT水平升高(P<0.05)(表2)。
2.3 ROC曲线分析相关检测指标对高危型患者的预测价值采用ROC曲线分析相关检测指标对高危型患者的预测价值,CS对高危型患者预测曲线下面积为0.868,CS/PP对高危型患者预测曲线下面积为0.858,IMT对高危型患者预测曲线下面积为0.771,见图1。CS对高危型患者预测敏感性87.88%(29/33)、特异性91.43%(96/105)、阳性预测值76.32%(29/38)、阴性预测值96.00%(96/100);CS/PP对高危型患者预测敏感性75.76%(25/33)、特异性88.57%(93/105)、阳性预测值67.57%(25/37)、阴性预测值92.08%(93/101);IMT对高危型患者预测敏感性78.79%(26/33)、特异性90.48%(95/105)、阳性预测值72.22%(26/36)、阴性预测值93.14%(95/102)。
3 讨论
冠心病、脑卒中是威胁人类健康的主要疾病,在全球范围内,心脑血管疾病已成为全球死亡原因的第一位[7]。动脉粥样硬化是心血管疾病发病的共同病理学基础,目前其发生机制尚未阐明,主要学说包括氧化学说、脂质沉积学说、炎症学说及平滑肌增生学说等[8-10]。由于冠状动脉粥样硬化患者可发生心肌梗死等心血管相关事件,因此对于心血管事件风险评估对于判断患者临床预后及选择治疗方式具有重要临床意义[11]。相关研究显示[12,13],动脉粥样斑块的形成与患者高血压、吸烟史、高龄、高三酰甘油、高密度脂蛋白降低等因素有关,因此,临床上普遍使用FRS给予临床危险因素对患者心血管事件发生风险进行评估判断。但由于FRS评估较为繁琐,给其临床应用造成了一定困难,因此研究者一直关注与寻找新的心血管风险评估方案。

表2 相关检测指标与心血管危险分层的关系
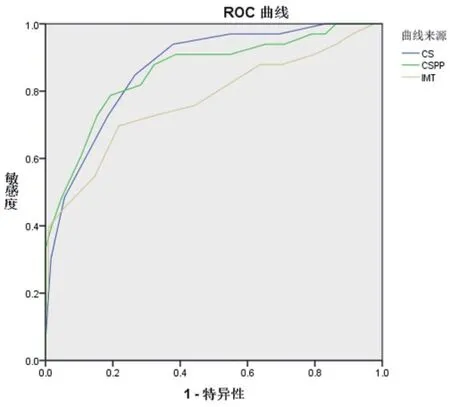
图1 相关检测指标对高危型患者的ROC预测价值
超声二位斑点追踪成像技术是近些年发展而来的一种超声定量分析技术,通过该技术可准确、无创测量左心室旋转及扭转的角度[14,15]。本研究探讨分析二维超声斑点追踪显像技术在心血管危险分层中的应用价值,采用斑点追踪手段对患者心动周期轨迹进行计算,从而有助于对患者心肌运动速度及圆周应变进行有效检测[16]。目前斑点追踪成像技术主要应用于心肌运动的研究中,对于颈动脉CS的测定,在心脏收缩时,弹性动脉或大动脉出现扩张或膨胀,从而在整个圆周方向上均可发生形变,促使心脏舒张时血液能够继续流动,根据其形变量便可对大动脉弹性进行估计[17,18]。本研究针对斑点追踪成像技术检测指标CS、CS/PP以及IMT对心血管危险分层的应用,比较结果显示,不同心血管危险分层患者CS、CS/PP以及IMT比较具有显著差异,其中随着患者心血管危险分层危险程度的增加,CS、CS/PP水平显著降低,而IMT水平显著升高。这与相关研究报道结果相似[19],CS、CS/PP及IMT能够有效反应患者颈动脉弹性状况及增厚情况,从而能够将其作为识别、判断有无斑块血管粥样硬化的检测指标。此外,研究采用ROC曲线分析相关检测指标对高危型患者的预测价值,结果显示,CS、CS/PP以及IMT对高危型患者预测曲线下面积分别为0.868、0.858及0.771。表明斑点追踪显像技术相关检测治疗对心血管高危型患者有着重要的预测价值。
综上所述,二维超声斑点追踪显像技术能够有效反应患者颈动脉弹性情况,并对心血管事件危险度进行评估和预测,具有重要临床价值。
[1]张国华,郑素君,郑海澜,等. SWI评估高血压患者心血管危险分层与脑内微出血相关性的研究[J]. 医学影像学杂志,2014,24(1):25-8.
[2]Matsuzawa Y,Svedlund S,Aoki T,et al. Utility of both carotid intimamedia thickness and endothelial function for cardiovascular risk stratification in patients with angina-like symptoms[J]. Int J Cardiol,2015,190(2):90-8.
[3]刘艳午,黄红梅,曹礼庭,等. 二维斑点追踪技术评价冠心病患者缺血心肌的应变、旋转和扭转的研究[J]. 中国超声医学杂志,2014,30(7):609-13.
[4]黄润青,邓又斌,王立平,等. 颈动脉圆周应变在心血管危险分层中的临床应用价值[J]. 中华超声影像学杂志,2012,21(12):1022-5.
[5]Boggia J,Asayama K,Li Y,et al. Cardiovascular risk stratification and blood pressure variability on ambulatory and home blood pressure measurement[J]. Curr Hypertens Rep, 2014, 16(9): 470-5.
[6]陈庆常,李天亮,胡新玲,等. 二维斑点追踪技术定量分析左室心肌纵向分层应变的临床研究[J]. 山西医科大学学报,2017,48(2):110-3.
[7]den Oord SC,Kate GL,Sijbrands EJ,et al. Effect of carotid plaque screening using contrast-enhanced ultrasound on cardiovascular risk stratification[J]. Am J Cardiol,2013,111(5):754-9.
[8]Greve SV,Blicher MK,Sehestedt T,et al. Effective risk stratification in patients with moderate cardiovascular risk using albuminuria and atherosclerotic plaques in the carotid arteries[J]. J Hypertens,2015,33(8):1563-70.
[9]靳鹏,郑慧,靳松,等. 斑点追踪显像技术与实时三平面组织同步显像技术评价不同构型高血压病患者左室心肌收缩功能[J]. 安徽医科大学学报,2013,48(3):290-4.
[10]Corrales A,González-Juanatey C,Peiró ME,et al. Carotid ultrasound is useful for the cardiovascular risk stratification of patients with rheumatoid arthritis: results of a population-based study[J]. Ann Rheum Dis,2014,73(4):722-7.
[11]孙敏敏,郭瑶,曹学森,等. 分层二维斑点追踪显像技术评价血液透析对左心室应变的影响[J]. 中华超声影像学杂志,2017,26(6):461-6.
[12]Rueda-Gotor J,Llorca J,Corrales A,et al. Carotid ultrasound in the cardiovascular risk stratification of patients with ankylosing spondylitis: results of a population-based study[J]. Clin Exp Rheumatol, 2016, 34(5):885-92.
[13]Perrone-Filardi P,Musella F,Savarese G,et al. Coronary computed tomography: current role and future perspectives for cardiovascular risk stratification[J]. Eur Heart J Cardiovasc Imaging,2012,13(6):453-8.
[14]刘洪,郑东,彭洪,等. 超声二维斑点追踪显像在缩窄性心包炎左室纵向运动定量评价中的应用[J]. 重庆医学,2015,44(15):2116-8.
[15]Elias-Smale SE,Kavousi M,Verwoert GC,et al. Common carotid intimamedia thickness in cardiovascular risk stratification of older people: the Rotterdam Study[J]. Eur J Prev Cardiol,2012,19(4): 698-705.
[16]新怡康. 高血压心血管危险分层与左室舒张功能障碍及NT-proBNP的相关性研究[J]. 临床和实验医学杂志,2015,14(23):1944-6.
[17]王磊,白龙. 老年高血压不同心血管危险分层LVMI、E/A、E/E'、IVRT及NT-proBNP分析[J]. 中国临床研究,2017,30(8):1113-5.
[18]李淑娟,朱玲,林约瑟,等. 斑点追踪显像技术定量评价不同年龄段正常儿童左、右心室纵向运动功能[J]. 中华超声影像学杂志,2016,25(9):750-6.
[19]Abbasi SA,Heydari B,Shah RV,et al. Risk stratification by regadenoson stress magnetic resonance imaging in patients with known or suspected coronary artery disease[J]. Am J Cardiol,2014,114(8):1198-203.
