喜勒可吸收生物修复膜治疗下颌角区骨缺损实验研究
2018-06-21张自强张以河徐荣荣刘明东
张自强,丁 芳,张以河,安 琪,徐荣荣,刘明东
引导骨再生(guided bone regeneration,GBR)技术采用生物膜阻挡周围软组织的成纤维细胞进入骨缺损区,保护缺损区具有成骨能力的血凝块的稳定,维护血块充填的间隙,最终实现缺损区的骨修复再生[1-2]。成骨过程中具有成骨潜能的细胞向缺损区生长、移行的速度慢于周围的结缔组织,可吸收生物修复膜的存在机械性地阻碍了纤维结缔组织和周围软组织进入骨缺损部位,保持骨缺损部位具有成骨潜能的间质细胞具有相对稳定的生长环境[3-4]。可吸收生物修复膜作为骨缺损修复的关键材料,临床上最早应用于引导牙周缺损的修复与再生,如种植牙前种植区骨量不足;即刻种植时种植体与拔牙创之间有间隙;种植时出现骨裂及种植体暴露;种植术后种植体周围炎症引起的病理性骨吸收等[5-6]。胶原作为天然的生物材料,广泛的应用于组织工程和再生医学中[7]。喜勒可吸收生物修复膜以牛跟腱为原料,采用酶解、透析、体外分子自组装、灭菌等工艺制得。本研究旨在对比喜勒可吸收生物修复膜与市售生物修复膜修复骨缺损的效果。
1 材料与方法
1.1 材料
1.1.1 实验动物 新西兰大白兔由北京金牧阳试验动物养殖有限责任公司提供[SCXK-(京)-2015-0005]。共选取健康成年新西兰大白兔12只,体重2~2.5 kg,雌雄不限,单笼喂养,自由饮水进食,在实验室饲养1周后进入实验。实验动物手术前1天禁食(不禁水)。
1.1.2 仪器和设备 喜勒可吸收生物修复膜由北京湃生生物科技有限公司生产(批号20160720)。市售生物修复膜为国家食品药品监督管理总局已批准的市售生物修复膜(批号160317-SS160102)。
1.2 方法
1.2.1 手术方法 新西兰大白兔称重后用3%戊巴比妥钠30 mg/kg经耳缘静脉滴注,全身麻醉。将兔仰卧位固定在手术台上,下颌角试验区用剪刀去毛。用2.5%的碘伏和75%的酒精进行常规皮肤消毒铺巾,无菌条件下,在下颌角区下缘做3 cm长的皮肤切口并切透骨膜,贴骨面向上剖离咬肌与翼内肌,充分暴露下颌角手术区[8]。
1.2.2 自体骨髂骨取骨 为保持髂嵴的外形和完整性,骨切口采取髂嵴上H型开窗术,暴露松质骨,用挖匙挖出块状松质骨,钢丝剪剪碎,无菌纱布包好待用,用可吸收线将髂嵴复位,皮下及皮肤逐层缝合,加压包扎。
1.2.3 骨缺损模型的建立 在生理盐水充分冷却的条件下,采用直径为6 mm的球钻在兔下颌骨左右两侧下颌角区分别制备直径6 mm洞穿性的骨缺损。覆盖生物膜,需超出缺损边缘2 mm,分层缝合创口。术后3 d每天皮下注射抗生素。分别于术后1个月、3个月采用空气栓塞法处死实验兔,取整个下颌骨。
1.2.4 骨缺损模型的分组 12只兔子分为2组:喜勒可吸收生物修复膜组6只(左侧植入自体骨覆盖喜勒可吸收生物膜,右侧不植骨不覆膜作为空白对照),分别在1个月时间点、3个月时间点处死3只实验兔取下颌骨;市售生物膜组6只(左侧不植骨不覆膜作为空白对照,右侧植入自体骨覆盖市售生物膜),分别在1个月时间点、3个月时间点处死3只实验兔取下颌骨。
1.3 观察方法 肉眼观察皮肤创口愈合情况,解剖观察创口处感染情况;X线观察:对处理过的下颌骨进行X光拍摄,并对X线图像进行处理,以便较直观地反映骨缺损愈合情况;组织学观察:常规石蜡包埋,脱钙切片,Masson染色,光镜下观察。
2 结果
2.1 肉眼观察 1个月时,6只兔子下颌骨表皮创口愈合良好,无感染现象,解剖时发现下颌骨膜植入位置创口愈合良好,无感染粘连现象;3个月时,毛已恢复正常长度,兔子下颌骨表皮创口愈合良好,下颌骨膜植入材料位点恢复良好。说明喜勒可吸收生物膜与市售生物修复膜生物相容性良好,不会引起机体炎性反应(图1)。
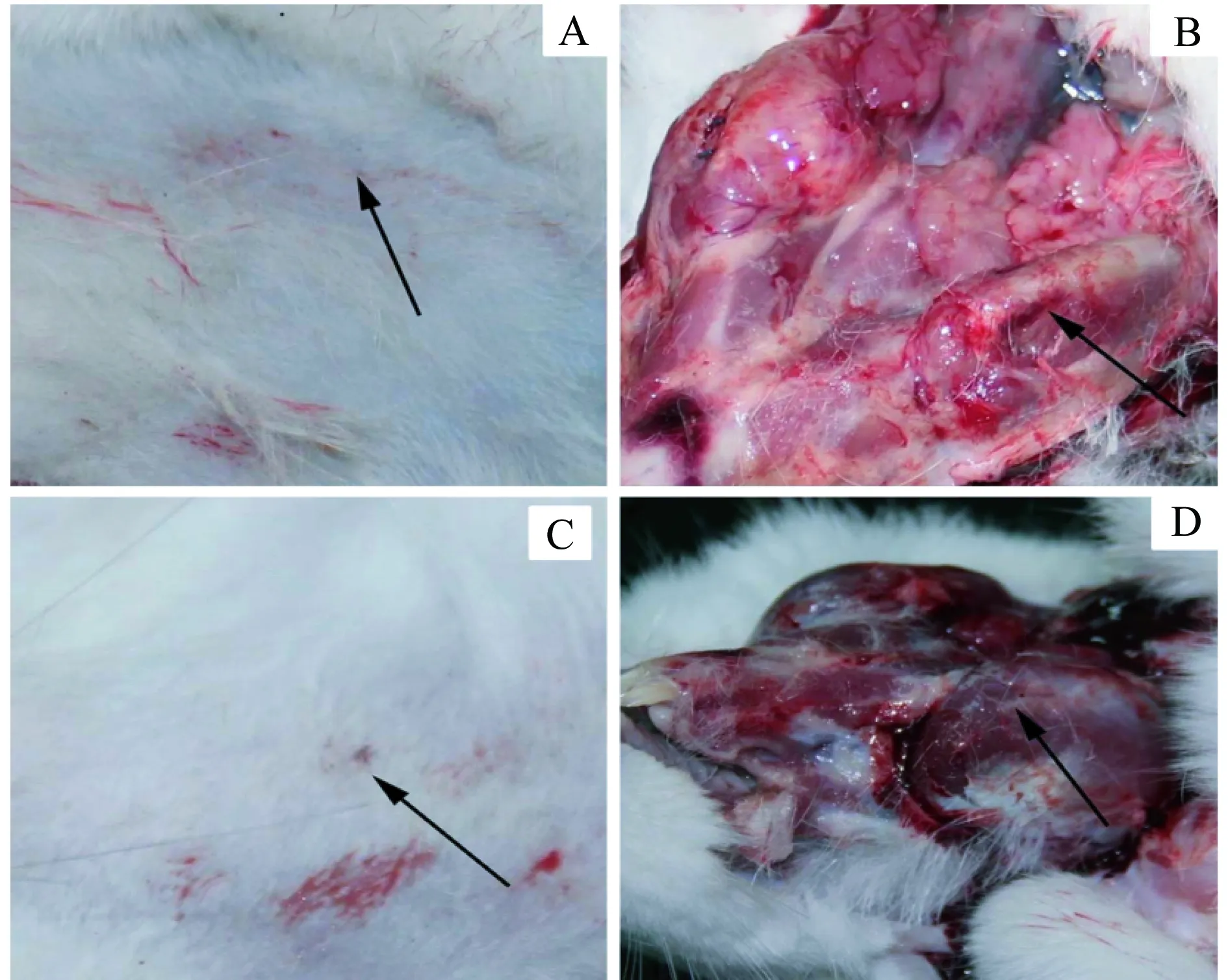
A:1个月时表皮伤口愈合良好;B:1个月时下颌角肌肉区创口愈合良好;C:3个月时表皮伤口愈合良好;D:3个月时下颌角肌肉区创口愈合良好图1 新西兰大白兔下颌角解剖图
2.2 X线观察 从X光图片可以看出,植入材料1个月后喜勒可吸收生物修复膜组和市售生物修复膜组的大白兔下颌骨孔洞都有不同程度的缩小,说明缺损处都有不同程度的新骨生成,骨生成情况无明显区别。但与空白对照相比,覆膜下颌骨孔洞明显缩小(图2)。
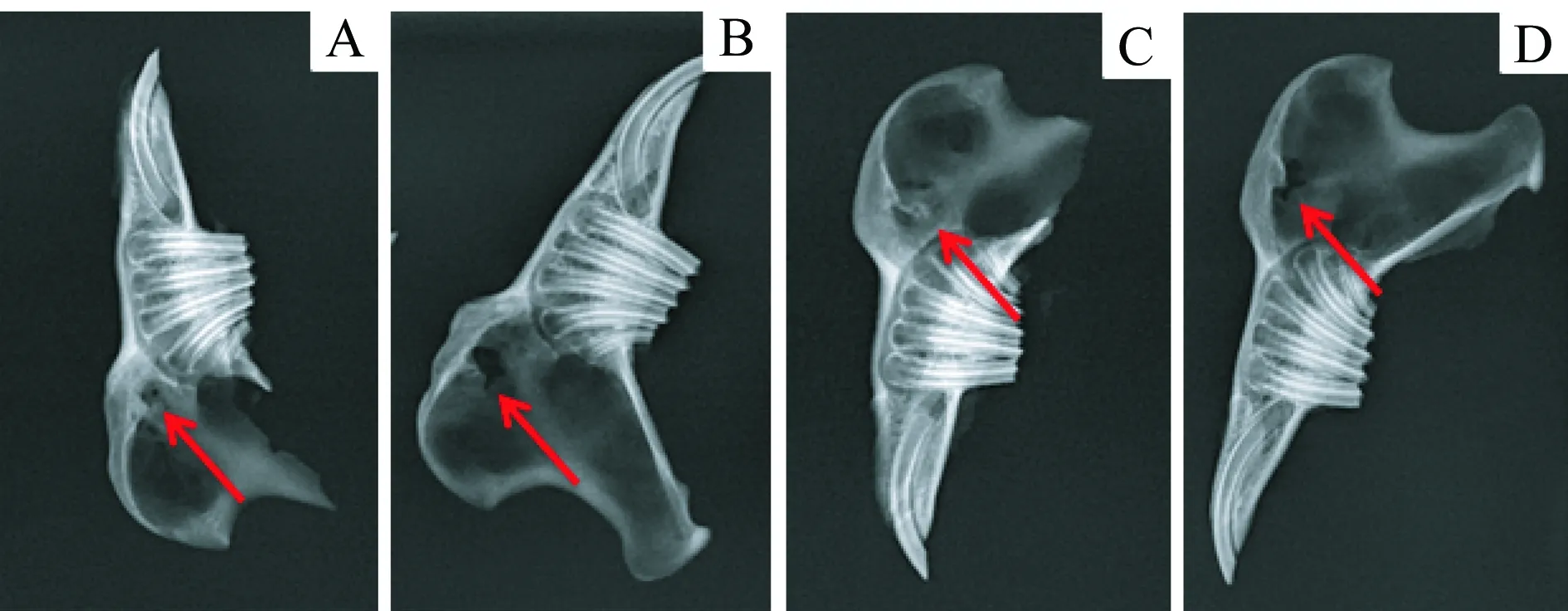
A:喜勒可吸收生物修复膜组左侧下颌骨新生骨组织已覆盖钻孔;B:空白对照组左侧下颌骨孔洞明显;C:市售生物修复膜组右侧新生骨组织已覆盖钻孔;D:空白对照右侧下颌骨孔洞明显
3个月时,喜勒可吸收生物修复膜组敷膜处骨缺损区消失,市售生物修复膜组敷膜处骨缺损消失,空白对照缺损区无明显变化。表明使用喜勒可吸收生物修复膜与市售生物修复膜后,经过3个月的修复生长,新生骨进一步增加,骨缺损已基本愈合,说明喜勒可吸收生物修复膜与市售生物修复膜都可以阻挡肌肉组织长入骨缺损部位,并引导骨缺损修复再生(图3)。
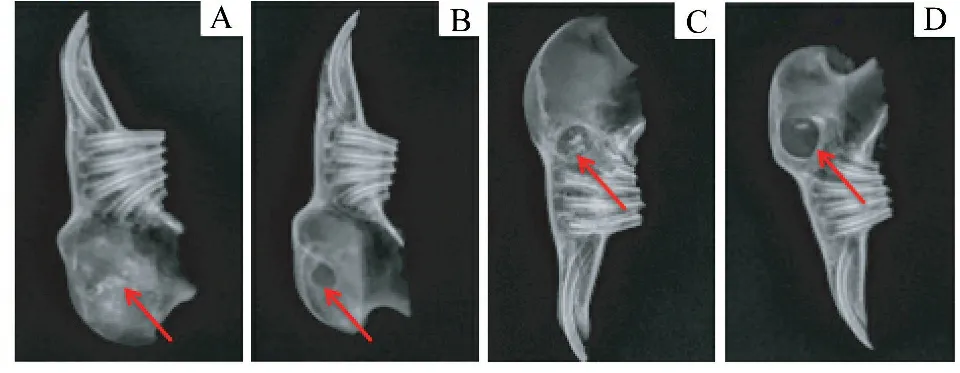
A:喜勒可吸收生物修复膜组左侧下颌骨新生骨组织已覆盖钻孔;B:空白对照左侧下颌骨孔洞明显;C:市售生物修复膜组右侧新生骨组织已覆盖钻孔;D:空白对照右侧下颌骨孔洞明显
2.3 组织学检查 取下颌角部位,剔除部分肌肉组织,以10%中性福尔马林固定,50%甲酸室温下脱钙处理,然后石蜡固定,脱钙切片,Masson染色,光镜下观察生物膜吸收、降解情况及骨缺损愈合情况,显微镜下观察(图4)。
从图中可以看出,植入材料1个月时,4倍镜下喜勒可吸收生物修复膜结构完整,紧贴骨组织,将骨缺损区与肌肉组织隔离,无炎性细胞。10倍镜下喜勒可吸收生物修复膜结构清晰,膜结构内及周围无炎性细胞。植入材料3个月时,喜勒可吸收生物修复膜消失,骨缺损区修复良好,无炎性细胞。
植入材料1个月时,4倍镜与10倍镜下市售生物修复膜消失,缺损区无炎性细胞,植入材料3个月时,骨缺损区修复良好,无炎性细胞。
1个月时喜勒可吸收生物修复膜膜结构依然完整,但市售生物修复膜已经消失。说明喜勒可吸收生物修复膜与市售生物修复膜生物相容性良好,但喜勒可吸收生物膜较市售生物修复膜抗降解能力强。
喜勒可吸收生物修复膜组左下颌角区,钻孔内植入自体骨覆盖喜勒可吸收生物修复膜,骨缺损区域具有类骨质生成,类骨质表面具有一层到多层成骨细胞;市售生物修复膜组右下颌角区,骨缺损区填充自体骨覆盖市售生物修复膜,骨组织修复良好,骨缺损区已连接植入自体骨,骨内膜和外膜层整齐排列一层呈柱状成骨细胞;空白对照左下颌角区,断骨区明显;空白对照右下颌骨区骨缺损区域明显,骨缺损区内被胶原纤维或成纤维细胞填充,无骨质样结构形成。
植入材料1个月时,喜勒可吸收生物修复膜与市售生物修复膜引导骨再生能力无明显区别,骨缺损区都已连接植入自体骨并有类骨质生成。覆盖喜勒可吸收生物修复膜的骨缺损区内有成骨细胞生成,而空白对照骨缺损区内被胶原纤维或成纤维细胞填充,无成骨细胞。说明喜勒可吸收生物修复膜能起到物理阻隔作用,能够有效的引导骨再生(图5)。
植入材料3个月时,喜勒可吸收生物修复膜与市售生物修复膜都降解完毕,2组骨缺损都修复良好,骨膜完整,骨外膜细胞为扁平状,骨组织完整,骨基质内有一层扁平状的成骨细胞,骨基质结构呈板层状较为致密;空白对照断骨区域明显,骨缺损区被间充质细胞填充,再次说明敷盖喜勒可吸收生物修复膜能够起到物理阻隔作用,可良好的引导骨组织再生(图5)。
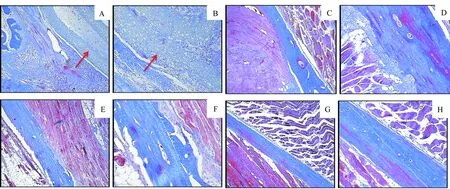
A:1个月时4倍镜下喜勒可吸收生物修复膜结构完整;B:1个月时10倍镜下喜勒可吸收生物修复膜结构完整;C:3个月时4倍镜下喜勒可吸收生物修复膜消失;D:3个月时10倍镜下喜勒可吸收生物修复膜消失;E:1个月时4倍镜下市售生物修复膜消失;F:1个月时10倍镜下市售生物修复膜消失;G:3个月时4倍镜下市售生物修复膜消失;H:3个月时10倍镜下市售生物修复膜消失
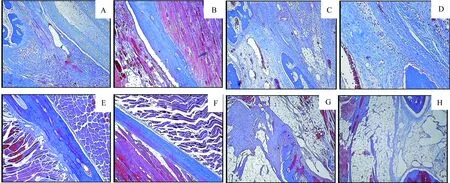
A:1个月喜勒可吸收生物修复膜组左侧下颌角区;B:1个月市售生物修复膜组右侧下颌角区;C:1个月空白对照左下颌角区;D:1个月空白对照右下颌角区;E:3个月喜勒可吸收生物修复膜组左侧下颌角区;F:3个月市售生物修复膜组右侧下颌角区;G:3个月空白对照左下颌角区;H:3个月空白对照右下颌角区(Masson染色,×4)
3 讨论
GBR技术应用了膜的屏障作用、空间保护作用、诱导引导作用,应用于牙种植,引导种植体周围骨再生,都取得了理想的骨再生效果。GBR技术通过膜的机械屏障作用,阻止了来自周围组织的成纤维细胞侵入骨缺损区,并通过缺损区植入材料的引导支架作用,使自体成骨细胞有足够时间在缺损区增殖、成骨,最终达到缺损区骨组织重建。
GBR技术中应用的可吸收生物修复膜材料分为可生物降解与不可生物降解2大类,其中第一代再生膜的材料是不可降解的钛膜、聚四氟乙烯等。这类材料易操作且具有较好的生物相容性和较理性的机械强度,但是这类膜通透性较差,影响营养物质进入上方瓣膜,易于引起牙龈退缩,从而引发感染及膜暴露,同时材料不能被组织吸收且无法与周围组织结合,因此不可避免的要经受二次手术,增加了创伤[9-10]。第二代再生膜材料为生物可降解材料,膜材料在机体内可降解吸收,从而避免了二次手术取出。可降解生物膜材料有聚乳酸、胶原、聚乙烯二醇、壳聚糖等,这些材料中,胶原膜具有纤维网架结构,有利于再生细胞附着,易于放置贴附,生物相容性好,在促进细胞的粘附、增殖和分化方面优于其他可吸收生物修复膜材料[11],因此在各类可吸收性GBR膜中,胶原膜备受关注。目前临床中应用较多的胶原膜为脱细胞真皮基质膜,脱细胞真皮基质膜去除了真皮的细胞成分,保留真皮内的细胞外基质,维持完整的胶原形态和基底膜结构[12]。脱细胞真皮基质膜采用Dispase-Triton法[13]或NaCl-SDS法[14]去除了基质外的细胞成分,但是膜中胶原分子内C、N末端区域的主要免疫原性位点“端肽”[15]无法去除,因此不能完全去除其免疫原性。而喜勒可吸收生物修复膜采用精准酶切技术从牛跟腱中提取Ⅰ型胶原蛋白,其纯度达99%以上,酶切去除了Ⅰ型胶原蛋白的端肽结构,彻底去除了其免疫原性。与脱细胞真皮基质膜不同,喜勒可吸收生物修复膜采用的是体外自组装工艺,运用了胶原蛋白大分子中携带不同电荷的基团,氢键、通过静电作用、疏水性作用等非共价键力自发地自组装形成的膜[16],这些分子键使其机械强度比脱细胞工艺基质膜高,组织相容性好。
可吸收性生物修复膜植入生物体后,在被吸收之前需要维持一定时间才能起到良好的修复作用,即膜的降解速率应当与组织愈合的速率保持一致。如果膜的降解时间低于骨的形成时间,骨的缺损修复效果将会大打折扣[17-18]。宋爱梅等[19]和Karring等[20]研究发现,术后2~3周是牙周再生愈合的关键时间,因此生物修复膜用于治疗牙周病时,降解周期需要在3~4周以上,膜材料用于修复骨缺损时,其降解周期应保持17周左右时间,以平衡人类骨的正常形成周期。市售生物修复膜在植入1个月时已经消失,而喜勒可吸收生物修复膜结构依然完整,且紧贴骨组织,无炎性细胞,表明喜勒可吸收生物修复膜的降解时间更长,抗降解能力优于市售组。
喜勒可吸收生物修复膜在进行GBR时,具有很好的安全性和有效性,能够起到生物屏障膜的作用,阻止来自周围软组织的成纤维细胞,让成骨细胞有足够的时间和空间增殖,最终达到引导组织再生、定向修复的目的,实现缺损区的骨修复再生。
【参考文献】
[1]马士卿,张旭,孙迎春,等.引导骨组织再生膜的研究进展[J].口腔医学研究,2016,32(3):308-310.
[2]Talreja PS,Gayathri GV,Mehta DS.Treatment of an early failing implant by guided bone regeneration using resorbable collagenmembrane and bioactive glass[J].J Indian Soc Periodontol,2013,17(1):131-136.
[3]郑汉峰.不同口腔修复膜材料在牙种植引导骨再生中的应用效果观察[J].临床医学工程,2016,23(8):1001-1002.
[4]蒋柳宏,董滢,景向东.引导骨再生技术在上前牙种植修复中的效果[J].中国组织工程研究,2015,19(7):1138-1142.
[5]赵进峰,尹蒙熔,樊马娟.改良式GBR技术联合即刻种植术后即刻修复上前牙的疗效分析[J].黑龙江医药科学,2015,38(4):151-152.
[6]黄宇文.牙周炎对种植体周围边缘骨吸收的影响[J].实用临床医学,2017,18(7):63-64,70.
[7]Mercado KP,Helguera M,Hocking DC,et al.Noninvasive quantitative imaging of collagen microstructure in three-dimensional hydrogels using high-frequency ultrasound[J].Tissue Eng Part C Methods,2015,21(7):671-682.
[8]胡秀莲,邱立新,林野,等.可吸收性Bio-Gide膜治疗下颌角区局部骨缺损实验研究[J].中国口腔种植学杂志,2002,7(1):10-12,24.
[9]马遥.静电纺PBS/PPC载rh-BMP2纳米纤维膜的制备及生物活性评价[D].长春:吉林大学,2015.
[10]白冰,朱静涛,王立威.作为GBR屏障膜的新型胶原膜的体内植入效果分析[J].口腔医学,2015,35(3):170-174.
[11]杜倩.壳聚糖-胶原角膜修复材料的制备及生物相容性[J].中国组织工程研究,19(52):8433-8437.
[12]侯劲松,黄洪章.脱细胞真皮基质在口腔医学领域的应用进展[J].中国口腔颌面外科杂志,2007,5(3):163-169.
[13]Takami Y,Matsuda T,Yoshitake M,et al.Dispase/deter-gent treated dermal matrix as a dermal substitute[J].Burns,22(3):182-190.
[14]Livesey SA,Herndon DN,Hollyoak MA,et al.Transplanted acellular allograft dermal matrix:potential as a template for the reconstruction of viable dermis[J].Transplantation,1998,60(1):1-9.
[15]杜晓丹,方玉,奚廷斐,等.动物源性胶原的生产、应用及其免疫原性[J].中国组织工程研究与临床康复,2008,12(23):4511-4514.
[16]李新明,刘欢,刘洁.基于多肽及多肽衍生物而构建的具有生物应用潜力的超分子自组装体的研究[C].苏州:全国高分子学术论文报告会,2015.
[17]周艺群.可吸收性GTR膜材料的研究现状与进展[J].中国口腔种植学杂志,2002,7(1):42-45.
[18]Zhang Y,Zhang X,Shi B,et al.Membranes for guided tissue and bone regeneration[J].Oral Maxillofac Surg Clin North Am,2013,1(1):1-10.
[19]宋爱梅,杨丕山,孙钦峰,等.屏障膜放置时间与牙周再生量关系的动物实验研究[J].牙体牙髓牙周病学杂志,2001,11(1):17-19.
[20]Karring T,Nyman S,Lindhe J,et al.Potentials for root resorption during periodontal wound healing[J].J Clin Periodontol,1984,11(1):41-52.
