3,6-二取代丙烯酰-9-乙基咔唑的合成及光谱研究
2018-06-19李志洲季晓晖邵先钊曹文秀
王 伟, 李志洲, 季晓晖, 邵先钊, 曹文秀
(陕西理工大学 化学与环境科学学院, 陕西省催化基础与应用重点实验室, 陕西 汉中 723000)
咔唑及其衍生物是一类很重要的含氮芳杂环化合物[1],具有特殊的刚性稠环结,分子内含有较大的共轭体系,具有较强的给电子和空穴传输能力。在光电致发光材料[2-7]、医药[8-10]、染料中间体[11-12]、金属离子探针[13-14]等领域均有较广泛的应用。Wang F F等[15]用烷基咔唑与对氟苯甲酰氯反应分别制得了3,6-二(4-氟苯甲酰)-9-乙基咔唑和3,6-二(4-氟苯甲酰)-9-甲基咔唑,然后与对苯二酚反应生成聚合物,该类聚合物具有良好的热稳定性、抗酸碱性和溶解性等优点。Li L等[16]利用咔唑经溴乙烷烷基化生成9-乙基咔唑,然后与三氯氧磷、N,N-二甲基甲酰胺反应生成3,6-二甲醛-9-乙基咔唑,最后与2-甲基喹啉反应制得9-乙基-3,6-二(2-(喹啉)乙烯基)咔唑,并对其紫外和荧光光谱进行了研究,该化合物有较强的荧光,有望应用于双光子吸收材料中。Shi H P等[17]在9-乙基咔唑的3和6位引入甲醛基和溴,然后进行自身偶联生成(E)-双-(3-溴-9-乙基咔唑-6-)乙烯,在丁基锂催化下溴被甲醛基取得,再与邻巯基苯胺反应制得(E)-双-(3-(2-苯并噻唑基)-9-乙基咔唑-6-)乙烯,最后研究了其光物理和电化学性能。然而,在咔唑的3和6位先引入乙酰基,然后在9位引入乙基,最后与糠醛、5-甲基糠醛和苯甲醛缩合反应引入呋喃环、苯环形成更大的共轭体系,作为有机光致/电致发光材料,未见报道。
本研究以咔唑作为原料,经Friedel-Crafts酰基化生成3,6-二乙酰咔唑,烷基化制得3,6-二乙酰-9-乙基咔唑(I),然后在碱性条件下分别与糠醛、5-甲基糠醛和苯甲醛反应,生成3,6-二(呋喃-2-)丙烯酰-9-乙基咔唑(II)、3,6-二(5-甲基呋喃-2-)丙烯酰-9-乙基咔唑(III)和3,6-二苯丙烯酰-9-乙基咔唑(IV),并通过1H、13CNMR、质谱及红外光谱对其进行结构表征;对其紫外-可见吸收光谱和荧光发射光谱进行了研究。合成路线如下:
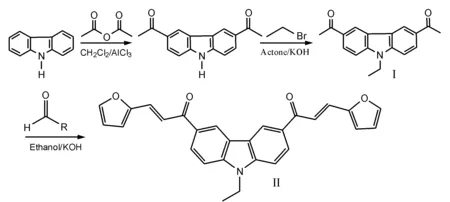
1 实验部分
1.1 试剂和仪器
咔唑、溴乙烷、氢氧化钾、丙酮、无水乙醇、二氯甲烷、三氯化铝、乙酸酐、糠醛、5-甲基糠醛、苯甲醛均为分析纯(成都格雷西亚化学技术有限公司)。
AVANCE Ⅲ 400 MHz型核磁共振波谱仪(瑞士Bruker公司),以氘代氯仿作为溶剂,四甲基硅烷为标准物,磁场频率400 MHz;F4600荧光光谱仪(日立高新技术公司);1290Infinity LC超高效液相;QTOF质谱(Agilent公司);红外光谱仪6700型(美国热电公司);紫外-可见分光光度计Cary 50型(美国VARIAN公司)。
1.2 合成步骤
1.2.1 3,6-二乙酰咔唑的合成
将7.06 g三氯化铝和10 mL二氯甲烷加入带有温度计、冷凝管和搅拌磁子的50 mL三口烧瓶中,用冰盐浴冷却至0 ℃下,滴加2.50 g(0.024 5 mol)乙酸酐和5 mL二氯甲烷混合溶液。反应至三氯化铝完全溶解,然后滴加1.67 g(0.010 0 mol)咔唑和15 mL二氯甲烷的混合溶液。滴加过程中保持反应溶液的温度维持在0 ℃以下,滴加完毕在0 ℃继续反应2 h。反应完毕后将反应液倒入50 mL的冰水中,蒸馏出二氯甲烷,大量白色固体析出,过滤,用去离子水洗涤3次(20 mL×3),在80 ℃烘箱中烘干,得产物2.63 g,产率为93.5%。
1.2.2 3,6-二乙酰-9-乙基咔唑(I)的合成
将1.20 g氢氧化钾和25 mL丙酮加入装有温度计、冷凝管和搅拌磁子的50 mL三口烧瓶中,在25 ℃下搅拌20 min,加入3.26 g(0.013 0 mol)3,6-二乙酰咔唑,反应40 min后,恒压滴加溶有2.2 g(0.020 2 mol)溴乙烷的10 mL丙酮溶液,滴加完毕,在25 ℃下反应4 h。将反应物倒入300 mL去离子水中,有大量白色沉淀析出,过滤,用水洗涤3次(30 mL×3),在80 ℃烘箱中烘干,得I产物3.15 g,产率为96.5%。
1.2.3 3,6-二取代丙烯酰-9-乙基咔唑(II)的合成
将0.50 g(0.001 8 mol)3,6-二乙酰-9-乙基咔唑、0.05 g氢氧化钾和15 mL无水乙醇加入带有温度计、冷凝管和搅拌磁子的50 mL三口烧瓶中。升温至40 ℃待I全部溶解后,滴加新蒸馏的糠醛0.35 g(0.003 6 mol)和5 mL乙醇溶液,滴加完毕恒温反应6 h。反应完毕后将30 mL去离子水加入反应液中,过滤,得到黄色固体II 0.64 g。
合成III的不同之处在于所加入的醛为0.40 g(0.003 6 mol)5-甲基糠醛,其他条件相同,所得黄色固体产物0.71 g。
合成IV的不同之处在于所加入的醛为0.38 g(0.003 6 mol)苯甲醛,其他条件相同,所得淡黄色固体产物0.65 g。
1.2.4 溶液荧光光谱扫描及图谱
以二氯甲烷为溶剂,将I、II、III和IV配成浓度为1.0×10-5mol/L的溶液。在测试前所有溶液均进行超声脱气处理。在25 ℃条件下,用石英比色皿(1 cm)装测定液,紫外-可见吸收光谱在200~800 nm范围内进行扫描。在25 ℃条件下,5 nm的狭缝宽度,120 nm/min的扫描速度,在200~900 nm范围内根据紫外吸收光谱的最大吸收峰进行发射光谱,根据发射光谱的最强发射峰进行激发波长扫描。
2 结果与讨论
咔唑与乙酸酐在氯化铝催化下进酰基化反应高产率的获得3,6-二乙酰咔唑,并且咔唑中N-H不需要保护。咔唑环中的N-H为仲胺,活性比伯胺要弱,所以反应过程中未生成酰胺。因此,可以高产率的获得目标产物。3,6-二乙酰咔唑与溴乙烷反应高产率的合成3,6-二乙酰-9-乙基咔唑(I),在25 ℃不能发生自身羟醛缩合,同时采用四氢呋喃代替丙酮有相似的结果。对3,6-二(呋喃-2-)丙烯酰-9-乙基咔唑(II),3,6-二(5-甲基呋喃-2-)丙烯酰-9-乙基咔唑(III)和3,6-二苯丙烯酰-9-乙基咔唑(IV)的紫外-可见光谱和荧光光谱进行详细研究。
2.1 产品表征
3,6-二乙酰咔唑:白色晶体,产率93.5%。1HNMR(400 MHz,CDCl3),δ:11.532(s,1H),8.726(s,2H),8.022~8.037(d,J=2.0 Hz,6H),7.474~7.490(d,J=6.4 Hz,2H),2.672(s,6H)。高分辨质谱正离子(M+1)质量数:252.102 4,理论质量数:251.094 6。红外光谱分析,3276 cm-1强吸收为3,6-二乙酰咔唑中N—H键的伸缩振动的特征吸收峰,1666 cm-1吸收峰为羰基的伸缩振动的特征吸收峰,1621和1619 cm-1为苯环骨架伸缩振动的特征吸收峰,。
3,6-二乙酰-9-乙基咔唑(I):白色晶体,产率96.5%。1HNMR(400 MHz,CDCl3),δ:8.765(s,2H),8.188~8.190(d,J=0.8 Hz,2H),7.442~7.460(d,J=7.2 Hz,2H),4.383~4.426(m,2H),2.75(s,6H),1.476~1.506(t,2H)。高分辨质谱正离子(M+1)质量数:280.134 7,理论质量数:279.125 9。红外光谱分析,与3,6-二乙酰咔唑比较,3276 cm-1N—H键的特征吸收峰消失,1672 cm-1吸收峰为羰基伸缩振动的特征吸收峰,1623、1589 cm-1为苯环骨架伸缩振动的特征吸收峰。
3,6-二(呋喃-2-)丙烯酰-9-乙基咔唑(II):黄色固体,产率82.1%,以咔唑计算产率为74.1%。1HNMR(400 MHz,CDCl3),δ:8.838~8.842(d,J=1.6 Hz,2H),8.215~8.219(d,J=1.6 Hz,1H),8.193~8.197(d,J=1.6 Hz,1H),7.630(s,2H),7.622(s,2H),7.510~7.514(d,J=1.6 Hz,2H),7.427(s,1H),7.406(s,1H),6.676~7.684(d,J=3.2 Hz,2H),6.465~6.478(m,2H),4.324~4.378(m,2H),1.403~1.440(t,3H);13CNMR(400 MHz,CDCl3),δ:188.7(2C),151.9(2C),144.7(2C),143.3(2C),130.5(2C),130.0(2C),127.3(2C),123.1(2C),122.1(2C),119.5(2C),115.8(2C),112.6(2C),106.9(2C),38.2(1C),13.9(1C)。高分辨质谱正离子(M+1)质量数:436.154 6,理论质量数:435.147 1。红外光谱,1656 cm-1为羰基伸缩振动的特征吸收峰,1623、1593、1483 cm-1为苯环骨架伸缩振动的特征吸收峰,1217 cm-1为呋喃环中碳—氧键伸缩振动的特征吸收峰。
3,6-二(5-甲基呋喃-2-)丙烯酰-9-乙基咔唑(III):黄色固体,产率85.2%,以咔唑计算产率为76.9%。1HNMR(400 MHz,CDCl3),δ:8.936~8.940(d,J=1.6 Hz,2H),8.297~8.301(d,J=1.6 Hz,2H),8.276~8.280(d,J=1.6 Hz,2H),7.634(s,4H),7.497(s,1H),7.76(s,1H),6.652~6.660(d,J=3.2 Hz,2H),6.156~6.162(d,J=2.4 Hz,2H),4.400~4.455(m,2H),2.458(s,6H),1.479~1.515(t,3H);13CNMR(400 MHz,CDCl3),δ:188.75(2C),155.70(2C),150.62(2C),143.32(2C),130.71(2C),130.21(2C),127.29(2C),123.18(2C),122.11(2C),117.86(2C),117.63(2C),109.31(2C),108.86(2C),38.21(1C),18.45(1C),14.11(2C)。高分辨质谱正离子(M+1)质量数:464.186 0,理论质量数:463.178 4。红外光谱分析,1652 cm-1吸收峰为羰基伸缩振动的特征吸收峰,1624、1593、1485 cm-1为苯环骨架伸缩振动的特征吸收峰,1206 cm-1为呋喃环中碳-氧键伸缩振动的特征吸收峰。
3,6-二苯丙烯酰-9-乙基咔唑(IV):淡黄色固体,产率79.1%,以咔唑计算产率为71.4%。1HNMR(400 MHz,CDCl3),δ:8.906~8.910(d,J=1.2 Hz,2H),8.283~8.287(d,J=1.2 Hz,1H),8.262~8.66(d,J=1.2 Hz,1H),7.929(s,1H),7.890(s,1H),7.795(s,1H),7.756(s,1H),7.736~7.741(d,J=2.0 Hz,2H),7.718~7.722(d,1.6H),7.507(s,1H),7.486(s,1H),7.407~7.472(m,6H),4.400~4.454(m,2H),1.484~1.519(t,3H);13CNMR(400 MHz,CDCl3),δ:189.3(2C),144.11(2C),143.42(2C),135.18(2C),130.60(2C),130.38(2C),128.98(4C),128.50(4C),127.47(2C),123.16(2C),122.23(2C),122.13(2C),33.24(1C),13.19(1C)。高分辨质谱正离子(M+1)质量数:456.196 2,理论质量数:455.188 5。红外光谱分析,1657 cm-1为羰基伸缩振动的特征吸收峰,1693、1593、1489 cm-1为苯环骨架伸缩振动的特征吸收峰,1206 cm-1为呋喃环中碳-氧键伸缩振动的特征吸收峰。
2.2 紫外-可见吸收光谱

图1 化合物I~IV在二氯甲烷中的紫外-可见吸收光谱
由I、II、III和IV配制的二氯甲烷溶液测得的紫外-可见吸收光谱如图1所示。由图1可以发现,化合物I~IV在紫外光区均表现出强且具有精细结构的特征吸收谱带,其中在290 nm左右的吸收峰来自于咔唑单元的π-π*电子跃迁[4]。化合物I在262、290、335 nm有强的吸收峰,化合物II、III、IV由于共轭体系的增大吸收谱带变得宽而强,明显向长波长方向移动。化合物II在283 nm为弱吸收,而在339 nm和380 nm为强吸收,与化合物I相比显著向长波长方向移动,并且吸收强度和信号都增强,最强吸收峰为339 nm。化合物III与化合物II相比在呋喃环中引入甲基,吸收光谱图与化合物II非常的相似,甲基供电子效应导致最强吸收峰向长波长方向移动15 nm位于356 nm处,且强度减弱,在387 nm处增加。化合物IV与化合物I相比向长波长方向移动,吸收信号增强;但化合物IV与化合物II和III比向短波长移动,且吸收信号减弱,最大吸收波长位于300 nm,次强吸收峰在363 nm处。化合物I(335 nm)、II(339 nm)、III(356 nm)、IV(363 nm)的摩尔吸光吸收分别为2.228 0×10-5、0.907 9×10-5、1.010 8×10-5、1.758 6×10-5L·cm-1·mol-1。由化合物I、II、III、IV吸收光谱表明,分子内引入供电子基,共轭增强,π电子向π*反键轨道跃迁,增强了π电子离域度,有利于电子向低激发态能级的跃迁,因而在紫外吸收光谱中表现为峰位的红移,有利于荧光产生。

图2 化合物I~IV在二氯甲烷中的荧光发射光谱
2.3 荧光发射光谱
化合物I、II、III、IV在二氯甲烷溶液中的荧光发射光谱如图2所示,激发波长分别为262、339、356、300 nm,其在紫外蓝光区域内表现出强烈的荧光激发光谱。由图2可以看出,化合物I~IV在二氯甲烷溶液中展现出具有精细结构的发射谱带,化合物I、II、III、IV最大发射峰分别位于304、342、364、334 nm,可归属于共轭分子π-π*激发态的荧光发射;可归因于分子内咔唑到取代丙烯酰基的电荷转移;在黄光区域表现出弱的发射峰位于606~729 nm。化合物II和III的谱图非常的相似,由于III中呋喃环多了一个供电子的甲基,图中特征发射峰向长波长方向红移了20 nm,而化合物IV苯环与呋喃环的不同之处在于向短波长方向蓝移40 nm。因此,在咔唑分子骨架结构引入双取代的丙烯酰,由于取代的丙烯酰与咔唑形成更大共轭结构,有助于提高分子内电荷转移产生较强的荧光性质。
3 结 论
通过Friedel-Crafts酰基化、N-烷基化和羟醛缩合设计合成了三种含双取代的丙烯酰咔唑的荧光材料。合成3,6-二(呋喃-2-)丙烯酰-9-乙基咔唑、3,6-二(5-呋喃-2-)丙烯酰-9-乙基咔唑、3,6-二苯丙烯酰-9-乙基咔唑的产率分别为74.1%、76.9%、71.4%。利用核磁共振碳谱、氢谱、高分辨质谱和红外光谱等方法对产物进行结构表征,并通过紫外-可见吸收光谱和荧光发射光谱对其发光性质进行了研究。结果表明,在分子结构中引入取代丙烯酰基,形成更大的共轭结构,分子内电荷转移能力以及荧光效应显著提高。
[ 参 考 文 献 ]
[1] 房旭彬,房雷,苟少华.咔唑及其衍生物合成方法研究进展[J].有机化学,2012,32(7):1217-1231.
[2] GAO Shou-qin, HAO Li-ling, LI Jun-fen, et al. Photophysical processes of an intramolecular charge transfer fluorescent dye with carbazole units[J]. Luminescence,2013,28(3):412-418.
[3] 边高峰,胡彬,欧阳密,等.多色显示树枝状聚(3,6-双噻吩咔唑)及其共聚物的电化学和电致变色性能[J].物理化学学报,2015,31(10):1888-1894.
[4] 黄诚,谷龙,张正,等.含咔唑基团芘类荧光材料的合成与发光性质[J].精细化工,2015,32(1):1-5.
[5] HUANG Bin, YIN Zhi-hui, BAN Xin-xin, et al. Nondoped deep blue OLEDs based on Bis-(4-benzenesulfonyl -phenyl)-9-phenyl-9H-carbazoles[J]. Journal of Luminescence,2016,172:7-13.
[6] SHI He-ping, XIN De-hua, GU Xing-gui, et al. The synthesis of novel AIE emitters with the triphenylethene-carbazole skeleton and para-/meta-substituted arylboron groups and their application in efficient non-doped OLEDs[J]. Journal of Material Chemistry C,2016,4(6):1228-1237.
[7] WANG Hao-wei, CHEN Yu, YE Wen-bo, et al. A facile and highly efficient green synthesis of carbazole derivatives containing a six-membered ring[J]. Dyes and Pigments,2013,96(3):738-747.
[8] PANESAR H K, SOLANO J, MINEHAN T G. Synthesis and DNA binding profile of N-mono- and N,N’-disubstituted indolo[3,2-b]carbazoles[J].Organic Biomolecular Chemistry,2015,13(10):2879-2883.
[9] 杜会茹,蒋翠岚,黄文杰,等.3,6-二氨基咔唑衍生物的合成及与DNA的相互作用[J].精细化工,2015,32(2):223-226.
[10] 简勇,李刚,杨鹏,等.新型咔唑类衍生物的合成、光谱性质及其Ct-DNA作用的研究[J].有机化学,2014,34(4):809-816.
[11] 穆丹华,刘杰,王亭,等.基于咔唑染料敏化剂的合成及电喷雾的DSSC器件制备[J].中国科学:化学,2014,44(11):1800-1806.
[12] 刘飞,吴彤,胡明明,等.一种新型咔唑类菁染料黏度荧光探针[J].高等学校化学学报,2012,33(10):2239-2243.
[13] 陈丽萍,殷芳芳,周鹏妹,等.含咔唑基氨基硫脲类汞离子探针的合成及其性能研究[J].功能材料,2015,46(21):21041-21044.
[14] LI Dao-xue, SUN Xin, HUANG Jian-min, et al. A carbazole-based “turn-on” two-photon fluorescent probe for biological Cu2+detection vis Cu2+-promoted hydrolysis[J]. Dyes and Pigments,2016,125:185-191.
[15] WANG Fei-fei, WANG Zhi-ping, WANG Hong-hua, et al. Synthesis and characterization of soluble poly(arylene ether ketone)s with high glass transition temperature based on 3,6-bi(4-fluorobenzoyl)- N -alkylcarbazole[J]. Polym International,2015,64(2):258-266.
[16] LI Liang, WANG Ping, ZHANG Yi-chi, et al. Synthesis, one and two-photon optical properties of two asymmetrical and symmetrical carbazole derivatives containing quinoline ring[J]. Journal of Molecular Structure,2013,1051:23-29.
[17] SHI He-ping, DAI Jian-xin, SHI Li-wen, et al. Synthesis, photophysical and electrochemical properties of a carbazole dimer-based derivative with benzothiazole units[J]. Spectrochimica Acta Part A:Moleculai and Biomolecular Spectroscopy,2012,93:19-25.
