费休氏容量法测量冻干人用狂犬病疫苗中水分含量的不确定度分析
2018-06-14邱文娜王永智方朝东
邱文娜 饶 玲 王永智 方朝东 李 磊
江苏省泰州医药高新技术产业园区疫苗工程中心,江苏泰州 225300
狂犬病是由狂犬病毒所致的人畜共患急性传染病,流行性广,病死率100%,有效预防该病的措施是接种狂犬病疫苗[1]。目前,上市的狂犬疫苗有两种剂型,冻干粉针剂因技术含量高、易于保存、免疫反应轻等特点,将逐步成为市场主流。水分含量是冻干粉针剂疫苗稳定性相关的一个重要参数,在日常质检过程中诸多因素会影响该检测结果的准确性[2-6]。
本实验室该项检测项目于2012年获得CNAS认可,曾两次参加CNAS组织的测量审核、能力验证,且结果均为满意。本文利用瑞士万通870型水分测定仪测定冻干人用狂犬病疫苗中的水分含量,根据日常检测经验对影响测定结果的四大因素进行不确定度评定,该因素包括测量重复性、卡尔费休试液滴定度、卡尔费休试液滴定体积、称样量[7-10]。依据不确定评定方法,建立不确定度分析的数学模型, 逐步考察各不确定度分量,找出分析过程中的关键点,为日常检测数据的准确性和可靠性提供依据[11-15]。
1 材料与方法
1.1 样品
冻干人用狂犬病疫苗,由中心内疫苗研发企业提供。
1.2 主要试剂及仪器
无水甲醇(分析纯,含水量<0.1%);卡尔费休试剂(批号 SZBD0490V,Sigma Fluka);标定用水;电子天平(Sartorius BSA224S-CW);卡尔-费休水分测定仪(瑞士万通KF 870型);微量注射器、药匙。凡与样品或费休氏试液直接接触的物品,如称量勺、玻璃器皿、橡皮塞均应在80℃干烤2h,取出置干燥器内冷却20min备用。
1.3 环境要求
环境湿度对检测结果影响较大,且卡尔费休试液具有吸水性,因此水分检测实验室湿度需低于50%,仪器干燥用分子筛需状态良好,与样品直接接触的称量纸、称量勺、捣碎工具均需80℃干燥。
1.4 检测方法
1.4.1 滴定杯微环境的平衡 加入50mL无水甲醇至滴定杯中,启动仪器平衡模式,消除滴定杯中存在多余水分干扰,等待仪器显示conditioning ok,即漂移值小于20µL/S时,即可开始标定。
1.4.2 卡尔费休溶液的标定 选择Titer标定模式,使用尖头微量注射器吸取约20mL标定用水,注意排除气泡,精密称定注射器和水样质量并做好记录,选择仪器进样键,快速加入水样至滴定杯中,再次精密称定注射器质量,两次质量之差即加入的标定用水质量,将进样量输入仪器,按start键开始滴定,滴定结束后,仪器自动显示本次标定消耗卡尔费休试液体积、滴定度F值,如此连续测定3次,3次连续标定结果相对标准偏差在±1%以内,以平均值作为卡尔费休试液的滴定度。
1.4.3 供试品的测定 选择KFT测定模式,天平去皮,精密称定供试品90~100mg置干燥的称量纸中,记录进样前质量,选择仪器进样键,快速加入供试品至滴定杯中,精密称定称量纸质量,两次质量之差即加入的供试品质量,将进样量输入仪器,按start键开始滴定,滴定结束后,仪器自动显示本次标定消耗卡尔费休试液体积、供试品含水量。
2 不确定度分析
2.1 数学模型和不确定度来源分析
依据中国药典2015版通则0832卡尔费休容量法测定原理及万通水分测定仪测定流程,供试品含水量公式为:
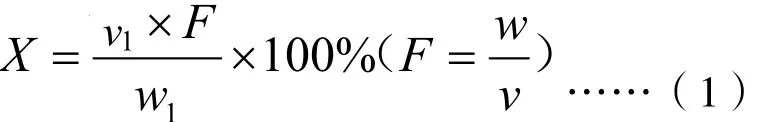
其中V1为称取的供试品消耗的费休氏试液的体积,mL;W1为供试品进样量,mg;F为卡尔费休试液标定F值的平均值,mg/mL;W为标定中消耗的标定用水的质量,mg;V为标定中标定用水消耗的费休氏试液的体积,mL。
根据公式(1)可知,卡尔费休容量法检测供试品含水量的不确定度主要来自:(1)测量重复性;(2)供试品进样量;(3)供试品消耗的卡尔费休试液体积;(4)卡尔费休试液滴定度F值。本实验在标定及检测开始前均有平衡过程,漂移值保持在20µL/s以内,消除了溶剂中水分的影响,所以本文忽略考察无水甲醇溶剂中水分带来的不确定度。实验采用的水分测定仪可自动判断滴定终点,消除人为影响,操作全过程环境湿度低于50%,与供试品接触直接接触实验材料均经过80℃干燥,且密闭的滴定杯连接有分子筛干燥剂,因此忽略考虑由终点判断和环境水分引起的不确定度。
2.2 各分量标准不确定的评估
2.2.1 测量重复性标准不确定度分量Urel(x)
称取同一批次样品3份,测定含水量,结果如下:2.54%,2.59%,2.57%;平均值为2.57%。
根据贝塞尔公式实验标准偏差为:
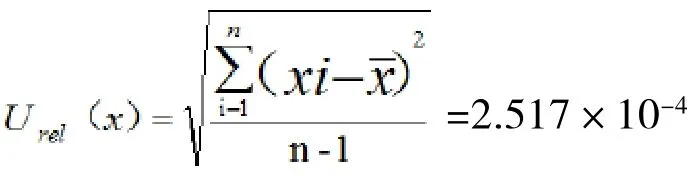
结果平均值的相对标准不确定度为:
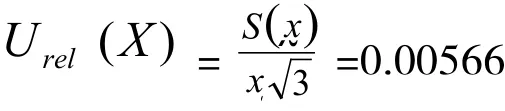
2.2.2 称取的供试品质量W1引入的相对标准不确定度Urel(W1) 供试品称量不确定度来自天平称量重复性和天平校准两个方面。本实验所用电子天平精度为d=0.01mg,天平检定证书列出的重复性误差为±0.05 mg,属 B 类不确定度,按矩形分布(包含因子),天平称量重复性的不确定度为天平校准产生的不确定度,所用电子天平(d=0.01mg)的检定证书给出的最大允差为±0.03 mg,属 B 类不确定度,按矩形分布(包含因子),天平校准产生的不确定度为:
因此,单次称量的标准不确定度为,样品称量带来的相对不确定度为(样品称样量为95.4mg,
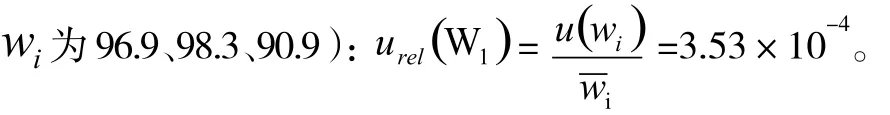
2.2.3 供试品消耗的费休氏试液的体积V1引入的相对标准不确定度Urel(V1)
该不确定度分量主要来源于滴定管校准和实验室温度波动两个方面,滴定管校准引入的标准不确定度U1(V1),根据水分测定仪技术报告得知10mL滴定管的最大允差为0.02mL,按三角分布,标准不确定度实验室温度变动引入的标准不确定度U2(V1),根据仪器资料,10mL滴定管校准温度为20℃,而本实验室温度在25℃,实验室温度变化近似为矩形分布,属于B类不确定度。本实验所用卡尔费休试剂膨胀系数为1.2×10-3/℃,V1均值为0.6044mL(0.6103,0.6280,0.5750),标 准 不 确 定 度 U2(V1)=0.6044×5×1.2×10-3/= 2.09×10-3mL,将U2(V1)两个分量进行合成,得到相对标准不确定度

2.2.4 标定结果F值引入的相对标准不确定度
卡尔费休试液滴定度F值引入的不确定度由标定用水质量、标定时消耗的卡尔费休试液体积、标定操作重复性、标定用水纯度构成,因本实验所用标定用水缺少证书,所以该项不确定度分量不予考虑。
标定用水质量引入的不确定度U1(m1),因与供试品称量共同同一台天平,由2.2.2可知单次称量的标准不确定度为:u(mi)=0.0337,标定用水称量带来的相对不确定度为(标定用水称样量mi为19.9mg,mi为 19.8、19.9、20.1):
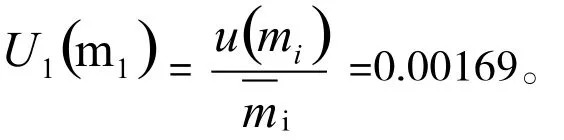
标定时消耗的卡尔费休试液体积引入的相 对 标 准 不 确 定 度 U2(V标),由 2.2.3可 知,U(V标1)=0.02/=0.00816mL,V 标 均 值为 4.9222mL(4.9114,4.9070,4.9481)U(V标2)=4.9222×5×1.2×10-3/= 1.705×10-2mL,将 U2(V标1)、U2(V标2)两个分量进行合成,得到相对标准不确定度

标定操作重复性引入的相对标准不确定度U3(x),通过平行试验3次,测得F值分别为4.0314,4.0554,4.0622,由2.2.1贝塞尔公式可知其标准偏差为0.01618,平均值为4.0497,相对标准不确定度U3(x)为 0.00400。
将 U2(m1)、U2(V标)、U3(x)进行合成,F 值的相对标准不确定度

2.2.5 合成标准不确定度的计算

表1 各分量的不确定度评估表
以相对标准不确定度的平方和进行合成,得到合成标准不确定度
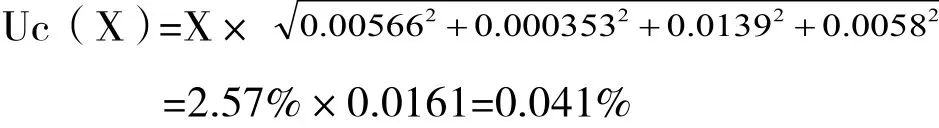
2.2.6 扩展不确定度的计算
取包含因子K=2,置信概率为95%,水分测定结果的扩展不确定度为:U(x)=K×Uc(X)=2×0.041%=0.082%。
2.2.7 报告不确定度
本实验室按照现行药典标准测定冻干人用狂犬病疫苗含水量,取包含因子K=2,置信概率为95%,检测结果可表示为含水量X=2.57%±0.082%。
3 讨论
本实验中,卡尔费休水分测定法不确定度来源主要涉及测量重复性、供试品质量、卡尔费休试液消耗体积及标定F值,其中供试品消耗的卡尔费休试液体积引入的相对标准不确定度为0.0139,所占比例最大,其次为标定结果F值和测量重复性引入的不确定度,影响标定结果F值的各不确定度分量中,标定时的卡尔费休试液体积和标定重复性引入的不确定度相当,且远大于标定用水质量引入的不确定度,标定重复性和测量重复性引入的不确定度属于A类不确定度,描述了各个测量值的分散度,因本实验室在长期日常检测中标定和测量重复性较好,所以观测次数n取了三次,当重复性较差时,n应相应增大,以客观计算该项不确定度值。由于本实验采用减量法称重,两次称量的校准偏差相互抵消,所以样品称量引入的不确定度最小,可以忽略不计。
由表1中各不确定度分量评估可知,使用费休氏容量法测量冻干人用狂犬病疫苗中水分含量时,需根据样品性质选用滴定度稳定的卡尔费休试剂,并严格控制水分检测实验室的温湿度环境条件(湿度控制在50%以内),每月更换水分测定仪干燥用分子筛,控制平衡时间在5min以内,平衡时间过长时需注意考虑卡尔费休试液稳定性、无水甲醇是否新换及滴定杯内微环境等因素,逐一排查。标定时控制连续三次测定的F值相对标准偏差在±1%以内,以最大降低由卡尔费休试液体积、F值带来的不确定度。样品称量引入的不确定度虽然最小,但当进样方式不正确时,质量比较轻的冻干粉类样品会飘溅到滴定杯壁上,本实验室经多次实验总结应选用质地较硬的硫酸纸进行称量,并将硫酸纸剪成合适的形状,以减少进样时的样品损失。检测实验室内应设置烘箱,凡与样品直接接触的称量勺、烧杯,都应进行80℃长时间烘干,并做到取样快, 称量快,转移快, 尽量使样品暴露在空气中的时间最短,以降低系统漂移。当两次检测间隔时间过长时,需更换滴定杯中溶剂无水甲醇,以降低反应微环境中水分的影响。
[1] 俞永新.狂犬病和狂犬病疫苗[M].北京:中国医药科技出版社,2009:150-165.
[2] 邵益斌,吴书,等.冻干人用狂犬病纯化疫苗稳定性观察 [J].中国生物制品学杂志,2004,17(5):313-315.
[3] 马超,陆俭,孙燕,等.冻干人用狂犬病疫苗(Vero细胞)稳定剂配方的筛选[J].微生物学免疫学进展,2016,44(1):28-31.
[4] 吕新军,申辛欣,唐青,等.改良抗体结合试验检测人用狂犬病疫苗效价方法的初步建立[J].中国疫苗和免疫,2014,20( 3) :250-253.
[5] Berny JF,Hennebert GL.Viability and stability of yeast cells and filamentous fungus spores during freeze-drying:effects of protectants and cooling rates[J].Mycologia,1991,83(6):805-815.
[6] 赵凯等.医学生物制品学[M].北京:人民卫生出版社,2007:851-890.
[7] 国家药典委员会.中华人民共和国药典(三部)[S].北京:中国医药科技出版社,2015:65-66.
[8] 谭伟.用Karl Fischer法、重量分析法和热解重量分析法测定冻干疫苗中的残留水分[J].国际生物制品学杂志,1983,11(5):224-225.
[9] 中国实验室国家认可委员会. 化学分析中不确定度的评估指南[M].北京:中国计量出版社,2002:4-5.
[10] 张成悌.测量不确定度评定中的若干问题[J].中国测试技术, 2007, 33(5):24-28.
[11] 倪育才.实用测量不确定度评定[M].北京:中国计量出版社,2007:50-58.
[12] 国家质量监督检验检疫总局.JJF 1059.1-2012 测量不确定度评定与表示[S].北京:中国标准出版社,2013:87-98.
[13] 中国实验室国家认可委员会.ISO/IEC 17025:2005 检测和校准实验室认可准则[S].中国实验室国家认可委员会,2005:20-42.
[14] 郜振华,刘小东.费休氏水分测定法不确定度评定[J].中外医疗,2009(16):191-194.
[15] 胡威盛.尿素中水分含量的不确定度评定[J].大氮肥,2009,32(1):61-63.
