磁性阳离子凝胶对活性橙K-GN染料废水吸附研究
2018-06-13张于弛吴华忠
张于弛,方 润,吴华忠
(闽江学院 海洋学院化工与材料系,福建 福州 350108)
1 前言
在印染工业中,偶氮类染料是应用最广泛的一类合成染料,使用量占到70%[1]。活性橙K-GN是一种典型的活性偶氮染料,使用量大,在印染行业广泛应用[2],因此,偶氮染料废水的高效降解问题一直是研究热点。吸附法能彻底地将染料从废水中去除,所用凝胶还可以多次再生使用。阳离子凝胶是一种具有强吸水性的三维高分子聚合物,其用作吸附剂去除水体中的污染物已有相关的研究[3-5]。磁性材料由于具有较好的分离特性而备受关注。本文采用水热法,以氯化铁为铁源,以PVP为表面活性剂,合成Fe2O3磁性材料,并通过分步聚合方法,以甲醛、丙酮、三乙烯四胺、Fe2O3磁性材料为原料制备磁性阳离子凝胶,考察新型磁性阳离子凝胶吸附剂对活性橙K-GN染料废水的吸附性能。
2 实验部分
2.1 试剂与仪器
2.1.1 试剂
三氯化铁(FeCl3·6H2O),聚乙烯吡咯烷酮(PVP),十六烷基三甲基溴化铵(CTAB),无水乙醇,三乙烯四胺,盐酸,甲醛(37 wt%水溶液),氢氧化钠,丙酮,均为分析纯,购自国药集团化学试剂有限公司,活性橙K-GN(工业级)(上海佳英化工有限公司),蒸馏水,自制。
2.1.2 仪器
THZ-82型水浴恒温振荡器(上海跃进医疗器械四厂),TG16-W 微量高速离心机(湖南仪器仪表总厂光华仪器厂),DF-101S集热式恒温加热磁力搅拌器(巩义市予华仪器有限责任公司),721可见分光光度计(上海精密科学仪器有限公司),X-射线粉末衍射仪(日本岛津)。
2.2 实验方法
2.2.1 水热法制备Fe2O3磁性材料[6]
1 mmol FeCl3·6H2O、0.6 g PVP、0.6 g CTAB、30 mLH2O配成溶液,转移至50 mL聚四氟乙烯高压反应釜中,在烘箱 120 ℃加热 24 h。反应结束后,离心分离,将产物放入烘箱中烘干后取出,得到Fe2O3磁性粒子。
2.2.2 磁性阳离子凝胶的制备
实验方法同文献[7]。
量取8 mL三乙烯四胺于烧杯中,浓HCl调pH=6-7备用。向装有回流冷凝管的三口瓶中加入12 mL甲醛、9 mL丙酮、三乙烯四胺溶液和制备的Fe2O3粉末,保持不断搅拌促使 Fe2O3粉末在溶液中分散,用浓HCl调pH=3,室温下反应1 h后加入NaOH水溶液(质量浓度33%)至pH=8。加入第二批甲醛12 mL,升温至65 ℃,恒温反应40-60 min(视反应情况而定),得到含磁性粒子的阳离子聚合物水凝胶,冷却出料,将产品密封70 ℃(6 h)成阳离子干凝胶。将干凝胶放入250目尼龙滤袋中水洗48 h后65 ℃烘箱中烘干,过筛收集60-120目凝胶粉末备用。
2.2.3 磁性阳离子凝胶对活性橙K-GN染料废水的吸附实验
称取0.01 g、目数为60-120目的干凝胶放入250 mL锥形瓶中,加入100 mL浓度为0.1 g·L1活性橙K-GN溶液,放在已预热的摇床中吸附一定时间,用分光光度计470 nm的吸光度值。溶液脱色率和凝胶平衡吸附量Qe根据公式(1)和(2)计算。

式中:V为溶液体积(mL),C0为初始浓度,Ce为平衡浓度,m为吸附剂质量(g)。
3 实验结果与讨论
3.1 Fe2O3的XRD图分析
Fe2O3材料的XRD如图1所示。
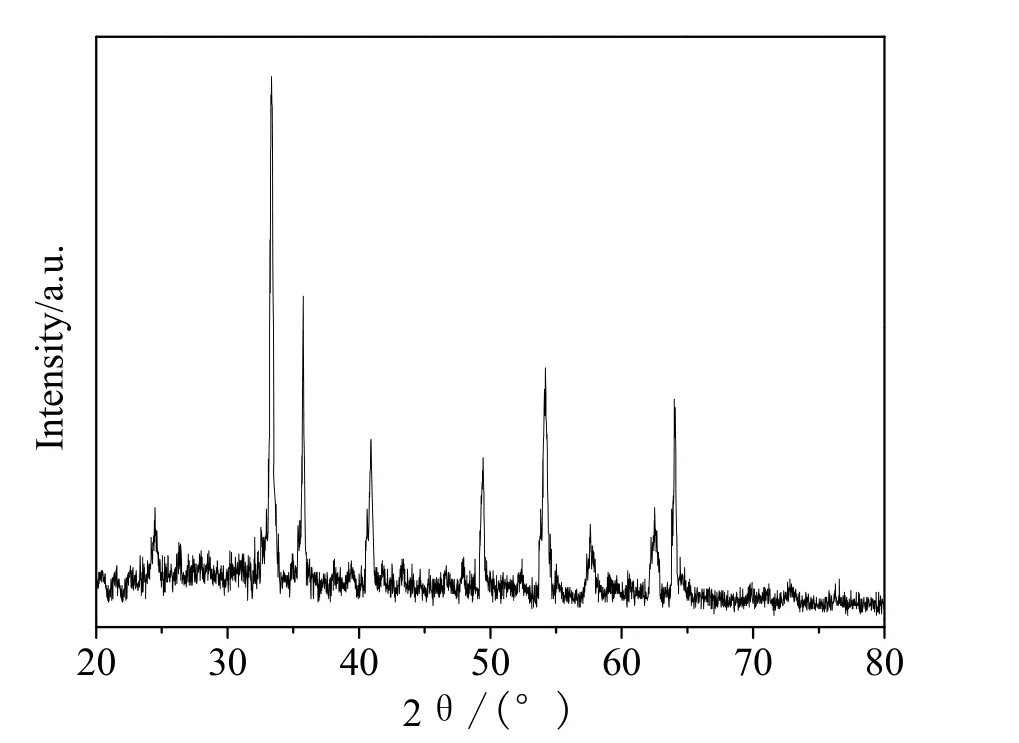
图1 样品的XRD图
据参考文献[6,8],将实验所得的 Fe2O3XRD图同Fe2O3标准卡片(JCPDS33-0664)进行对比,发现实验所得的 XRD图同 Fe2O3的标准卡片中各个特征的衍射峰相符,谱图中无明显其他衍射峰,说明水热法制备的产物确为Fe2O3。
3.2 Fe2O3添加量对活性橙 K-GN吸附量Qe的影响
Fe2O3不同添加量对活性橙 K-GN吸附量的影响如图2所示。
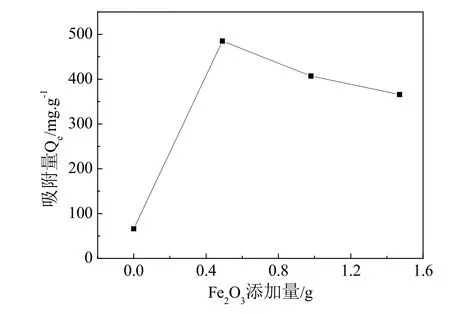
图2 Fe2O3添加量对活性橙K-GN溶液吸附量的影响
由图2可以看出,加入Fe2O3的新型磁性阳离子水凝胶的吸附量比未添加Fe2O3的阳离子凝胶吸附量大幅度增加,加入0.49 g Fe2O3制备的阳离子凝胶对活性橙K-GN溶液吸附效果最佳。增加Fe2O3量,吸附效果下降,可能原因是Fe2O3的添加量越多,竞争吸附越强,吸附效果反而不好。下面实验选择的是0.49 g的Fe2O3添加量。
3.3 磁性阳离子凝胶的用量对活性橙K-GN吸附效果的影响
磁性阳离子凝胶的用量对活性橙K-GN吸附效果影响结果如图3所示。

图3 磁性阳离子凝胶用量对吸附效果的影响
由图3可以知道,活性橙K-GN的脱色率随磁性阳离子凝胶的增加而逐渐增大,这是因为吸附过程中,吸附剂越多,对活性橙K-GN吸附的位点越多,吸附脱色越充分。吸附量 Qe的变化则相反,随着吸附剂用量增加,吸附量有所下降,可能是因为由吸附剂吸附间的竞争吸附引起,吸附效果下降。图 3中当磁性阳离子水凝胶用量0.18 g·L-1,磁性阳离子凝胶对活性橙K-GN的脱色率已经超过98%。
3.4 pH对磁性阳离子凝胶吸附活性橙K-GN的影响
不同 pH对磁性阳离子凝胶吸附活性橙K-GN的影响如图4所示。

图4 溶液初始pH值对吸附效果的影响
由图4可知,随着溶液pH增大,磁性阳离子凝胶对活性橙 K-GN的吸附量 Qe都呈现下降趋势,酸性条件有利于磁性阳离子凝胶对活性橙K-GN的吸附,这是因为酸性环境下,体系中H+浓度升高,凝胶分子上的胺基质子化程度提高,其所带正电荷数量增加使得饱和吸附量增加,更有利于吸附进行。若在碱性环境下,体系中的OH-会与溶液中的染料分子发生竞争,导致吸附量下降[5]。
3.5 磁性阳离子凝胶对活性橙 K-GN的吸附动力学研究
吸附动力学通常用来描述吸附剂吸附溶质的速率特征,准一级和准二级动力学模型,其方程表达形式如下:

其中,k1(min-1)和 k2(g·mg-1·min-1)分别是磁性阳离子凝胶吸附活性橙K-GN的准一级和准二级动力学方程的吸附常数;Qe和Qt分别是磁性阳离子凝胶吸附活性橙K-GN的平衡吸附量和t时刻的吸附量(mg·g-1)。
实验数据拟合结果如图5所示,其动力学模型参数如表1所示。
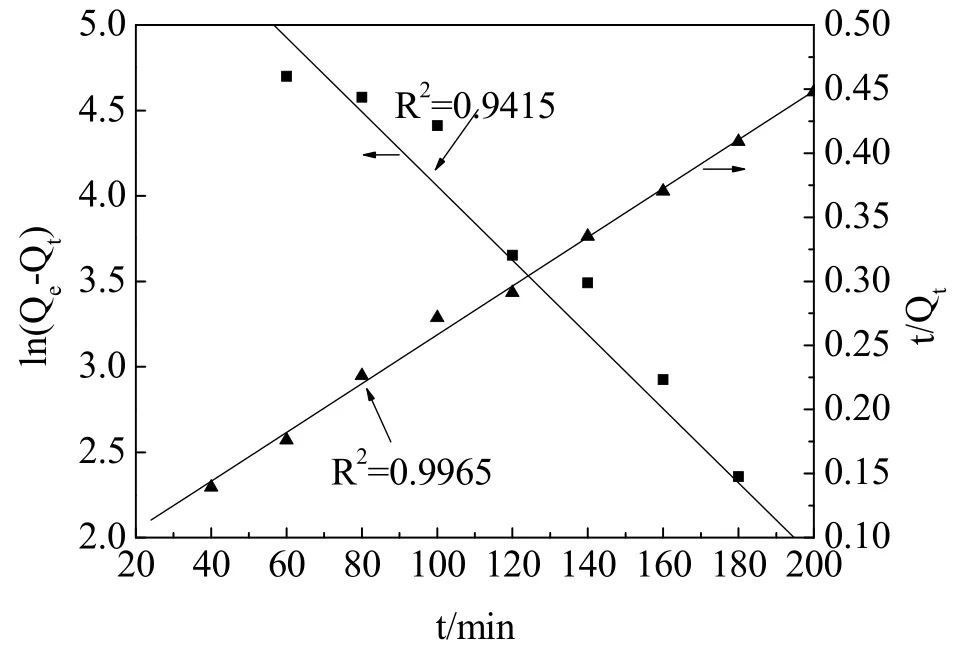
图5 准一级和准二级动力学模型拟合曲线

表1 动力学模型参数
由图5可以看出,拟合的准一级和准二级的力学模型都可以较好描述磁性阳离子凝胶对活性橙K-GN的吸附过程。由表1可知,拟一级动力学模型的平衡吸附量Qe为533.6 mg·g-1,R2为0.941 5;拟二级动力学模型的Qe为 526.3 mg·g-1,R2为 0.996 5。这说明实验结果更符合准二级动力学模型。根据二级动力学原理,吸附过程受磁性阳离子凝胶的性质和染料溶液共同影响。
3.6 等温吸附平衡研究
分别研究30 ℃、40 ℃、50 ℃三种温度下的Qe-C吸附等温线如图6所示。
数据采用 Langmuir吸附模型和 Freundlich吸附模型对等温吸附平衡进行分析,两种吸附模型分别由公式(5)和(6)表示,拟合结果如图7、图8和表2。

其中,Qe和Qm分别是吸附平衡时吸附容量和单分子层吸附时最大吸附量(mg·g-1);Ce是吸附平衡时浓度(mg·L-1);k则是 Langmuir吸附平衡常数;K是Freundlich吸附平衡常数;n则是吸附过程指标,1/n小于 0,吸附是物理吸附,反之,则为化学吸附。

图6 活性橙K-GN的Qe-C吸附等温线图
由图6可知,三种温度下,磁性阳离子凝胶对活性橙K-GN染料的吸附量呈现先增大后趋于平衡的趋势。
由图6可得,磁性阳离子凝胶吸附的活性橙K-GN浓度越大,平衡吸附量Qe越大,活性橙K-G0N的初始浓度越低,吸附量随浓度变化明显,活性橙K-GN的初始浓度较高时平衡吸附量Qe趋于平缓,这主要是因为随着磁性阳离子凝胶与活性橙 K-GN模拟废水染液之间的浓度差加大,两者之间产生的传质推动力也随着增大,这就促进吸附过程的进行,吸附量增大[9];但当染料分子占满磁性水凝胶的三维网络空间之后,染料的吸附达到饱和,吸附量趋于平衡[10]。由图6还可看出,不同温度下的饱和吸附量也不一样。提高温度,磁性阳离子凝胶对活性橙K-GN的吸附量逐渐上升。这是因为升高温度,活性橙K-GN的染料分子活性增加,加剧运动,促进吸附。
从表2可以看出 Langmuir模型拟合的效果更好,磁性阳离子凝胶的吸附量随着温度的升高而增大。Freundlich模型中,n-1为吸附指数,n-1<0.5 易吸附;n-1=0.5~1 较难吸附;n-1>1 难以吸附[11,12]。由表1可知,n-1均小于0.2,表明磁性阳离子凝胶对活性橙K-GN具有较好的吸附性能,可作为吸附活性染料的吸附剂。

图7 Langmuir等温线拟合曲线
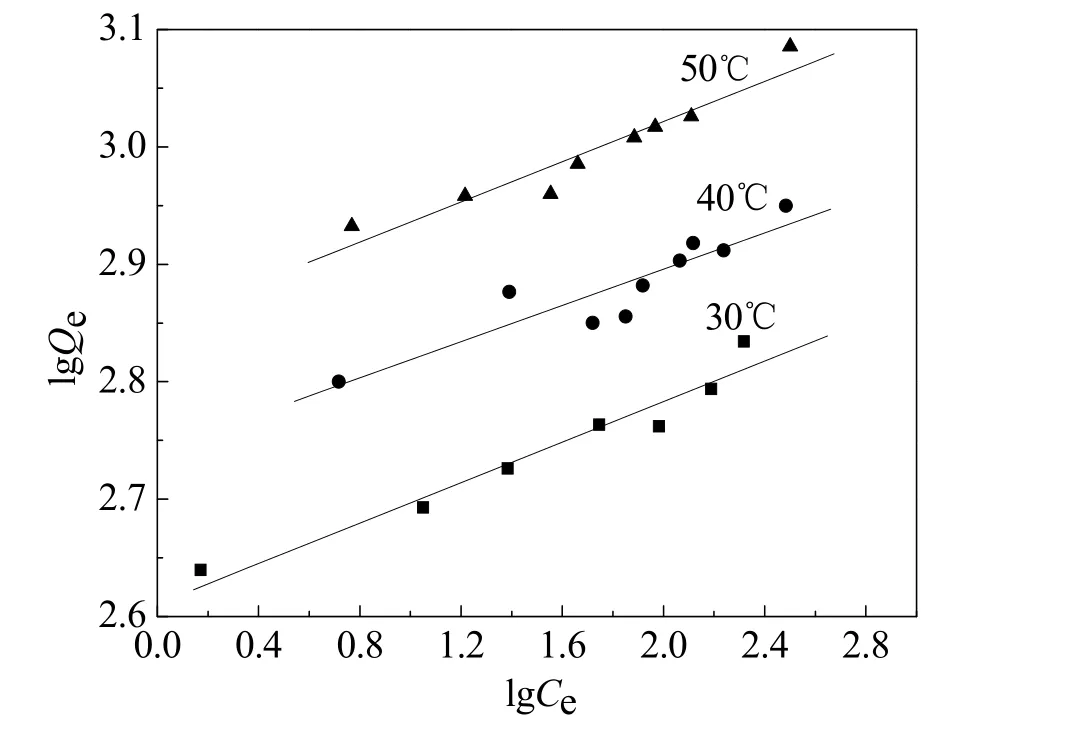
图8 Freundlich等温线拟合曲线
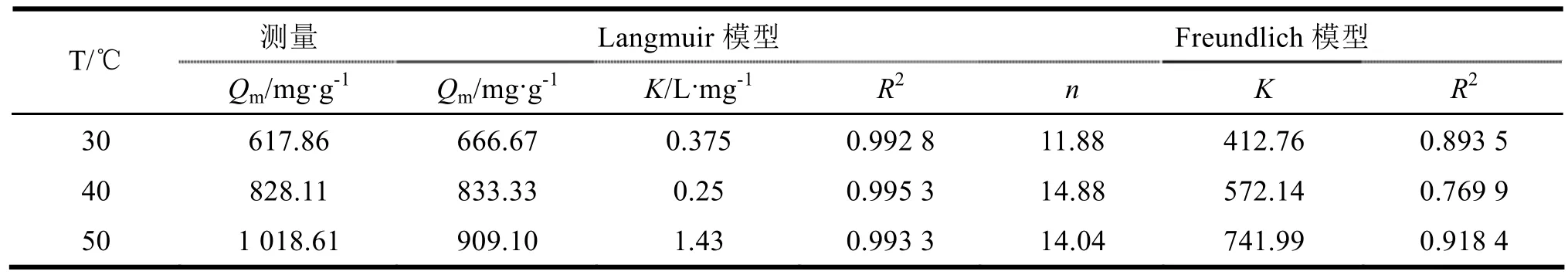
表2 磁性水凝胶对活性橙K-GN吸附的等温吸附参数
3.7 磁性阳离子水凝胶对活性橙 K-GN吸附的热力学参数
磁性阳离子凝胶分别在30 ℃、40 ℃和50 ℃下对染料溶液进行恒温吸附,ΔG、ΔH和ΔS是测定吸附过程自发性和热量变化的标准态热力学参数[13]。假设在低温下,活度系数不发生变化,ΔH和ΔS为常数,热力学参数可通过对热力学参数按公式(7)和(8)进行拟合处理[14,15]。式中k为Langmuir等温方程中的吸附平衡常数k,拟合结果如表3所示。

由表 3中数据可知,ΔG<0,表明反应体系是自发进行的,ΔH>0则表明反应过程是吸热的,ΔS>0,则表明温度影响反应体系自发程度,温度越高,越有利于反应正向自发进行。
3.8 重复利用的可行性
从图4中pH值对吸附效果的影响可知,在碱性条件下,磁性水凝胶球对活性橙K-GN吸附作用下降。采用0.1 mol·L-1NaOH和去离子水对磁性水凝胶进行降活清洗4次后,磁性水凝胶对活性橙K-GN溶液的去除率分别为94%,92%,88%,85%。
4 结论
吸附量随着吸附剂用量增大而减小,脱色率随着吸附剂用量的增大而增大,当吸附剂用量达到0.18 g·L-1时,活性橙K-GN溶液的脱色率达到 98%以上。酸性环境下更有利于吸附剂吸附,在pH=4的时候吸附效果最好,吸附量达到 435.8 mg·g-1。磁性水凝胶对活性橙 K-GN的吸附过程符合拟二级动力学模型,平衡吸附量为526.3 mg·g-1。在 30 ℃、40 ℃、50 ℃三个温度下的吸附量分别为 666.67 mg·g-1、833.33 mg·g-1、909.10 mg·g-1。等温吸附平衡用 Langmuir模型拟合的效果更好,R2均大于0.99。热力学研究结果表明,反应为吸热反应,升高温度有利于吸附,且吸附过程以物理吸附为主。经过4次重复使用,磁性水凝胶仍具有较好的吸附效果,可进行多次循环使用。
[1] Barros W R P, Steter J R, Lanza M R V, et al.Degradation of Amaranth Dye in Alkaline Medium by Ultrasonic Cavitation Coupled with Electrochemical Oxidation Using a Boron-doped Diamond Anode[J].Electrochimica Acta, 2014, 143(10): 180-187.
[2] Elghenymy A, Centellas F, Garrido J A, et al. Decolorization and Mineralization of Orange G Azo Dye Solutions by Anodic Oxidation with a Boron-doped Diamond Anode in Divided and Undivided Tank Reactors [J]. Electrochimica Acta, 2014, 130(130): 568-576.
[3] Baran A, Bicak E, Baysal S H, et al. Comparative studies on the adsorption of Cr(VI) ions on to various sorbents[J] Bioresource Technology, 2006, 98(3): 661- 665.
[4] Boddu V M, Abburi K, Talbott J L, et al. Removal of hexavalent chromium from wastewater using a new composite chitosan biosorbent[J]. Environ Sci Technol,2003, 37(19): 4449-4456.
[5] 陈丽滨,方润,王淑玲.新型阳离子凝胶吸附剂对活性橙的吸附研究[J].广州化学,2015,40(3):7-12.
[6] 杜庆波,蔡红,朱军,等.水热法制备Fe2O3微纳米材料及其磁性研究[J].硅酸盐通报,2015,34(11):3287-3291.
[7] 方润,陈毅挺,吴华忠.球形阳离子凝胶的制备及吸附性能研究[J].高分子通报,2017,(2):39-45.
[8] 周国江,刘红斌,刘丽来,等.PVP辅助水热法制备Fe2O3/石墨烯纳米复合材料[J].黑龙江科技大学学报,2014,44(1):70-73.
[9] 许慧丽,徐铸德,黄宛真.不同形貌的 α-Fe2O3的水热控制合成[J].浙江大学学报(理学版),2008,(5):546-549.
[10] 李小红,江向平,文思逸,等.不同形貌纳米 α-Fe2O3粉体水热合成及其催化高氯酸铵热分解研究[J].人工晶学学报,2013,(6):1132-1137.
[11] Klimaviciute R, Bendoraitiene J, Rutkaite R, et al.Adsorption of Hexavalent Chromium on Cationic Cross-linked Starches of Different Botanic Origins[J].J. Hazard. Mater., 2010, 181: 624-632.
[12] Stellacci P, Liberti L, Notamicola M, et al. Valorization of Coal Fly Ash by Mechano chemical Activation: Part I. Enhancing Adsorption Capacity[J]. Chem. Eng. J.,2009, 149: 11-18.
[13] 张志辉,刘晓伟,宋来洲.DTPA-MA/PVDF共混膜对Ni2+吸附性能的研究[J].唐山师范学院学报,2010,32(2):16-20.
[14] 周伟,唐宇,谢欢,等.离子交换树脂吸附更昔洛韦的动力学与热力学研究[J].中国药学杂志,2009,17(44):1327-1331.
[15] 彭书传,王诗生,陈天虎,等.凹凸棒石吸附水溶性染料的热力学研究[J].硅酸盐学报,2005,33(8):1012-1017.
