注射用黄芪多糖单糖鉴别及游离单糖检查方法研究
2018-06-12赵剑锋张建宝金红宇马双成
王 赵 ,赵剑锋 ,王 莹 ,张建宝 ,金红宇 ,马双成 △
(1.中国食品药品检定研究院,北京 100050; 2.国家药典委员会,北京 100061;3.天津赛诺制药有限公司,天津 301700)
注射用黄芪多糖为肿瘤辅助用药,功能益气补虚,用于倦怠乏力,少气懒言,自汗、气短、食欲不振,属气虚证因化学治疗后白细胞减少,生活质量降低,免疫功能低下的肿瘤患者[1]。注射用黄芪多糖是利用现代分离技术提取分离黄芪中的多糖有效部位,并纯化精制而成。注射用黄芪多糖由天津赛诺制药有限公司生产,于2001年取得新药证书,现行标准为WS-330(Z-030)-2001(试行),其中前处理过程需使用高毒试剂(碳酸钡与硫酸溶液反应产生Ba2+),此外,纸色谱目前已较少使用,且3种单糖分离效果不明显。基于以上不足,本研究中对质量标准“单糖鉴别”“游离单糖检查”项[2]进行了深入探讨,改进样品前处理方法,采用硅胶G板优化分离条件,建立了注射用黄芪多糖水解产物的鉴别方法及注射用黄芪多糖中游离单糖的检查方法。现报道如下。
1 仪器与试药
Linomat-Ⅳ型薄层自动点样仪(瑞士CAMAG公司);Visualizer型薄层色谱照相系统型,包括VinCAYTS薄层色谱软件(瑞士CAMAG公司);KQ-30012D型超声波清洗器(昆山市超声仪器有限公司);AE-240型分析天平(万分之一,Metter公司);P-1型双槽展开缸(200 mm×100 mm);3030-861型硅胶 G 板(20 cm×20 cm,德国默克公司),3030-861型微晶纤维素板(20 cm ×20 cm, whatmanTM),纸薄层板(型号不详)。葡萄糖对照品(Glu,批号为 110833-201205,含量为99.5% ),半乳糖对照品(Gal,批号为 100226 - 201105,含量为99.9%),半乳糖醛酸对照品(批号为111646-200301,纯度大于98%),均购自中国食品药品检定研究院;阿拉伯糖对照品(Ara,批号为 C10297500,含量为 99.0% ),鼠李糖 对照 品(Rha,C16813500,含 量为98.3%),均购自 Dr.EhrenstoferGmbH;注射用黄芪多糖(批号为 150702,151201,151101,M150701,M151001,天津赛诺制药有限公司);所用试剂均为分析纯。
2 方法与结果
2.1 单糖鉴别
2.1.1 现行方法[3]
鉴别:取本品 0.2 g,加 1 moL /L 硫酸溶液 25 mL,置水浴中水解 7 h,取出,放冷,取 5 mL,加碳酸钡(固体)中和至中性,滤过,滤液作为供试品溶液。另取葡萄糖和阿拉伯糖对照品,分别加水制成每1 mL含5 mg的溶液,作为对照品溶液。照纸色谱法试验,吸取上述供试品溶液10 μL、对照品溶液各4 μL,分别点于同一新华中速层析滤纸上,以醋酸乙酯-甲酸-水(6∶2∶2)为展开剂,展开,取出,晾干,喷以苯胺-邻苯二甲酸溶液(取苯胺0.93 g和邻苯二甲酸1.66 g,溶于水饱和正丁醇100 mL中),在105℃烘约5 min。供试品溶液色谱中,在与对照品溶液色谱相应位置上显相同颜色的斑点。纸色谱图见图1。

图1 纸色谱图
检查:取本品,加水制成每1 mL含20 mg的溶液,作为供试品溶液。另取葡萄糖和阿拉伯糖对照品,分别加水制成每1 mL含5 mg的溶液,作为对照品溶液。照2000年版《中国药典(一部)》附录ⅥB薄层色谱法试验,吸取上述供试品溶液 10 μL,对照品溶液各 2 μL,分别点于同一硅胶G薄层板上,以正丁醇-0.1 moL/L磷酸二氢钠溶液-丙酮(4∶1∶5)为展开剂,展开,取出,晾干,喷以 α-萘酚试液,在 90~100℃烘约 5 min。供试品溶液色谱中,在与对照品溶液色谱相应位置上,未显相同颜色的斑点。
2.1.2 改进方法
鉴别:取黄芪多糖20 mg,加水5 mL使溶解。取1 mL,加 6 mol/L 三氟乙酸(TFA)1 mL,密封,于 110 ℃反应6 h;氮气吹干,加甲醇约1 mL,吹干,再重复操作1次,以除尽剩余的TFA,残渣加水0.5 mL溶解,作为供试品溶液。另取葡萄糖、阿拉伯糖、半乳糖适量,加水制成每1 mL分别含1 mg的溶液,作为对照品溶液。照薄层色谱法(2015年版《中国药典<四部>》通则 0502)试验,吸取上述供试品溶液 5 μL、对照品溶液 1 ~5 μL,分别点于同一Merck硅胶G60薄层板上,以正丁醇-乙酸乙酯 -异丙醇 -乙酸 -吡啶 -水(7∶20∶12∶7∶6∶5)为展开剂,二次展开,展距9 cm,取出,晾干,喷以苯胺-邻苯二甲酸溶液(取苯胺0.93 g和邻苯二甲酸1.66 g,溶于水饱和正丁醇100 mL中),在105℃烘约5 min,置紫外光灯(365 nm)下检视。供试品溶液色谱中,在与对照品溶液色谱相应位置上,显相同颜色的荧光斑点。色谱图见图2。
图2 薄层色谱图
检查:取本品20 mg,加水1 mL使溶解,作为供试品溶液。照鉴别方法试验。供试品溶液色谱中,在与对照品溶液色谱相应位置上未显相同颜色的荧光斑点。
2.1.3 方法学考察
薄层板考察:首先考察纤维素板的分离效果[5],结果单糖斑点较大,产生拖尾现象,各单糖分离效果不明显,详见图3。比较硅胶H板与硅胶G板的差异,发现硅胶H板因不含黏合剂,在展开过程中经常出现吸附薄层脱落的现象,且分离效果不好,硅胶G板效果较好,且硅胶略带酸性,适于分离酸性及中性物质,目前应用广泛,便于实验室准备耗材。最终选择硅胶G板。

图3 微晶纤维素薄层色谱图
展开系统考察:参考文献[6-9],考察了不同展开剂系统(Ⅰ~Ⅳ)的分离效果,系统Ⅰ正丁醇-0.1 mol/L磷酸二氢钠溶液-丙酮(4∶1∶5)、系统Ⅱ正丁醇-丙酮-水(5∶1∶1)、系统Ⅲ正丁醇 -乙酸乙酯 -水(7∶2∶1)、系统Ⅳ正丁醇-醋酸乙酯-异丙醇-乙酸-吡啶-水(7∶20∶12∶7∶6∶5);同时,采用展开剂系统Ⅳ二次展开。结果展开剂系统Ⅰ展开,单糖斑点较大,有拖尾现象;展开剂系统Ⅱ,Ⅲ,Ⅳ展开,单糖斑点较好,但水解黄芪多糖样品分离不完全。最终选择了使用展开剂系统Ⅳ(正丁醇-醋酸乙酯-异丙醇 -乙酸 -吡啶 -水 =7∶20∶12∶7∶6∶5)二次展开作为修订标准的展开系统。薄层色谱图见图4。
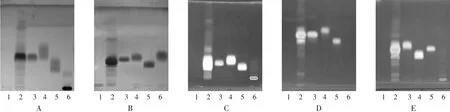
图4 展开系统薄层色谱图
显色剂考察[8-10]:考察苯胺-邻苯二甲酸显色剂在日光、366 nm荧光、茴香醛及α-萘酚显色剂的显色效果,以展开剂系统Ⅳ作为展开剂及展开方法,点样量分别为 10,10,10,5,2,10 μL。结果见图 4 E 和图 5。最终确定使用苯胺-邻苯二甲酸显色剂(366 nm荧光下)检视。

图5 展示系统二次展开显色剂薄层色谱图
展开温度和湿度考察:考察薄层板展开过程中温度和相对湿度对结果的影响,结果表明,温度为10,20,30℃时,各指标成分斑点的 Rf值影响不大,对分离效果几乎无影响;相对湿度为30%,50%,75%时,各指标成分斑点的 Rf值影响不大,对分离效果也几乎无影响。
点样量考察:经试验对比发现,减少点样量有利于提高分离效果,建议点样量固定为“供试品溶液5 μL,对照品溶液 1 ~5 μL”。
2.2 游离单糖检查
2.2.1 色谱条件[4-11]与系统适用性试验
色谱柱:Spolar C18柱(250 mm × 4.6 mm,5 μm);流动相:乙腈 -0.1 mol/L 乙酸铵(体积比为 21 ∶79,加冰醋酸调节 pH 为 5.5);流速:1.0 mL /min;柱温:35 ℃;检测波长:250 nm;进样量:10 μL。水解后黄芪多糖样品中出现5个单糖的色谱峰,以葡萄糖、半乳糖和阿拉伯糖色谱峰为主,未水解黄芪多糖样品中未出现单糖色谱峰。色谱图见图6。
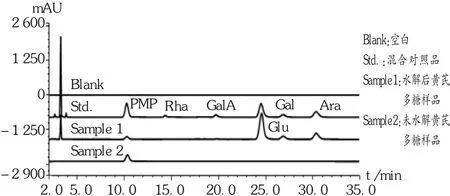
图6 高效液相色谱图
2.2.2 溶液制备
分别精密称取鼠李糖、半乳糖醛酸、葡萄糖、半乳糖、阿拉伯糖适量,配制成适宜浓度的混合对照品溶液。定量吸取上述溶液 500 μL,加 0.3 mol/L 氢氧化钠溶液 67 μL,再加入 0.5 mol/L PMP 甲醇溶液 150 μL,搅拌均匀,于 70 ℃反应 90 min。冷却至室温,加 0.3 mol/L盐酸溶液67 μL中和。加1 mL氯仿萃取,分去下层有机层,重复萃取3次,取上层溶液,作为对照品溶液。
取黄芪多糖样品约20 mg,精密称定,加水制成每1 mL约含4.0 mg的溶液,定量吸取250 μL,置安瓿中,加入等体积的6 mol/L三氟乙酸,密闭,于110℃反应6 h。氮气吹干,加适量甲醇,再吹干,重复3次,以除尽剩余三氟乙酸。加水500 μL,使残渣溶解。照对照品溶液制备“加 0.3 mol/L 氢氧化钠溶液 67 μL”起同法处理,取上层溶液,作为供试品溶液1。另取黄芪多糖,加水制成每1 mL含1 mg的溶液,定量吸取500 μL,照对照品溶液制备“加 0.3 mol/L 氢氧化钠溶液 67 μL”起同法处理,取上层溶液,作为供试品溶液2。
2.2.3 方法学考察
日间精密度试验:取样品(批号为151101),按不同日期依法制备供试品溶液,依法测定。结果见表1。可见,日间精密度 RSD偏大,重复性差,建议仅用作定性鉴别。
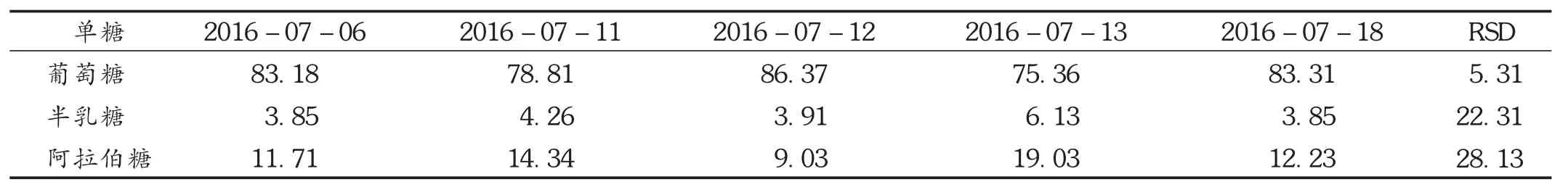
表1 日间精密度试验结果(%,n=6)
稳定性试验:取样品(批号为151101),精密称取20 mg,于 0,1,2,6,12,24,36 h 时依法测定,结果见表 2。其中,半乳糖 RSD偏大,但符合鉴别方法要求,表明葡萄糖和阿拉伯糖在36 h内基本稳定。
加样回收试验:取样品(批号为151101)适量,依法制备供试品溶液,按拟订色谱条件测定。结果见表3。
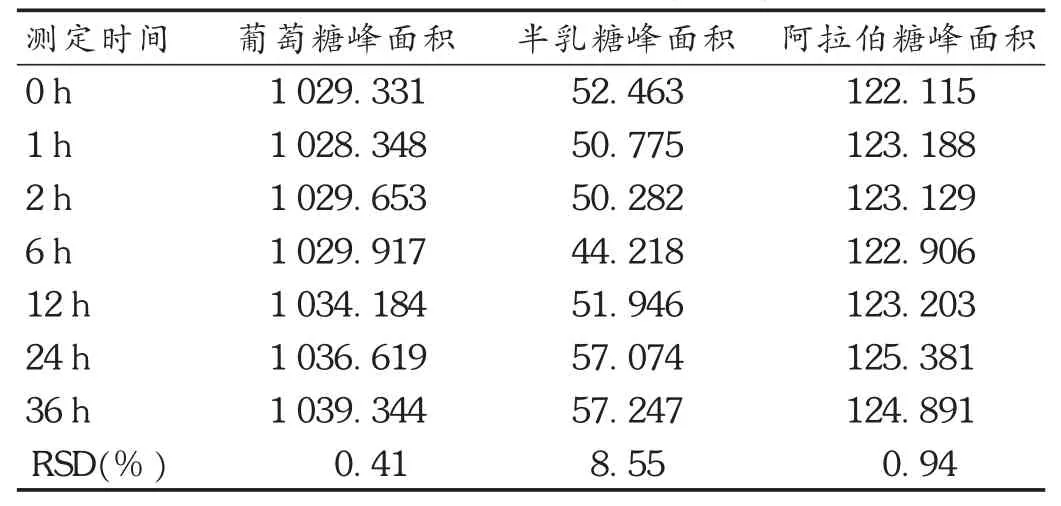
表2 稳定性试验结果(n=7)

表3 加样回收试验结果(n=6)
3 讨论
通过对质量标准“单糖鉴别”“游离单糖检查”项进行研究,改进了样品前处理方法,避免出现高毒离子(Ba2+),此外,通过采用实验室常用的硅胶G板分离黄芪多糖水解产物,优化了分离条件,使单糖分离效果明显。将原标准中检查项下“游离单糖”的检查与此薄层鉴别方法合并,同时进行单糖鉴别和游离单糖的检查,大大提高了工作效率,减少了试剂的使用。
对混合单糖进行分离比较困难,尤其是葡萄糖和阿拉伯糖在硅胶板上的分离。本研究中对多种薄层色谱条件进行了考察,对于其他单糖的薄层鉴别具有参考价值。
本研究中采用高效液相色谱法对注射用黄芪多糖的单糖组成进行了初步研究,先将注射用黄芪多糖用三氟乙酸水解,然后进行PMP衍生化处理,紫外吸收后进行高效液相色谱数据采集,色谱峰峰形较好,5种单糖分离完全。故可用于注射用黄芪多糖中单糖组成的鉴别及游离单糖的检查。
高效液相色谱法方法学考察结果显示,葡萄糖、半乳糖、阿拉伯糖回收率及稳定性结果基本符合定量测定要求,但日间精密度 RSD值偏大,重复性差,建议仅作定性鉴别使用。
薄层色谱方法是中药鉴别常用方法之一,其简单、方便、经济等优势在中药质量控制中有着不可替代的地位,由于纸色谱目前已逐渐被其他方法取代,本研究将硅胶G板薄层鉴别替代纸色谱鉴别用于黄芪多糖注射液质量标准中单糖的研究,并建立了黄芪多糖的高效液相色谱鉴别和检查方法,安全、准确,可用于注射用黄芪多糖的质量控制。
[1]张 莹,王 蕾,杜梦楠.注射用黄芪多糖治疗肿瘤的临床研究进展[J].药物评价研究,2016,39(6):1092 -1094.
[2]范慧红.2010年版中国药典中多糖类药物标准的修订[J].中国药学杂志,2010,45(17):1294 - 1297.
[3]WS-330(Z-030)-2001,国家药品监督管理局标准(试行)注射用黄芪多糖[S].
[4]许杜鹃,夏 泉,刘 钢,等.高效液相法测定黄芪中性多糖的单糖组成[J].中国实验方剂学杂志,2008,14(9):4-6.
[5]刘 柳,李 莉,张庆林,等.微晶纤维素薄层色谱法分析荨麻多糖中的单糖组成[J].中国实验方剂学杂志,2008,14(6):17-18.
[6]刘秀花,王 莉,张淑红,等.玉米芯降解液糖类成分薄层色谱法分析技术优化[J].商丘师范学院学报,2014,30(9):56.
[7]颜 军,郭晓强,李晓光,等.TLC快速分析多糖的单糖组成[J].食品科学,2006,27(12):603-606.
[8]钱夕惠.薄层色谱法分析灵芝多糖中的单糖组成[J].中国现代药物应用,2013,7(18):13-14.
[9]李继民,王彦吉,邹 宁,等.薄层色谱法测定纸张水解液中单糖的研究[J].纤维素科学与技术,2008,16(2):43-47.
[10]国家药典委员会.中华人民共和国药典(一部)[M].北京:中国医药科技出版社,2015:188.
[11]陈虎虎,孙 静,杨金颖,等.柱前衍生化-高效液相色谱法测定蒙古黄芪多糖中单糖的组成[J].现代药物与临床,2012,27(5):468-470.
