葡萄糖注射液中注射用血栓通与胰岛素配伍稳定性考察*
2018-06-12王耀华孙志强孙冬晓贾聚坤任晓华
彭 雯 ,王耀华 ,孙志强 ,孙冬晓 ,贾聚坤 ,孟 岩 ,任晓华
(1.河北省石家庄市第一医院,河北 石家庄 050011; 2.河北大学附属医院,河北 保定 050017)
注射用血栓通是从中药三七中提取有效活性成分制成的一种纯中药制剂,主要成分为三七总皂苷,具有活血祛瘀、通脉活络的功效,主要用于治疗中风偏瘫、瘀血阻络及脑血管疾病后遗症、视网膜中央静脉阻塞属瘀血阻滞证[1],广泛用于心脑血管系统、呼吸系统及内分泌系统疾病等[2]。其药品说明书规定:本品应以10%葡萄糖注射液250~500 mL稀释后缓慢静脉滴注,1日1次。临床部分患者会同时患有糖尿病,因此需要在注射用血栓通与葡萄糖配伍溶液中加入胰岛素,以防糖耐量异常或血糖升高。此方法为临床经验性配伍用药,其安全性无确切依据,国内外文献鲜有报道。本研究中考察了注射用血栓通与胰岛素在葡萄糖注射液中的配伍稳定性,现报道如下。
1 仪器与试剂
1.1 仪器
LC-10ATVP型高效液相色谱仪(日本岛津公司);UV-1901型双光束紫外分光光度计(普析通用,检测精度为2%);DELTA320型 pH计(梅特勒-托利多仪器有限公司,检测精度为0.1);GWF-5J型微粒分析仪(天津天河医疗仪器有限公司)。
1.2 试药
注射用血栓通(广西梧州制药股份有限公司,批号为20160107,规格为每支250 mg);胰岛素注射液(江苏万邦生化医药股份有限公司,批号为1601103,规格为每支10 mL∶400 U),10%葡萄糖注射液(北京双鹤药业股份有限公司,批号为1602025,规格为每瓶250 mL);胰岛素对照品(中国食品药品检定研究院,批号为7337865,规格为2 mg);三七总皂苷对照品(中国食品药品检定研究院,批号为150720-201509,规格为20 mg);甲醇(Fisher公司,4 L,色谱纯),乙腈(Fisher公司,4 L,色谱纯);水(屈臣氏蒸馏水,批号为 20160201);磷酸(H3PO4,批号为 79622 - 500 g),无水硫酸钠(Na2SO4,批号为 239313-500 g),均购自 Sigma公司,均为分析纯。
2 方法与结果
2.1 三七总皂苷含量测定方法的建立[3-5]
2.1.1 检测波长选择
精密称取三七总皂苷,加乙醇溶解,稀释至0.1 g/L,乙醇为空白对照,在190~400 nm波长范围内进行扫描。检测到三七总皂苷在317 nm波长处有较大吸收。重复实验并参考文献[5-7],确定317 nm为三七总皂苷的检测波长。
2.1.2 方法学考察
线性关系考察:取三七总皂苷标准品,精密称取0.016 0 g,置100 mL容量瓶中,加乙醇超声溶解定容,得质量浓度为0.16 g/L的贮备液,精密量取该贮备液1,2,4,8,10 mL,分别置 5 个 100 mL 容量瓶中,并加乙醇定容,超声充分溶解,制得不同质量浓度的溶液。以质量浓度为横坐标(X)、吸光度为纵坐标(Y)进行线性回归,得回归方程 Y=4.357×10-3X+9.216×10-3,r=0.999 9。结果三七总皂苷质量浓度在 1.6 ~ 16.0 μg/mL 范围内与吸光度线性关系良好。
精密度试验:取线性关系考察项下 6.4 μg/mL的供试品适量,依法制备供试品溶液,连续测定6次。结果的RSD为1.21%(n=6),表明仪器精密度良好。
稳定性试验:取精密度试验项下的供试品溶液,分别于 0,1,2,4,6,8,12 h 时测定吸光度值。结果的 RSD 为1.08%(n=6),表明供试品溶液在12 h内稳定性良好。
重复性试验:取同一批三七总皂苷对照品,按线性关系项下方法制备5份供试品溶液,分别精密吸取1.6 μg/mL进样测定,记录峰面积。结果三七总皂苷的RSD为1.31%(n=5),表明方法重复性良好。
加样回收试验:取样品(批号为20160107),精密称定6份,每份约1 mg,分别加入一定量的三七总皂苷标准品,置100 mL容量瓶中,加乙醇摇匀,充分溶解后定容。测定其吸光度值,计算回收率,结果见表1。

表1 三七总皂苷加样回收试验结果(n=6)
2.1.3 干扰试验
模拟临床用药,取样品250 mg溶于10%葡萄糖注射液500 mL中,并加入8 U胰岛素作为供试品;取样品250 mg溶于500 mL乙醇作为空白对照,分别均匀混合后测定其吸光度值,平行测定3次,结果无差异。表明此条件下加入胰岛素的葡萄糖注射液不影响三七总皂苷的含量测定。
2.2 胰岛素含量测定方法的建立[6-7]
2.2.1 色谱条件
色谱柱:Phenomenex luna C18柱(250 mm ×4.6 mm,5 μm);流动相:0.2 mol/L 硫酸盐溶液(取无水硫酸钠 28.4 g,加水溶解并加磷酸 2.7 mL,用乙醇胺调节pH 至 2.3,定容至 1 000 mL)-乙腈(74 ∶26);流速:1.0 mL /min;柱温:40 ℃;检测波长:317 nm;进样量:20 μL。
2.2.2 溶液制备
按照临床经验性用药,将注射用血栓通250 mg与10%葡萄糖注射液500 mL溶解后加入8 U胰岛素,充分混合均匀,得供试品溶液。取胰岛素对照品1.923mg,精密称定,用0.01 mol/mL稀盐酸配制成10 U/mL对照品贮备液。
2.2.3 方法学考察
线性关系考察:分别精密量取上述对照品贮备液0.05,0.10,0.30,0.50,1.00 mL 定容至 100 mL 容量瓶中,得质量浓度为 0.005,0.01,0.03,0.05,0.10 U /mL的胰岛素溶液。取上述溶液各20 μL进样,按拟订色谱条件进样分析,记录峰面积,以质量浓度为横坐标(X)、峰面积为纵坐标(Y)绘制标准曲线,得回归方程 Y=6.192 3×103X-4.028 1,r=0.999 9。结果表明,胰岛素质量浓度在0.005~0.100 U/mL范围内与峰面积线性关系良好。
精密度试验:取线性关系项下配置的10 U/mL胰岛素溶液连续进样6次,按拟订色谱条件分析,记录峰面积。结果的 RSD为0.87%(n=6),表明仪器精密度良好。
稳定性试验:取线性关系项下配置的10 U/mL胰岛素溶液,在放置 0,1,2,4,6,8 h 后分别进样,按拟订色谱条件分析,记录峰面积。结果的 RSD为1.04%(n=6),表明供试品溶液在8 h内稳定性好。
重复性试验:取同一批胰岛素对照品,按拟订方法制备供试品溶液5份,分别精密吸取供试品溶液进样,记录峰面积。结果的 RSD为1.25%(n=6),表明方法重复性良好。
加样回收试验:取线性关系项下配置的10 U/mL供试品溶液,分别加入8,10,12 U胰岛素注射液,每组重复进样2次,计算回收率。结果见表2。

表2 胰岛素加样回收试验结果(n=6)
2.2.4 干扰试验
模拟临床用药,将注射用血栓通冻干粉250 mg溶于10%葡萄糖注射液500 mL中,并加入8 U胰岛素,按拟订色谱条件进样测定,记录色谱图(图1)。可见,此条件下注射用血栓通与葡萄糖注射液的配伍不会影响胰岛素的含量测定。
2.3 配伍稳定性试验
模拟临床用药方式,分别配置配伍液(A溶液、B溶液),A溶液为注射用血栓通冻干粉250 mg溶于10%葡萄糖注射液500 mL中,B溶液为注射用血栓通冻干粉250 mg溶于10%葡萄糖注射液500 mL后加入8 U胰岛素注射液,充分摇匀并置于室温下,在 0,1,2,4,6,8,12 h时分别观察及测定其外观、pH、不溶性微粒、含量[8-9]。

图1 高效液相色谱图
外观:将A溶液和B溶液分别加入干净的10 mL具塞比色管中,在澄明度检测仪下对其进行澄明度、颜色的观察,记录 0,1,2,4,6,8,12 h 时瓶中药液有无变化,是否存在白点、碎屑、不溶物等及颜色改变。结果显示,在不同时间点内,A溶液、B溶液外观均澄清透明、无浑浊、沉淀产生,但在6 h后均有颜色变深的趋势。
pH:将A溶液和B溶液在精密酸度计下测定0,2,4,6,8,12 h 时的 pH,结果见表 3。对两组数据进行 t检验,无显著性差异(P>0.05)。表明注射用血栓通与胰岛素在10%葡萄糖注射液中的配伍液12 h内pH稳定。
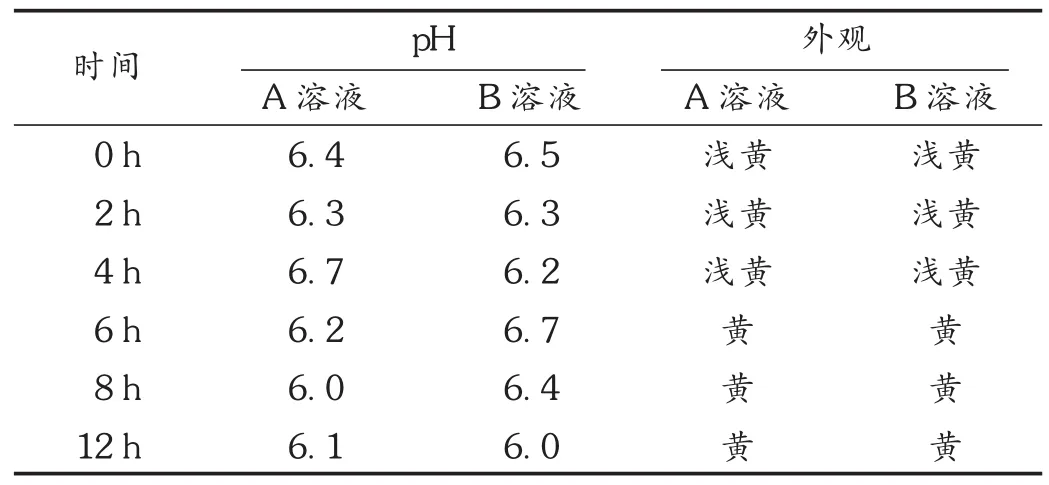
表3 配伍液在不同时间点pH和外观变化
不溶性微粒:将A溶液、B溶液配伍液在澄明度检测仪下按照2015年版《中国药典(二部)》微粒检测法中的光阻法检查不同时间点的微粒数,记录≥10 μm、≥25 μm的微粒数,同一样品连续测定5组,取平均值[10-12],结果见表4。药典规定大于10 μm不溶性微粒数应不大于25粒/mL,大于25μm的不溶性微粒数应不大于3粒/mL。由表4可见,两组配伍液微粒数在2 h内变化不大;2~8 h配伍液微粒数有所上升,但均符合药典规定;12 h测定的微粒数已超出药典要求。

表4 配伍液不溶性微粒数试验结果(n=5,粒/mL)
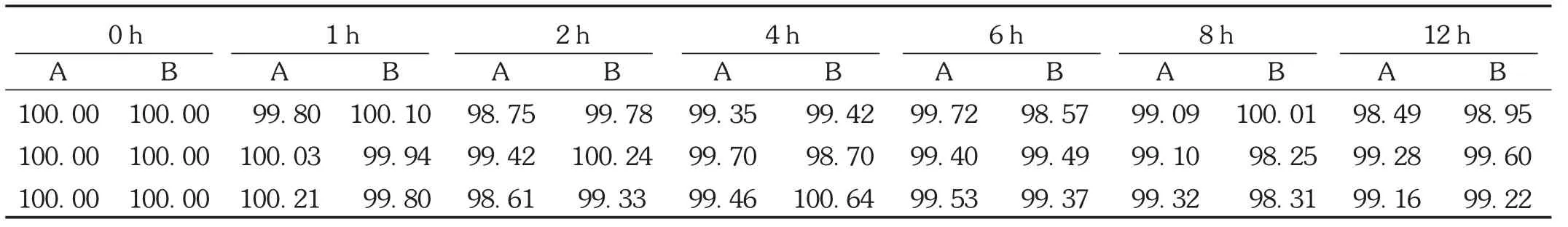
表5 配伍液中三七总皂苷和胰岛素含量测定结果(n=3,%)
含量测定:取B溶液,在317 nm波长下对三七总皂苷的含量进行紫外分光光度检测,记录其吸光度值;再精密量取 10 μL,按 2.2项下色谱条件进样分析,记录色谱峰面积和保留时间。以0 h时的含量为100.00%,分别测定配伍液中三七总皂苷和胰岛素的含量变化情况,平行测定3次,详见表5。结果表明,12 h内配伍液中三七总皂苷和胰岛素的含量略有下降,但变化很小,相对含量均大于98.25%。
3 讨论
采用2015年版《中国药典(二部)》中高效液相色谱法考察胰岛素在配伍液中的变化,结果重复性好、灵敏度高,结果可靠。三七总皂苷的含量测定方法有重量法、比色法、高效液相色谱法。其中,重量法由于杂质不易除净,试验结果通常偏高;高效液相色谱法测定较复杂,需要对三七总皂苷中的每种成分分别进行方法学考察。因此,本试验采用比色法对三七总皂苷进行研究。
由本研究结果可知,在室温下,注射用血栓通与胰岛素在10%葡萄糖注射液中配伍,12 h内无浑浊及沉淀产生,pH稳定,无明显变化;溶液外观在6 h内无变化,6 h后颜色均有变深趋势;不溶性微粒2 h内稳定,2~8 h有所上升,但仍符合药典要求,12 h后不溶性微粒超过药典规定的数值;配伍液中的主要成分三七总皂苷及胰岛素含量无明显变化,且胰岛素保留时间稳定。可见,注射用血栓通与胰岛素在10%葡萄糖注射液中的配伍液在6 h内稳定。
中药注射液成分复杂,其中的主要成分和未能除尽的杂质成分与溶剂配伍后,随着放置时间的延长发生一系列复杂的化学反应,导致溶液外观颜色改变、微粒数增加[12-13],因此配伍液应在6 h内使用,并建议使用精密输液器或采用终端过滤装置,减少微粒对人体造成的损害[14]。临床使用中也尽量缩短放置时间,现配现用,以确保用药的安全性。通过以上内容的研究,并对研究结果进行全面评价,可基本阐明注射用血栓通与胰岛素在葡萄糖注射液中配伍后的稳定性,为临床合理应用提供了理论参考。
[1]井 静.注射用血栓通的临床研究及机理探讨[J].湖北中医杂志,2016,38(9):58-59.
[2]李学林,李宇辉,唐进法,等.注射用血栓通(冻干)UPLC指纹图谱研究[J].中国新药杂志,2016,25(14):1641-1646.
[3]Shen Y,Li YQ,Li SP,et al.Alleviation of ovariectomy- induced osteoporosis in rats by Panax notoginseng saponins[J].Journal of Natural Medicines,2010,64(3):336 - 345.
[4]陈 旭,党晓芳,曹飒丽,等.三七中总皂苷含量测定的对照品筛选[J].中国实验方剂学杂志,2013,19(7):66-68.
[5]郑丽华,卢昌均,周志昆,等.HPLC测定三七总皂苷中5种皂苷的含量及稳定性考察[J].中医药临床杂志,2012,24(1):73-75.
[6]国家药典委员会.中华人民共和国药典(二部)[M].北京:中国医药科技出版社,2015:1166.
[7]吴 斌,沈夕坤,张夏兰.胰岛素与其他药物在葡萄糖注射液中的配伍稳定性研究进展[J].中国处方药,2015,13(6):26-27.
[8]周惠卿.注射用血塞通在5%葡萄糖注射液和0.9%氯化钠注射液溶媒中的稳定性考察[J].中国医药指南,2012,10(17):103-104.
[9]陈志坚,黄罕妮,秦 晓.注射用血栓通与4种注射剂配伍稳定性考察[J].轻工科技,2014,30(3):103-104.
[10]诸林俏,黄 晨,王增寿,等.注射用血栓通在4种输液中的不溶性微粒考察[J].中国药业,2010,19(2):27.
[11]梁武英,韩 勇.血栓通与3种溶媒配伍的稳定性观察[J].临床合理用药杂志,2013,6(19):44 -45.
[12]Wang C,Li YJ,Chen L,et al.Compatible stability of Insulin injection mixing with pirarubicin hydrochloride for glucose injection[J].Chin Pharm J,2010,45(22):1758 - 1760.
[13]李雅静,王 晨,陈 雷,等.注射用盐酸柔红霉素与胰岛素在葡萄糖注射液中的配伍稳定性考察[J].中国药师,2011,14(9):1359 - 1360.
[14]王桂芝,胡海涛,董大伟,等.胰岛素注射液与红花注射液的配伍稳定性研究[J].中国药物与临床,2016,16(9):1295-1296.
