前房放液联合药物治疗白内障超声乳化人工晶状体植入术后早期高眼压的有效性
2018-06-06刘文龙董敏
刘文龙 董敏
白内障的致盲率较高,同时也是临床中十分多见的一类眼部疾病。患者接受白内障超声乳化人工晶体植入术之后,容易出现早期高眼压,若不能有效控制患者眼压并缓解其不良症状,将导致患者视神经等高眼压并发症,容易造成眼部的永久性损伤[1]。常规治疗方案中以药物治疗方案为主,但患者的眼压控制效果有限。本次研究将着重探讨白内障超声乳化人工晶状体植入术后针对患者早期高眼压联合应用药物治疗方案与前房放液治疗的可行性及安全性。
1 资料与方法
1.1 一般资料
选择我院2017年1月至2018年1月期间诊治的行超声乳化人工晶体植入术治疗的白内障患者术后出现高眼压120例(134眼)作为研究样本,以随机抽样法将患者进行分组,每组均为60例,并分别纳入至观察组和对照组当中。观察组:60例(66眼),男34例,女26例;患者年龄47~89岁,平均年龄(63.2±0.6)岁;术后症状出现时间1~3h,平均(1.3±0.4)h;眼压32.2~44.6mmHg,平均(43.16±4.17)mmHg。对照组:60例(68眼),男32例,女28例;患者年龄44~87岁,平均年龄(62.6±0.4)岁;术后症状出现时间1~2.5h,平均(1.4±0.2)h;眼压31.2~43.7mmHg,平均(40.28±3.95)mmHg。两组病人的线性资料对比,无统计学意义(P>0.05)。
1.2 方法
对照组患者单独采取局部药物治疗方案,甘露醇行静脉滴注1次;马来酸噻吗洛尔滴眼液点滴患眼,2滴/次,2次/天;观察组患者在此基础上联合采取前房放液治疗,具体方法如下:应用浓度为2%的无菌利多卡因注射液对患眼表面进行局部麻醉,在裂隙灯显微镜辅助下应用一次性无菌针头对角膜缘行切口,缓缓释放出房水,并观察患者前房深度。在放液时应确保前房深浅维持不变,例如患者虹膜中央组织出现轻微前突或者角膜存在变形时应停止放液。患者治疗前后均在结膜囊内以浓度为0.3%的氧氟沙星抗生素滴眼液进行滴眼治疗,每隔5min滴眼一次,共计治疗3次。患者前房放液治疗均由同一名医生在发现患者高眼压后15min内完成治疗。
1.3 评价指标
利用眼压测量仪对两组患者治疗前后的眼压进行测量与对比;眼压控制标准:患者的眼痛症状完全消失,眼压≤21mmHg;观察两组患者治疗后的并发症情况。
1.4 统计学方法
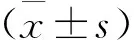
2 结果
2.1 两组患者治疗前后眼压水平对比
两组患者治疗前眼压水平均较高(P>0.05);治疗3~48h后观察组患者的眼压水平下降幅度显著高于对照组患者,两组间差异显著,有统计学意义(P<0.05)。见表1。

表1 两组患者治疗前后眼压水平对比
2.2 两组患者眼压控制有效率对比
观察组患者24h、48h眼压控制有效率分别为63.64%和98.48%,显著高于对照组患者的45.59%和76.47%,两组间差异显著,有统计学意义(P<0.05)。见表2。
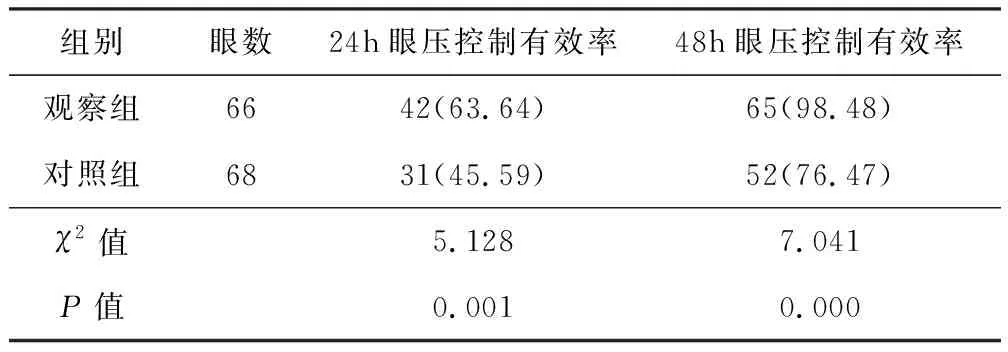
表2 两组患者眼压控制有效率对比[n(%)]
2.3 两组患者并发症情况对比
两组患者治疗期间均未出现前房出血、眼内感染、黄斑囊样水肿、人工晶体异位等并发症。
3 讨论
白内障是临床中的高致盲眼病,同时也是临床中的常见眼部疾病。近年来随着临床医学技术的不断进步,以超声乳化术为基础的白内障治疗方案得到广泛应用。白内障超声乳化吸除术具有良好临床疗效及安全性,该技术较为成熟,具有手术用时短、切口小、对组织产生损伤小、术后视力恢复快等优势。然而白内障患者接受超声乳化术与人工晶状体植入术后容易出现高眼压,这也是该术式十分常见的并发症,若不能及时有效控制患者眼压,缓解其临床症状,非常容易导致视神经等相关高眼压的永久性损伤。
3.1 术后早期高眼压发病原因
白内障超声乳化人工晶体植入术后患者早期高眼压其临床症状集中表现为眼部疼痛,伴随同侧偏头痛也有部分患者并无显著眼痛症状。通常在手术后第1天检查中发现患者角膜的上皮出现弥漫性水肿,经检测眼压显著升高。引起术后眼压升高的原因较多,有报道指出[2],手术中所残留的部分黏弹物质对小梁网产生阻塞作用,术中的超声能量将对虹膜与角膜产生损伤。而炎性渗出物制对房角形成阻塞,进而导致眼压升高。而角巩膜切口和进入眼内的治疗器械对房角组织产生损伤,也是引发小梁网水肿的主要原因,容易导致房水排出量减少,致使眼压升高。也有研究指出[3],超过50%的患者出现术后高眼压与患者与术中应用黏弹剂密切相关。本次研究发现,患者手术中黏弹剂残留是导致术后早期高眼压的重要原因。引起术中粘弹剂发生残留的原因较多,例如在术中植入人工晶体之后,在进行换吸黏弹剂时,为了避免发生后囊膜裂口继续扩大和玻璃体涌入其前房内,导致注吸不充分,而出现黏弹剂残留[4]。其次是由于手术过程中,采取的连续环形撕囊,使得植入人工晶状体具有居中性,连续撕囊口将对人工晶状体的光学面产生覆盖作用的同时,黏弹剂非常容易滞留在患者人工晶状体之后的囊袋中。最后是在植入晶状体时将对虹膜产生刺激,使得瞳孔缩小,引发换吸黏弹剂时不够充分[5]。
3.2 高眼压的临床治疗
手术后患者出现高眼压,此类患者多数均存在显著的眼痛和头痛等症状。因此临床医生在发现患者高眼压症状时,需在最短的时间内实现患者眼压有效控制,以缓解其不良症状,减少对于患者视功能产生的损伤。临床治疗中,常采用的控制患者术后高眼压的治疗药物包括高渗剂、β受体阻滞剂和碳酸酐酶抑制剂等[6]。应用甘露醇等相关药物,虽然可以有效控制患者眼压,然而此类药物在眼压控制速度中不甚理想。行甘露醇静脉滴注30min以后才可以实现降压效果。在1~2h内可达到最强作用,治疗,3~4h后患者眼压才能够恢复到治疗前的眼压水平。若静脉滴注药物治疗后患者眼压仍不能有效控制,此时患者的头痛和眼痛症状等均会显著增强,需要增加患者甘露醇的滴注剂量。然而可能增加患者肾衰竭等全身疾病风险。应用噻吗洛尔滴眼液之后30min能够发挥降眼压功效,2h后作用效果最显著[7]。然而术后高眼压应该在极短时间内迅速将眼压水平降到正常范围之内。白内障超声乳化术之后患者角膜边缘通常会存在辅助切口,因此可充分利用好该辅助切口实施房水放液。在进行房水放液之后,应立即将患者眼压降低到正常范围内,以确保尽快缓解病人的不良症状并保护其视功能[8]。放液之后患者眼压也有可能发生再次升高的情况,因而通过联合运用降眼压药物具有必要性。行侧切口放液治疗后,可能出现感染等并发症。在放液治疗过程中,由于患者眼内高压的影响,房水由切口向外溢出,并不会出现房水倒流等情况。在操作过程中,使针头不进入到患者前房,通过应用球内外形成的压力梯度促进房水自然流出。值得注意的是在放液操作过程中,应确保动作缓慢,同时需要密切观察患者前房的深浅,应保证前房深浅维持不变。诸如虹膜中央组织出现轻度前突或者角膜存在变形情况时,应该停止放液操作。本次研究中,观察组患者接受前房放液治疗机制之前,均采取结膜囊内滴注抗生素滴眼液治疗来预防感染,再放液治疗后继续应用抗生素滴眼液进行治疗。
3.3 术后高眼压预防
白内障超声乳化晶状体植入手术后发生高眼压的患者,多数均属于手术顺利完成者,为了降低后发性的白内障产生,目前临床中在进行白内障超声乳化手术过程中,通常采取连续光滑撕囊口[9]。撕囊口将对患者人工晶状体的光学面产生覆盖,同时可确保人工晶状体位于袋囊中保持居中性。术中操作可能导致黏弹剂滞留于人工晶状体之后,因而在手术过程中进行换吸黏弹剂时,应注意吸头向上下左右移动,来促进晶状体之后的黏弹剂发生前移,以便于黏弹剂的吸出。尽可能将吸头直接伸到晶状体后侧的黏弹剂处进行换吸,此项操作有助于防止手术之后患者发生高眼压[10]。而针对后囊破裂、皮质残留在囊袋中、玻璃体嵌顿等患者,预防术后高眼压原则与机制是综合性的,可结合实际情况选择科学的后续治疗措施,控制患者眼压水平。
本次研究中,观察组60例患者通过前房放液治疗联合药物方案,该组患者治疗后的眼压降低幅度显著优于同期对照组患者,同时观察组患者眼压控制有效率显著高于对照组,两组患者治疗期间均未发生前房出血和眼内感染等不良并发症。本次研究结果进一步提示,针对行白内障超声乳化人工晶状体植入手术后,发生早期高眼压的患者联合采取药物治疗方案与前房放液治疗,能够有效快速的降低患者高眼压水平,并且具有较高的安全性。该联合治疗方案在术后高眼压患者的治疗中具有较高临床应用价值。
综上所述,针对白内障超声乳化人工晶状体植入术后出现的早期高眼压,通过药物治疗方案联合前房放液治疗可有效降低患者高眼压,具有作用效果良好、起效速度快等优势,是术后早期高眼压患者的有效安全治疗方案。
