长期口服华法林治疗的心房颤动患者起搏器植入围手术期不同抗凝方式的比较
2018-06-05朱继红李炳强汪砚雨
朱继红,李炳强,汪砚雨
(河南科技大学第一附属医院心内科,河南 洛阳 471003)
研究显示在需要植入起搏器的患者中,出血及囊袋血肿的发生与接受口服抗凝药物治疗相关[1]。其中心房颤动(房颤)是主要的抗凝适应证之一。华法林是目前房颤患者最常使用的口服抗凝药,指南[2]推荐对于 CHA2DS2-VASc评分≥2 分的房颤患者,应长期服用华法林抗凝治疗,且要求控制国际标准化比值(INR)在 2.0~3.0。但对于需要植入起搏器的房颤患者如何选择围术期抗凝方案,以平衡术中、术后出血与血栓栓塞的风险,是一个较为棘手的问题。指南[3]推荐此类患者应用治疗剂量的静脉肝素或皮下低分子肝素作为桥接治疗,然而肝素桥接治疗可增加囊袋出血与其他出血并发症风险。目前许多中心采用不停用华法林的抗凝方案,然而这种治疗手段的安全性尚需进一步证实,笔者对此做进一步探讨。
1 资料与方法
1.1一般资料2013年7月至2017年7月在河南科技大学第一附属医院心内科住院的长期口服华法林治疗过程中需要植入起搏器的110例患者资料。入选标准:①患者年龄≥18岁;②按照 2014 AHA/ACC/HRS 房颤指南的诊断标准诊断为持续性房颤的患者或者病窦综合征合并阵发性房颤需要抗凝的患者,长期(>3 个月)服用华法林抗凝治疗,且INR控制在 2.0~3.0;③符合起搏器植入的适应症[4]。④CHA2DS2-VASc 评分≥2 分;⑤病例资料完整。排除标准:①既往有风湿性心脏瓣膜病或有心脏瓣膜置换手术史;②心肺功能严重损害或双侧心室明显扩大;③中风、全身性栓塞、或在过去12个星期内短暂性脑缺血发作;④之前的4周内有出血史;⑤肝/肾功能异常(肌酐清除率<30 ml/(min·1.73 m2)或肝脏转氨酶>正常上限 3 倍以上);⑥血小板计数<50×103个/mm3。
1.2方法回顾性分析所有入选患者的病例资料。记录所有入选患者的年龄、性别、起搏器型号(单腔起搏器或双腔起搏器)、CHA2DS2-VASc评分、血清肌酐、谷丙转氨酶、血小板计数、伴发疾病情况、围手术期华法林应用方法及剂量、入院INR值、术后伤口出血情况及血栓栓塞并发症情况,分析不同抗凝方式与住院期间出血和栓塞事件风险的关系。出血事件:手术切口情况、囊袋愈合情况、囊袋相关并发症如囊袋血肿、囊袋破溃等以及其他出血症状(包括出血部位,出血量);栓塞事件:血栓栓塞的部位、栓塞程度。
1.3统计学方法采用GraphPad Prism 5.0统计软件进行数据分析。采用单样本 K-S 拟合优度检验分析计量资料是否符合正态分布;偏态分布的计量资料以 M(Q1~Q3)表示,组间的比较采用 Mann-Whitney 秩和检验;正态分布的计量资料以均数±标准差表示,两组间的比较采用t检验;计数资料用例数(%)表示,两组间比较用χ2检验;组间比较用One-way ANOVA检验。P<0.05 为差异有统计学意义。
2 结果
2.1一般临床资料比较根据围手术期抗凝方式的选择将患者分为三组:①停用组33例:术前停用华法林4~5天,维持INR<2.0,术后当晚应用华法林,围术期不用肝素桥接。②桥接组37例:术前停用华法林4~5天,以低分子肝素替代,术前12 h停用,维持INR<2.0,术后给予华法林,治疗量的皮下低分子肝素桥接治疗一直到INR达到治疗范围;③继续组40例:整个围手术期继续华法林治疗,维持INR在1.5~2.5。3组患者年龄、性别、起搏器型号、CHA2DS2-VASc评分、血清肌酐、谷丙转氨酶、血小板计数、伴发疾病情况、入院INR值比较,差异均无统计学意义(P>0.05),见表1。
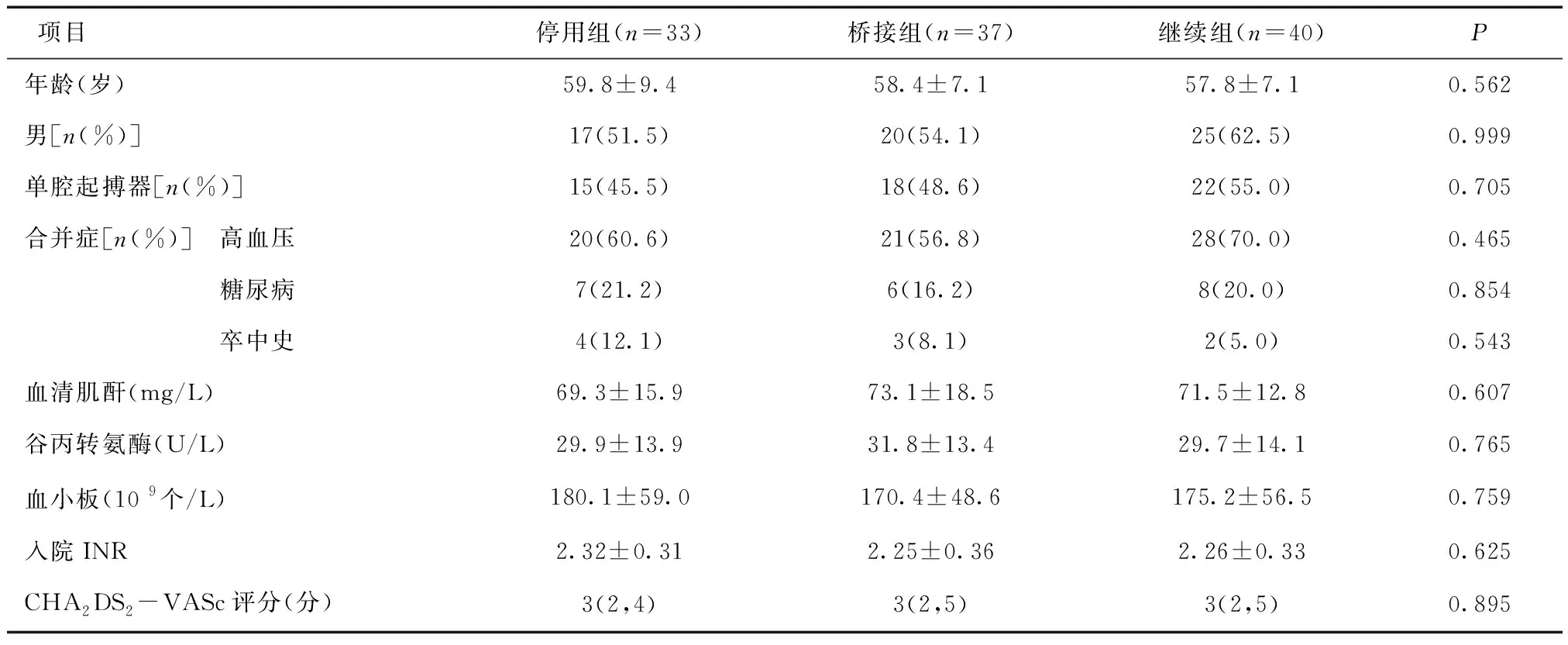
表1 三组患者一般临床资料
2.2三组患者切口及囊袋并发症发生率的比较围手术期内,桥接组出血及囊袋血肿发生率高于其他两组(P<0.05),三组间切口渗血发生率比较,差异无统计学意义(P>0.05),见表2。

表2 三组围手术期出血并发症及血栓栓塞事件发生率比较 [n(%)]
*与停用组比较,P< 0.05
2.3不良反应围手术期内,三组患者均无血栓栓塞事件发生。
3 讨论
许多房颤患者需长期口服华法林来预防血栓栓塞事件的发生,其降低房颤患者缺血性脑卒中及周围血管栓塞危险性的效果优于氯吡格雷[5]。房颤的发生率与年龄有明显的相关性,随着年龄的增长,房颤发生率明显升高,欧美国家一般人群的房颤患病率约为0.4%~1%,80岁以上人群患病率高10%;周自强等报道国内房颤患病率约为0.77%,其中60岁以上人群约为1.3%,而80岁以上人群已升至7.5%[6]。而高龄患者更易发生窦房结功能障碍及房室传导系统功能障碍,需植入起搏器,同时这类患者出血及血栓栓塞风险均较高,如何确保这类患者起搏器植入围术期的安全性,一直是临床上较为棘手的问题。如果抗凝方案不合理可能导致栓塞的发生,引起致残甚至致死;也可导致出血的发生,例如囊袋血肿、切口渗血,严重的血肿可能影响术区的愈合,需要注射器抽吸甚至进行血肿清创,而这些均可能增加起搏系统感染的发生,甚至发生起搏相关性感染性心内膜炎,一旦发生感染,多数需要拔除电极移除起搏系统。尽管指南建议对于长期口服抗凝药的患者,起搏器植入围手术期停用华法林,并使用低分子肝素作为桥接治疗[3],但越来越多的临床研究表明,围手术期桥接治疗,不能减少血栓栓塞事件,反而增加术后出血的风险。Douketis等[7]的研究中纳入了1884例需行起搏器植入术的房颤患者,根据围术期抗凝方式的不同分为桥接组与安慰剂组。结果显示,桥接组出血并发症的发生率高于安慰剂组,两组间术后一个月动脉栓塞的发生率差异无统计学意义。
越来越多的证据表明,对于长期口服抗凝药的房颤患者,围手术期继续使用华法林是相对安全的。Tolosana 等[8]进行的一项前瞻性、随机对照研究,对101 例高危血栓患者植入或更换起搏器的患者进行了对比分析,101例患者被随机分为肝素替代组和持续口服抗凝药组,两组囊袋血肿的发生率无差异,但肝素替代组住院时间明显延长(P< 0.001)。结果认为:起搏器植入术前华法林持续口服与肝素替代治疗同样安全、有效,而且未停用华法林组住院时间明显缩短。
本研究显示,在起搏器围术期桥接组的出血并发症显著增高,尤其是囊袋血肿明显高于其他两组(P<0.05),说明肝素桥接抗凝明显增加了围术期出血并发症的发生率。继续组围术期的INR值相对高于桥接组和停用组,但出血并发症无明显增加,显示了围术期继续应用华法林抗凝治疗的安全性。三组患者均无血栓栓塞事件发生,但由于本研究纳入患者例数较少,不能说明停用华法林的安全性,停用华法林无疑使患者暴露在血栓栓塞的风险中。本研究显示,围术期不停用华法林,并不增加出血的风险。对于栓塞事件的安全性,尚需要较大规模的研究。
也有一些和本研究相似的研究,提示对于此类患者继续应用华法林的优越性,尤其是对于有中重度血栓栓塞风险的患者[9,10]。笔者认为继续华法林抗凝的安全性可能在于,起搏器的植入部位在胸肌筋膜以上,此处血管较少,术中止血彻底,则较少发生渗血。同时持续应用华法林避免了肝素的应用,后者可增加住院时间,易引起出血并发症。
综上所述,本研究提示对于需要植入起搏器的口服华法林的心房颤动患者,术前继续华法林抗凝治疗不会增加起搏器植入围手术期出血事件的发生率。但本研究样本量较小,且为回顾性研究,心脏瓣膜病及瓣膜置换的血栓栓塞高危患者并未纳入到本次研究中,且并未收集到栓塞事件相关病例;没有根据 HAS-BLED 评分来对出血风险进行进一步的分组及分析;起搏器植入围手术期不间断应用华法林对不同危险分层的个体是否均是最佳的抗凝策略,仍需要更大样本的随机、双盲、对照研究来证实。
[1] Özcan KS,Osmonov D,Yldrm E,et al.Hematoma complicating permanent pacemaker implantation:Therole of periprocedural antiplatelet or anticoagulant therapy[J].Journal of Cardiology,2013,62(2):127-130.
[2] January CT,Wann LS,Alpert JS,et al.2014 AHA/ACC/HRS guideline for the management of patients withatrial fibrillation:a report of the american college of cardiology/american heart association task force on practice guidelines and the heart rhythm society[J].Circulation,2014,130(23):e199267.
[3] DnuketisJD,Berger PB,Dunn AS,et al.The perioperative management of antithrombotictherapy[J].Chest,2008,133:299S.
[4] Michele B,Angelo A,Gonzalo BE,et al.2013 ESC Guidelines on cardiac pacing and cardiac resynchronization ther-apy[J].Revista Espanola de Cardiologia (English Ed.),2014,67(1):58.
[5] 赖金川,李英,姜荣建,等.华法林与氯吡格雷预防心房纤颤患者缺血性脑卒中临床观察[J].实用医学临床杂志,2005,2(3):32-33.
[6] 周自强,胡大一.中国心房颤动现状的流行病学研究[J].中华内科杂志,2004,43(7):491-494.
[7] Douketis JD,Spyropoulos AC,Kaatz S,et al.Perioperative Bridging Anticoagulation in Patients with Atrial Fibrillation[J].Journal of Vascular Surgery,2016,63(1):823.
[8] Tolosana JM,Berne P,Mont L,et al.Preparation for pacemaker or implantable cardiac defibrillator implants in patients with high risk of thrombo-embolic events:oral anticoagulation or bridging with intravenous heparin A prospective randomized trial[J].Eur Heart,2009,30(15):1880-1884.
[9] Tischenko A,Gala U,Yee R,el a1.1 mplanlalionof cardiac rhythm devices without interruption of oral anticoagulation compared with perioperative bridgingwith low-molecular weight hepafin[J].Am Heart J,2009,158(2):252.
[10]AhmedI,Genner E,Nelson WB,et al.Continuing warfarin therapyissuperior interrupting warfarin with or withoutbridginganticoag-ulationtherapy inpatients undergoing pacemakerand defibrillatorimplantation[J].Heart Rhythm,2010,7:745.
