锂-氧电池用石墨烯/层状双金属氢氧化物纳米复合材料的制备及性能研究*
2018-06-04李恬恬陈子昂
李 芳,王 倩,李恬恬,陈子昂,王 伟
(西安工业大学 材料与化工学院,西安 710021)
随着化学电源(电池)广泛应用于人类社会的各个领域,安全、绿色和高效二次电池的开发与利用逐渐成为一个全球性课题.其中,锂-氧电池以其超高理论能量密度备受关注,该电池主要由锂负极、电解质和空气正极组成,正极活性物质源于大气中“取之不尽、用之不竭”的氧气,锂负极的电化学当量高达3 860 mA·h·g-1,基于Li+O2Li2O2的电化学反应,电池的理论能量密度高达11 140 W·h·kg-1,高于现有锂离子电池1~2个数量级[1].可以预见,锂-氧电池的成功开发将对储能、便携设备等领域产生巨大的影响.
然而,现阶段锂-氧电池的电化学性能较低,开发高效催化剂提升氧还原反应(Oxygen Reduction Reaction,ORR)和氧析出反应(Oxygen Evolution Reaction,OER)动力学是增强电池性能的有效措施之一[2].在目前研究的催化剂材料中,贵金属展现出优异的ORR或OER活性,但是高昂的价格限制了其实际应用.理想催化剂应满足以下几个要求:① 高效的ORR或OER催化特性;② 结构稳定;③ 价廉易得,制备简单.目前,含有过渡金属元素的物质在锂-氧电池中表现出优异的催化特性,文献[3]采用含钴氧化物有效提升了电池的放电容量,同时降低了过电位.文献[4]采用Fe3O4作为锂-氧电池催化剂,使得电池在大气下获得了1 427 mA·h·g-1的放电容量,同时有效提升了电池的OER活性.相比于单一金属及其氧化物对电池性能的提升,复合金属化合物表现出更为优异的催化特性.文献[5]制备了ZnCo2O4催化剂,在提升电池实际能量输出的基础上,在电池充电过程中使得电池充电电压平台降低了900 mV.层状双金属氢氧化物(Layered Double Hydroxide,LDH)是一种类似蒙脱石的新型矿物材料,具有组分可调、结构稳定等优点,通过引入过渡金属元素可以赋予其优异的ORR或OER 特性[6-7],然而,鲜有将其应用于锂-氧电池的报道.
文中采用含过渡金属元素的钴铝复合金属氢氧化物(CoAl-LDH)作为催化剂,利用制备工艺简单的共沉淀法制备石墨烯/CoAl-LDH纳米复合材料(简称rGO/CoAl-LDH)作为锂-氧电池正极材料,对电池的性能和催化剂的作用机制进行研究.
1 实验材料与方法
1.1 实验材料
膨胀石墨(EG)(化学纯);N-甲基吡咯烷酮(NMP)、聚偏氟乙烯(PVDF)、硝酸钠、浓硫酸、高锰酸钾、过氧化氢(30%)、盐酸、抗坏血酸、硝酸钴、硝酸铝、尿素、无水碳酸钠和氢氧化钠(粒)均为分析纯,上述试剂均在避光条件下保存.
电解液为含双三氟甲烷磺酰亚胺锂(LiTFSI)的四乙二醇二甲醚(TEGDME),锂片规格为∅16 mm,Celgard2500隔膜规格为∅18 mm,三者均存放于充满Ar气保护的手套箱中,其中水、氧含量低于1 μg·L-1.
选用泡沫镍作为集流体,在使用前用丙酮洗涤三次,蒸馏水洗涤三次,置于60 ℃的真空干燥箱中备用.
1.2 材料制备
1.2.1 氧化石墨的制备
采用改良Hummers法制备氧化石墨[8],基本工艺流程如下:称取2 g膨胀石墨和2 g硝酸钠加入到500 mL三口烧瓶中,然后加入96 mL浓硫酸在冰水浴中搅拌15 min,缓加12 g KMnO4并且继续搅拌90 min,接着将混合液升温到35 ℃搅拌2 h,在30 min内缓慢加入80 mL去离子水,再加入200 mL、35 ℃左右的去离子水进行稀释,随后向混合液中加入10 mL H2O2(30%),溶液变为黄色,继续搅拌10 min以后超声30 min,最后用500 mL(5% )的稀盐酸对产物进行酸洗,水洗至中性后在60 ℃真空干燥箱中干燥24 h,得到氧化石墨.
1.2.2 rGO及rGO/CoAl-LDH纳米复合材料的制备
将制得的氧化石墨加入一定量的去离子水中,超声震荡12 h得到氧化石墨烯乳液,添加氨水调节pH至9.0,然后加入1 g抗坏血酸磁力搅拌30 min,将溶液升温至95 ℃搅拌1 h,得到的黑色产物经洗涤、冷冻干燥48 h后得到rGO.
rGO/CoAl-LDH纳米复合材料制备采用如下方式:称取1.164 g Co(NO3)2·6H2O和0.75 g A1(NO3)3·9H2O溶于去离子水中,并定容到100 mL,简称溶液A;称取0.424 g Na2CO3和3.84 g NaOH溶于去离子水中,并定容到100 mL,简称溶液B;将溶液A和溶液B以相同的恒定速率(200 mL·h-1)同时滴加到100 mL含有40 mg氧化石墨烯的乳液中,整个滴定过程保持搅拌.待滴定完成后,在烧杯中加入一定量的抗坏血酸然后转移至80 ℃恒温水浴锅中静置3 h.将所得产物用大量的去离子水洗涤,冷冻干燥48 h得到rGO/CoAl-LDH.
1.3 电极制备与电池组装
将rGO/CoAl-LDH纳米复合材料和黏结剂(PVDF)按质量比9∶1分散于NMP分散剂中,制成均匀浆料涂覆在泡沫镍(∅14 mm)上,并于100 ℃下真空干燥12 h,得到石墨烯/CoAl-LDH空气电极.
无催化剂的rGO电极中rGO与PVDF质量比为9∶1,按上述rGO/CoAl-LDH空气电极制备方法涂极片.
采用模具电池在充满Ar气保护(水、氧含量低于1 μg ·L-1)的手套箱中依次将锂片负极、Celgard 2500隔膜和泡沫镍正极组装成锂电池,滴入70 μL电解液使三者得到充分润湿.
1.4 表征与测试
1.4.1 材料表征
采用日本岛津 X射线衍射仪( X-Ray Diffraction,XRD)对样品进行结构分析,射线源为CuKα.测试条件:扫描速率为4(°)·min-1,扫描范围为10°~80°.
采用拉曼光谱仪(Raman)对材料进行表征,设置激发波长为532 nm,位置为0~3 500 cm-1,在常温常压下直接对材料进行测试.
采用同步热分析仪(Thermogravimetric Analysis and Differential Thermal Analysis,TGA/DSC)对材料的热稳定性及组分含量进行表征,测试在空气氛围下进行,升温速率为10 ℃·min-1,温度范围为35~600 ℃.
1.4.2 电池的电化学性能测试
采用新威电池测试系统在纯氧气氛下对电池的恒流充放电性能进行测试,放电与充电电流密度均为0.1 mA·cm-2,放电与充电截止电压分别为2.0 V(vs.Li/Li+)和4.5 V(vs.Li/Li+).电池的循环性能测试采用限容500 mA·h·g-1的方式进行.
2 结果与讨论
2.1 材料表征
2.1.1 材料的XRD表征
图1为双滴法制得的CoAl-LDH和rGO/CoAl-LDH纳米复合材料的XRD谱图.对于单纯的CoAl-LDH材料,由图1可知,在11.5°,23.2°和34.5°三处出现了清晰的衍射峰,分别对应于CoAl-LDH的(003)、(006)和(012)三个衍射面,显示其具备层状双金属氢氧化物的特征衍射峰,表明双滴法可以获得晶态的CoAl-LDH,且结晶性高,晶相单一,含杂质较少.所制备的rGO/CoAl-LDH复合材料中也有明显的CoAl-LDH的特征衍射峰,在XRD谱图的20°~35°之间有比较宽的衍射峰,该衍射峰为混乱堆垛的还原氧化石墨烯,表明在成功制备层状双金属氢氧化物的基础上,氧化石墨烯也被还原成了石墨烯,而这有利于锂-氧电池获得较好的电化学性能[9].

图1 CoAl-LDH和rGO/CoAl-LDH纳米复合材料的XRD谱图
2.1.2 材料的拉曼表征
图2是氧化石墨烯(GO)、还原氧化石墨烯及rGO/CoAl-LDH纳米复合材料的拉曼谱图.曲线a GO的拉曼光谱中,1 350 cm-1和1 590 cm-1处分别是氧化石墨烯的D峰和G峰,D峰是碳结构的缺陷峰,代表了碳材料的无序性,G峰代表sp2碳骨架的平面振动峰[10].由曲线b rGO的拉曼光谱可知,氧化石墨烯还原后,D峰和G峰发生了红移,分别在1 348 cm-1和1 584 cm-1处,这是由于部分sp3杂化的C在水热还原过程中脱氧转变成了sp2杂化[11],sp2区域尺寸变小,数量增多,D峰和G峰强度的比值(ID/IG)由0.91(14 596/15 886=0.91)增大到1.25(16 041/12 832=1.25),表明氧化石墨烯被抗坏血酸成功还原[12-14].由曲线c rGO/CoAl-LDH纳米复合材料的拉曼谱图可知,复合材料的D峰和G峰位置与还原氧化石墨烯相同,同时ID/IG从1.25进一步增强到1.32(13 672/10 358=1.32),显示双滴法制备过程不仅有利于氧化石墨烯的还原,同时也使得复合材料中还原氧化石墨烯微晶平均尺寸降低[15].
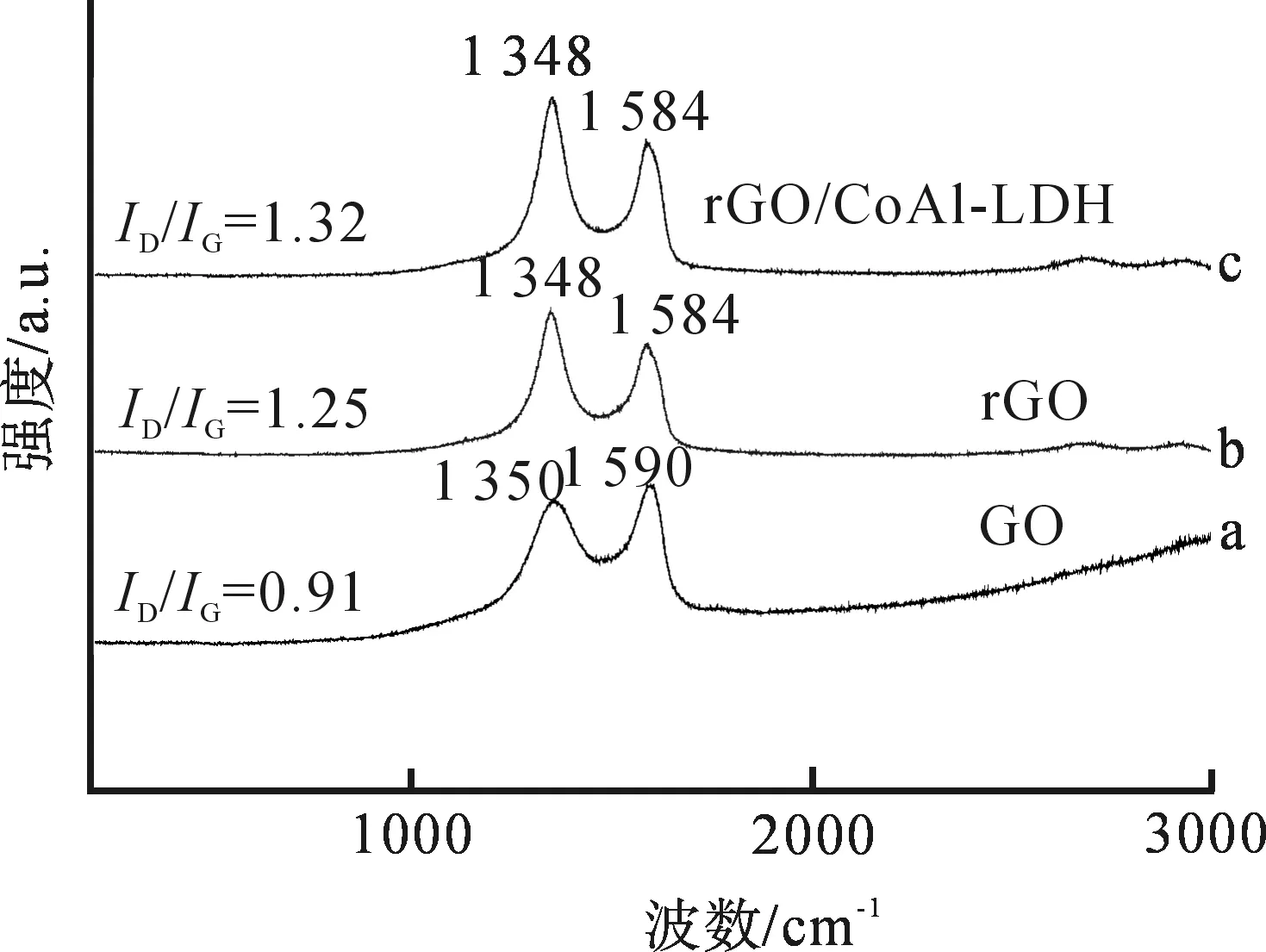
图 2 氧化石墨、还原氧化石墨烯及rGO/CoAl-LDH纳米复合材料的拉曼谱图
2.1.3 材料的同步热分析表征
为确定复合材料中石墨烯含量,采用热重及同步热分析仪对复合材料进行热重分析,其结果如图3所示.
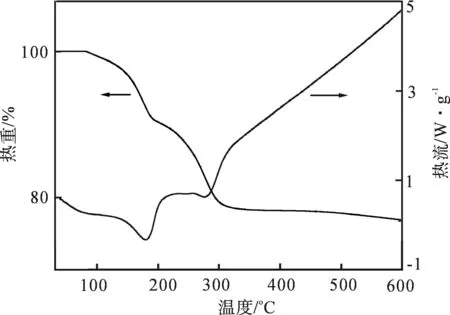
图3 rGO/CoAl-LDH纳米复合材料的TGA/DSC图
2.1.4 材料的形貌表征
图4为所制备材料的扫描电子显微镜(Scanning Electronic Microscopy,SEM)图,其中图4(a)为CoAl-LDH的微观形貌,由图4(a)可看出,材料形貌呈现片层结构,颗粒尺寸较大,同时材料尺寸大小不规则,分布范围为0.2~2.0 μm.由图4(b)可知,当CoAl-LDH与石墨烯进行复合后,材料呈现出纳米颗粒形态,颗粒尺寸细小且尺寸均匀,分布范围为0.05~0.10 μm.其原因可能是石墨烯的加入使CoAl-LDH产生较多的形核点, 其在后期长大过程中得以均匀生长,同时也使得石墨烯与CoAl-LDH得以有效接触,有利于纳米碳材料和CoAl-LDH均匀分散.两种材料在锂氧电池中同时发挥各自的优势,即石墨烯的均匀分布有利于提升电池的放电比容量,CoAl-LDH作为催化剂的均匀分布有利于产物的生产和降解,提升电池的循环性能,最终使锂氧电池的整体电化学性能得以提升.
2.2 性能测试
2.2.1 充放电性能测试
为避免大气中水分、二氧化碳对电池的影响,在纯氧气氛下对锂-氧电池进行性能测试,其结果如图5所示,其中电池比容量以正极材料中石墨烯质量计算.由图5(a)可以看出,使用rGO/CoAl-LDH纳米复合材料为正极材料组装的锂空气电池与单纯使用石墨烯为正极材料组装的锂空气电池相比,比电容有明显的上升,其首次放电比容量为2 662 mA·h·g-1.而相同情况下以rGO为正极组装的锂-氧电池首次放电比容量为1 757 mA·h·g-1.放电过程中二者放电平台没有明显区别,均为2.54 V,然而,对于充电过程来说,其充电电压平台有明显的区别,rGO/CoAl-LDH正极的充电电压平台为4.05 V,而rGO正极的充电电压平台高达4.48 V,显示出CoAl-LDH催化剂能有效提升电池放电比容量,降低电池过电位.从图5(b)中可以看出,在前5次循环过程中,虽然电池均呈现比容量下降的趋势,然而对于rGO/CoAl-LDH正极的电池来说,其放电比容量一直高于rGO正极,其首次库伦效率为98.49%,第五次循环时库伦效率为92.23%.而rGO正极首次库伦效率为91.12%,第五次循环的库伦效率为75.78%,显示出循环过程中CoAl-LDH对其能量输出得到了较好的维持.

图4 材料微观形貌

图5 锂-氧电池电化学性能曲线
2.2.2 交流阻抗测试
交流阻抗测试(Electrochemical Impedance Spectroscopy,EIS)测试有助于直观的反映电化学反应的能力,可以判断电池放电时极片钝化和充电时去钝化能力.图6为两种电极组装的锂-氧电池初始和放电后的EIS图谱,其中横坐标Z′为阻抗实部,纵坐标Z″为阻抗虚部.从图6可以看出,两种情况下电极相应的阻抗均包含中频域的一个扭曲半圆和低频域的一条斜线,其中中频域的阻抗弧(或半圆)对应于由ORR反应引起的电荷转移阻抗,低频域斜线代表韦伯阻抗,用于模拟材料的半无限扩散.对于初始态来说,rGO/CoAl-LDH电极的电荷转移阻抗明显小于rGO的,显示出较强的ORR反应动力学,放电后两种电极的电荷转移阻抗均有明显增大,显示放电后产物对电极表面产生了钝化.从图6(b)可以看到,放电后rGO电极电荷转移阻抗大于rGO/CoAl-LDH电极,意味着rGO电极放电后其表面钝化更为严重,而该钝化导致后期OER动力学减缓,使充电电压较rGO/CoAl-LDH电极高.
2.2.3 线性扫描伏安测试
图7为两种电极的线性扫描伏安(Linear Sweep Voltammetry,LSV)曲线,当电极从OCP往阴极方向扫描时,LSV曲线上都有一个阴极峰出现,对应于氧分子的还原反应,但还原电流密度呈现出明显的差异.rGO/CoAl-LDH电极的还原峰电流(0.405 mA)比rGO电极还原峰电流(0.202 mA)更大,显然rGO/CoAl-LDH电极的电极反应更快,ORR动力学性能更好,这与EIS所得结论一致.rGO/CoAl-LDH电极较好的ORR动力学使得在相同情况下能量输出较rGO更好,同时从充电曲线(图5(a))可以看出,rGO/CoAl-LDH电极的充电电压比rGO电极的降低了430 mV,显示出rGO/CoAl-LDH电极优异的可再充性能.因此,CoAl-LDH在氧正极中起到了提升ORR和降低充电过电位的双重作用,使得电池可以获得良好的性能.
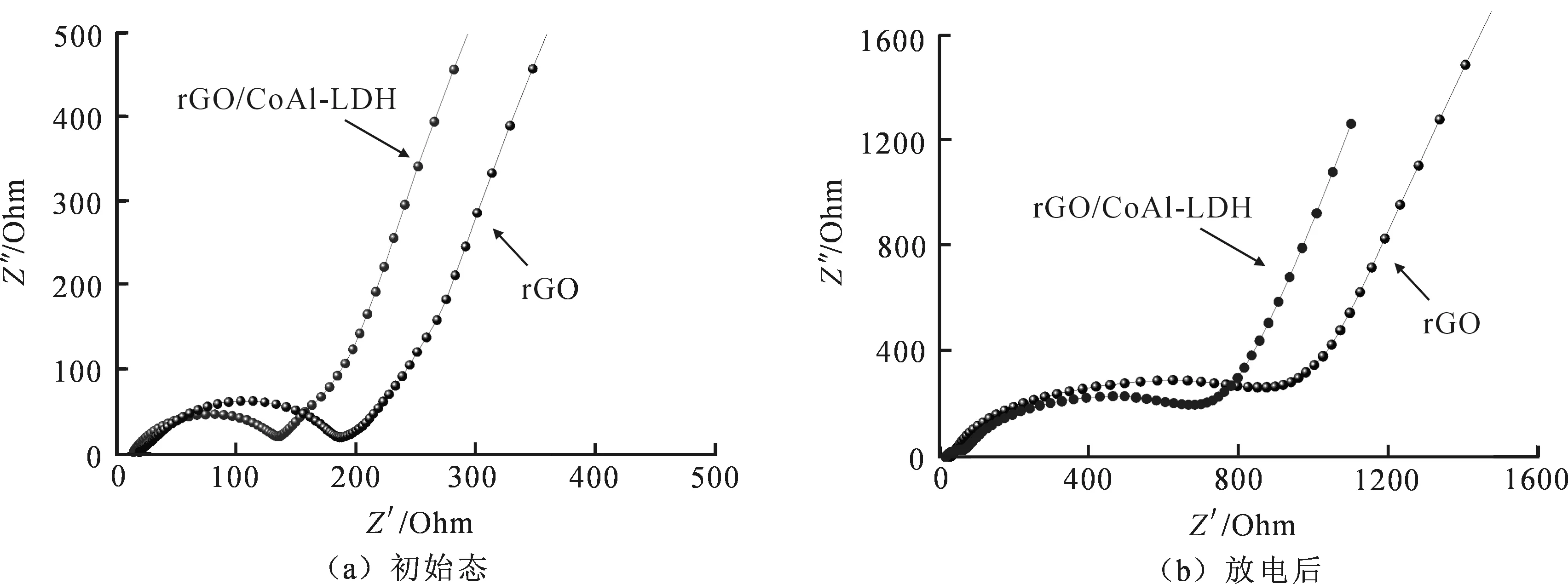
图6 锂氧电池充放电前后的EIS图谱
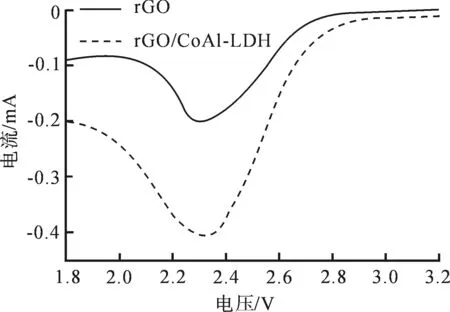
图 7 rGO电极和rGO/CoAl-LDH电极的LSV曲线
2.2.4 电池的循环性能测试
锂-氧电池的循环性能采用限容循环方式进行研究,选择的容量为500 mAh·g-1,图8为rGO电极和rGO/CoAl-LDH电极前10次循环过程的第1,5和10次的充放电曲线(图8(a)和图8(b))以及不同循环阶段电压平台对比曲线(图8(c)).从图8可以看出,对于两种电极来说,随着循环过程的进行,放电电压均呈现下降的趋势,然而相同循环次数下rGO/CoAl-LDH电极的放电电压高于rGO电极,且放电曲线较为平坦.对于充电过程来说,从图8(c)可以看出,rGO/CoAl-LDH电极较rGO电极充电平台低,然而从充电曲线可以看出,rGO/CoAl-LDH电极更低且更为陡峭,显示出rGO/CoAl-LDH电极整体呈现出较好的可逆性.

图8 锂-氧电池循环性能
3 结 论
1) 采用工艺简单的共沉淀法制备了rGO/CoAl-LDH纳米复合材料,其中石墨烯的含量为31.40%,在复合过程中氧化石墨烯得到了有效的还原,所得纳米复合材料中CoAl-LDH与石墨烯分散均匀,且CoAl-LDH尺寸分布由0.2~2.0 μm降至0.05~0.10 μm,尺寸均一性得到明显提升.
2) 制备的rGO/CoAl-LDH应用于锂-氧电池后,首次放电比容量为2 662 mA·h·g-1,比未负载CoAl-LDH催化剂的电极高51.5%,同时电压平台降低了430 mV.
3) LSV和EIS测试显示,rGO/CoAl-LDH电极具有更高的ORR活性,由于CoAl-LDH对电极具有良好的充电可逆性,使得在循环过程中rGO/CoAl-LDH电极表现出更好的性能.CoAl-LDH可以作为一种优良的锂-氧电池催化剂提升电池的性能.
参 考 文 献:
[1] BRUCE P G,FREUNBERGER S A,HARDWICK L J,et al.Li-O2and Li-S Batteries with High Energy Storage[J].Nature Materials,2012,11(1):19.
[2] LU J,LI L,PARK J B,et al.Aprotic and Aqueous Li-O2Batteries[J].Chemical Reviews,2014:114(11):5611.
[3] SHEN C,WEN Z Y,WANG F,et al.Cobalt-metal-based Cathode for Lithium-oxygen Battery with Improved Electrochemical Performance[J].Acs Catalysis,2016,6(7):4149.
[4] LV H,JIANG R,ZHANG X,et al.Self-assembled Mace-like Fe3O4Nanostructures as a Lithium-air Battery Cathode Material[J].Australian Journal of Chemistry,2016,69(6):683.
[5] LIU B,XU W,YAN P F,et al.In Situ-grown ZnCo2O4on Single-walled Carbon Nanotubes as Air Electrode Materials for Rechargeable Lithium-oxygen Batteries[J].Chemsuschem,2015,8(21):3697.
[6] CHITRAVATHI S G,SURENDER K,MUNICHANDRAIAH N.NiFe-layered Double Hydroxides a Bifunctional O2Electrode Catalyst for Non-aqueous Li-O2Batteries[J].RSC Advances,2016,6(105):103106.
[7] HAN X T,YU C,YANG J,et al.Electrocatalysts:Mass and Charge Transfer Coenhanced Oxygen Evolution Behaviors in CoFe-layered Double Hydroxide Assembled on Graphene[J].Advanced Materials Interfaces,2016,3(7):1500782.
[8] 张伟丰.过渡金属氧化物/石墨烯复合材料的制备及其超级电容性能研究[D].杭州:浙江大学,2013.
ZHANG Weifeng.Synthesis of Composite of Transition Metal Oxide and Grapheme and Their Supercapacitor Properties[D].Hangzhou:Zhejiang University,2013.(in Chinese)
[9] STORM M M,OVERGAARD M,YOUNESI R,et al.Reduced Graphene Oxide for Li-air Batteries:The Effect of Oxidation Time and Reduction Conditions for Graphene Oxide[J].Carbon,2015,85:233.
[10] TUINSTRA F,KOENIG J L.Raman Spectrum of Graphite[J].The Journal of Chemcal and Physilcal,2003,53(3):1126.
[11] 兰蒙.某子层状双金属氢氧化物的碳基杂化催化材料的制备、结构及性能[D].北京:北京化工大学,2015.
LAN Meng.Synthesis,Characterization and Catalytic Performance of Layered Double Hydroxides Carbon Based Composite Materials[D].Beijing:Beijing University of Chemical Technology,2015.
(in Chinese)
[12] SU L H,MA C L,HOU T,et al.Selective Synthesis and Capacitive Characteristics of CoNiAl Three Component Layered Double Hydroxide Platelets[J].RSC Advances,2013,3(43):19807.
[13] REN P G,YAN D X,JI X,et al.Temperature Dependence of Graphene Oxide Reduced by Hydrazine Hydrate[J].Nanotechnology,2011,22(5):055705.
[14] 杨宇雯,冯刚,卢章辉,等.原位合成钴/还原氧化石墨烯纳米粒子催化氨硼烷制氢[J].物理化学学报,2014,30(6):1180.
YANG Yuwen,FENG Gang,LU Zhanghui,et al.In Situ Synthesis of Reduced Graphene Oxide Supported Co Nanoparticles as Efficient Catalysts for Hydrogen Generation from NH3BH3[J].Acta Physico-Chimica Sinica,2014,30(6):1180.(in Chinese)
[15] ZHANG J,YANG H,SHEN G,et al.Reduction of Graphene Oxide via L-ascorbic Acid[J].Chemical Communications,2010,46(7):1112.
