医疗机构碳青霉烯类耐药肠杆菌科细菌感染防控指南简介
2018-05-30胡付品朱德妹
胡付品, 朱德妹
当前,碳青霉烯类耐药肠杆菌科细菌(carbapenem-resistantEnterobacteriaceae,CRE)在医疗机构的快速流行和播散,已成为全球公共卫生的重大问题。加强CRE菌株的检测和有效的医院感染控制措施干预,是遏制CRE菌株进一步流行播散的关键环节。本文对国际上关于CRE菌株的检测方法和防控指南(主要包括世界卫生组织、美国疾病预防控制中心和英国公共卫生中心发布的指南文件)进行简单描述,以供参考。
近年来,CRE的检出率在全球范围内呈逐年增高趋势,给社会公共健康领域带来严重的威胁。CHINET细菌耐药性监测网历年监测结果显示,肺炎克雷伯菌对碳青霉烯类的耐药率亦呈快速上升趋势,从2005年其对亚胺培南的耐药率3.0%上升至2016年的16.1%[1-2]。CRE菌株所致感染往往伴随高死亡率,研究显示,CRE所致侵袭性感染(如血流感染)的死亡率可达40%~50%甚或更高。此外,CRE菌株常同时携带对其他抗菌药物耐药的基因,导致其对目前临床常用的所有抗菌药物耐药,即全耐药。当前,CRE菌株在我国主要分离自住院患者,但需引起高度重视的是,该类耐药菌株存在随时向社区播散的可能。
1 CRE最新定义 [3]
肠杆菌科细菌满足以下任一条件,该菌即为CRE:①对任一碳青霉烯类抗菌药物耐药,亚胺培南、美罗培南或多立培南的最低抑菌浓度(MIC)≥4 mg/ L,或厄他培南MIC≥2 mg/L;②产生碳青霉烯酶;③对于天然对亚胺培南非敏感的细菌(如摩根摩根菌、变形杆菌属、普罗威登菌属),需参考除亚胺培南外的其他碳青霉烯类抗菌药物的MIC。
2 肠杆菌科细菌对碳青霉烯类药物的耐药机制
2.1 产生碳青霉烯酶
产生碳青霉烯酶是肠杆菌科细菌对碳青霉烯类耐药最主要机制,该酶可直接破坏碳青霉烯类抗菌药物。由于碳青霉烯酶基因大多位于可移动基因元件上,导致其很容易在不同肠杆菌科细菌以及其他革兰阴性杆菌间转移,在短时间内可导致大范围的流行播散[4]。目前我国临床分离的CRE菌株主要产生KPC型碳青霉烯酶和NDM-1型金属β内酰胺酶,其他的碳青霉烯酶尚有SME、IMI、NMC和GES等A类碳青霉烯酶,VIM、IMP、SPM和GIM型金属β内酰胺酶等B类碳青霉烯酶,以及OXA型碳青霉烯酶(如OXA-48、OXA-181和OXA-232型)等[5]。
2.2 其他机制
某些肠杆菌科细菌可通过非产碳青霉烯酶机制,如AmpC和/或超广谱β内酰胺酶(ESBL)合并膜孔蛋白突变,以及青霉素结合蛋白靶位结构改变等导致其对碳青霉烯类抗菌药物耐药。
3 碳青霉烯酶的检测
实验室检测碳青霉烯酶的方法众多。主要包括改良Hodge试验、Carba NP试验、改良碳青霉烯灭活试验(modified carbapenem inactivation method,mCIM)、酶抑制剂增强试验、免疫金标试验以及分子生物学方法等。
3.1 改良Hodge试验[6]
其操作步骤按CLSI推荐的方法进行。将0.5麦氏浊度的大肠埃希菌ATCC 25922稀释10倍后涂布于MH 平皿,中间贴厄他培南(10 μg)纸片,接种环自纸片外缘向平皿边缘划线接种待检菌,注意不要划破培养基表面。35 ℃过夜培养,次日,厄他培南抑菌圈处出现矢状生长者为待检菌产碳青霉烯酶。见图1。
由于该试验可出现检测结果假阳性或假阴性,2018年CLSI文件已删除改良Hodge试验。
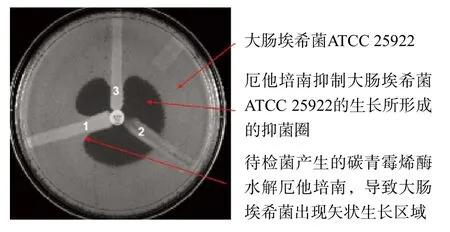
图1 改良Hodge 试验检测碳青霉烯酶
3.2 酶抑制剂增强试验[7]
以3-氨基苯硼酸(600 μg/片)和EDTA(292 μg/片)分别作为KPC型碳青霉烯酶和金属β内酰胺酶抑制剂。操作按CLSI推荐的纸片法进行,含酶抑制剂合剂的抑菌圈直径与单药相差≥5 mm以上,即可判断该受试菌株产生A类或B类碳青霉烯酶。见图2。

图2 3-氨基苯硼酸和EDTA联合碳青霉烯类抗菌药检测碳青霉烯酶
3.3 Carba_NP试验[6]
CLSI于2015年引入Carba_NP试验,用于检测肠杆菌科、铜绿假单胞菌和不动杆菌属细菌中碳青霉烯酶的表型确证试验。该试验采用比色法,目前主要用于流行病学研究或感染控制。研究表明,Carba_NP试验在检测KPC、NDM、VIM、IMP、SPM和SME型碳青霉烯酶方面具有较好的敏感度(>90%)和特异度(>90%)。Carba_NP试验结果解释见表1。
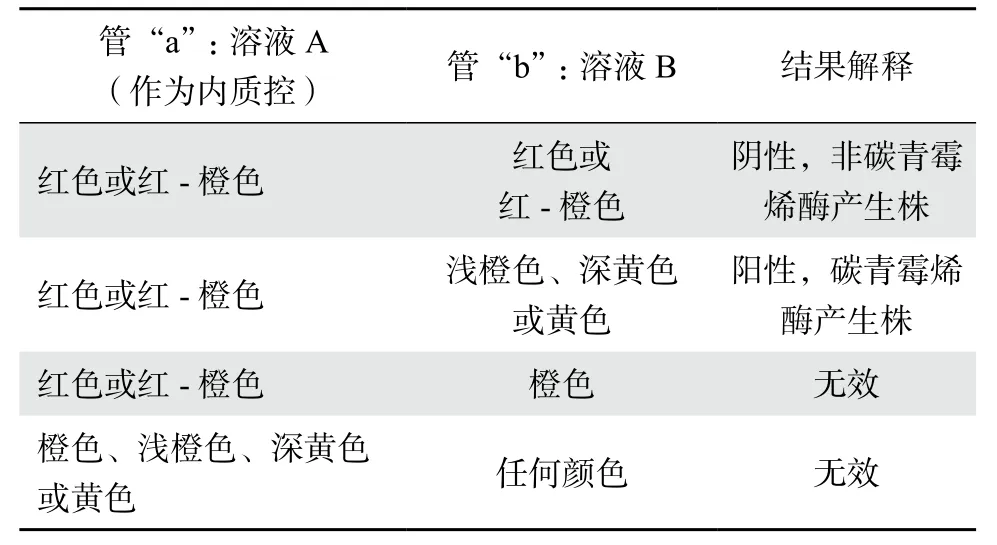
表1 Carba_NP试验结果判读
3.4 mCIM试验[6]
其原理是碳青霉烯类抗菌药物(通常为美罗培南)与受试菌悬液混合,若受试菌产生碳青霉烯酶,可破坏美罗培南的抗菌活性;若受试菌不产碳青霉烯酶,无法破坏美罗培南的抗菌活性,美罗培南仍可保持其对大肠埃希菌ATCC 25922的抗菌活性。结果判断:美罗培南抑菌圈直径6~15 mm为阳性,16~18 mm但圈内存在散在菌落亦为阳性,≥19 mm为阴性结果。见图3、图4。
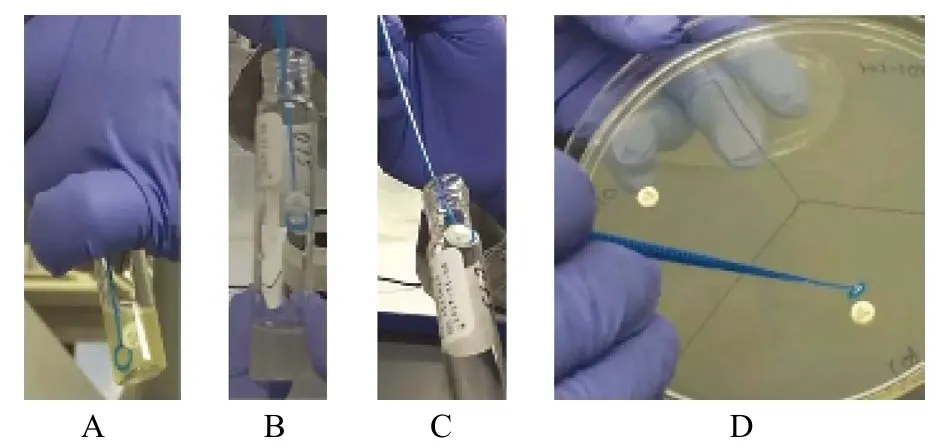
图3 mCIM试验检测碳青霉烯酶操作步骤

图4 mCIM试验检测碳青霉烯酶结果判断
3.5 碳青霉烯酶检测纸片组合
当前商品化可检测碳青霉烯酶的纸片中,推荐英国MAST公司的碳青霉烯酶检测纸片组合。该组合共包含5张纸片,以法罗培南和替莫西林为底物,辅以A类和B类碳青霉烯酶抑制剂,可同时检测KPC型碳青霉烯酶、B类金属酶和OXA-48型碳青霉烯酶,并可通过结果组合判断非产碳青霉烯酶的AmpC酶合并膜孔蛋白缺失所致碳青霉烯类耐药机制。见图5。
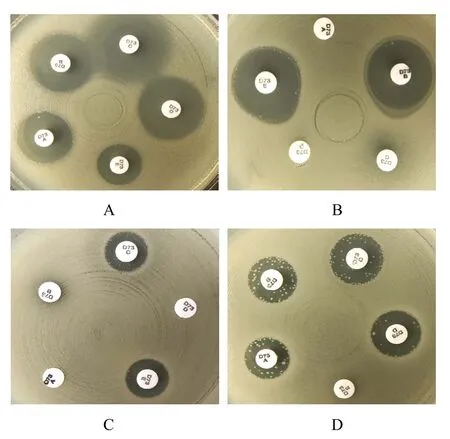
图5 碳青霉烯酶检测纸片组合检测碳青霉烯酶
3.6 免疫金标试验
这是目前以菌落为基础的最快速的检测碳青霉烯酶的方法。挑取一接种环待测菌菌落与裂解液混合,然后将此混合液滴加在加样孔中,15 min后即可观察结果。若板上标记线条由绿色变为红色,提示该菌产生碳青霉烯酶(图6)。目前该金标测试条可快速检测KPC、NDM和OXA-48型碳青霉烯酶。
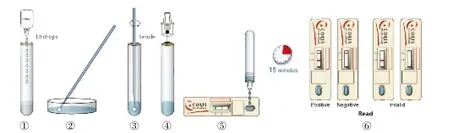
图6 免疫金标试验快速检测碳青霉烯酶示意图
3.7 快速分子诊断技术[8-9]
分子诊断技术可直接检测标本中碳青霉烯酶基因,实现快速筛查CRE菌株的目的。如Cepheid公司的Carba检测试剂盒,该试剂盒可同时检测KPC、NDM、IMP、VIM和OXA型碳青霉烯酶,检测时间一般在1 h左右,其检测灵敏度和特异度可达96%以上。
3.8 质谱技术[10]
基质辅助激光解吸电离飞行时间质谱(MALDITOF MS) 是近年来发展的简便、快速、准确的病原微生物鉴定方法。质谱技术通过比较不同细菌间质谱峰强度差异,可快速对碳青霉烯类耐药细菌进行检测。
4 感染预防控制措施
采取有效的医院感染控制措施遏制CRE菌株在不同患者和不同区域间的流行播散是当务之急。预防策略:一般流行情况下,采用标准预防控制措施防CRE菌株的流行播散,如手卫生和接触隔离警示。对于严重的CRE流行区域(如感染暴发或CRE检出率呈上升趋势区域),需采用更多的预防控制措施。对于无法开展碳青霉烯酶检测的机构,任何表型确认为携带CRE菌株的患者,均应采取预防控制措施[12]。此外,研究显示,肠道作为肠杆菌科细菌的储存库,CRE菌株的定植是其迁移至机体其他部位导致感染的重要危险因素[13]。Gorrie等[14]对498例患者肛拭子筛查结果显示,10.8%患者肠道定植有碳青霉烯类耐药的肺炎克雷伯菌。CRE肠道携带与非携带患者中继续其他部位感染的发生率分别为16%和3%。近期,世界卫生组织(WHO)在全球召集感染病、感染防控领域的顶级专家,制定耐药菌防控指南,为国家和医疗机构层面制定和实施碳青霉烯类耐药肠杆菌科细菌、鲍曼不动杆菌和铜绿假单胞菌的科学有效防控工作,提供策略性指导。在WHO发布的关于碳青霉烯类耐药革兰阴性杆菌的防控指南中[15],强调对于此类耐药细菌,其所致感染或定植的防控应多管齐下,至少包括手卫生、监测(特别是CRE)、接触预防、患者隔离(单间隔离或集中隔离)和环境清洁等策略。有效的感染预防控制措施包括如下。
4.1 加强监测
医疗机构应时刻关注是否有携带CRE菌株的患者入院,同时应了解本机构实验室是否有能力开展碳青霉烯酶的检测。若不具备检测实验条件,必要时可请有资质机构实验室协助检测。
开展细菌耐药性监测工作,了解本机构临床分离CRE菌株的流行播散趋势。收集CRE定植或感染患者的基础流行病学资料以了解不同人群特征,包括地理分布、入院时间、预后、基础条件和常规暴露(如病房、外科操作、从其他机构转移等)。
4.2 手卫生
加强手卫生,跟踪手卫生依从性。好的手卫生依从性被认为是所有良好感染防控项目,和控制包括CRE在内的多种重要耐药病原体传播的基础。在有关CRE的研究中,11项研究中6项将手卫生(例如教育、依从性和执行情况的督查)纳入他们评估干预的一部分。6项研究中的5项,报告在干预后CRE显著减少。
4.3 接触预防
CRE可通过直接或间接接触患者以及患者环境发生传播。接触预防干预措施被证明在降低CRE传播时的有效性和实用性。国际上公认的指南将“接触预防”定义为:①确保恰当的患者安置;②使用包括手套和隔离衣在内的个人防护用品;③限制运送和移动患者;④使用一次性或专用的患者医疗设备,尽可能避免侵袭性操作;⑤优先清洁和消毒患者房间,个人健康护理教育。
4.4 环境清洁
使用多模式策略来实施环境清洁至关重要。包括规范制度、结构化教育和监测清洁方案的依从性。与环境清洁相关的“患者区域”包含患者和其临近的周围环境,包括患者触碰的和直接接触患者身体的所有器具表面,如床栏、床头柜、床单、输液管、便盆、尿壶和其他医疗设备。也包括患者护理期间医务人员频繁接触的物体表面,如监护仪、把手和按钮,以及其他“高频”接触物表面。厕所内和相关物品上也可能有污染。环境清洁方案中最佳清洁剂的选择还不明确,有些研究推荐使用次氯酸盐(常用浓度为1∶1 000)以进行环境清洁。在某些CRE暴发流行情况下,有必要暂时关闭相应病房并加强清洁。尽管患者定植和/或感染CRE时,常常可以观察到环境中有此类耐药病原菌的污染,但环境污染对于临床检出的准确归因并不清楚,除了作为医院彻底清洁的标志。然而,环境监测可能是一个潜在有用的措施来评估污染水平和CRE感染患者周围的清洁效果。有研究显示,环境清洁干预后CRE感染率有较明显的下降,包括斜率(即,趋势;-0.32)和水平估计值(即,即刻的改变;-3.93)的显著改变。
4.5 患者隔离
患者隔离是接触预防的重要组成部分,通过单间病房(首选)或集中分类(次选)收治的方式将患者实施物理分隔,以预防患者之间的感染传播。值得注意的是,“隔离”和“集中分类收治”在一些医疗机构中存在术语使用不一致性。一般情况下,使用下述标准定义:①隔离,有条件的话,应将患者安排在单间(最好有独立卫生间);②集中分类收治。单间不足情况下,可选择集中分类收治,将定植/感染同种微生物的患者归为一组,在一个划定的区域提供护理,防止与其他患者接触;③隔离的目的是将定植/感染患者与非定植/非感染患者分隔开。
4.6 CRE筛查
应以当地流行病学和风险评估为指导,对无症状CRE定植进行监测培养。这一监测的人群应考虑包括既往有CRE定植的患者、与CRE定植/感染患者有接触的患者或近期在CRE流行的医疗机构有住院史的患者。目前在医疗机构提供的常规标准照护中,还缺少关于患者CRE定植的信息。但是在暴发时,或者在获得CRE风险很高的情况下(如,有可能与CRE定植或感染的患者接触、CRE区域性流行时),应该要知晓CRE的定植情况。确定CRE定植的监测培养,对于被筛查的患者来说,获益不会立竿见影,但的确有助于对CRE整体的感染防控。而这类筛查患者有可能发展为CRE感染,CRE定植状态的信息对于其经验性抗生素治疗计划,具有潜在重要的有益影响。
5 结语
耐碳青霉烯类革兰阴性杆菌,尤其是CRE感染已成为全球性的公共卫生问题。此类超级耐药细菌往往伴随着高发病率和高死亡率,临床抗感染治疗经常面临无药可用的困境,疾病的痛苦和经济负担显著增大。面对这样的“超级细菌”,如何科学防控是感染防控领域的重要命题。由于CRE等“超级细菌”不同于以往所发现的耐药细菌,必要情况下,建议将其防控级别上调,如参考我国香港地方政府将社区获得性甲氧西林耐药金黄色葡萄球菌作为法定须申报传染病的做法[16],对CRE的防控亦提升至需法定申报防控级别并贯彻实施,这将大大推进CRE感染防控的进程。
[1] HU FP, GUO Y, ZHU DM,et al. Resistance trends among clinical isolates in China reported from CHINET surveillance of bacterial resistance, 2005-2014[J]. Clin Microbiol Infect, 2016,22 (Suppl 1):s9-s14.
[2] 胡付品, 郭燕, 朱德妹, 等. 2016 年中国CHINET细菌耐药性监测 [J]. 中国感染与化疗杂志, 2017, 17(5): 481-491.
[3] Centers for disease control and prevention. Facility guidance for control of carbapenem-resistantEnterobacteriaceae(CRE) 2015 update[EB/OL]. [2017-07-29]. https://www. cdc. gov/hai/pdfs/cre/cre-guidance-508. pdf.
[4] FRIEDMAN ND, CARMELI Y, WALTON AL, et al.Carbapenem-resistant enterobacteriaceae: a strategic roadmap for infection control[J]. Infect Control Hosp Epidemiol,2017,38(5):580-594.
[5] YIN D, DONG D, LI K, et al. Clonal dissemination of oxa-232 carbapenemase-producingKlebsiella pneumoniaein neonates[J].Antimicrob Agents Chemother,2017,61(8): e00385-17.
[6] Clinical and Laboratory Standards Institute. Performance standards for antimicrobial susceptibility testing[S]. Twentyseventh informational supplement, 2017, M100-S27 Vol 37 No. 1.
[7] DOI Y, POTOSKI BA, ADAMS-HADUCH JM, et al. Simple disk-based method for detection ofKlebsiella pneumoniaecarbapenemase-type β-Lactamase by use of a boronic acid compound[J]. J Clin Microbiol, 2008,46(12):4083-4086.
[8] TATO M, RUIZ-GARBAJOSA P, TRACZEWSKI M,et al.Multisite evaluation of cepheid xpert carba-r assay for detection of carbapenemase-producing organisms in rectal swabs[J]. J Clin Microbiol,2016,54(7):1814 -1819.
[9] MOORE NM, CANTÓN R, CARRETTO E, et al. Taczewski,for the carba-r study team. rapid identification of five classes of carbapenem resistance genes directly from rectal swabs by use of the xpert carba-r assay[J]. J Clin Microbiol,2017,55(7):2268-2275.
[10] 李媛睿, 刘婧娴, 俞 静,等. 应用基质辅助激光解析电离飞行时间质谱检测产碳青霉烯酶肠杆菌科细菌对厄他培南的水解能力 [J]. 中国感染与化疗杂志, 2016, 16(5): 608-613.
[11] Centers for Disease Control and Prevention (CDC).Guidance for control of infections with carbapenem-resistant or carbapenemase-producingEnterobacteriaceaein acute care facilities[J]. MMWR Morb Mortal Wkly Rep, 2009,58(10):256-260.
[12] Agency for Healthcare Research and Quality. CarbapenemresistantEnterobacteriaceae(CRE) control and prevention toolkit[EB/OL]. [2017-07-29]. https://www. ahrq. gov/professionals/quality-patient-safety/patient-safety-resources/resources/cretoolkit/index. html.
[13] GIANNELLA M, TRECARICHI EM, DE ROSA FG, et al.Risk factors for carbapenem-resistantKlebsiella pneumoniaebloodstream infection among rectal carriers: a prospective observational multicentre study[J]. Clin Microbiol Infect,2014,20(12):1357-1362.
[14] GORRIE CL, MIRCETA M, WICK RR, et al. Gastrointestinal carriage is a major reservoir ofKlebsiella pneumoniaeinfection in intensive care patients[J]. Clin Infect Dis,2017,65(2):208-215.
[15] World Health Organization. 2017. Guidelines for the prevention and control of carbapenem-resistantEnterobacteriaceae,Acinetobacter baumanniiandPseudomonas aeruginosain health care facilities[EB/OL]. [2017-07-29]. http://apps. who. int/iris/bitstream/10665/259462/1/9789241550178-eng. pdf?ua=1.
[16] Centre for health protection. Statutory notifiable diseases[EB/OL]. [2017-07-29]. https://cdis. chp. gov. hk/CDIS_CENO_ONLINE/disease. html.
