谷维素/谷甾醇与单甘酯复合凝胶油形成过程及分子作用特性
2018-05-23马传国司天雷
李 胜,马传国,,*,刘 君,司天雷
(1.河南工业大学粮油食品学院,河南 郑州 450001;2.小麦和玉米深加工国家工程实验室,河南 郑州 450001)
通常认为凝胶剂分子和植物油在冷却的过程中,体系变得过饱和并形成化学电势,化学电势是导致相分离和形成晶核的驱动力,凝胶剂分子开始在非共价作用下随机成核、组装,通过结晶错配支化机制改变结构中结晶分支程度,促使结晶沿着一维生长并缠绕形成相互交联的三维网络。Roger[1]和Wright[2-3]等研究12-羟基硬脂酸菜籽油凝胶和蓖麻油酸菜籽油凝胶,认为凝胶油形成机制遵循成核-生长-分支-生长方式。Israelachvi等[4-5]发现可以通过临界堆积参数来解释凝胶剂分子在溶剂中形成自组装结构这一现象,根据这一理论,两亲性凝胶剂分子具有特殊的临界堆积参数,根据分子的形状和特性在极性-非极性界面会产生垂直曲率,利用临界堆积参数可以有效预测在植物油环境中凝胶剂分子优先形成何种组装聚集相。当临界堆积参数大于1时,会形成反向圆锥几何形态的反向中间相[6-7]。这种情况下凝胶剂分子亲水头部面积比疏水尾部面积小。相反,当临界堆积参数小于1时,形成正向中间相,正向中间相中凝胶剂分子头部横截面比尾部更大。当临界堆积参数为1时,两者相等导致形成层状中间相。
Edmund等[8]认为材料的微观结构直接影响固体材料的宏观特性(如硬度、弹性、油结合能力、透明度)。微观结构单元间的交联区数量、交联区类型(永久交联或瞬时交联)、纤维微观结构横截面厚度以及交联区相互作用的强度,决定了凝胶油的物理特性,其他宏观特性如浊度和油结合能力依赖于网络的微观结构尺寸和交联网络的结构及类型。因此对凝胶油形成过程及机理的研究可以充分理解微观结构的改变是如何影响凝胶油的形成,从而为凝胶性质的改善以及应用提供理论及实践指导。
1 材料与方法
1.1 材料与试剂
一级压榨葵花籽油 中粮集团有限公司;γ-谷维素(纯度≥99%) 济宁市安康制药有限责任公司;β-谷甾醇(纯度≥99%) 湖北只启生物化工有限公司;分子蒸馏单甘酯(glycerol monostearate,GM)(纯度≥90%,食品级) 郑州晨旭化工产品有限公司;氘代氯仿 美国剑桥化学CIL公司;溴化钾 济宁市百川化工有限公司。
1.2 仪器与设备
DF-101Z集热式恒温加热磁力搅拌器 巩义市京华仪器责任有限公司;SHZ-DIII循环水多用真空泵河南予华仪器设备有限公司;MQC-23脉冲式核磁共振仪英国Oxford公司;TAQ20差示扫描量热仪 美国TA公司;D8 Advance X-射线衍射(X-ray diffraction,XRD)仪德国Bruker公司;Rheostress60型哈克流变仪美国赛默飞世尔科技有限公司;小角X-射线散射(small angle X-ray scattering,SAXS)仪 奥地利安东帕公司;XPV-203型偏振光显微镜 上海长方光学仪器有限公司;标准数字系列制冷/加热型循环水浴 美国Polyscience公司;WQF-510型傅里叶变换红外光谱仪北京北分瑞利分析仪器公司。
1.3 方法
1.3.1 样品的制备
分别向葵花籽油中加入添加量(质量分数)为0%、1.2%、2.4%、3.6%、6.0%、8.4%和9.0%的分子蒸馏GM和添加量(质量分数)为9.0%、7.8%、6.6%、5.4%、4.0%、0.6%和0%的谷维素/谷甾醇(谷维素和谷甾醇质量比3∶2),然后样品在90 ℃、0.1 MPa的真空条件下磁力搅拌加热40 min,置于5 ℃冷却12 h后室温储藏至少3 d备用。
1.3.2 凝胶油结晶及组装过程测定
参照Amanda等[9]的方法并作修改,取适量样品于流变仪样品台上,先升温至90 ℃,以10 ℃/min的速率降到20 ℃,用直径为35 mm、角度为1°的锥板,间隙设置为1 mm,进行温度扫描。然后在20 ℃条件下,保持应变为0.01%,对凝胶油进行时间扫描,测定弹性模量(G’)和黏性模量(G”)随时间变化的曲线,时间范围为0~3 600 s。
另各取适量样品于流变仪样品台上,先升温至90 ℃,然后分别以1、5、10、15、20 ℃/min的速率冷却至20 ℃,将样品放置在载玻片上,盖上盖玻片,用木塞将样品压平使其均一分布,在偏振光显微镜下对样品的微观晶体形态进行观察。
1.3.3 甘油三酯及凝胶剂分子状态测定
参照Shapiro等[10]方法并作修改,取6 mL植物油或熔融的凝胶油样品加入到核磁管中,若管壁沾有样品,可在80 ℃水浴中加热,至无样品沾在壁上为止;用毛细管吸取适量氘代重水,然后灼烧毛细管两端,封口;将毛细管插入植物油或熔融的凝胶油样品中,冷却至形成稳定的凝胶油,放入500 MHz布鲁克核磁共振谱仪中采集谱图。样品质子的一维氢谱采用30°脉冲代替90°脉冲激发,纵向弛豫时间(T1)的测量采用反转恢复法,横向弛豫时间(T2)的测量采用CPMG脉冲序列,自扩散系数的测量采用LEDBPGP脉冲序列。
1.3.4 晶型的测定
参照朱小勇等[11]方法,取适量凝胶油样品平铺于检测片上的圆孔内,用XRD仪测定。测定条件:Cu靶,工作电压40 kV,电流40 mA,发射及防反射狭缝为1.0 mm,接受狭缝0.1 mm,室温20 ℃,2θ扫描范围3°~40°,扫描速率4°/min。使用JADE 5.0软件对扫描谱图进行分析。
1.3.5 聚集结构的测定
采用韩丽娟[12]方法,将样品用锡箔纸包好固定在样品室中,平行于线光源方向放置,角度范围为0.068°~25°,光源采用单色Cu-Kα,工作电压为40 kV,工作电流为50 mA,测试时间为5 min,温度为20 ℃,利用影像板收集小角部分的二维散射信号强度分布,经成像系统读取散射信号,利用SAXS quant3.1软件将二维信号积分转换为关于散射矢量的模(q)的一维函数,并扣除锡箔纸背景信号。q定义为q=4π×sinθ/λ,其中,λ为入射光波长,2θ为入射光的散射角。
1.3.6 红外光谱测定
取适量样品与KBr混合,研磨,制片,然后用红外光谱仪测定谷维素、谷甾醇与GM的红外光谱即可。将KBr研磨,制片,然后取适量微溶的凝胶油样品,均匀涂布在KBr薄膜上,冷却一段时间,至形成稳定的凝胶时,再用红外光谱仪测定。
2 结果与分析
2.1 凝胶油结晶及组装过程分析
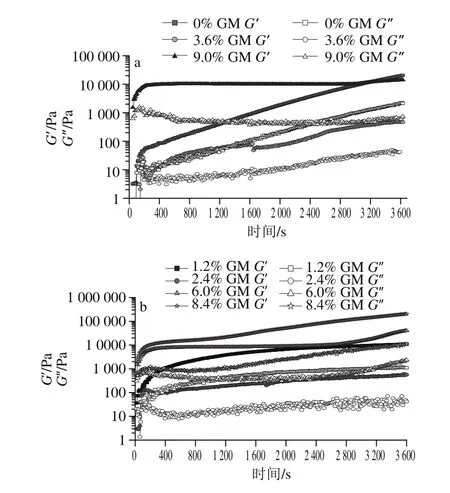
图1 不同GM添加量的凝胶油结晶过程中黏弹性模量随时间的变化Fig. 1 Change in viscoelastic modulus during crystallization of organogels with different concentrations of monoglycerides
从图1可以看出,凝胶油的形成过程中黏弹性模量随时间变化呈S型曲线增加,为了更好的理解其形成过程,可以将凝胶油的形成分成3 个阶段:平衡期、对数期和线性期。在平衡期所有样品弹性模量均大于黏性模量(图1a),说明凝胶油从此时开始形成,平衡期为分子达到过冷、过饱和的过渡期。对数期凝胶油弹性模量急剧增加,可以看成是成核聚集的过程。线性期为晶体生长和组装的过程。
当系统的温度(T)在熔化温度(Tm)以下时就会出现过冷状态,过冷状态下,系统是过饱和的,这就意味着溶解的分子在这一温度下呈固态,温度差(Tm-T)代表着热力学过冷,样品在平衡期的时间相差不大,这是因为相对于内部因素凝胶剂的组成,达到过饱和状态所需时间受温度差的影响更大。
在对数期凝胶剂开始聚集成核,成核是指一旦满足某种特定的热力学条件时,分子聚集在一起形成的晶种,晶种相分离成一个微小的晶体并成为晶体生长的基质。有两个热力学因素决定是否能形成核,正吉布斯自由能(ΔGS)与形成新的边界有关,负吉布斯自由能(ΔGv)与导致焓和熵改变的新相形成有关,总吉布斯自由能可表示为公式(1)[13]:
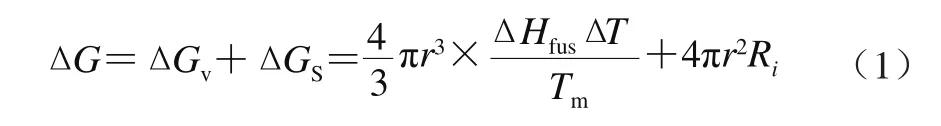
式中:r为核半径;ΔT为Tm(熔化温度)与样品温度的差值(过冷);ΔHfus为形成新固相时单位体积焓的变化值(负值);Ri为界面张力。
与形成新边界有关的正吉布斯自由能正比于新晶体的表面张力,负吉布斯自由能是熵和焓的部分,与新核的体积成正比,随着晶体体积的增加,表面积与体积的比值减少,最终导致新相的总吉布斯自由能为负值。因此临界半径rc(它是最小的核)为公式(2)[14]:

在此临界半径以上时,负吉布斯自由能占主导,这将导致形成核,而在此临界半径以下时,正吉布斯自由能占主导,由于布朗运动聚集的分子分散,使系统的吉布斯自由能增加,不能成核[15]。
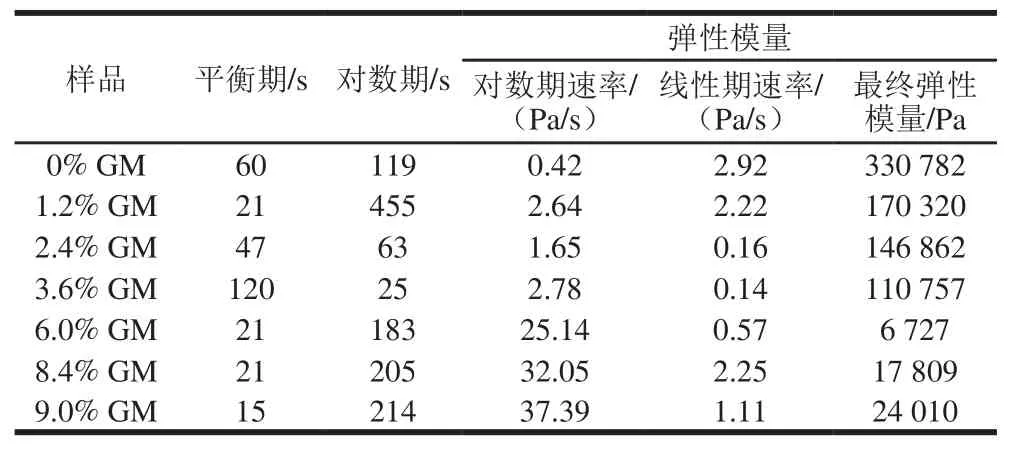
表1 不同GM添加量凝胶油的结晶过程参数Table 1 Crystallization process parameters of organogels with different concentrations of monoglycerides
从表1可以看出,GM含量越高,对数期弹性模量随时间延长的速率越大,表明GM增加了单位体积结晶焓值ΔHfus(负值),从而降低了总吉布斯自由能,使成核更有利。
线性期为晶体生长、组装的过程,凝胶油晶体通常具有3 种水平的结构,一级结构为凝胶剂分子进行晶体堆积,二级结构为晶体结构进行形态上的组装,如纤维,三级结构为二级结构之间相互作用形成的超分子结构,三级结构通常是与宏观特性最紧密相关的,尤其是流变学特性[8],整个线性期包含了这3种结构的形成。表1中最终弹性模量为凝胶油稳定后测定的,最终弹性模量随GM添加量增加呈先减小后增加的趋势,与整个线性期速率变化规律基本一致,而流变学性质是由三级结构决定,也就是说,三级结构决定了线性期的趋势。
将纤维聚集在一起形成三级结构的作用,基于交联区特性可以分为2 种[16]:即瞬时交联和永久交联。瞬时交联是由于凝胶剂粒子间的力,如偶极/范德华力。永久交联是由于两个纤维通过结晶缠绕结合在一起或更普遍的是单个纤维通过结晶错配支化机制分支成多个子纤维形成的,通常,这两种相互作用之间的比例决定凝胶油网络的物理特性,永久交联所占比例越大,晶体分支程度越大,从而弹性模量也就越大。结合表1可知,最终弹性模量的变化趋势说明永久交联和瞬时交联的比例随GM添加量的增加呈先增加后减小的趋势,且谷维素/谷甾醇凝胶油中永久交联的比例远大于GM凝胶油。
在2.4%和3.6% GM添加量的凝胶油中可以明显地看到对数增长到200 s之后(如图1b和图1d),弹性模量突然减少。Morales等[17]研究小烛树蜡和三十二烷红花籽油凝胶的流变学性质时也发现了弹性模量随时间突然减少的现象,认为此时同时存在强的凝胶结构和弱的凝胶结构。Toro等[18]研究三棕榈酸甘油酯对小烛树蜡高油酸红花籽油凝胶流变学性质的影响中,发现同时含3%小烛树蜡和1%三棕榈酸甘油酯的凝胶油中出现弹性模量突然减小,而在单独含3%小烛树蜡或1%三棕榈酸甘油酯的样品中没有出现这种现象,但对这种现象并没有作深入的解释。在本实验中这种现象说明这种结构很可能同时含有强的谷维素/谷甾醇纤维结构和弱的GM结晶的结构。
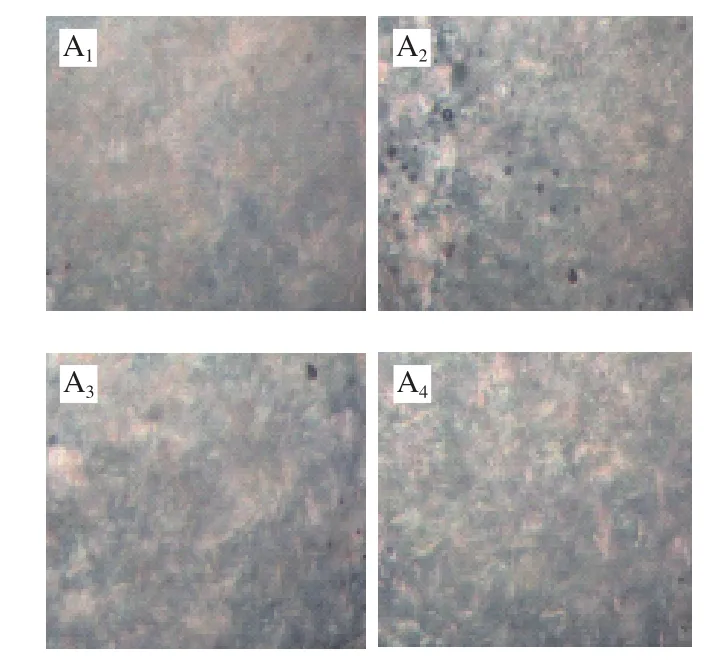

图2 不同冷却速率下3 种凝胶油的结晶及组装形态偏光显微镜图Fig. 2 The crystallization and assembly polarizing microscope graph of three kinds of organogels
三级结构中结晶错配支化通常受热力学的过饱和或依赖于时间的冷却速率控制,高的冷却速率或过饱和会导致更大的结晶错配支化发生率,图2反映地是不同冷却速率下3种凝胶油的结晶形态。从图2B可知,以复合凝胶油,尤其是以10 ℃/min冷却速率下形成的复合凝胶油中存在着高度结晶错配支化的小的树状晶体,类似于Rogers等[19]在神经酰胺凝胶油中观察到的形态,这些小的树状晶体可能是由于凝胶剂(谷维素/谷甾醇和单甘酯)分子中支链长度的高度差异化导致的。从图2A可知,GM凝胶油中单甘酯分子由于过饱和和过冷,经历成核、生长形成球状或针状结晶,这些结晶中没有出现树状结晶结构。图2C为谷维素/谷甾醇凝胶油在不同冷却速率下的纤维网状结构,在20 ℃/min速率冷却形成的凝胶油中也存在着小的树状纤维结构。这种树状结构在凝胶剂分子超过两个的凝胶油中更明显,说明这种结晶错配支化现象有些类似于异相成核。
2.2 复合凝胶油中甘油三酯及凝胶剂分子状态分析
凝胶油的形成机理通常可以认为是凝胶剂在植物油中通过共价短程作用力发生结晶或自组装,在一维方向上形成较长的纤维状、管状或螺旋状结构。这些较长的结构再通过机械缠绕或相互重叠形成空间三维网络结构,将植物油捕获在这种空间结构中形成的。研究凝胶油的形成机制,可以从植物油、凝胶剂、非共价作用力以及形成的聚集结构来分析。
从图3可以看出,凝胶油中主要的峰有9 个,而植物油中也是9 个峰且化学位移基本一致,这说明凝胶油中的这9 个峰为油脂中甘油三酯分子的峰;其他一些较小的峰则为凝胶剂分子的峰。对这9 个峰进行了归属[20],并根据葵花籽油脂肪酸组成中含量较高的脂肪酸是亚油酸和油酸,画出甘油三酯结构图,如图4所示,归属出的甘油三酯不同位置H对应的化学位移关系,如表2所示。

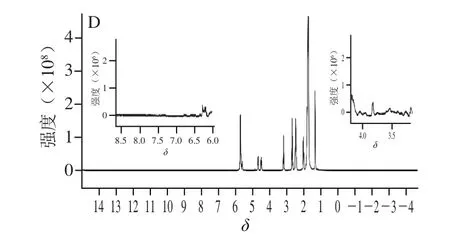
图3 植物油及其凝胶油的1H-NMR谱图Fig. 3 1H-NMR spectra of sunflower seed oil and organogels

图4 葵花籽油含量较多甘油三酯结构式Fig. 4 Structural formula of main triglycerides in sunflower seed oil

表2 1H-NMR谱图中甘油三酯分子峰化学位移与不同基团位置氢的关系Table 2 Relationship between triglyceride molecular peak chemical shift and hydrogen at different positions in 1H-NMR spectra
从表3可以看出,凝胶油和葵花籽油9 个油脂峰的T2/T1以及自扩散系数相差不大,表明单一凝胶油以及复合凝胶油中葵花籽油仍然主要以液态形式存在,油脂结合能力是凝胶油的一种重要特性,有多种结合机制固体结晶相结合油,每种机制代表特定的长度范围[21],用水的存在状态类推,油可以分为多种不同类型:结构油、单层油、多层油、物理截留油。结构油是指分子水平捕获的油,如将液态甘油三酯分子捕获到脂肪结晶的晶粒间界。单层油是指在凝胶油结晶中直接发生相互作用(通过范德华力)的油。多层油是指与结合在结晶表面单层油相互作用的油,从某种程度上说,多层油是被单层油结合的油。物理截留油是指将油包裹到凝胶油结晶颗粒间隙中,这些间隙就像毛细血管使油保留在通道中,因为其优先浸入缠绕的结晶中[8]。本实验中油脂主要以液体形式存在,说明物理捕获是复合凝胶油截留液体油最主要的机理。随着GM添加量的增加,T2/T1以及自扩散系数呈降低趋势,此结果说明GM对油脂中甘油三酯分子有更明显的限制作用,由表4可知,GM使谷维素分子的运动受到了轻微的限制,在图3B中GM的出峰位置与油脂中甘油三酯基本重叠,从自扩散系数的对比上大致可以看出,添加量3.6% GM样品中谷维素分子比GM自扩散系数大,因此谷甾醇更倾向于和谷维素结合,这可能是由于它们的结构相似,空间壁垒更小。
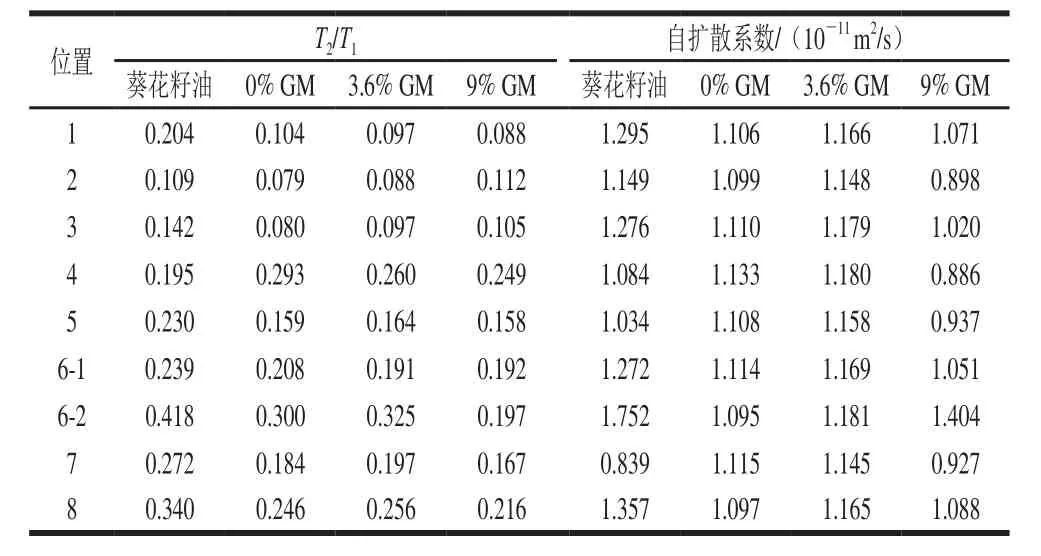
表3 油脂的自扩散系数及弛豫时间分析Table 3 Self-diffusion coefficient and relaxation time analysis of sunflower seed oil and GM
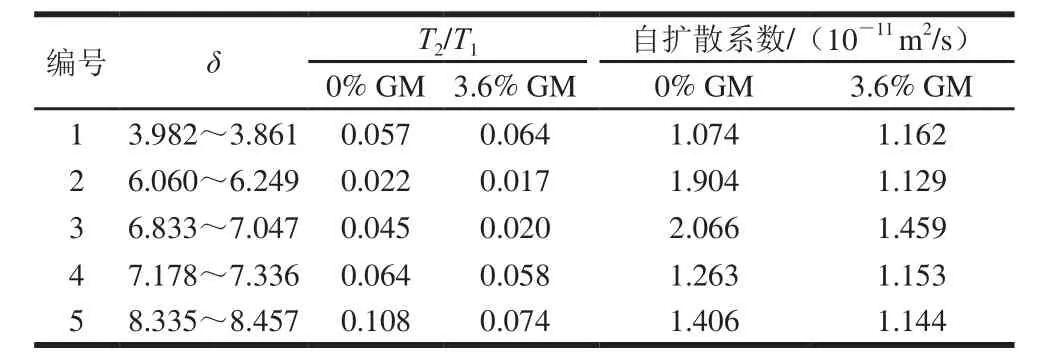
表4 凝胶剂的自扩散系数及弛豫时间分析Table 4 Self-diffusion coefficient and relaxation time analysis of gelators
2.3 GM添加量对复合凝胶油红外光谱特征的影响
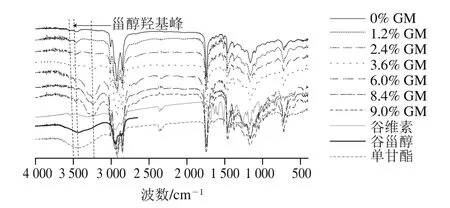
图5 GM添加量对复合凝胶油红外特征的影响Fig. 5 Effect of monoglyceride concentration on infrared characteristics of organogels
如图5所示,谷甾醇的羟基峰为3 459 cm-1,谷维素中没有羟基峰,GM中存在甘油羟基峰为3 477 cm-1。而GM凝胶油中则看不到明显的羟基峰位移变化,尽管GM结构中含有羟基和羰基基团,也有文献中分析认为理论上单甘酯分子能形成分子内和分子间氢键[22],但实际上,从图5可以推断GM凝胶油中羟基峰为3 477 cm-1,因此,结构中很可能没有形成氢键。在谷维素/谷甾醇凝胶油中甾醇羟基峰明显向低波位移动至3 436 cm-1,说明谷维素/谷甾醇凝胶油中形成了氢键,从氢键的形成机理分析,β-谷甾醇可以通过羟基(R—O—H)与γ-谷维素中电负性强的羰基(—C=O)氧原子形成分子间氢键R—O—H…O—R'[23-27],此外,还可以看到,随着复合凝胶油中GM所占比例的增加,羟基峰向低波位移动逐渐减小,氢键减弱;而当GM添加量超过6%时,氢键作用几乎不存在。谷维素、谷甾醇、GM及复合凝胶油甾醇羟基峰位置见表5。
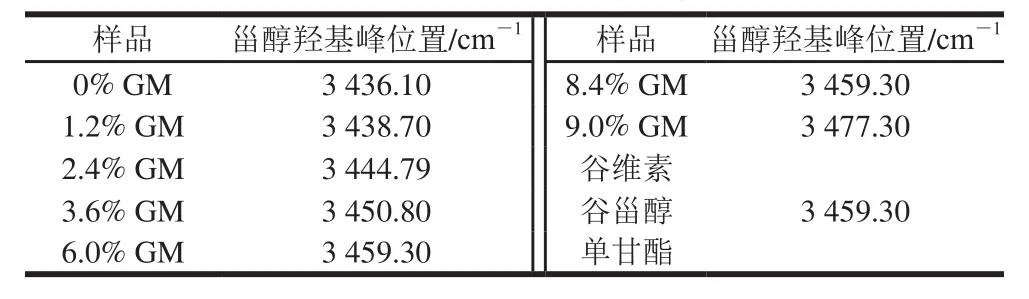
表5 谷维素、谷甾醇、GM及复合凝胶油甾醇羟基峰位置Table 5 Sterol hydroxyl peak positions of oryzanol, sitosterol,monoglycerides and organogels
2.4 GM添加量对复合凝胶油热力学性质的影响
凝胶油的聚集结构通过XRD和SAXS进行分析,其中XRD测定的为小于1 nm范围的晶体结构(图6),而SAXS测定的是1~100 nm范围样品粒度、孔径、有序性等信息。
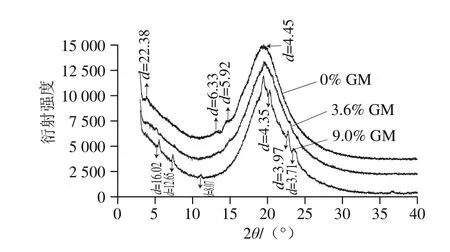
图6 不同GM添加量复合凝胶油的XRD谱图Fig. 6 XRD spectra of organogels with different concentrations of GM
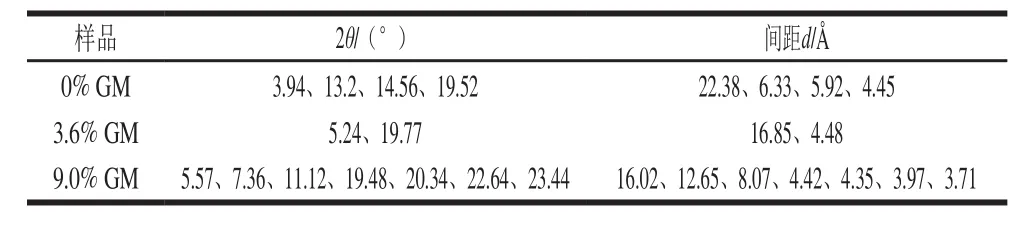
表6 GM凝胶油、谷维素/谷甾醇-GM复合凝胶油和谷维素/谷甾醇凝胶油的XRD参数Table 6 XRD parameters of monoglycerides organogels, oryzanol/sitosterol-monoglycerides organogels and oryzanol/sitosterol organogels
由表6可知,GM凝胶油分别在8.07、4.42 Å处存在尖的衍射峰,表明结构中形成了β结晶,而在4.35、3.97、3.71 Å处的峰说明还存在着β’结晶;复合凝胶油中仅在2θ为20°附近呈现了一个弱的弥散峰,说明样品中可能存在着少量弱的晶格结构,更多的是无定形结构,谷维素/谷甾醇凝胶油虽然含有一些小峰,表示含有一些谷甾醇结晶,但在2θ为20°附近为平缓的馒头峰,说明谷维素/谷甾醇凝胶油为非晶结构。
在SAXS中单分散的球形体系单位体积内含有n 个相同粒子的总散射强度(I)关于散射矢量(q)可以表示为公式(3):

式中:P(q)是形状因子的平均值;S(q)是表征颗粒间相互位置的结构因子(在稀溶液体系中S(q)一般为1)。
P(q)可以通过对距离分布函数p(r)经以下傅里叶红外光谱变换得到:
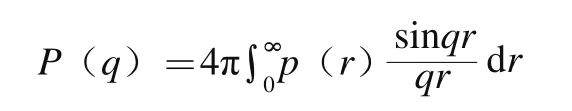
式中:dr为对半径r进行积分。
而结构因子S(q)可表示为:

式中:g(r)为径向分布函数[28]。
对谷维素/谷甾醇凝胶油SAXS曲线进行傅里叶变换得到的距离分布函数曲线(图7b),结果表明其形成了直径7.2 nm,长度37 nm中空管状结构。根据文献[29-31],一级散射和高级散射Bragg空间关系比例为1∶2∶3∶4∶5时为层状对称,比例为时为立方对称,比例为时为六边对称。对3 种凝胶油峰位置对应q值比例分析如表7所示,这些数据表明谷维素/谷甾醇凝胶油形成的为六边对称结构,GM凝胶油形成的为层状对称结构,复合凝胶油中虽然含有两种结构但在组装聚集时形成的是形态单一的中尺度立方对称结构。
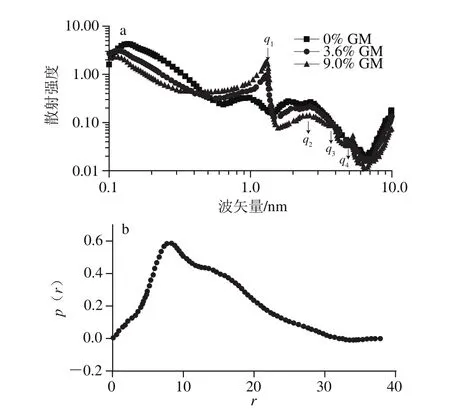
图7 不同GM添加量复合凝胶油的SAXS谱图(扣除背景后)Fig. 7 SAXS spectra of organogels with different concentrations of GM
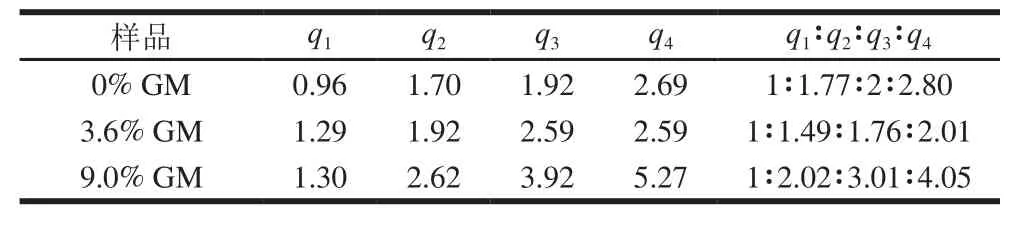
表7 GM凝胶油、谷维素/谷甾醇-GM复合凝胶油和谷维素/谷甾醇凝胶油的SAXS参数Table 7 SAXS parameters of monoglycerides organogels, oryzanol/sitosterol-monoglycerides organogels and oryzanol/sitosterol organogels
3 结 论
对凝胶油的形成过程及分子作用特性分析表明,凝胶剂分子和植物油在冷却的过程中,体系变得过饱和并形成化学电势,导致相分离和随机成核,凝胶剂分子进行晶体堆积、形态上的组装以及交联形成特定的结构。在此过程中植物油主要以液体的状态存在,说明物理截留油是凝胶剂固化植物油的主要机理;在仅含GM的单一凝胶剂情况下,GM分子间没有形成氢键,而含谷维素/谷甾醇的凝胶油中,谷维素会与谷甾醇形成分子间氢键,其结构比GM凝胶油更复杂,强度也更大。利用谷维素/谷甾醇和GM三者形成的凝胶油,达到过冷、过饱和时间几乎不受影响,但聚集成核以及形成一级、二级和三级结构所经历的时间明显比其他两种凝胶油更长,且结构也更复杂。这是因为凝胶剂之间还存在着范德华力、疏水作用力、π-π堆积等比氢键稍弱的作用力,凝胶剂的种类越多,形成结构的微观单元及其作用也越多。此外,凝胶剂组成越复杂,内外界条件对凝胶油的影响也越大,工业上可以通过优化合适的工艺条件得到的适合不同需要的产品。
参考文献:
[1]ROGERS M A, WRIGHT A J, MARANGONI A G. Nanostructuring fiber morphology and solvent inclusions in 12-hydroxystearic acid/canola oil organogels[J]. Current Opinion in Colloid & Interface Science, 2009, 14(1): 33-42. DOI:10.1016/j.cocis.2008.02.004.
[2]WRIGHT A J, MARANGONI A G. Formation, structure, and rheological properties of ricinelaidic acid-vegetable oil organogels[J].Journal of the American Oil Chemists’ Society, 2006, 83(6): 497-503.DOI:10.1007/s11746-006-1232-9.
[3]WRIGHT A J, MARANGONI A G. Time, temperature, and concentration dependence of ricinelaidic acid-Canola oil organogelation[J]. Journal of the American Oil Chemists’ Society,2007, 84(1): 3-9. DOI:10.1007/s11746-006-1012-6.
[4]ISRAELACHVILI J N, MITCHELL D J, NINHAM B W. Theory of self-assembly of hydrocarbon amphiphiles into micelles and bilayers[J]. Journal of the Chemical Society Faraday Transactions,1976, 72(24): 1525-1568. DOI:10.1039/f29767201525.
[5]MARANGONI A G, GARTI N. Edible oleogels: structure and health implications[M]. San Diego, United States: Elsevier Science Publishing Co Inc, 2011.
[6]SVENSON S. Self-assembly and self-organization: important processes, but can we predict them?[J]. Journal of Dispersion Science &Technology, 2004, 25(2): 101-118. DOI:10.1081/DIS-120030657.
[7]VAN W K, DOUGLAS J F. Symmetry, equivalence, and molecular self-assembly[J]. Physical Review E, 2006, 73(3): 031502.DOI:10.1103/PhysRevE.73.031502.
[8]CO E D. The Effect of shear and thermal gradients on the solidification of an edible oil organogel[M]. Guelph: University of Guelph, 2011.
[9]WRIGHT A J, MARANGONI A G. Formation, structure, and rheological properties of ricinelaidic acid vegetable oil organogels[J].Journal of the American Oil Chemists’ Society, 2006, 83(6): 497-503.DOI:10.1007/s11746-006-1232-9.
[10]SHAPIRO Y E. Structure and dynamics of hydrogels and organogels:an NMR spectroscopy approach[J]. Progress in Polymer Science,2011, 36(9): 1184-1253. DOI:10.1016/j.progpolymsci.2011.04.002.
[11]朱小勇, 孟宗, 李进伟, 等. 凝胶剂种类对凝胶油物性及结晶形态的影响[J]. 中国粮油学报, 2013, 28(10): 37-43.
[12]韩立娟. 超分子油脂凝胶微观结构衍变与宏观性能变化的关系研究[D]. 广州: 华南理工大学, 2014.
[13]DAMODARAN S, PARKIN K L, FENNEMA O R. Fennema’s Food Chemistry[M]. 4th. Boca Raton: CRC Press, 2007.
[14]MARANGONI A G. Fat crystal network[M]. Boca Raton: CRC Press, 2004.
[15]WALSTRA P. Physical chemistry of foods[M]. Boca Raton: CRC Press, 2003. DOI:10.1201/9780203910436.
[16]WANG R, LIU X Y, XIONG J Y, et al. Real-time observation of fiber network formation in molecular organogel: supersaturation-dependent microstructure and its related rheological property[J]. The Journal of Physical Chemistry B,2006, 110(14): 7275-7280. DOI:10.1021/jp054531r.
[17]MORALES-RUEDA J A, ELENA D-A, CHARÓ-ALONSO M A, et al. Thermo-mechanical properties of candelilla wax and dotriacontane organogels in safflower oil[J]. European Journal of Lipid Science &Technology, 2010, 111(2): 207-215. DOI:10.1002/ejlt.200810174.
[18]TORO-VAZQUEZ J F, ALONZO-MACIAS M, DIBILDOXALVARADO E, et al. The effect of tripalmitin crystallization on the thermomechanical properties of candelilla wax organogels[J]. Food Biophysics, 2009, 4(3): 199-212. DOI:10.1007/s11483-009-9118-7.
[19]ROGERS M A, WRIGHT A J, MARANGONI A G. Oil organogels:the fat of the future?[J]. Soft Matter, 2009, 5(8): 1594-1596.DOI:10.1039/b822008p.
[20]杨扬, 殷乐, 尹芳华, 等. 几种食用油的核磁共振光谱特征与地沟油的快速检测[J]. 中国油脂, 2015, 40(7): 45-50. DOI:10.3969/j.issn.1003-7969.2015.07.010.
[21]ROGERS M A, WRIGHT A J, MARANGONI A G. Crystalline stability of self-assembled fibrillar networks of 12-hydroxystearic acid in edible oils[J]. Food Research International, 2008, 41(10): 1026-1034. DOI:10.1016/j.foodres.2008.07.012.
[22]CHEN C H, TERENTJEV E M. Aging and metastability of monoglycerides in hydrophobic solutions[J]. Langmuir, 2009, 25(12):6717-6724. DOI:10.1021/la9002065.
[23]池建伟, 李阳, 张虹, 等. β-谷甾醇与γ-谷维素键合特征的红外光谱分析[J]. 中国粮油学报, 2013, 28(8): 97-101. DOI:10.3969/j.issn.1003-0174.2013.08.020.
[24]傅红, 张虹, 郑丽婷, 等. 有机凝胶构筑液态油脂晶体网络的研究进展[J]. 中国粮油学报, 2015, 30(2): 136-141.
[25]BOT A, WGM A. Structuring of edible oils by mixtures of γ-oryzanol with β-sitosterol or related phytosterols[J]. Journal of the American Oil Chemists’ Society, 2006, 83(6): 513-521. DOI:10.1007/s11746-006-1234-7.
[26]ARJEN B, RUUD D A, ELIC R. Fibrils of γ-oryzanol + β-sitosterol in edible oil organogels[J]. Journal of the American Oil Chemists’Society, 2008, 85(12): 1127-1134. DOI:10.1007/s11746-008-1298-7.
[27]SAWALHA H, MARGRY G, ADEL R D, et al. The influence of the type of oil phase on the self-assembly process of γ-oryzanol +β-sitosterol tubules in organogel systems[J]. European Journal of Lipid Science & Technology, 2013, 115(3): 295-300. DOI:10.1002/ejlt.201100395.
[28]SHRESTHA L K, SATO T, ACHARYA D P, et al. Phase behavior of monoglycerol fatty acid esters in nonpolar oils: reverse rodlike micelles at elevated temperatures[J]. Journal of Physical Chemistry B,2006, 110(25): 12266-12273. DOI:10.1021/jp060587p.
[29]WIEBA H H, BROWN G H, WOLKEN J J. Liquid crystals and biological structures[J]. Bioscience, 1979, 29(12): 181-182.DOI:10.2307/1307677.
[30]NILSSON F, SÖDERMAN O, JOHANSSON I. Physical-chemical properties of the n-octyl β-D-glucoside/water system. a phase diagram,self-diffusion NMR, and SAXS study[J]. Langmuir, 2002, 12(4): 902-908. DOI:10.1021/la950602+.
[31]SIDDIG M A, RADIMAN S, MUNIANDY S V, et al. Structure of cubic phases in ternary systems glucopone/water/hydrocarbon[J].Colloids & Surfaces A Physicochemical & Engineering Aspects, 2004,236(1/2/3): 57-67. DOI:10.1016/j.colsurfa.2004.01.023.
