芝麻林素的酸催化反应与抗氧化性分析
2018-05-23李晓栋汪学德王楠楠马宇翔
李晓栋,汪学德*,王楠楠,马宇翔
(河南工业大学粮油食品学院,河南 郑州 450001)
芝麻林素是芝麻油中特有的一种具备生理活性的木脂素类化合物,在芝麻油中平均质量分数为0.27%,仅次于芝麻素(均值0.36%)[1],可采用高效液相色谱(high performance liquid chromatography,HPLC)和紫外检测器检测芝麻林素,其紫外最大吸收波长为287 nm和235 nm[2],甲醇或乙醇是芝麻林素提取的常用溶剂[3]。
芝麻林素具有降低血浆和肝脏中胆固醇含量、抑制Δ5去饱和酶、抗肿瘤等生理功能[4-6],由于芝麻林素不含有酚羟基,其体内的脂质抗氧化作用则不如芝麻酚、特丁基对苯二酚(tertiary butylhydroquinone,TBHQ)等抗氧化剂[7]。结构上,芝麻林素与芝麻素最大的区别就是芝麻林素含有乙缩醛氧桥结构,正因为此结构芝麻林素的稳定性较差,180 ℃高温作用2 h,芝麻林素热损耗达23.8%,生成芝麻酚等[8];Fukuda[9]、Huang Jinian[10]和李雪芳[11]等的研究表明在芝麻油和石油醚等非极性溶剂中芝麻林素遇酸不稳定,在乙缩醛氧桥处断裂,转化为芝麻酚和芝麻素酚,并给出了相应的转化历程,见图1。芝麻素酚表现出极高的热稳定性[12]、独特的体内生理活性[13-14]和突出的抗氧化能力[15-16]。本实验发现芝麻林素在不同极性的溶剂体系具有不同的酸催化反应现象,产物不尽相同,因而研究了石油醚、甲醇和乙醇体系中芝麻林素酸催化反应现象,以期更加了解芝麻林素的酸催化特性。冷榨芝麻油存在氧化稳定性较差的现象,因此设想利用芝麻林素酸催化产生芝麻酚和芝麻素酚,在一定条件下使得冷榨芝麻油中的芝麻林素转化为芝麻酚和芝麻素酚,从而提高冷榨芝麻油的氧化稳定性,对此设想的理论依据和可行性进行了初步探索。
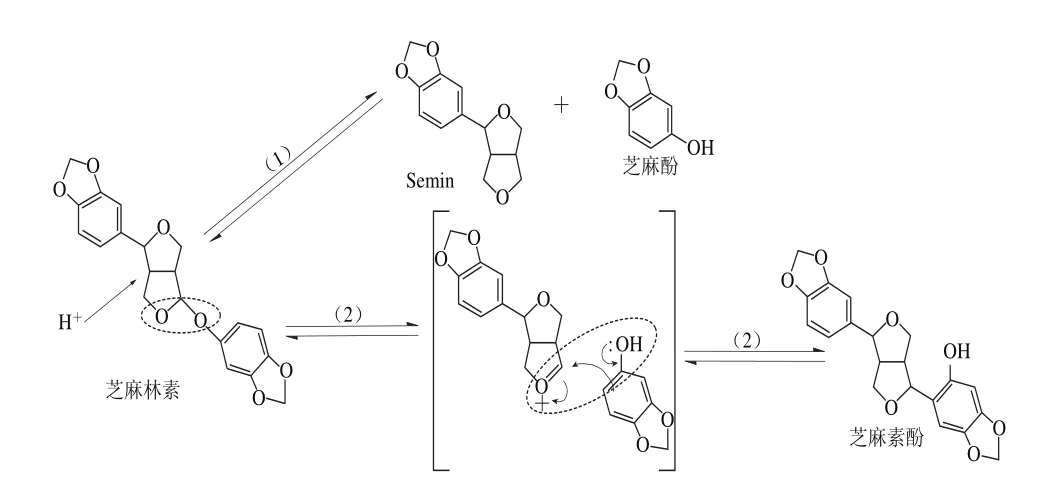
图1 芝麻林素酸催化反应过程Fig. 1 Reaction mechanism of sesamolin acid catalysis
1 材料与方法
1.1 材料与试剂
芝麻林素纯品 上海源叶生物科技有限公司;冷榨芝麻油由实验室自制。
芝麻林素、芝麻酚、芝麻素、TBHQ、丁基羟基茴香醚(butylated hydroxyanisole,BHA)、丁基羟基甲苯(butylated hydroxytoluene,BHT)、1,1-二苯基-2-三硝基苯肼(1,1-diphenyl-2-picrylhydrazyl,DPPH)(标准品) 上海阿拉丁生化科技股份有限公司;石油醚(60~90 bp)、盐酸、甲醇、乙醇、氨水(均为分析纯)洛阳化学试剂厂;磷钨杂多酸(phosphotungstic heteropoly acid,HPW) 国药集团化学试剂有限公司;甲醇(色谱纯) 美国VBS公司。
1.2 仪器与设备
e2695HPLC仪(配2489紫外检测器,Empower3软件数据处理系统) 美国Waters公司;UV759S紫外-可见分光光度计 上海精密科学仪器有限公司;Rancimat743氧化酸败仪 瑞士万通公司;AL204分析天平 梅特勒-托利多仪器(上海)有限公司。
1.3 方法
1.3.1 芝麻林素及酸催化产物的检测方法[17]
采用HPLC色谱仪和紫外检测器进行检测,色谱条件如下:色谱柱Sunfire C18(250 mm×4.6 mm,5 μm);柱温30 ℃;流动相甲醇-水(70∶30,V/V);流速0.8 mL/min;检测波长287 nm;进样量10 μL。
1.3.2 芝麻林素的酸催化反应
1.3.2.1 石油醚体系芝麻林素的酸催化反应
参考张丽霞[18]和孙强[19]等的研究,准确配制300 μg/mL的芝麻林素石油醚(60~90 bp)溶液,然后分别准确移取10 mL该溶液于反应管中,添加30 mg固体HPW,在60 ℃、500 r/min磁力搅拌条件下反应0、6、12、18、24、30、45、60 min,反应结束后快速冷却至室温,然后5 000 r/min离心10 min,将上层清液转移至10 mL离心管中,-20 ℃低温保存,备用。
分别取各反应时间下的芝麻林素反应液0.5 mL于试管中,氮气吹干,加1 mL甲醇复溶,过0.22 μm有机滤膜,HPLC法测定芝麻林素分解率。
1.3.2.2 甲醇体系芝麻林素的酸催化反应
称取约10 mg芝麻林素标准品溶解在47.5 mL的甲醇溶液中,完全溶解后加入2.5 mL的浓盐酸,室温下500 r/min磁力搅拌,在反应至0、1、3、6、10、15、20、25 min时分别取样1 mL于10 mL容量瓶中,滴加一滴甲基橙指示剂,用氨水调节至黄色时溶液呈中性,然后用甲醇定容,过0.22 μm滤膜后,HPLC法分析芝麻林素在5%盐酸-甲醇溶液中的转化情况。
1.3.2.3 乙醇体系芝麻林素的酸催化反应
芝麻林素溶解在乙醇溶液中,处理方法同1.3.2.2节。
1.3.3 芝麻林素的抗氧化性测定
1.3.3.1 多种抗氧化物质的抗氧化活性对比
分别配制300 μg/mL的芝麻素、芝麻林素、芝麻酚、TBHQ、BHA、BHT的乙醇溶液,并将其分别稀释至5、10、20、30、50、100、200 μg/mL,通过测定不同种类不同质量浓度抗氧化剂对DPPH自由基的清除能力评价其抗氧化活性。
配制0.02 mmol/L的DPPH-乙醇溶液,加样测定样液517 nm波长下的吸光度,以蒸馏水为空白[20]。DPPH自由基清除率公式如下:

式中:A1为3 mL抗氧化剂溶液+2 mL DPPH溶液的吸光度;A2为3 mL抗氧化剂溶液+2 mL无水乙醇溶液的吸光度;A3为3 mL乙醇溶液+2 mL DPPH溶液的吸光度。
1.3.3.2 石油醚体系芝麻林素分解产物的抗氧化活性测定
以1.3.2.1节备用样为样品,分别取2 份不同分解程度的芝麻林素反应液各0.1、0.3、0.5、3 mL于试管中,氮气吹干,加3 mL无水乙醇复溶,分别制成芝麻林素反应液稀释30、10、6 倍和未稀释样液,然后按照1.3.3.1方法测定其DPPH自由基清除率,与未分解芝麻林素溶液进行对比,分析酸催化后的芝麻林素反应产物清除DPPH自由基能力的变化。
1.3.4 酸催化芝麻林素提高冷榨芝麻油氧化稳定性的测定
称取50 g冷榨芝麻油,分别添加芝麻油质量的0.2%、0.4%、0.6%、0.8%、1.0%、1.2%的固体HPW于冷榨芝麻油中,反应温度60 ℃,常压下磁力搅拌反应1 h,然后离心,抽滤,水洗,真空干燥得到酸处理的冷榨芝麻油。测定各芝麻油中芝麻林素、芝麻酚的含量,采用氧化酸败仪测定各芝麻油样120 ℃的氧化诱导时间(oxidation induction time,OIT),评价其氧化稳定性[21]。
1.4 数据处理
采用Excel 2013、Origin 8.0软件进行数据处理。
2 结果与分析
2.1 芝麻林素的酸催化反应结果
芝麻林素分子结构中的乙缩醛氧桥不稳定,遇酸、遇热均会断开,芝麻林素裂解成芝麻酚和其他物质,并且在特殊酸性条件下芝麻林素还能异构化生成芝麻素酚,浸出芝麻油中芝麻林素的含量在精炼脱色阶段降低,其原因正是在酸性白土的作用下,芝麻林素发生了分解[9]。实验发现芝麻林素溶解在石油醚、甲醇、乙醇中时,采用不同的酸,芝麻林素均会损耗,但生成的物质不尽相同。
2.1.1 石油醚体系芝麻林素酸催化反应
由图2可知,随着反应时间的延长,在HPW作用下芝麻林素被逐渐转化,其含量逐渐下降。在反应的前18 min芝麻林素的转化速率很快,迅速被转化成芝麻酚和芝麻素酚,随后反应速率则逐渐变小,在反应1 h后,芝麻林素的分解率达到84.7%。图3反映出芝麻酚的生成情况,反应前期先是快速升高,然后达到顶值后缓慢下降,分析认为HPW催化芝麻林素分解,在反应前期主要分解为芝麻酚,反应后期主要为芝麻素酚,并且在后期芝麻酚在酸性条件下可能发生了聚合,导致含量下降[22]。
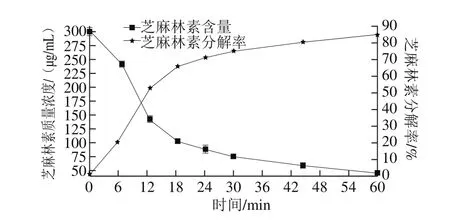
图2 石油醚中芝麻林素的含量及分解率变化Fig. 2 Changes in sesamolin content and degradation percentage in petroleum ether

图3 石油醚中芝麻酚含量变化Fig. 3 Change in sesamol content in petroleum ether
2.1.2 甲醇和乙醇体系芝麻林素酸催化反应
芝麻林素的提取工艺一般所用的试剂为甲醇和乙醇,研究中发现芝麻林素溶解在甲醇或乙醇中,在盐酸的作用下不稳定,也会发生酸催化反应。甲醇和乙醇体系盐酸催化芝麻林素反应中芝麻林素含量的变化情况见图4和图5。
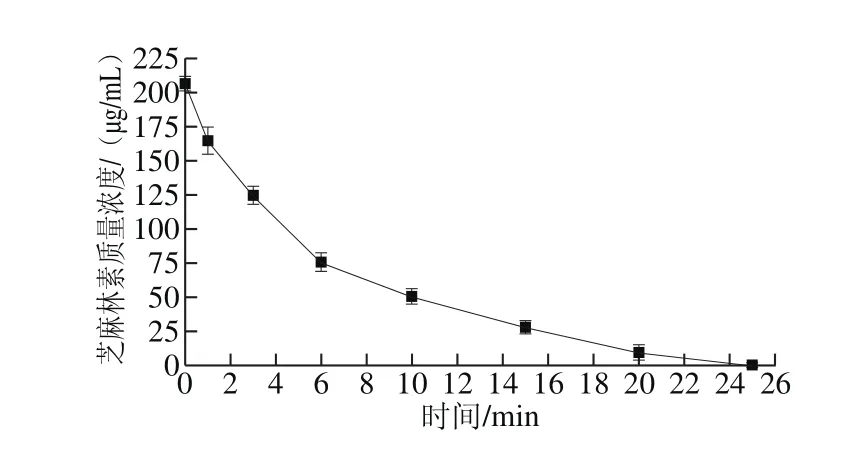
图4 甲醇体系芝麻林素含量的变化Fig. 4 Change in sesamolin content in methanol
由图4和图5可知,芝麻林素溶解在甲醇和乙醇中,加入5%的盐酸后,芝麻林素发生了反应,并且在2 种溶剂中芝麻林素含量的变化情况大体相同,芝麻林素的含量逐渐下降,反应速率由快变慢,25 min时芝麻林素消耗几近完全。实验表明甲醇和乙醇中溶解的芝麻林素在酸性条件下不稳定,也发生了转化。
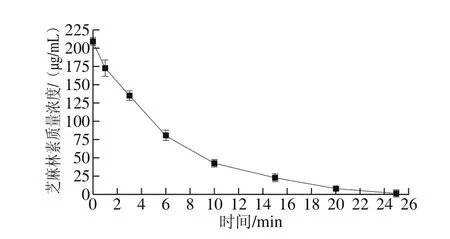
图5 乙醇体系芝麻林素含量的变化Fig. 5 Change in sesamolin content in ethanol
2.1.3 3 种体系芝麻林素酸催化反应产物
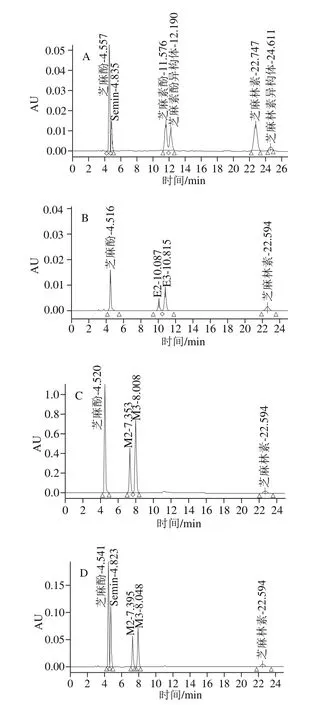
图6 不同溶剂体系芝麻林素酸催化反应液的HPLC图Fig. 6 HPLC profiles of sesamolin acid catalysis in different solvents
上述研究表明芝麻林素遇酸不稳定,易发生转化,芝麻林素溶解在甲醇、乙醇和石油醚3 种溶剂中酸催化的产物均不尽相同,芝麻林素溶解在3 种溶剂中酸催化反应产物HPLC图见图6。
由图6可知,芝麻酚是3 种溶剂体系中芝麻林素酸催化反应的共有产物。在石油醚体系中还生成了Semin(结构见图1)、芝麻素酚及其空间异构体,同时部分芝麻林素发生空间异构化。研究表明,HPW催化芝麻林素转化为芝麻素酚属于傅克-烷基化反应,反应历程是芝麻林素从乙缩醛氧桥处断开,生成芝麻酚和Semin中间体,两者部分结合成芝麻素酚,芝麻素酚又发生空间异构化[21];在乙醇和甲醇体系除了生成芝麻酚外,则各自生成不同于芝麻素酚的未知物E2、E3和M2、M3,采用适量的HPW催化甲醇和乙醇体系中的芝麻林素,反应产物与盐酸催化时相同,表明与催化剂无关,同时实验发现采用盐酸催化一定比例的甲醇-水溶解的芝麻林素时,反应产物中又出现了Semin,并且M2、M3的含量相对降低(图6D)。乙醇体系中也发现相同的情况,推测分析甲醇和乙醇溶剂本身参与了盐酸催化芝麻林素的反应。以甲醇为例,浓盐酸使得甲醇中醇羟基的H电离生成CH3—O-,充足的CH3—O-能够与Semin中间体结合,再经过未知的反应生成M2和M3,此时几乎没有Semin的产生,甲醇中加入水后,盐酸促进水电离,甲醇中醇羟基的H电离程度下降,没有足够的CH3—O-,反应则主要生成芝麻酚和Semin。本实验只揭示了芝麻林素在甲醇和乙醇中具有不同于石油醚中的酸催化反应现象及反应产物,E2、E3和M2、M3的结构则需要进一步的研究确定,进而才能更好地分析相应的反应机理。
2.2 芝麻林素的抗氧化性结果
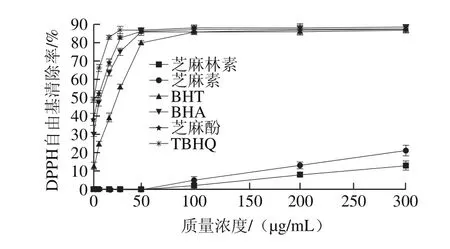
图7 不同抗氧化剂DPPH自由基清除率曲线Fig. 7 Concentration-dependent DPPH radical scavenging effects of different antioxidants
采用DPPH自由基清除率来评价抗氧化剂的抗氧化能力时,常选择清除率达到50%时抗氧化剂的物质的量浓度作为评价指标,即半数抑制浓度IC50,数值越小抗氧化能力则越强[23-24]。由图7可看出,TBHQ、芝麻酚、BHA和BHT的IC50质量浓度分别约为5、9、12 μg/mL和27 μg/mL,对应物质的量浓度依次为0.033、0.065、0.067 mmol/L和0.123 mmol/L,而芝麻素和芝麻林素质量浓度为300 μg/mL(物质的量浓度分别为0.847 mmol/L和0.810 mmol/L)时DPPH自由基清除能力分别仅为21.2%和11.2%,对比分析可知芝麻林素和芝麻素的自由基清除能力远低于其他4 种抗氧化剂,即芝麻林素和芝麻素的抗氧化能力远低于其他4 种抗氧化剂。前4 种抗氧化剂均含有酚羟基,可提供氢原子使得自由基转化为稳态物质,抗氧化剂自身形成的酚类自由基可形成稳定的共振体[25-26],因而具备较强的自由基清除能力,芝麻素和芝麻林素不含酚羟基,故而自由基清除能力较弱。
DPPH自由基清除实验表明,芝麻林素和芝麻素的抗氧化能力很弱,但芝麻酚的抗氧化能力则相对较强,而2.1.1节研究表明HPW可催化石油醚体系中的芝麻林素转化为芝麻酚和芝麻素酚,其反应产物的抗氧化能力将会升高,随着石油醚体系中芝麻林素的逐渐分解,其反应产物抗氧化能力的变化,由于芝麻酚的DPPH自由基清除能力很强,所以将不同分解率的芝麻林素反应液稀释不同的倍数,并与未分解的芝麻林素原液进行比较,结果见图8。
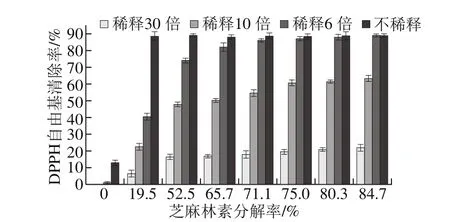
图8 不同分解率的芝麻林素反应液DPPH自由基清除能力Fig. 8 DPPH radical scavenging capacity of sesamolin with different degradation degrees
由图8可知,芝麻林素酸催化后,不同分解程度下反应产物的DPPH自由基清除能力均有很大幅度的提升,即使分解率仅为19.5%的芝麻林素反应液稀释10 倍后清除自由基的能力仍然大于300 μg/mL的芝麻林素原液,芝麻林素分解率不小于52.5%的反应液即使再稀释30 倍,其清除自由基的能力仍大于芝麻林素原液。以分解率为65.7%、稀释10 倍时50.2%的DPPH自由基清除能力计算,约20 μg/mL(0.054 mmol/L)芝麻林素的完全转化产物就可以达到自由基的半数清除率,其抗氧化活性仅次于IC50为0.033 mmol/L的TBHQ。
综合上述两部分的研究可知,6 种抗氧化剂的清除DPPH自由基能力为TBHQ>芝麻酚>BHA>BHT>芝麻素>芝麻林素,一定程度上代表了6 种抗氧化物质抗氧化能力的相对大小;芝麻林素的抗氧化能力很弱,但是经HPW催化后其反应产物表现出较强的抗氧化能力。
2.3 酸催化芝麻林素提高冷榨芝麻油氧化稳定性结果
研究表明[27],120 ℃热榨芝麻油的OIT为13.46 h,冷榨芝麻油仅为4.43 h,意味着冷榨芝麻油的氧化稳定性较差,货架期较短,亟待提高。芝麻油中芝麻林素含量在123~459 mg/100 g范围内,根据HPW催化石油醚体系中芝麻林素转化为芝麻酚和芝麻素酚的研究结果来设想,石油醚溶解芝麻林素几乎等同于油脂溶解芝麻林素,如果直接在冷榨芝麻油中添加HPW使得芝麻林素全部转化,则生成的芝麻酚和芝麻素酚可以提高冷榨芝麻油的氧化稳定性。HPW是“绿色”固体酸催化剂,催化活性高,环境良好[28],HPW相对分子质量超过2 880,易溶于水,通过简单的离心和水洗就能从油脂中脱除[22],同时HPW的大鼠口服半数致死剂量为3 300 mg/kg,半数致死剂量与食盐相当,毒性较小,并无已知的过敏性现象,相对安全[29],因此采用不同添加量的HPW在60 ℃处理冷榨芝麻油(芝麻林素含量为366.02 mg/100 g),初步探索HPW催化芝麻林素提高冷榨芝麻油氧化稳定性的可能。
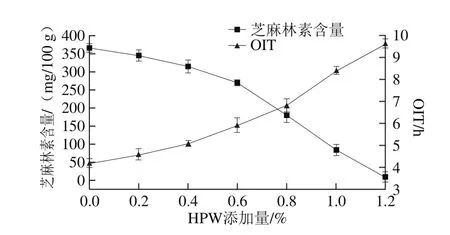
图9 HPW添加量对芝麻林素含量及芝麻油OIT值的影响Fig. 9 Effect of HPW concentration on sesamolin content and OIT value

图10 HPW添加量对芝麻油中芝麻酚含量的影响Fig. 10 Effect of HPW concentration on sesamol content in sesame oil
由图9和图10可以看出,随着催化剂HPW添加量的增加,芝麻油中的芝麻林素含量逐渐降低,最终芝麻林素几乎完全转化,芝麻酚和芝麻素酚的含量逐渐升高,最终芝麻酚的含量高达86.64 mg/100 g;冷榨芝麻油的OIT值也具有显著地提高,从4.2 h提升到9.74 h,提升了1.32 倍,表明酸催化芝麻林素分解产生的芝麻酚和芝麻素酚确实提高了冷榨芝麻油的氧化稳定性。
初步探索实验结果表明,酸催化芝麻林素确实可以提高冷榨芝麻油的氧化稳定性,并且是利用固体酸催化剂在冷榨芝麻油的内部将芝麻林素转化为具有较强抗氧化能力的芝麻酚和芝麻素酚,避免了具有潜在危害的合成抗氧化剂TBHQ等的使用[30]。但相应催化剂的选择、工艺参数的优化以及酸催化处理对芝麻油理化指标的影响需要进一步的研究。
3 结 论
芝麻林素遇酸不稳定,在不同溶剂体系酸催化反应的产物不尽相同,芝麻酚是共同产物,石油醚体系产生Semin和芝麻素酚,甲醇和乙醇体系均出现不同未知物;6 种抗氧化剂的DPPH自由基清除能力大小为TBHQ>芝麻酚>BHA>BHT>芝麻素>芝麻林素,300 μg/mL石油醚体系芝麻林素酸催化反应所得反应产物的DPPH自由基清除能力则大幅度提高,转化率仅为19.5%的反应液DPPH自由基清除能力就远超芝麻林素原液,芝麻林素的酸催化反应产物表现出较强的抗氧化能力;将催化剂HPW直接添加到冷榨芝麻油中,在一定反应条件下随着HPW催化剂添加量的增加,冷榨芝麻油中的芝麻林素含量逐渐减少,生成芝麻酚和芝麻素酚,同时冷榨芝麻油的OIT值逐渐升高,氧化稳定性增强,表明酸催化芝麻林素提高冷榨芝麻油氧化稳定性的设想可行,值得进一步研究。
参考文献:
[1]张海洋. 芝麻加工技术[M]. 郑州: 河南人民出版社, 2011: 34.
[2]黄纪念, 宋国辉, 孙强, 等. HPLC测定芝麻油中木脂素类化合物含量研究[J]. 中国粮油学报, 2011, 26(1): 120-123.
[3]黄纪念, 宋国辉, 孙强, 等. 芝麻林素和芝麻素分离纯化研究[J].河南农业科学, 2009, 38(9): 79-82.
[4]SUGANO M, INOUE T, KOBA K, et al. Influence of sesame lignans on various lipid parameters in rats[J]. Agricultural & Biological Chemistry, 1990, 54(10): 2669-2673. DOI:10.1080/00021369.1990.10 870374.
[5]SHIMIZU S, AKIMOTO K, SHINMEN Y, et al. Sesamin is a potent and specific inhibitor of delta 5 desaturase in polyunsaturated fatty acid biosynthesis[J]. Lipids, 1991, 26(7): 512-516. DOI:10.1007/BF02536595.
[6]冯志勇, 谷克仁. 芝麻中木脂素的组成、结构及其生理功能[J]. 中国油脂, 2004, 29(7): 56-59.
[7]NAMIKI M. The chemistry and physiological functions of sesame[J]. Food Reviews International, 1995, 11(2): 281-329.DOI:10.1080/87559129509541043.
[8]王蒙, 张丽霞, 黄纪念, 等. 高温下芝麻林素对大豆油的抗氧化及其作用机理初探[J]. 食品工业科技, 2015, 36(22): 76-80.DOI:10.13386/j.issn1002-0306.2015.22.007.
[9]FUKUDA Y, NAGATA M, OSAWA T, et al. Contribution of lignan analogues to antioxidative activity of refined unroasted sesame seed oil[J]. Journal of the American Oil Chemists’ Society, 1986, 63(8):1027-1031. DOI:10.1007/BF02673792.
[10]HUANG J N, SONG G, ZHANG L, et al. A novel conversion of sesamolin to sesaminol by acidic cation exchange resin[J]. European Journal of Lipid Science & Technology, 2012, 114(7): 842-848.DOI:10.1002/ejlt.201100247.
[11]李雪芳, 黄纪念, 张丽霞, 等. 反应介质对芝麻林素转化生成芝麻素酚的影响[J]. 中国粮油学报, 2015, 30(3): 111-115.
[12]NAMIKI M. Nutraceutical functions of sesame: a review[J]. Critical Reviews in Food Science and Nutrition, 2007, 47(7): 651-673.DOI:10.1080/10408390600919114.
[13]UM M Y, AHN J Y, KIM M K, et al. Sesaminol glucosides protect β-amyloid induced apoptotic cell death by regulating redox system in SK-N-SH cells[J]. Neurochemical Research, 2012, 37(4): 689-699.DOI:10.1007/s11064-011-0658-0.
[14]KANG M H, KATSUZAKI H, OSAWA T. Inhibition of 2,2’-azobis(2,4-dimethylvaleronitrile)-induced lipid peroxidation by sesaminols[J]. Lipids, 1998, 33(10): 1031-1036. DOI:10.1007/s11745-998-0302-y.
[15]DACHTLER M, PUT F H M V D, STIJIN F V, et al. On-line LCNMR-MS characterization of sesame oil extracts and assessment of their antioxidant activity[J]. European Journal of Lipid Science &Technology, 2010, 105(9): 488-496. DOI:10.1002/ejlt.200300835.
[16]FUKUDA Y, OSAWA T, KAWAKISHI S R, et al. Chemistry of lignan antioxidants in sesame seed and oil[C]. ACS symposium series (USA),1994, 547(27): 264-274. DOI:10.1021/bk-1994-0547.ch027.
[17]卢跃鹏, 胡筱静, 汪芳芳, 等. 高效液相色谱法同时测定芝麻油中芝麻素和芝麻林素含量[J]. 食品科技, 2013, 38(5): 297-302.DOI:10.13684/j.cnki.spkj.2013.05.019.
[18]张丽霞, 孙强, 宋国辉, 等. 一种催化芝麻林素制备芝麻素酚的方法:CN104059081A[P]. 2014-09-24.
[19]孙强, 宋国辉, 詹传保, 等. 一种芝麻素酚的制备方法: CN101648957 B[P]. 2011.
[20]杨虎, 张生堂, 高国强. 玫瑰黄酮的提取及其清除DPPH自由基活性研究[J]. 食品科学, 2012, 33(24): 152-155. DOI:10.7506/spkx1002-6630-201224031.
[21]孙曙庆. 油脂氧化稳定性的研究[J]. 食品与发酵工业, 1999, 25(3):20-22.
[22]李雪芳. 磷钨酸催化芝麻林素转化制备芝麻素酚的研究[D]. 郑州:河南农业大学, 2014: 42-53.
[23]张志国, 陈锦屏, 邵秀芝, 等. 红枣核类黄酮清除DPPH自由基活性研究[J]. 食品科学, 2007, 28(2): 67-70. DOI:10.3321/j.issn:1002-6630.2007.02.014.
[24]王会. 筛选和评价天然抗氧化剂的方法-DPPH法[J]. 广州化工,2013, 41(22): 30-32.
[25]蔡新华, 钱小君. 油脂抗氧化剂的研究进展[J]. 粮食与食品工业,2013, 20(4): 33-36.
[26]毕艳兰. 油脂化学[M]. 北京: 化学工业出版社, 2009: 81-87.
[27]刘玉兰, 陈刘杨, 汪学德, 等. 不同压榨工艺对芝麻油和芝麻饼品质的影响[J]. 农业工程学报, 2011, 27(6): 382-386.
[28]童金辉, 李臻, 夏春谷. 环境友好催化氧化研究进展[J]. 化学进展,2005, 17(1): 96-110.
[29]磷钨酸. 化学品数据库[DB/OL]. [2017-06-14]. http://www.basechem.org/chemical/35109.
[30]BAST A, HAENEN G R. The toxicity of antioxidants and their metabolites[J]. Environmental Toxicology & Pharmacology, 2002,11(3/4): 251-258. DOI:10.1016/S1382-6689(01)00118-1.
