HPLC-ICP-MS法测定牛肝菌中汞的形态
2018-05-15杨玲春丁元明王英张薇张银殷红陈宏仙李云飞朱红玉陈芸陈丽萍
杨玲春,丁元明,王英,张薇,张银,殷红,陈宏仙,李云飞,朱红玉,陈芸,陈丽萍
(云南出入境检验检疫局检验检疫技术中心,云南昆明650228)
汞(Hg)是一种对人体健康产生危害的重金属元素,具有强挥发性、生物富集性和高毒性,普遍存在于大气、土壤及水体中[1-3]。Hg及其化合物可通过呼吸道、食物链和皮肤接触等多种途径侵入人体,由于Hg特殊的理化性质,不易排出体外,超出一定限量时可以造成大脑、中枢神经系统、消化系统及肝、肾的损害,严重危害人体健康[4-5];自然界的汞主要以金属汞、无机汞(Hg2+)和有机汞(MeHg、EtHg、PhHg)的形式存在,其对生物体毒性的大小并不仅仅取决于该元素的总量,而是与该元素的化学形态密切相关,同种元素不同形态之间的毒性及可利用性常存在较大差异。有机汞因具有脂溶性,易被机体所吸收,其毒性远大于无机汞,尤其是甲基汞对中枢神经系统易造成不可逆的损害[6-7]。因此,有必要建立快速、有效的汞形态分析方法。
牛肝菌(Boletus fungi)是一种珍稀名贵的野生食用菌,富含蛋白质、氨基酸、多糖、维生素及多种矿物质元素,因其味道鲜美,营养丰富,被认为是理想的绿色健康食品,深受国内外消费者喜爱,在国际贸易中牛肝菌是重要的创汇农副产品[8]。多数野生食用菌对重金属Hg有很强的富集能力,子实体中的重金属含量与土壤、水分、大气等生长环境因子具有密切联系[9]。牛肝菌在生长过程中对Hg、As、Cd、Pb等多种有毒重金属元素均具有强富集作用,尤其是Hg含量超标问题凸显,对消费者身体健康和生命安全造成威胁[10]。因此,研究牛肝菌或牛肝菌制品中汞元素的化学形态对正确认识牛肝菌中汞元素对人体的危害具有重要意义。
目前测定汞形态的方法很多[11]。最早的方法为气相色谱法,上世纪80年代以后,原子发射光谱(atomic emission spectroscopy,AES)、原子荧光光谱(atomic fluorescence spectrometry,AFS)、电感耦合-等离子体质谱(inductively coupled plasma-mass spectrometry,ICPMS)等元素分析仪器与高效液相色谱(high performance liquid chromatograph,HPLC)联用技术发展的日趋完善,已广泛应用于材料和生命科学样品中元素的形态分析[12-14]。其中ICP-MS具有极低的检出限、较宽的线性范围、可同时测定多种元素、分析速度快、线性范围宽、灵敏度高等优点,成为形态分析中首选的检测方法[15]。本文采用微波萃取并结合高效液相色谱-电感耦合等离子体质谱联用技术,建立了快速、准确测定牛肝菌中不同形态汞元素的方法,为全面客观评价牛肝菌中汞元素的危害提供基础数据。
1 材料与方法
1.1 材料与试剂
5个批次的牛肝菌干片均来源于云南省楚雄州南华县,试验编码为S1~S5。
醋酸铵(分析纯)、甲醇(色谱纯):默克公司;盐酸(36.0%~38%,分析纯):西陇科学股份有限公司;L-半胱氨酸(分析纯):上海阿拉丁生化科技股份有限公司;甲基汞标准溶液[(GBW08675,76.6mg/kg(以甲基汞计)]:中国计量科学研究院;乙基汞标准溶液[(GBW(E)081524,75.3mg/kg(以乙基汞计)]:中国计量科学研究院;二价汞离子标准溶液[(GSB04-1729-2004,1 000mg/kg(以 Hg计)]:国家有色金属及电子材料分析测试中心;试验用水:超纯水。
1.2 仪器与设备
1200型高效液相色谱仪、8800型三重四级杆电感耦合等离子体质谱仪:美国Agilent科技有限公司;GM300型刀式混合研磨仪:德国Retsch公司;XPE204型电子天平:瑞士Mettler公司;4-start9609BNWP型pH计:美国奥立龙;Milli-Q纯水系统:美国Millipore公司;3K15型高速冷冻离心机:德国SIGMA公司。
1.3 方法
1.3.1 仪器条件
色谱柱(150 mm×4.6 mm,5μm):Agilent Eclipse plus C18色谱柱;进样量:100μL;柱温:30℃;流速为1.0mL/min;流动相:A相为甲醇,B相为10mmol/L醋酸铵(含0.12%L-半胱氨酸)并用10%氨水调节pH值至 7.5,A ∶B(8∶92,体积比)混合等度淋洗。
RF入射功率:1 550W;RF匹配电压1.74 V;同心圆雾化器,载气为纯度≥99.99%的氩气,等离子体气体流速:15.0 L/min;载气流速:0.65 L/min;辅助气体流速:0.45 L/min;蠕动泵转速:0.1 r/s;采样深度:8mm;检测质量数:m/z=202(Hg);停留时间为 0.5 s(m/z=202)。
1.3.2 混合标准储备液的配制
精密吸取二价汞、甲基汞和乙基汞标准溶液用甲醇配成质量浓度为1 000μg/L的混合标准储备液,置于棕色试剂瓶中,避光保存于4℃冰箱中备用。
1.3.3 样品前处理方法
称取研磨仪磨细的牛肝菌样品0.2 g于萃取用玻璃管中,放入磁性搅拌子,加入10mL萃取液(0.07mol/L的HCl),用微波萃取仪在55℃,压力15MPa,功率110W,保持15min的条件下进行萃取。萃取完成后放入冰箱中静置5 min,将上清液转移至离心管中,14 000 r/min,4℃,5min条件下离心,吸取上清液经0.2μm水相针式滤器过滤。过滤后吸取500μL样品溶液用流动相1∶1稀释,混匀,得到待测样液,同时做空白对照试验。
1.3.4 标准曲线及线性范围
将混合标准储备液用流动相稀释成浓度为1、10、25、50、100、200μg/L 的系列混合标准使用液(现用现配),进样量 100μL,以二价汞(Hg2+)、甲基汞(MeHg)、乙基汞(EtHg)的色谱峰面积与相应浓度分别进行线性回归分析,得到各自的标准曲线、相关系数和线性范围。以空白溶液基线信号3倍(即信噪比S/N为3 ∶1)时 Hg2+、MeHg、EtHg 对应的浓度为检出限。
1.3.5 方法学考察
1.3.5.1 精密度试验
精密吸取“1.3.2”项下制备混合标准储备液(10μg/L),按照“1.3.1”项下的仪器条件连续重复进样10次进样分析,记录峰面积。
1.3.5.2 重复性试验
取同一批次样品平行称取10份,经过样品前处理制备待测样液,按照“1.3.1”项下的试验条件依次进样分析,记录峰面积。
1.3.5.3 稳定性试验
取同一批次样品平行称取1份,经过样品前处理制备待测样液,按照“1.3.1”项下的试验条件,分别于0、2、4、6、8、12、24、48 h 进样分析,记录峰面积。
1.3.5.4 加标回收试验
应用本文建立的方法对已知含有量的牛肝菌样品进行测定,向牛肝菌提取液中分别添加3个不同浓度水平的二价汞、甲基汞、乙基汞的混合标准溶液,按照“1.3.1”项下的试验条件同时测定6个平行样计算加标回收率和相对标准偏差(RSD)。
2 结果与分析
2.1 色谱柱的选择
分别使用AgilentEclipseplus-C18(150mm×4.6mm,5μm)和Athena C18(250mm×4.6mm,5μm)两根色谱柱在其它试验条件不变的情况下分离标准样品,二价汞(Hg2+)出峰时间分别为1.98min和5.73min并且Athena C18色谱峰明显展宽,因此选用AgilentEclipse plus-C18(150mm×4.6mm,5μm)做为色谱分析柱。
2.2 色谱流速的选择
保持仪器其他试验参数不变的情况下考察了流动相流速分别为 0.6、0.8、1.0、1.2、1.4mL/min 时,3 种形态汞的分离情况。试验结果表明随着流动相流速的增加3种汞形态的保留时间明显缩短,信号强度明显增强,但是当流速高于1.0mL/min后,3种汞形态分离度开始下降,故试验选择流动相流速为1.0mL/min。
2.3 流动相的选择
在流动相中加入亲水性较强的L-半胱氨酸作为汞形态分析的络合物,可以明显缩短检测时间,同时考虑到L-半胱氨酸浓度太大对色谱柱有损害,因此选择0.12%L-半胱氨酸作为汞形态分析的络合剂。
选用质量浓度为8%(体积分数)的甲醇作为有机相有利于ICP-MS分析信号的稳定及消除汞的记忆效应;同时在流动相中加入适量的缓冲盐醋酸铵,能够有效改善拖尾现象,试验结果显示当醋酸铵含量增加到10mmol/L时,峰形和出峰时间达到最佳。
2.4 洗脱方式的选择
保持1.0mL/min流速条件下,当流动相中甲醇含量从5%增加至50%时,3种不同形态的汞出峰时间明显缩短,但各自的分离效果差,无法做到基线分离。因此,通过试验选择等度洗脱的方式有效解决了分离度差和洗脱时间长的问题。
2.5 等离子体质谱条件的优化
试验分别对载气流速以及采样深度进行考察,载气流速影响着雾化效率,对质谱信号的影响明显。随着载气流量的增大,质谱信号也随之增大,当载气流速达到0.65 L/min时信号值达到最大,继续增大载气流速,质谱响应信号反而减小,因此,试验采用的载气流速为0.65 L/min。采样深度对分离效果的影响不大,但对信号强度有很大影响,在采样深度为8mm时信号最强,故试验选择采样深度为8mm。
采用上述试验条件混合标准使用液(10μg/L)中的二价汞(Hg2+)、甲基汞(MeHg)、乙基汞(EtHg)色谱分离图见图1。
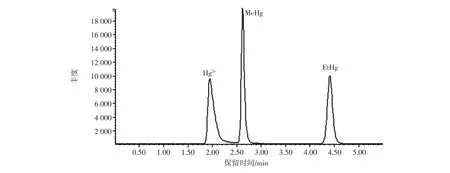
图1 标准溶液中二价汞(Hg2+)、甲基汞(MeHg)、乙基汞(EtHg)色谱图(10μg/L)Fig.1 Chromatogram of Hg2+,MeHg and EtHg(10 μg/L)
从图1可以看出3种形态的汞出峰顺序为二价汞、甲基汞、乙基汞,保留时间分别为1.98、2.64、4.47min,在5min之内二价汞、甲基汞、乙基汞实现了基线分离且峰形对称。
2.6 线性关系考察结果
计算得到二价汞(Hg2+)、甲基汞(MeHg)、乙基汞(EtHg)的标准曲线回归方程,试验结果见表1。

表1 二价汞、甲基汞和乙基汞的标准曲线Tab le1 Linear equation,correlation coefficientand detection lim itof Hg2+,M eHg and EtHg
由表1可以看出3种不同形态的汞在1μg/kg~200μg/kg范围内呈现出良好的线性关系且相关系数均大于0.999,二价汞、甲基汞和乙基汞检出限分别为0.005、0.008mg/kg和 0.005mg/kg
2.7 方法学考察
2.7.1 精密度试验
10次试验结果的二价汞(Hg2+)、甲基汞(MeHg)、乙基汞(EtHg)RSD值分别为1.95%、1.67%,1.83%均小于2%,表明仪器性能稳定,精密度良好。
2.7.2 重复性试验
10次试验结果的二价汞(Hg2+)、甲基汞(MeHg)峰面积的RSD值分别为1.95%、1.67%,均小于2%,表明方法重复性良好。
2.7.3 稳定性试验
计算结果显示二价汞(Hg2+)、甲基汞(MeHg)峰面积的的RSD值分别为2.38%、2.75%,均小于3%,表明供试品溶液在48 h内稳定。
2.7.4 加标回收试验
样品加标回收率见表2。试验结果表明在牛肝菌样品中,二价汞、甲基汞、乙基汞的6次平行测定值的相对标准偏差(RSD)均小于7%,加标平均回收率在72%~93%之间,表明加标回收率良好且具有良好的精密度。
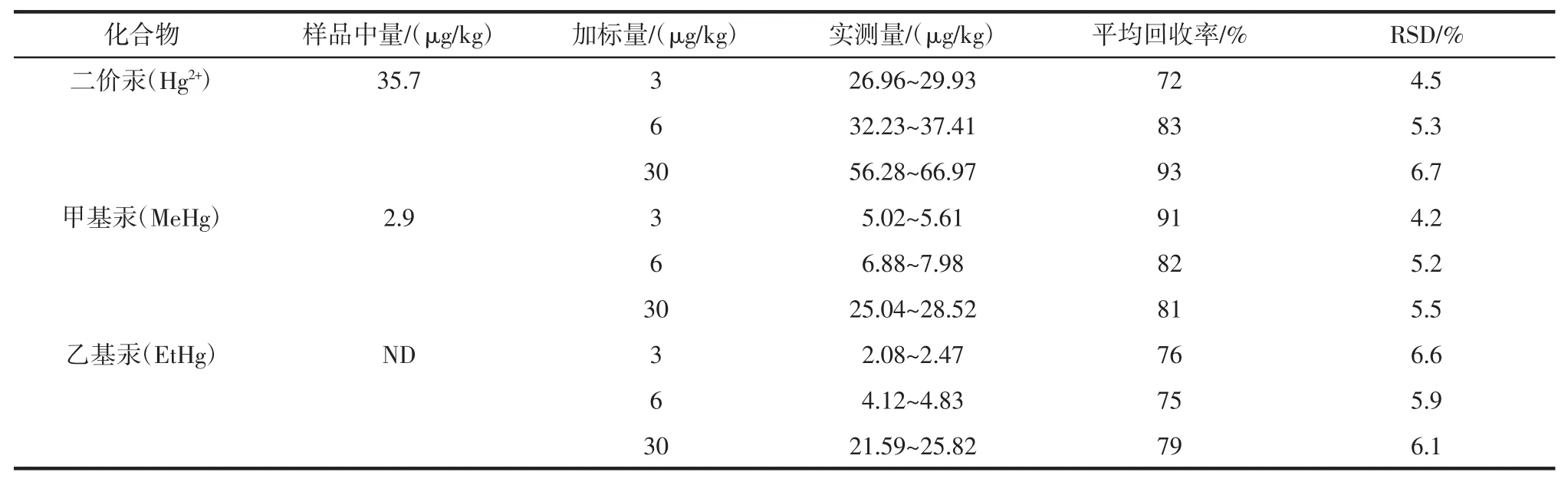
表2 样品加标回收率(n=6)Table2 Recovery testof Sam ple
2.8 实际样品的测定
应用本文建立的方法对市售的5个批次牛肝菌样品进行测定(表3)。结果表明在牛肝菌中主要以无机汞(Hg2+)的形式存在,含有少量甲基汞(MeHg)。该方法分离效果好,快速准确,具有检出限低、灵敏度高、重复性好等优点。
3 结论
试验建立了高效液相色谱-电感耦合等离子体质谱联用检测牛肝菌中不同价态汞元素的分离测定方法。样品采用微波萃取结合HPLC-ICP-MS联用的方法实现了对牛肝菌中不同价态汞元素的分离检测,方法加标平均回收率范围在72%~93%之间,相对标准偏差均小于7%,该方法操作简便、分离效果好、检出限低、灵敏度高、重复性好,检测时间短,5min内能够完全出峰,洗脱时间短,能够在亚浓度(μg/kg)水平检测不同价态汞元素;本研究可为今后制定野生食用菌中无机汞、甲基汞、乙基汞的标准检测方法提供参考,同时也对完善食用菌质量控制、检测方法及相关技术有重要意义。
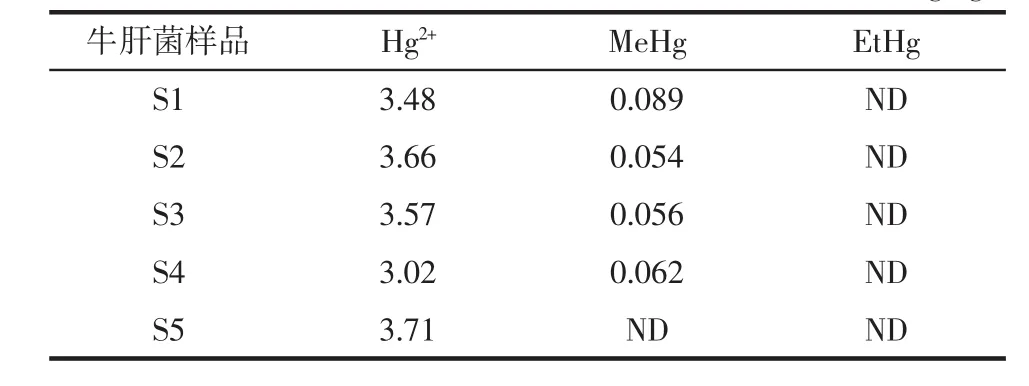
表3 牛肝菌样品中不同价态汞的含量Tab le3 The contentof Hg2+,M eHg and EtHg in Boletus fungi mg/kg
参考文献:
[1]Zhu S,Chen B,He M,et al.Speciation ofmercury in water and fish samplesby HPLC-ICP-MSaftermagnetic solid phaseextraction[J].Talanta,2017,171:213-219
[2]Bjørklund G,Dadar M,Mutter J,etal.The toxicology ofmercury:Current research and emerging trends[J].EnvironmentalResearch,2017,159:545-554
[3]吴晓云,郑有飞,林克思.我国大气环境中汞污染现状[J].中国环境科学,2015,35(9):2623-2635
[4]Kim K H,Kabir E,Jahan SA.A review on the distribution of Hg in the environment and its human health impacts[J].Journal of HazardousMaterials,2016,306:376-385
[5]Ha E,Basu N,Bose O S,et al.Current progress on understanding the impact ofmercury on human health[J].Environmental Research,2017,152:419-433
[6]Wai KM,Dai J,Yu PK,etal.Public health risk ofmercury in China through consumption of vegetables,amodelling study[J].EnvironmentalResearch,2017,159:152-157
[7]Karri V,Schuhmacher M,Kumar V.Heavymetals(Pb,Cd,As and MeHg)as risk factors for cognitive dysfunction:A general review of metalmixturemechanism in brain[J].Environmental Toxicology and Pharmacology,2016,48:203-213
[8]周玲仙,殷建忠.云南野生食用牛肝菌营养成分分析及评价[J].食用菌,2008,30(4):61-62
[9]杨天伟,张霁,Jerzy FALANDYSZ,等.云南常见牛肝菌属真菌中汞含量及食用安全评价[J].生态学杂志,2015,34(12):3518-3525
[10]马培,张丹,杨丽标,等.野生食用牛肝菌的重金属富集研究[J].环境科学与技术,2012,35(5):5-8
[11]杨凡,孟庆雄,彭珍华,等.电感耦合等离子体质谱联用技术应用进展[J].现代仪器,2012,18(5):1-6
[12]刘国珍,金泽祥.汞的形态分析进展[J].理化检验-化学分册,2000,36(1):38-41
[13]Díez S,Bayona JM.Determination of Hg and organomercury species following SPME:A review[J].Talanta,2008,77:21-27
[14]冯先进,屈太原.电感耦合等离子体质谱法(ICP-MS)最新应用进展[J].中国无机分析化学,2011,1(1):46-52
[15]祖文川,汪雨,李冰宁,等.ICP-MS相关联用技术在食品元素形态分析中的应用及进展[J].质谱学报,2013,34(4):247-256
