超声波处理对花生蛋白分子结构的影响
2018-05-15张文张丽芬陈复生王培
张文,张丽芬,陈复生,王培
(河南工业大学粮油食品学院,河南郑州450001)
花生是全球四大油料作物之一,在世界农业生产和贸易中占有重要地位。花生中蛋白含量为25%~35%,是植物蛋白质的第三大重要来源,占世界蛋白质供应量的11%,其营养价值与动物蛋白相似,且不含胆固醇,是一种较理想的可食用蛋白质资源[1]。但相对于大豆蛋白,花生蛋白的功能性质如乳化性、起泡性和凝胶性质都比较差,极大限制了其在食品领域的使用[2]。研究超声波处理对花生蛋白分子结构的影响,对于改变花生蛋白的功能特性进而拓宽花生蛋白的应用领域具有重要的意义。
超声波是一种高效可靠的改变蛋白质分子结构的方法,它产生的机械效应和空化作用能够破坏天然蛋白质分子之间的非共价相互作用,使肽键断裂并诱导亚基解离或聚集,导致蛋白质功能特性的变化[3]。相较于传统的几种物理改性方法如加热、冷冻、微波、高速搅拌处理和高压均质等,超声波具有快速有效的改性效果且不损失营养物质以及无毒无害等优点[4]。石燕等认为超声波处理后酪蛋白某些功能性质如起泡性和乳化性等改善,可能是超声波作用使酪蛋白分子中的螺旋结构部分展开,蛋白质分子的柔顺性增加所致[5]。此外,Zhang等研究发现超声波处理后花生蛋白的表面疏水性增加的同时有助于提高其乳化性能,其原因可能是超声作用诱导蛋白质解折叠,暴露出更多的疏水基团[6]。利用超声波这种新型物理改性方法,能有效改善花生蛋白的功能性质。但目前国内外对花生蛋白的改性研究主要集中在理化和功能性质方面,就超声波改性对花生蛋白分子结构的影响鲜有报道。因此,本文以花生蛋白粉为原料,通过HPLC、SDS-PAGE和FT-IR等方法研究了超声波改性后花生蛋白分子结构的变化规律,研究结果为超声波技术在蛋白质改性领域的应用提供了理论依据。
1 材料与方法
1.1 材料与仪器
帝心花生蛋白粉(花生蛋白样品蛋白含量为42.75%,纯化后样品蛋白含量为70.55%):河南帝鑫食品有限公司;SCIENTZ-IID型超声波细胞粉碎机、DC-2006节能型智能恒温槽:宁波新芝生物科技股份有限公司;90-2型恒温磁力搅拌器:上海亚荣生化仪器厂;GL-20C型高速冷冻离心机:上海安亭科学仪器厂;TU-1901双光束紫外可见分光光度计:北京谱析通用仪器有限公司;DDY-6D型电泳仪:北京市六一仪器厂;LGJ-25型冷冻干燥机:北京四环科学仪器厂有限公司。
1.2 试验方法
1.2.1 样品的纯化
花生蛋白粉→按料液比1∶8(g/mL)加入稀碱液(pH 8.0)→搅拌分散→离心20min(4 000 r/min)→取上清液→调pH值至4.5→离心15min(4 000 r/min)→收集沉淀→水洗后离心→调pH值到7.0→沉淀复溶→4℃透析24 h→冷冻干燥→样品保存至4℃备用
1.2.2 花生蛋白溶液的配置
将6 g花生蛋白粉溶于1 L pH 8.0的NaOH溶液,在25℃下以300 r/min的转速磁力搅拌2 h使花生蛋白均匀分散,待用。
1.2.3 超声波处理
将超声波探头置于花生蛋白悬浮液(70mL)液面下方3 cm处,恒温水槽控制温度,设置超声波占空比为50%,超声功率分别为336、672、1 008、1 344、1 680W/cm2;时间为 10、20、30、40、50min;温度为 5、15、25、35、45 ℃,超声波处理样品冻干备用。
1.2.4 高效凝胶渗透色谱(SE-HPLC)
采用TSK SEC 4000柱对标准蛋白进行分离。洗脱液为色谱级乙腈和娃哈哈纯净水(含0.05%三氟乙酸)(体积比),采样时间为25min。在280 nm的波长下进行蛋白质的检测。标准蛋白的分子量(kDa)如下所述:核糖核酸酶 A(13.7),卵清蛋白(44.3),醛缩酶(150)和甲状腺球蛋白(670)。每个样品平行测量3次。标准曲线:log(M)=-0.290 92x+4.714 5;R2=0.990 6。式中:x为出峰保留时间;M为标准蛋白分子质量。
1.2.5 十二烷基硫酸钠-聚丙烯酰胺凝胶电泳(SDSPAGE)
SDS-PAGE电泳依照Laemmli的方法改进[7]。制备12%的分离胶,4%的浓缩胶进行电泳。将样品溶解于pH=8的NaOH溶液后与样品缓冲液 (pH=6.8的0.5mol/LThis-HCl,巯基乙醇,10%SDS 溶液,0.5%的溴酚蓝,甘油,蒸馏水)按1∶1的体积比混合,然后沸水浴4min。取10μL处理后的样品上样,采用低分子量蛋白 markers(14 400Da~97 400Da)作为对照。电极缓冲液为 0.025mol/LTris、0.1%SDS、0.192mol/L 甘氨酸缓冲液,先将电流调至20mA进行电泳,至溴酚蓝前沿进入分离胶,再将电流调至30mA下进行1.5 h。电泳结束后,采用考马斯亮蓝R-250染色1.5 h,再用脱色液(95%乙醇、冰醋酸、蒸馏水按体积比25∶8∶67混合)进行脱色,直至可以清楚地辨别条带为止。
1.2.6 傅里叶红外光谱(FT-IR)分析
将1mg干燥后的花生蛋白样品与100mg干燥的溴化钾研磨至完全均匀,通过HY-12型压片机和压片模具,将样品混合物压制成透明薄片,扫描其红外光谱。在分辨率4 cm-1、扫描次数16次的条件下,采用全反射装置测定透明薄片在400 cm-1~4 000 cm-1范围内的吸收。
2 结果与讨论
2.1 超声波对花生蛋白分子量及其分布的影响研究
2.1.1 超声波强度对花生蛋白分子量分布的影响研究
超声波强度对花生蛋白分子量分布的影响如表1所示。
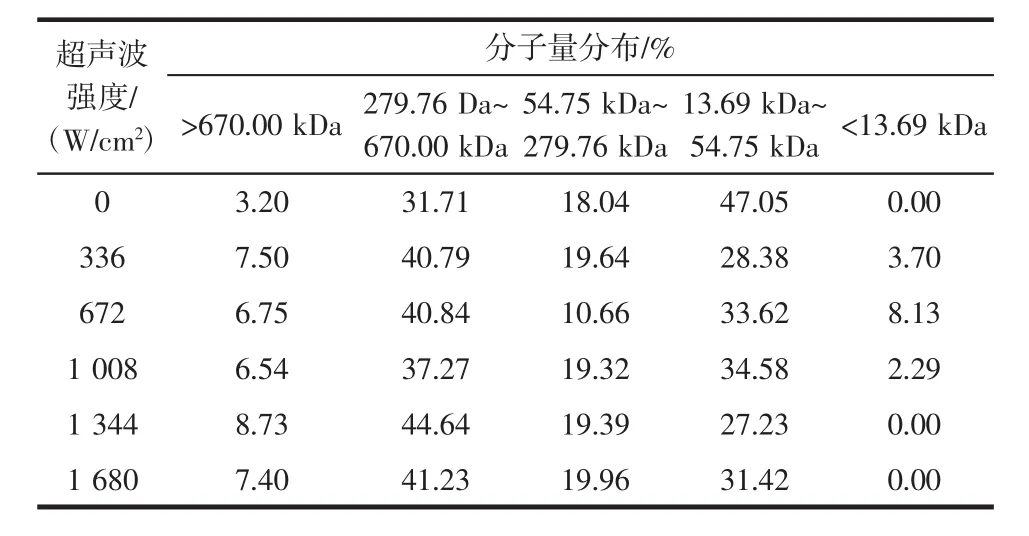
表1 超声波强度对花生蛋白分子量分布的影响Table 1 Effectofultrasound intensity on themolecular weight distribution of peanut protein
由表1可知,花生蛋白的分子量主要分布在279.76 kDa~670.00 kDa和 13.69 kDa~54.75 kDa范围之间。随着超声波强度的增大,分子量大于279.76 kDa的蛋白片段整体呈增加趋势,而分子量介于13.69 kDa~54.75kDa之间的蛋白片段减少,且分子量小于13.69kDa的蛋白片段随超声波强度的增强先增加后减少。结果表明,低强度超声波处理花生蛋白有小片段生成,而较高强度超声波处理可能会使蛋白发生聚集,生成大分子量的蛋白片段。此试验结果与孙英杰等的研究结果一致[8]。
2.1.2 超声波时间对花生蛋白分子量分布的影响研究
超声波时间对花生蛋白分子量分布的影响如表2所示。
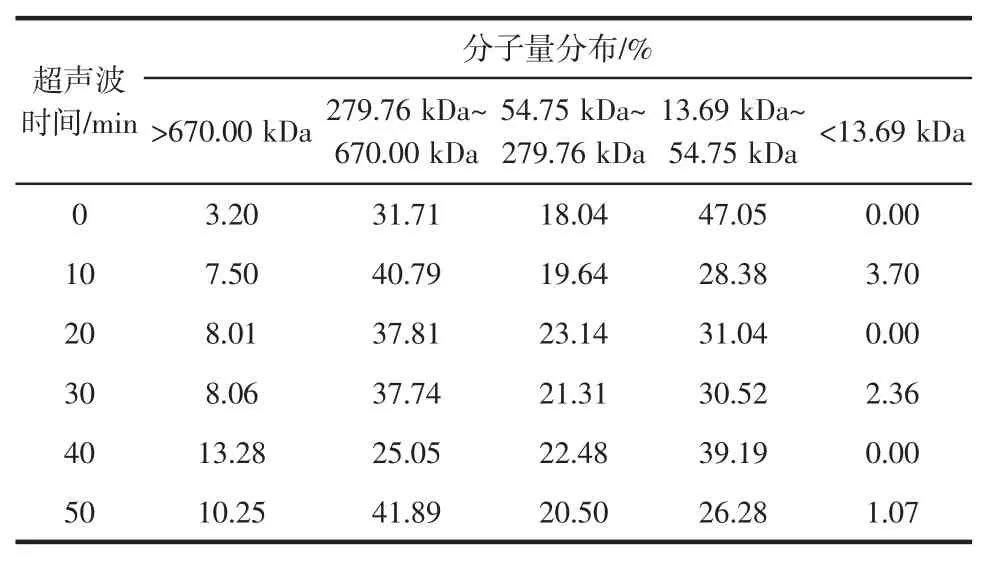
表2 超声波时间对花生蛋白分子量分布的影响Tab le2 Effectof ultrasound tim eon themolecularweight distribution of peanut protein
由表2可知,随超声波时间的延长,分子量在670.00 kDa以上的蛋白片段显著增加,而分子量分布在13.69 kDa~54.75 kDa范围之间的蛋白片段逐渐减少,且在超声时间为50min时达到最低值;此外,与空白样品相比,超声处理后的花生蛋白在分子量低于13.69 kDa处有新片段产生,说明超声作用使蛋白质的肽键断裂,促进了小分子的产生,但长时间的超声作用产生瞬时极端温度和压力导致蛋白变性,暴露出疏水基团使蛋白质产生聚集[9]。
2.1.3 超声波温度对花生蛋白分子量分布的影响研究
不同超声波温度处理下的花生蛋白分子量分布如表3所示。
由表3可知,与空白相比较,随超声波温度的升高分子量在279.76 kDa~670.00 kDa的蛋白片段增加,并在超声温度为45℃时达到最大为43.84%;而分子量分布在13.69 kDa~279.76 kDa范围之间的蛋白片段则逐渐减少,且超声温度为25℃时有少量小分子量片段生成。试验结果表明,花生蛋白部分亚基发生了降解,而大分子量片段的生成可能是加热过程中R基基团发生聚合现象[10]。
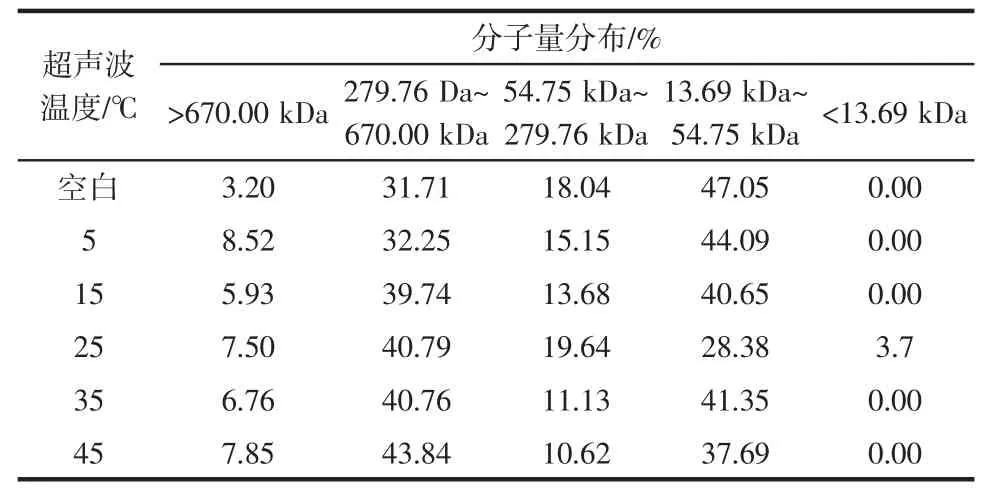
表3 超声波温度对花生蛋白分子量分布的影响Table3 Effectofultrasound temperatureon themolecularweight distribution of peanut protein
2.2 超声波处理对花生蛋白亚基的影响研究
超声波处理对花生蛋白亚基的影响见图1。

图1 超声波处理对花生蛋白亚基的影响Fig.1 Effectof u ltrasound on the subunitsof peanut protein
2.2.1 超声波强度对花生蛋白亚基的影响研究
如图1A所示为不同超声波强度处理后花生蛋白样品的SDS-PAGE电泳图。该花生蛋白呈现出典型的花生球蛋白、伴花生球蛋白Ⅰ和伴花生球蛋白II。与未经超声波处理的花生蛋白相比,不同超声波强度处理的花生蛋白条带分布没有明显的变化,说明超声波强度对花生蛋白亚基没有显著地影响。
2.2.2 超声波时间对花生蛋白亚基的影响研究
如图1B所示为不同超声波时间处理后花生蛋白样品的SDS-PAGE电泳图。与未经超声波处理的花生蛋白相比,不同超声波时间处理的花生蛋白在分子量为66.2 kDa附近条带增加,且在分子量为14.4 kDa处形成新条带。可能是超声波作用破坏了天然蛋白聚集颗粒间的非共价作用,并使其肽键断裂,导致部分蛋白亚基产生了不可逆降解[11],但随超声波时间的延长蛋白质变性发生聚集现象。此试验结果与超声波时间对花生蛋白分子量分布的影响结果一致。
2.2.3 超声波温度对花生蛋白亚基的影响研究
如图1C所示为不同超声波温度处理后花生蛋白样品的SDS-PAGE电泳图。与空白相比,分子量在66.2 kDa附近的条带有所增加,说明有大分子量的片段生成,可能是超声波作用产生的瞬时极端温度和压力共同导致蛋白质变性,暴露出更多的疏水集团导致蛋白质的聚集。
2.3 超声波处理对花生蛋白二级结构的影响研究
2.3.1 超声波处理对花生蛋白红外光谱特性的影响研究
超声波处理对花生蛋白红外光谱特性的影响见图2。
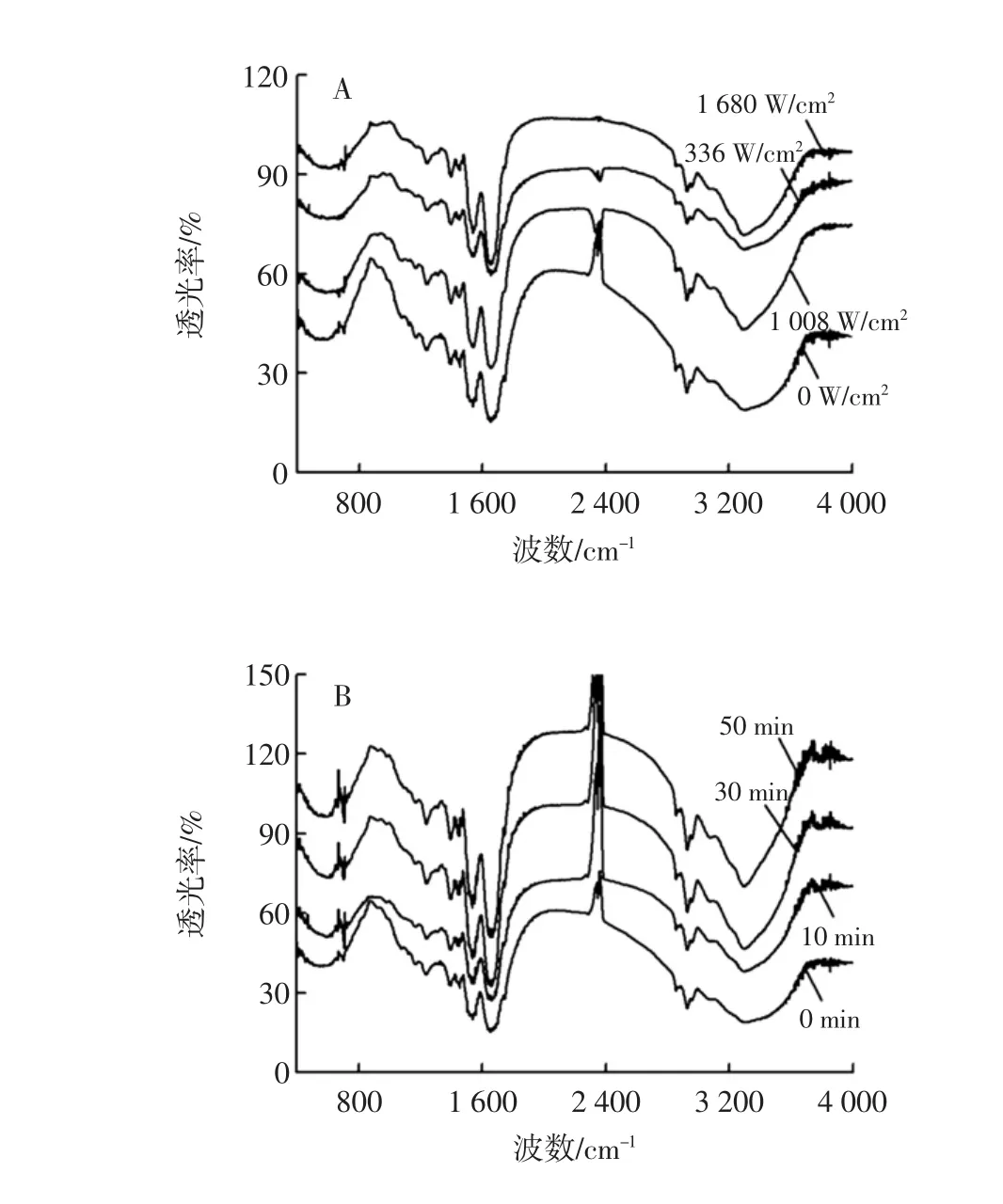

图2 超声波处理对花生蛋白FT-IR光谱特性的影响Fig.2 Effectof u ltrasonic treatmenton the FT-IR spectra of peanut protein
由图2可知,花生蛋白的酰胺I带(1 700 cm-1~1 600 cm-1)信号较强,由羰基(C=O)键伸缩振动产生,其峰型受蛋白质特定二级结构影响[12]。随超声波作用强度的增大和温度的升高,酰胺I带吸收峰发生蓝移,可能是超声波的空化作用和高温破坏了蛋白质分子内氢键,使峰位向高波的方向移动[13]。由图2A与2C可以看出,随超声波强度和温度的增加2 400 cm-1附近的吸收峰逐渐减弱甚至消失,可能是由于高强度超声使花生蛋白肽键断裂,导致其结构发生了改变[14];而图2B中此处的吸收峰却随超声时间的延长逐渐增强,可能是蛋白质的聚集所致。
2.3.2 超声强度对花生蛋白二级结构的影响研究
根据已有研究,蛋白质二级结构与各子峰间的对应关系为[15]:α-螺旋结构对应波数1 650 cm-1~1 658 cm-1,β-转角结构对应波数 1 660 cm-1~1 700 cm-1,无规卷曲结构对应波数 1 640 cm-1~1 650 cm-1,β-折叠结构对应波数为1 610 cm-1~1 640 cm-1。采用Peakfit软件对蛋白质酰胺Ⅰ带进行傅里叶去卷积光谱拟合分析,通过峰位归属确定二级结构种类和含量,计算结果见表4。
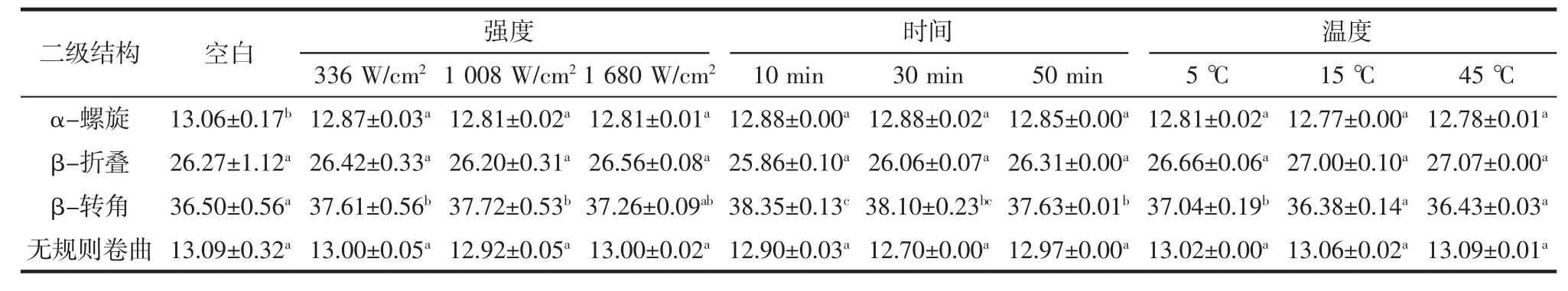
表4 超声波对花生蛋白二级结构的影响Table4 Effectof ultrasound on thesecondary structureof peanut protein%
由表4可以看出,花生蛋白主要组成为β-转角,占二级结构总量的36.50%。与空白相比,超声波处理后花生蛋白的α-螺旋结构比例整体呈下降趋势,β-转角结构比例增加,超声波处理形成的“空穴效应”及伴随着温度升高,对蛋白质二级结构的破坏作用比较明显,易造成二级结构的相互转化[16]。而不同超声波强度处理组之间花生蛋白二级结构变化并无显著差异(P>0.05),说明超声波强度对花生蛋白二级结构的影响并不显著。
随超声波时间的延长,花生蛋白的α-螺旋、β-折叠以及无规则卷曲结构比例无显著变化;而β-转角结构比例虽逐渐减少,但其含量相比于未经超声波处理样品均有不同程度增加,可能是超声波处理使蛋白质结构更加松散,导致β-转角结构比例增加,但随超声波时间的延长,蛋白质变性暴露出更多的疏水集团使蛋白质产生聚集,进而使其比例减少[17]。经不同超声波温度处理后,花生蛋白的α-螺旋结构比例有所降低,但各温度之间并无显著差异(P>0.05)。当超声波温度为5℃时,β-转角结构比例最大为37.04%;当温度升高到15℃时其比例略有降低,可能是加热过程中氢键断裂所致[18]。
3 结论
超声波改性使花生蛋白低分子量(13.69 kDa~54.75 kDa)片段分布比例降低,高分子量(>279.76 kDa)片段分布比例增加。电泳结果显示,超声波作用后花生蛋白亚基片段发生了不同程度的降解,但随超声波作用的增强,部分蛋白质发生了聚集。通过红外光谱对花生蛋白二级结构进行表征发现,超声波改性后花生蛋白的α-螺旋结构减少、β-转角结构增加,而β-折叠和无规则卷曲结构无显著变化;研究结果表明,超声波处理能够使花生蛋白结构发生改变。花生蛋白结构的改变势必会对其功能性质产生影响,而超声波对花生蛋白功能性质影响的机理还有待进一步研究,以便指导超声波技术更好地应用于蛋白质改性领域。
参考文献:
[1]赵晓燕,孙秀平,陈锋亮,等.花生蛋白的研究进展与开发利用现状[J].中国粮油学报,2011,26(12):118-122
[2]ZhaoG,Liu Y,ZhaoM,etal.Enzymatic hydrolysisand their effects on conformationaland functionalpropertiesofpeanutprotein isolate[J].Food Chemistry,2011,127:1438-1443
[3]Liurong H,Xiaona D,Chunhua D,et al.Changes in the structure and dissociation of soybean protein isolate induced by ultrasoundassisted acid pretreatment[J].Food Chemistry,2017,232:727-732
[4]Leila M,Saeedeh SA,Seyede M H.Recent approaches in physical modification of protein functionality[J].Food Chemistry,2016,199:619-627
[5]石燕,葛辉,涂宗财,等.超声波对酪蛋白结构与功能性质的影响[J].食品与发酵工业,2014,40(2):16-21
[6]Zhang Q T,Tu ZC,Xiao H,et al.In?uence of ultrasonic treatment on the structure and emulsifying propertiesof peanutprotein isolate[J].Food and BioproductsProcessing,2014,92:30-37
[7]LaemmliU K.Cleavageofstructuralproteinsduring theassembly of thehead ofbacteriophage T4[J].Nature,1970,227(5259):680-685[8]孙英杰.超声波处理对大豆分离蛋白结构和功能性质影响研究[D].哈尔滨:东北农业大学,2014
[9]Soria A C,Villamiel M.Effect of ultrasound on the technological properties and bioactivity of food:a review[J].Trends Food Science And Technology,2010,21:323-331
[10]王长远,郝天舒,张敏.干热处理对米糠蛋白结构与功能特性的影响[J].食品科学,2015,36(7):13-18
[11]黄六容,张勋发,李宇翔,等.超声复合酸处理促进花生分离蛋白的亚基解离[J].农业工程学报,2016,32(18):285-290
[12]Marion M,Fanny G,Stephane P.On how κ-casein affects the interactionsbetween theheat-induced whey protein/κ-casein complexes and the caseinmicellesduring theacid gelation ofskimmilk[J].InternationalDairy Journal,2011,21:670-678
[13]石燕,刘凡,葛辉,等.微胶囊形成过程中蛋白质二级结构变化的红外光谱分析[J].光谱学与光谱分析,2012,32(7):1815-1819[14]叶林,廖钰,赵谋明.花生分离蛋白氧化过程中的结构变化[J].食品与机械,2015,31(2):3-6
[15]Zhang X,Huang LX,Nie SQ.FTIR characteristic of the secondary structureofinsulinencap sulatedwithin liposome[J].Journal ofChinese Pharmaceutical Science,2003,12(1):11-14
[16]冯景丽,贾峰,王金水,等.超声波处理对酪蛋白结构特性的影响[J].中国乳品工业,2015,43(6):20-23
[17]杨勇,毕爽,王中江,等.超声波处理对绿豆蛋白结构及功能特性的影响[J].食品工业科技,2016,37(9):69-73
[18]王晓琳,朱力杰,陈妍婕,等.不同干热处理对花生蛋白二级结构及乳化性的影响[J].食品与发酵工业,2016,42(5):86-90
