沉默Ephrin B2基因表达对结直肠癌细胞侵袭和迁移的影响及其机制
2018-05-15张旭陈旺盛文坤明张梦娇梁雪梅
张旭,陈旺盛,文坤明,张梦娇,梁雪梅
(1 西南医科大学附属医院,四川泸州646000;2 遵义医学院附属医院)
促红细胞生成素产生的肝细胞受体(EPH)家族是受体酪氨酸激酶家族中最大的亚族,在肿瘤发生、发展过程中具有重要作用[1]。EPH家族包括受体Eph和配体肝配蛋白(Ephrin)。肝配蛋白B2(Ephrin B2)是配体Ephrin的亚型之一,作为一种跨膜蛋白通过其胞外部分与相应受体Eph B4结合,激活Eph B4介导的正向信号通路,同时受体Eph B4也会使Ephrin B2胞内部分发生磷酸化,从而激活Ephrin B2介导的逆向信号通路,形成特有的双向信号调节通路,在肿瘤侵袭和转移过程中发挥双重调节作用[2,3]。目前关于Ephrin B2介导的逆向信号通路在肿瘤中的作用仍存在争议,多数研究倾向于经Ephrin B2介导的逆向信号通路与肿瘤侵袭和转移有关[4~6],但其作用机制尚不清楚。近年研究证实,上皮间质转化(EMT)在肿瘤侵袭和转移过程中具有重要作用[7]。而Ephrin B2是否通过调控EMT过程参与肿瘤侵袭和转移尚不十分清楚。2016年8月~2017年7月,本研究观察了沉默Ephrin B2基因表达对结直肠癌细胞侵袭和迁移的影响,并探讨其可能机制。
1 材料与方法
1.1 材料 人结直肠癌SW480细胞(以下称SW480细胞),购自中国科学院上海细胞库。Ephrin B2干扰质粒载体(Ephrin B2-siRNA)及对照质粒载体(NC-siRNA),由天津赛尔生物技术有限公司构建、筛选、包装。所有引物序列由深圳华大基因科技服务有限公司设计合成。Transwell小室,美国Millipore公司;PCR逆转录试剂盒、TRIzol、SYBR®Premix Ex TaqTM,日本TaKaRa公司。兔抗人Ephrin B2、E-cadherin、N-cadherin、Vimentin一抗,美国Epitomics公司;兔抗人GAPDH一抗及HRP标记的山羊抗兔二抗,北京中杉金桥生物技术有限公司;BCA蛋白定量试剂盒、ECL发光试剂盒、SDS-PAGE凝胶配制试剂盒、Loading buffer、蛋白质Marker、Lipofectamine2000、结晶紫染液,上海碧云天生物技术有限公司。
1.2 沉默Ephrin B2基因表达及其效果验证 将SW480细胞置于含10% FBS的RPMI 1640培养基中,37 ℃、5% CO2恒温培养箱中常规培养。选择对数生长期、生长状态良好的细胞用于后续实验。收集SW480细胞,0.25%胰酶消化,制成细胞悬液,以2×105个/孔接种于6孔板(内含10% FBS的RPMI 1640培养基),置于37 ℃、5% CO2恒温培养箱中培养。随机将细胞分为Ephrin B2组、阴性对照组、空白对照组,当细胞融合至70%~80%时,更换为无血清的RPMI 1640培养基,Ephrin B2组加入Ephrin B2-siRNA 1 μg+Lipofectamine2000 3 μL,阴性对照组加入NC-siRNA 1 μg+Lipofectamine2000 3 μL,空白对照组仅加入Lipofectamine2000 3 μL。各组转染8 h,更换新的含10% FBS RPMI 1640培养基,继续培养48 h,收集细胞。采用TRIzol法提取细胞总RNA,经蛋白核酸分析仪检测,OD260/OD280为1.8~2.0。根据逆转录试剂盒说明将总RNA逆转录为cDNA。以cDNA为模板,按SYBR®Premix Ex TaqTM说明进行PCR扩增。引物序列:Ephrin B2上游引物5′-CGATTGAGCCTTACGACAC-3′,下游引物5′-TTTTAAGCGCTGAGCATTG-3′;内参GAPDH上游引物5′-TGACTTCAACAGCGACACCCA-3′,下游引物5′-CACCCTGTTGCTGTAGCCAAA-3′。PCR反应体系共25 μL:ddH2O 8.5 μL,5 pmol/μL Primer1 1 μL,5 pmol/μL Primer2 1 μL,cDNA 2 μL,SYBR Green Mix Taq 12.5 μL;反应条件:94 ℃ 30 s,94 ℃ 5 s、56 ℃ 30 s共40个循环,65 ℃ 5 s,72 ℃ 5 min。以GAPDH为内参,采用2-ΔΔCt法计算目的基因相对表达量。实验重复3次,取平均值。结果显示,Ephrin B2组、阴性对照组、空白对照组Ephrin B2 mRNA相对表达量分别为0.283±0.060、0.813±0.050、1.000±0.000。Ephrin B2组Ephrin B2 mRNA相对表达量明显低于阴性对照组和空白对照组(P均<0.05),而阴性对照组与空白对照组比较P>0.05。证实Ephrin B2-siRNA能够沉默Ephrin B2基因表达。
1.3 沉默Ephrin B2基因表达对SW480细胞侵袭能力影响的观察 采用Transwell侵袭实验。将Martrigel胶置于4 ℃冰箱中过夜解冻,以无血清的RPMI 1640培养基∶Martrigel胶=1∶8比例稀释。取100 μL稀释后的Martrigel胶置于Transwell小室底部,将小室置于37 ℃下风干。取对数生长期、生长状态良好的SW480细胞,按1.2方法进行分组、转染,转染8 h,更换新的含10% FBS RPMI 1640培养基,继续培养48 h,收集细胞,0.25%胰酶消化,制成密度为6×105个/mL的细胞悬液。取细胞悬液0.4 mL加入Transwell小室上室,下室加入含10% FBS RPMI 1640培养基0.6 mL,将Transwell小室置于37 ℃、5% CO2恒温培养箱中培养。培养24 h,取出小室,吸尽上室培养基,PBS清洗,多聚甲醛固定20 min,自然风干后用0.1%结晶紫染色15 min,用棉签擦去上室未穿透细胞及Martrigel胶。PBS冲洗干净,自然风干,甘油封片,显微镜下计数穿膜细胞数,以此反映细胞侵袭能力。实验重复3次,取平均值。
1.4 沉默Ephrin B2基因表达对SW480细胞迁移能力影响的观察 采用划痕修复实验。选择1.3中的细胞悬液1 mL接种于6孔板(内含10% FBS的RPMI 1640培养液),置于37 ℃、5% CO2恒温培养箱中培养。待细胞贴壁后,用10 μL枪头划过细胞,用PBS洗尽漂浮的细胞;加入含1.5% FBS的RPMI 1640培养基,置于37 ℃、5% CO2恒温培养箱中培养。显微镜下拍照观察培养0、24 h细胞迁移情况,Image-Pro Plus软件测量划痕24 h细胞迁移距离。实验重复3次,取平均值。
1.5 沉默Ephrin B2基因表达对SW480细胞E-cadherin、N-cadherin、Vimentin表达影响的观察 ①E-cadherin、N-cadherin、Vimentin蛋白表达:采用Western blotting法。按1.2中方法进行分组、转染。转染8 h,更换新的含10% FBS的RPMI 1640培养基,继续培养48 h,收集细胞。按全蛋白提取试剂盒说明提取细胞总蛋白,BCA法蛋白定量后,加入上样缓冲液,100 ℃水浴10 min,使蛋白充分变性。取变性蛋白50 μg恒压下行SDS-PAGE,按湿转法将蛋白电泳产物转印至PVDF膜。取出PVDF膜,5%脱脂奶粉封闭1 h,分别加入E-cadherin(1∶2 000)、N-cadherin(1∶2 000)、Vimentin(1∶5 000)、GAPDH(1∶5 000)一抗,4 ℃孵育过夜;TBST洗膜10 min×3次,加入HRP标记的山羊抗兔二抗(1∶5 000),室温避光孵育1 h。ECL发光显影,Bio-Rad凝胶成像系统扫描蛋白电泳条带,Quantity One软件分析各蛋白电泳条带的灰度值。以目的蛋白电泳条带灰度值/内参蛋白电泳条带灰度值作为目的蛋白相对表达量。实验重复3次,取平均值。②E-cadherin、N-cadherin、Vimentin mRNA表达:采用qRT-PCR法。具体步骤参照1.2。引物序列:E-cadherin上游引物5′-CTTCTCTCACGCTGTGTCATC-3′,下游引物5′-CTCCTGTGTTCCTGTTAATGGT-3′;N-cadherin上游引物5′-ACTCGGCTTAATGGTGAT-3′,下游引物5′-CACTGGCAAACCTTCACG-3′;Vimentin上游引物5′-AGGCAAAGCAGGAGTCCA-3′,下游引物5′-TATCAACCAGAGGGAGTG-3′。以GAPDH为内参,采用2-ΔΔCt法计算目的基因相对表达量。实验重复3次,取平均值。
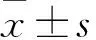
2 结果
2.1 各组细胞侵袭和迁移能力比较 见表1。
2.2 各组N-cadherin、Vimentin、E-cadherin蛋白和mRNA表达比较 见表2、3。
3 讨论
结直肠癌是严重危及人民生命健康的恶性肿瘤,近年来虽然在全球范围内结直肠癌的发病率及病死率有所下降,但由于我国人口基数大,每年的发病例数及死亡例数均居世界第1位,并呈年轻化趋势[8]。虽然手术方式不断改进、抗肿瘤新药不断涌现,但结直肠癌患者的总生存期仍不理想,尤其是中晚期结直肠癌患者。侵袭和转移是导致结直肠癌患者预后不良的最重要原因,也是治疗失败导致患者死亡的重要原因。因此,探索结直肠癌侵袭和转移的机制具有重要意义。
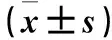
表1 各组细胞侵袭和迁移能力比较
注:与空白对照组比较,*P<0.05;与阴性对照组比较,#P<0.05。
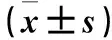
表2 各组N-cadherin、Vimentin、E-cadherin蛋白相对表达量比较
注:与空白对照组比较,*P<0.05;与阴性对照组比较,#P<0.05。
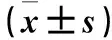
表3 各组N-cadherin、Vimentin、E-cadherin mRNA相对表达量比较
注:与空白对照组比较,*P<0.05;与阴性对照组比较,#P<0.05。
近年来,EPH家族在肿瘤中的作用逐渐被重视。EPH家族包括Eph受体(Eph A1~Eph A10,Eph B1~Eph B6)和配体Ephrin(Ephrin A1~Ephrin A6,Ephrin B1~Ephrin B6)两部分,其家族成员在肿瘤的发生、发展过程中具有重要作用[9]。Ephrin B2是一种跨膜的内嵌蛋白,由通过GPI与受体连接的胞外区、含PDZ结构域和酪氨酸激酶结合位点的胞内区组成。Ephrin B2主要与受体Eph B4、Eph B3、Eph B2结合。但Ephrin B2与Eph B4的亲和力更高,可形成特有的双向信号传导通路,即由配体Ephrin B2为媒介作用于受体Eph B4使其发生磷酸化,从而激活下游信号传导分子形成正向信号传导通路,同时受体Eph B4介导激活配体Ephrin B2胞外区,使其发生磷酸化,继而激活其下游信号传导分子所形成的反向信号传导通路。Ephrin B2与Eph B4形成的双向信号通路在血管生成、神经发育、骨骼再生、细胞迁移等多种病理生理过程中发挥重要作用[10,11]。但目前关于Ephrin B2在肿瘤中的作用仍有争议。有研究发现,Ephrin B2在食管癌、乳腺癌、卵巢癌等多种恶性肿瘤组织中高表达,并与肿瘤的侵袭和转移有关[12,13]。而Depner等[14]研究发现,下调Ephrin B2表达可抑制某些肿瘤的侵袭和转移。由此可见,Ephrin B2在肿瘤中的作用即可发挥癌基因作用,又能发挥抑癌基因作用。但其在结直肠癌细胞中的作用及其机制尚不十分清楚,仍需进一步研究。
普遍认为,EMT在肿瘤侵袭和转移过程中发挥了至关重要的作用[15]。EMT可使具有极性的、相对稳定的上皮细胞通过一系列生化过程转变成能在细胞基质间自由移动的间质细胞。EMT是一个非常复杂的分子过程,涉及多个信号通路,如TGF-β1通路、Hedgehog通路、Notch通路、Wnt通路等。各信号通路间彼此相互作用,激活一些转录因子,如锌指转录因子Snail、碱性螺旋-环-螺旋转录因子Twist、锌指E盒结合蛋白ZEB,共同参与导致上皮细胞标志分子E-cadherin下调及间质细胞标志分子N-cadherin、Vimentin表达上调。EMT可使肿瘤细胞丧失细胞极性和细胞彼此间的连接,使其侵袭和转移能力增强[16]。但EMT并不是一成不变的,肿瘤细胞通过EMT获得更强的侵袭和转移能力,在到达一个新的生长环境后,又可通过一些转录因子的调节发生间质上皮转化(MET),从而获得具有上皮细胞表型和特性的细胞固定下来,继而增殖形成新的病灶。众多转录因子在肿瘤细胞发生EMT和MET过程中发挥了重要作用,有可能成为预测肿瘤侵袭和转移的分子标志物。Ephrin B2是否通过调控肿瘤细胞的EMT过程发挥作用尚不清楚。
本研究通过RNA干扰技术沉默SW480细胞Ephrin B2基因表达,观察沉默Ephrin B2基因表达对SW480细胞侵袭和迁移的影响。结果发现,Ephrin B2组细胞侵袭和转移能力均明显低于阴性对照组和空白对照组,而阴性对照组与空白对照组比较差异无统计学意义。说明沉默Ephrin B2基因表达能抑制SW480细胞侵袭和迁移。本研究结果还发现,Ephrin B2组E-cadherin蛋白和mRNA表达均明显低于阴性对照组、空白对照组,N-cadherin、Vimentin蛋白和mRNA表达均明显高于阴性对照组、空白对照组,而阴性对照组与空白对照组比较差异均无统计学意义。表明沉默Ephrin B2基因表达抑制SW480细胞侵袭和迁移的机制可能与调控EMT过程有关。
综上所述,沉默Ephrin B2基因表达可抑制结直肠癌细胞侵袭和迁移,其机制可能与调控EMT过程有关。但其具体调控机制尚需进一步研究。
参考文献:
[1] Li RX, Chen ZH, Chen ZK. The role of EPH receptors in cancer-related epithelial-mesenchymal transition[J]. Clin J Cancer, 2014,33(5):231-240.
[2] Djokovic D, Trindade A, Gigante J, et al. Combination of Dll4/Notch and EphrinB2/EphB4 targeted therapy is highly effective in disrupting tumor angiogenesis[J]. BMC Cancer, 2010(10):641-652.
[3] Arvanitis D, Davy A. Eph/ephrin signaling: networks[J]. Genes Dev, 2008,22(4):416-429.
[4] 张旭,陈秀,陈旺盛.结直肠癌组织Ephrin B2表达变化及其对上皮间质转化的影响[J].山东医药,2017,57(36):65-68.
[5] Li X, Song C, Huang G, et al. The coexpression of EphB4 and EphrinB2 is associated with poor prognosis in HER2-positive breast cancer[J]. Onco Targets Ther, 2017(10):1735-1742.
[6] Alam SM, Fujimoto J, Jahan I, et al. Overexpression of ephrinB2 and EphB4 in tumor advancement of uterine endometrial cancers[J]. Ann Oncol, 2007,18(3):485-490.
[7] Chen S, Zhu J, Zuo S, et al. 1,25(OH)2D3attenuates TGF-β1/β2-induced increased migration and invasion via inhibiting epithelial-mesenchymaltransition in colon cancer cells[J]. Biochem Biophys Res Commun, 2015,468(1-2):130-135.
[8] Chen W, Zheng R, Baade PD, et al. Cancer statistics in China, 2015[J]. CA Cancer J Clin, 2016,66(2):115-132.
[9] Kandouz M. The Eph/Ephrin family in cancer metastasis: commu-nication at the service of invasion[J]. Cancer Metastasis Rev, 2012,31(1-2):353-373.
[10] Sturz A, Bader B, Thierauch KH, et al. EphB4 signaling is capable of mediating Ephrin B2-induced inhibition of cell migration[J]. Biochem Biophys Res Commun, 2004,313(1):80-88.
[11] Davies MH, Zamora DO, Smith JR, et al. Soluble Ephrin B2 mediates apoptosis in retinal neovascularization and in endothelial cells[J]. Microvasc Res, 2009,77(3):382-386.
[12] Adams RH, Wilkinson GA, Weiss C, et al. Roles of ephrinB ligands and EphB receptors in cardiovascular development: demarcation of arterial/venous domains, vascular morphogenesis, and sprouting angiogenesis[J]. Gene Dev, 1999,13(3):295-306.
[13] Zhang R, Zhao Y, Zhang S, et al. The expressions of EphrinB2 and VEGF in nasopharyngeal carcinoma and their clinical significance[J].Lin Chung Er Bi Yan Hou Tou Jing Wai Ke Za Zhi, 2013,27(4):178-180.
[14] Depner C, Zum Buttel H, Bogurcu N, et al. EphrinB2 repression through ZEB2 mediates tumour invasion and anti-angiogenic resistance[J]. Nat Commun, 2016(7):1-15.
[15] Yeung KT, Yang J. Epithelial-mesenchymal transition in tumor metastasis[J]. Mol Oncol, 2017,11(1):28-39.
[16] Smith BN, Bhowmick NA. Role of EMT in metastasis and therapy resistance[J]. J Clin Med, 2016,5(2):1-17.
