多种统计方法比较黄连姜制工序中影响生物碱含量的因素*
2018-05-10袁金凤彭诗涛张语凡张先灵
王 鑫,袁金凤,彭诗涛,张语凡,王 蕾,张先灵,李 飞
(北京中医药大学中药学院 北京 102488)
黄连为毛茛科植物黄连(Coptis chinensis Franch.)、三角叶黄连(Coptis deltoidea C.Y.Cheng et Hsiao.)、云连(Coptis teeta Wall.)的干燥根茎。黄连生品味苦、性寒;具有清热燥湿、泻火解毒的作用[1]。姜黄连为黄连的炮制品之一,姜炙后可缓和生品的苦寒之性,善治胃热呕吐。历版药典和各地炮制规范[2-15]中姜黄连的炮制工艺不尽相同。其中辅料姜汁的制备工艺有榨生姜汁、煮干姜汁、煮生姜汁;辅料姜汁与黄连饮片有拌匀吸尽和润至透心的不同。生姜味辛性温,具有温中止呕,解表散寒之功;干姜性热,长于温中散寒,回阳通脉,有学者认为四川干姜为真正的“药姜”,不同姜汁对黄连生物碱的影响未见报道。故本研究选择生姜、四川干姜、同批次生姜切片晒干制得的干姜制备姜汁。由于传统炙法全凭操作者的主观判断,不易量化,部分学者采用烘法替代炙法,两种加热方式对姜黄连的质量影响是否一致尚不明确,故采用文献[16]报道的姜黄连最优烘制工艺,对传统炙法和烘法进行比较。本实验通过查阅历版药典和各地炮制规范,发现姜炙法中姜汁的制备、闷润节点等工序中各地各法,无规范化的炮制工艺,不能明确各工序中影响饮片质量的因素。这些问题的存在,使得姜黄连饮片的质量很难达到稳定、可控,不能保证临床用药的安全、有效。故本研究采用同批次黄连片制备姜黄连,在2015版《中国药典》规定的4种生物碱含量标准的基础上,以6种生物碱含量作为评价指标,比较不同方法制备的姜汁、闷润程度、姜的来源、加热方式对黄连生物碱含量的影响,并采用多种统计方法进行分析,寻找姜制工序中影响姜黄连质量的因素,旨在为姜黄连炮制工艺及质量标准的完善提供依据。
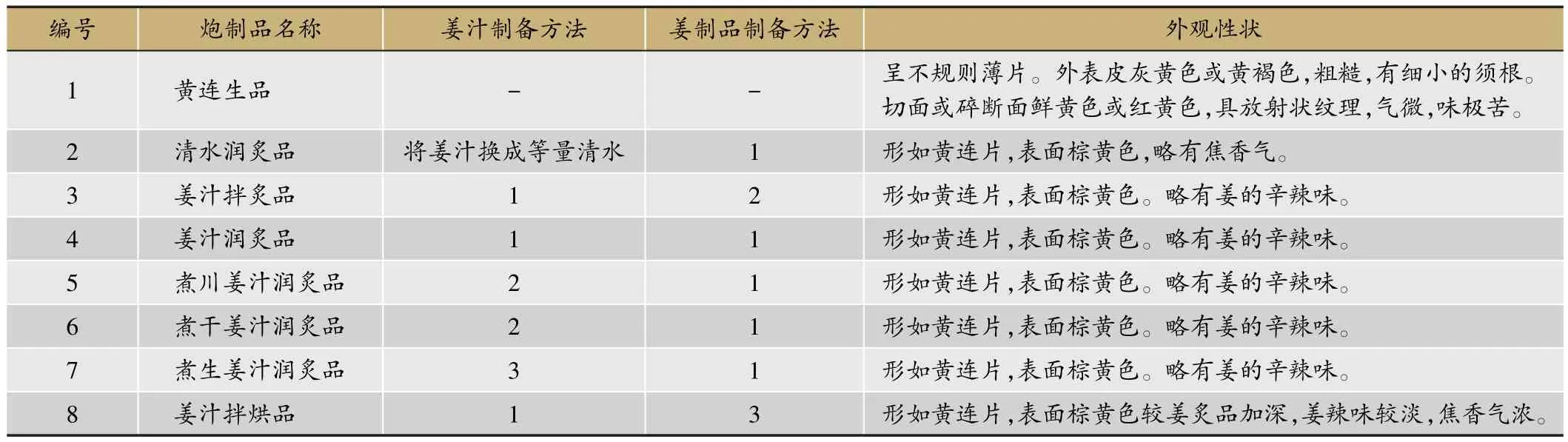
表1 黄连炮制品的制备及外观性状
1 仪器与试药
1.1 仪器
Waters 2695高效液相色谱仪(2489紫外检测器,Empower色谱工作站);SB25-12DTDN型超声波清洗器(宁波新芝生物科技股份有限公司);SHB-3型循环多用真空泵(郑州长城科工贸有限公司);BT-25S型电子分析天平(北京赛多利斯仪器有限公司);AR882+型在线式红外测温仪(深圳市富兰克仪器仪表有限公司)。
1.2 试药
盐酸药根碱(上海诗丹德标准技术服务有限公司,批号:ST03080120MG,纯度≥98%);非洲防己碱(上海源叶生物科技有限公司,批号:W30M7Z15501,纯度≥98%);表小檗碱(批号:PRF8041721,纯度≥98%)、盐酸黄连碱(批号:PRF7091402,纯度≥98%)、盐酸巴马汀(批号:PRF8030248,纯度≥98%)、盐酸小檗碱(批号:PRF8040742,纯度≥98%)均购自成都普瑞法科技开发有限公司。乙腈(美国Fisher公司,色谱纯),其余试剂均为分析纯。
黄连购于北京市双桥燕京中药饮片厂,产地为湖北,批号:1604084。经北京中医药大学中药学院杨瑶珺教授鉴定为毛茛科植物黄连(Coptis chinensis Franch)根茎切成的饮片;干姜购于北京市双桥燕京中药饮片厂,产地为四川,批号:1603060;生姜购于本地农贸市场。
2 方法与结果
2.1 炮制品的制备
黄连:取黄连饮片,净制备用,得生品1。
姜汁的制备:分别取生姜、同批次生姜切片晒干制得的干姜(以下简称“干姜”)、四川干姜制备姜汁。三种辅料姜汁的制备方法如下:①榨生姜汁:按2015版《中国药典》炮制通则制备[1];②煮干姜汁:按1988年版《全国中药炮制规范》炮制通则制备[3];③煮生姜汁:按1990年版《山东省中药饮片炮制规范》炮制通则[7]制备。即得不同方法制备的辅料姜汁,备用。
姜制品的制备方法:①姜汁润炙品的制备[3]:取黄连片,加入姜汁拌匀,闷润至透,文火加热(温度为95-105℃),炒干;②姜汁拌炙品的制备[1]:取黄连片,加姜汁拌匀至吸尽,置热锅内,文火(温度为95-105℃)炒干;③姜汁拌烘品的制备[16]:取黄连片与生姜汁拌匀,闷润60 min后于100℃下烘制3 h。对各个样品进行炮制后,观察其性状(表1)。
上述炮制品所用的黄连生品均来自同一批次,并在相同温度下炒干。在姜制品的炮制方法上,主要以1988年版《全国中药炮制规范》的润炙方法为主。同时,以姜汁拌炙品为对照比较加辅料润透及吸尽有无区别;以川姜汁润炙品比较不同来源的姜所制姜汁有无区别;以清水润炙品为对照比较加与不加姜汁的黄连润炙品有无区别;以姜汁拌烘品为对照比较加热方式对黄连姜炙品的影响。分别将上述炮制品粉碎,过2号筛,备用。
2.2 生物碱含量测定[17]
2.2.1 色谱条件
XtimateTMC18色谱柱(4.6 mm×250 mm,5 μm);流动相A为30 mmol·L-1碳酸氢铵水溶液(每1 L碳酸氢铵溶液7 mL氨水及1 mL三乙胺),B相为纯乙腈,线性梯度洗脱程序为0-15 min,10-25%B;15-25 min,25-30%B;25-40 min,30-45%B;流速为1 mL·min-1;检测波长为270 nm;柱温为30℃;进样量为10 μL。在上述色谱条件下,理论塔板数按盐酸药根碱、盐酸非洲防己碱、盐酸表小檗碱、盐酸黄连碱、盐酸巴马汀、盐酸小檗碱峰计算均不低于10 000。分离度符合含量测定要求。空白对照品、混合对照品及样品色谱图见图1。
2.2.2 对照品溶液的制备
分别精密称取盐酸药根碱、盐酸非洲防己碱、盐酸表小檗碱、盐酸黄连碱、盐酸巴马汀、盐酸小檗碱10.44、10.35、9.45、9.39、7.99、9.04 mg,分别置于 10、10、50、25、25、25 mL量瓶中,用甲醇-盐酸溶液(100∶1)溶解并稀释至刻度,即得各对照品储备液。
分别吸取上述对照品储备液盐酸药根碱0.5 mL、盐酸非洲防己碱0.5 mL、盐酸表小檗碱5.5 mL、盐酸黄连碱5.0 mL、盐酸巴马汀4.5 mL、盐酸小檗碱18.5 mL于50 mL量瓶中,用甲醇-盐酸溶液(100∶1)定容至刻度(与储备液一致),即得混合对照品储备液。
2.2.3 供试品溶液的制备
将制备好的样品粉末混合均匀,取供试品粉末约0.1 g,精密称定,置100 mL锥形瓶中,精密加入甲醇-盐酸溶液(100∶1)50 mL,密塞,称定重量,超声处理(功率:250 W,频率:40 kHz)30 min,放冷,再称定重量,用甲醇-盐酸溶液(100∶1)补足减失的重量,摇匀,经0.45 μm微孔滤膜滤过,取续滤液,即得供试品溶液。
2.2.4 线性关系考察
分别精密量取混合贮备液0.5、1.0、2.5、5、10 mL置10 mL容量瓶中,加甲醇-盐酸溶液(100∶1)稀释至刻度,即得不同浓度的系列混合对照品溶液,分别精密吸取混合对照品储备液及上述混合对照品溶液各10 μL,按上述色谱条件进行测定,以峰面积积分值(Y)对各生物碱浓度(mg·L-1)(X)进行线性回归绘制标准曲线。盐酸药根碱:Y=3.06×107X-7 858.90,r=0.999 9;盐酸非洲防己碱:Y=4.11×107X-898.49,r=0.999 8;盐酸表小檗碱:Y=5.17×107X-24 177,r=1.000 0;盐酸黄连碱:Y=3.89×107X-41 610,rr=0.999 9;盐酸巴马汀:Y=4.29×107X-20 112,r=1.000 0;盐酸小檗碱:Y=4.14×107X-84183,r=1.000 0。结果表明,上述生物碱分别在0.004 4-0.087 3、0.010 2-0.204 1、0.018 0-0.360 6、0.014 4-0.287 6、0.066 2-1.323 5 μg进样量与峰面积呈良好的线性关系。
2.2.5 精密度试验
精密吸取同一混合对照品溶液,在上述色谱条件下重复进样6次,记录6种生物碱峰面积。计算得盐酸药根碱、盐酸非洲防己碱、盐酸表小檗碱、盐酸黄连碱、盐酸巴马汀、盐酸小檗碱峰面积的RSD分别为2.2%,2.8%,1.8%,2.4%,2.4%,1.9%。表明仪器精密度良好。
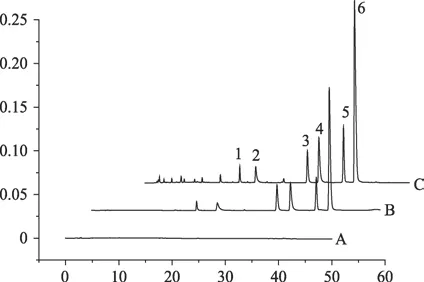
图1 空白对照品(A)、混合对照品(B)、姜黄连样品(C)的液相色谱图
2.2.6 稳定性试验
取同一供试品溶液,室温放置,分别在0、2、4、8、12、24 h各进样一次,记录6种生物碱峰面积。计算得盐酸药根碱、盐酸非洲防己碱、盐酸表小檗碱、盐酸黄连碱、盐酸巴马汀、盐酸小檗碱峰面积RSD分别为2.4%、2.3%、2.8%、2.1%、1.6%、1.5%。表明供试品溶液在24 h内稳定性良好。
2.2.7 重复性试验
取黄连生品粉末,精密称定6份,按照2.2.3项下方法平行制备6份供试品溶液,在上述色谱条件下进行测定。盐酸药根碱、盐酸非洲防己碱、盐酸表小檗碱、盐酸黄连碱、盐酸巴马汀、盐酸小檗碱峰面积RSD分别为2.2%、2.8%、1.8%、2.4%、2.4%、1.9%,重复性良好。
2.2.8 加样回收率试验
取已知含量的黄连生品粉末6份,每份0.05 g,精密称定,分别精密加入一定量的生物碱混合对照品储备溶液,按2.2.3项下方法制成供试品溶液,按上述色谱条件定量测定。盐酸药根碱、盐酸非洲防己碱、盐酸表小檗碱、盐酸黄连碱、盐酸巴马汀、盐酸小檗碱的平均回收率分别为97.37%、98.81%、98.03%、102.10%、96.80%、101.42%,RSD分别为2.22%、1.43%、1.59%、1.31%、0.85%、1.63%。
2.2.9 样品测定
取黄连及各炮制品粉末,按2.2.3项下方法制备供试品溶液,按2.2.1项下色谱条件进行测定,外标法计算样品含量,样品测定结果见表2。
由表2可知,黄连经姜炙后,表小檗碱、黄连碱含量略有上升,药根碱、非洲防己碱、巴马汀、小檗碱含量略有下降。在6种生物碱含量上,传统姜炙品均高于烘制品。
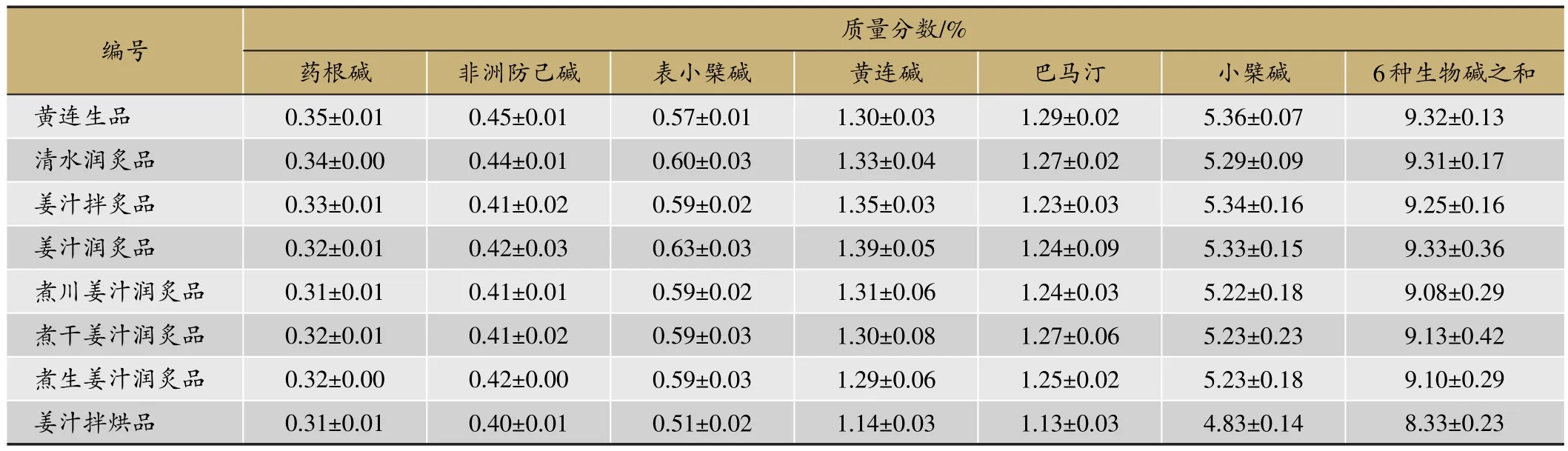
表2 黄连及各炮制品中6种生物碱的含量(n=3)
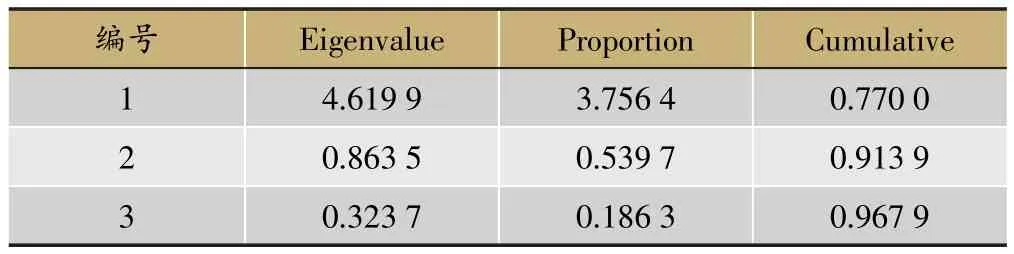
表3 黄连姜制品的特征根和方差贡献率
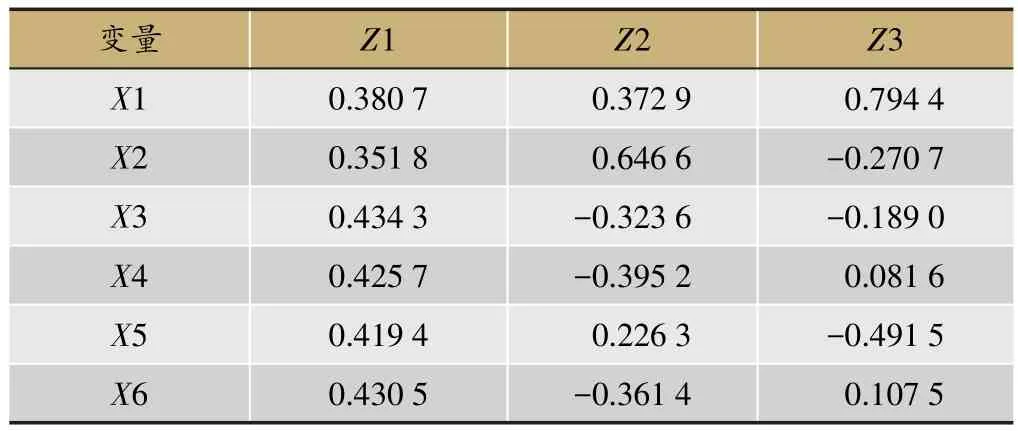
表4 黄连姜制品的主成分向量
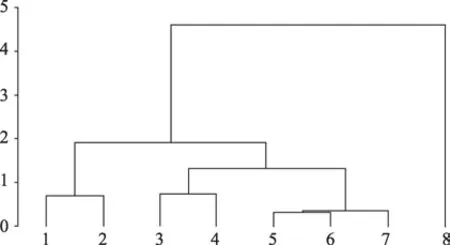
图2 黄连及各炮制品样品聚类图
2.3 数据处理
2.3.1 主成分分析
以6种生物碱为指标,将黄连姜制品数据输入SAS 9.3进行主成分分析,相关系数的特征值和方差贡献率见表3,各主成分对应的特征向量见表4。
由表3可以看出:第1、2、3的主成分的累计方差贡献率为96.79%>85%。故选择前3个主成分进行评价。它代表了姜黄连中6种生物碱信息量的96.79%。由表4可知,根据主成分所对应的特征向量,可得前3个主成分的表达式为:

由此可见,第一主成分Z1主要受表小檗碱(X3)的影响,第二主成分Z2主要受非洲防己碱(X3)的影响,第三主成分Z3主要受药根碱(X1)的影响。黄连经姜制后各生物碱含量略有变化,经主成分分析,不同姜制品之间生物碱含量的差异主要体现在各样品所含表小檗碱、非洲防己碱、药根碱含量的不同,故以6种生物碱含量评价姜黄连质量具有一定科学性。
2.3.2 聚类分析
以6种生物碱的均值为指标,采用SAS 9.3分层聚类分析软件对样品进行聚类分析,运用欧氏距离(Euclidean)作为样品的测度,结果见图2。
由图2可知,当欧氏距离λ=4时,烘法和传统炙法具有明显不同的聚类,说明烘品与炙品不同,这可能与加热方式有关;λ=2时,生品和清水炙品为一类,姜炙品为一类,说明辅料姜汁的加入对黄连产生影响,加辅料与不加辅料是有区别的。
2.3.3 LSD检验
以6种生物碱之和为指标,采用LSD检验对生品及姜制品进行两两比较,各组数据均符合正态且方差齐。在多个样本均数比较的方差分析中,F=6.28,P=0.000 7,P<0.05认为差异有统计学意义,总体均数不全相等。多个样本均数间的多重比较见表5。
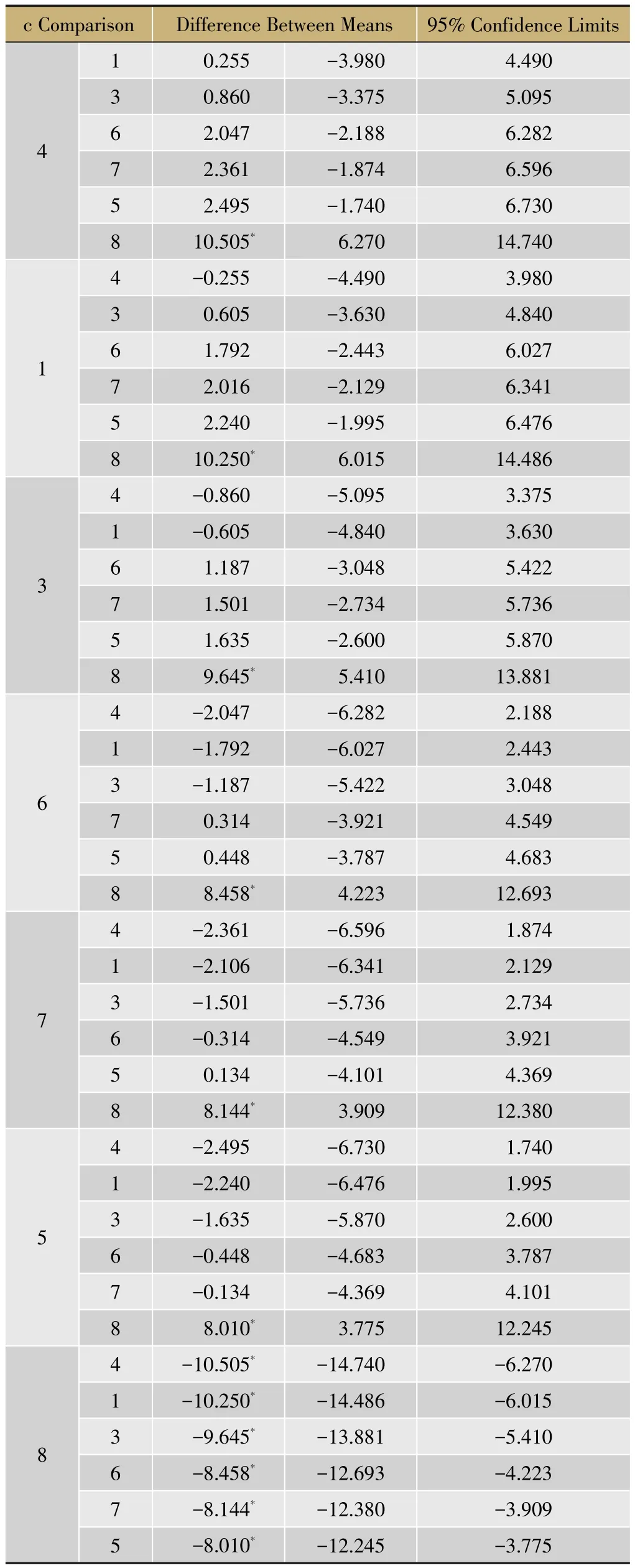
表5 黄连及姜制品中6种生物碱之和的多重比较
由表5可知,烘法与炙法具有显著性差异,而采用传统炙法炮制的姜炙品之间无显著性差异。加热方式可能是影响姜黄连生物碱含量的主要因素,而用不同方法制备的姜汁对姜黄连的6种生物碱之和影响不大,该结果与聚类分析的结果一致。
2.3.4 独立t检验
为了更好的比较榨汁组“姜汁拌炙品”与“姜汁润炙品”有无区别,选择独立t检验对各生物碱进行两两比较,结果见表6。
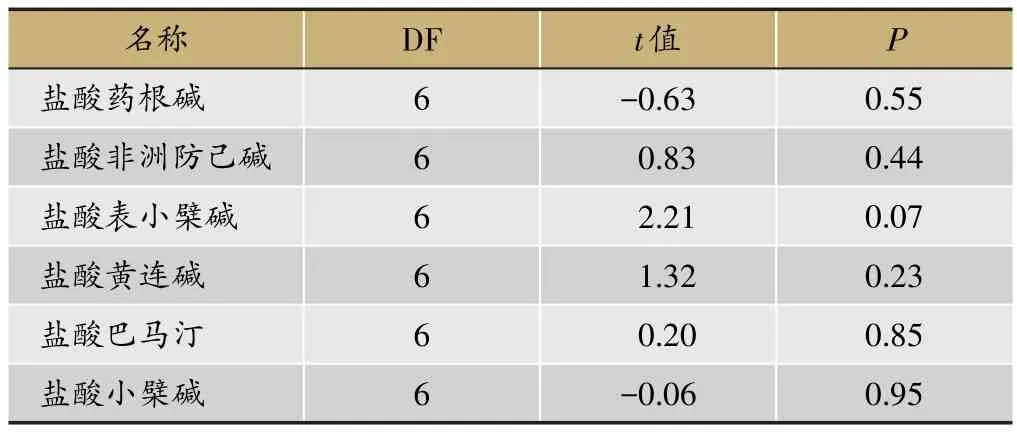
表6 两组姜黄连中各生物碱的独立t检验
由表6可见,各生物碱的P值均大于0.05,无显著性差异。在辅料姜汁与黄连饮片拌润的工序中,姜汁与黄连饮片“拌匀吸尽”或“润至透心”在6种生物碱含量上没有区别,该结果与聚类分析及LSD检验的结果一致。
3 总结与讨论
3.1 闷润工序中加水量的确定
黄连在姜炙时,饮片与姜汁闷润至透心,其液体辅料稀释时的加水量没有明确规定。为保证实验结果的准确性和可重复性。对闷润工序中的加水量进行考察,即:取适量黄连饮片,重量为M,加适量水V1浸泡,待饮片全部润透,内无干心时,过滤,未被吸收的水为V2。则饮片吸水率为:
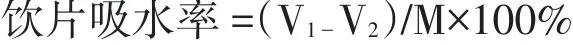
重复3次,黄连饮片的平均吸水率为50%,即1 kg黄连饮片吸收的液体量大约为500 mL。根据黄连饮片吸水率测定的结果,量化出其“闷润至透心”时的加水量,以保证水的加入对黄连影响的一致性。
3.2 辅料姜的来源对姜黄连生物碱的影响
有学者认为四川干姜为真正的“药姜”,本实验对四川干姜和生姜晒干姜进行比较,聚类分析与LSD检验均表明两种姜汁制备的姜黄连在6种生物碱含量上无显著性差异。
3.3 小结
本实验采用同一批次黄连炮制样品,姜炙法达到传统质量要求的炒干程度时,润炙法所需时间较拌炙法长,但外观性状一致,均符合“表面棕黄色,略有姜的辛辣味”。烘制法炮制的姜黄连颜色较炙法颜色加深,姜辣味淡,焦香气浓。本研究采用聚类分析、LSD检验、独立t检验对6种生物碱含量进行分析,结果表明烘制品与传统炙品具有明显差异,烘制品的6种生物碱总量较姜炙品下降10%左右;而传统炙法中姜的种类、不同方法制备的姜汁及闷润程度对姜黄连的6种生物碱含量影响不大。鉴于炒炙温度控制在95-105℃,烘制温度为100℃,两种加热方式温度基本一致,外观性状与成分的差异可能与烘制时间长达3 h有关。在没有更多科学依据之前,仍应采用传统的姜炙方法制备姜黄连。考虑到若加入姜汁润至透心,则因需加水量大稀释姜汁,炒干需要的工时长,故在加入辅料工序中,辅料姜汁与黄连饮片拌匀吸尽即可。
1 国家药典委员会.中华人民共和国药典(四部).北京:中国医药科技出版社,2015:31.
2 辽宁省卫生局.辽宁省中药炮制规范.沈阳:辽宁省卫生局,1975:48.
3 卫生部药政管理局.全国中药炮制规范.北京:人民卫生出版社,1988:96,113.
4 江西省卫生厅药政管理局.江西省中药炮制规范.上海:上海科学技术出版社,1991:106.
5 江苏省卫生局.江苏省中药饮片炮制规范.南京:江苏科学技术出版社,1980:105.
6 吉林省卫生厅.吉林省中药炮制标准.长春:吉林科学技术出版社,1987,32.
7 山东省卫生厅.山东省中药炮制规范.济南:山东科学技术出版社,1990:76.
8 安徽省食品药品监督管理局.安徽省中药饮片炮制规范.合肥:安徽科学技术出版社,2005:98.
9 浙江省食品药品监督管理局.浙江省中药炮制规范.杭州:浙江科学技术出版社,2005:124.
10 河南省食品药品监督管理局.河南省中药饮片炮制规范.郑州:河南人民出版社,2005:118.
11 贵州省食品药品监督管理局.贵州省中药饮片炮制规范.贵州:贵州科技出版社,2005:222.
12 广西壮族自治区食品药品监督管理局.广西壮族自治区中药饮片炮制规范.南宁:广西科学技术出版社,2007:314.
13 北京市药品监督管理局.北京市中药饮片炮制规范.北京:化学工业出版社,2008:226-227.
14 江西省食品药品监督管理局.江西省中药饮片炮制规范.上海:上海科学技术出版社,2008:135.
15 湖南省食品药品监督管理局.湖南省中药饮片炮制规范.长沙:湖南科学技术出版社,2007:57.
16 王德珍,易骏,张翼,等.酒黄连、姜黄连、萸黄连最佳炮制工艺研究.中药材,2013,36(1):35-37.
17 耿志鹏,郑海杰,张艺,等.RP-HPLC测定不同产地黄连中6种生物碱的含量.中国中药杂志,2010,35(19):2576-2580.
