股骨头坏死成骨特征与髓芯减压治疗效果的关系
2018-05-02王春生艾克热木江阿尔肯张子琦李有平同志琴杨佩王坤正
王春生,艾克热木江·阿尔肯,张子琦,李有平,同志琴,杨佩,王坤正
(西安交通大学第二附属医院骨一科,陕西 西安 710004)
髓芯减压是治疗股骨头坏死(osteonecrosis of femoral head,ONFH)的常用方法,但疗效存在争议[1-4],目前认为影响其疗效的主要因素是坏死区的范围、位置和是否塌陷,但即使对这些问题细致分析,仍不能很好预测髓芯减压的预后[5-9],我们认为可能存在其他影响髓芯减压预后的因素。髓芯减压治疗的目的是对坏死区修复并获得软骨下支撑[10-11],而股骨头坏死本身即存在不同的坏死区修复方式[12-13],我们认为坏死区的修复成骨能力可能会影响髓芯减压治疗的疗效,因而进行了本研究。
1 资料与方法
收集2005年2月至2015年2月在西安交通大学第二附属医院行髓芯减压的ONFH患者,纳入标准为符合ONFH的诊断标准[14],处于ONFH中骨循环协会(association research circulation osseous,ARCO)分期[15]Ⅱ期或Ⅲ期,同意其病例资料用于研究并获得随访,排除标准为处于ARCO分期的其他分期,患有系统性疾病需继续应用激素,或继续酗酒及不能获得随访者,以行髋关节置换手术或坏死分期进展作为终点,其他终点为研究结束、死亡、或行其他髋部手术。共46例(59髋)符合研究条件,其中男性39例(51髋),女性7例(8髋),年龄19~59岁(平均38岁),其中13例患者为双侧股骨头坏死,33例为单侧股骨头坏死,特发性股骨头坏死23例(29髋),激素性股骨头坏死12例(17髋),酒精性股骨头坏死9例(11髋),创伤性股骨头坏死2例(2髋)。
患者X线片的股骨头坏死ARCO分期由3位医生进行分析,然后讨论,根据多数意见获得结果。
参考Sternberg[16]和日本学者[13]对股骨头坏死的分析,我们将股骨头坏死区成骨情况分为3种,A型坏死区X线表现与正常骨相近;B型坏死区X线表现为斑点状或硬化,C型坏死区X线表现为囊性或低密度信号。3名医生分别对坏死情况进行分析,然后讨论,以多数意见为准。
患者在硬外麻醉下行标准8 mm孔道髓芯减压术,坏死区植入人工骨并用纳米骨柱保护股骨颈[17]。
术后前两年每3个月对患者进行一次随访;其后每一年进行一次随访直至患者进行全髋关节置换术或本研究结束。随访内容:询问患者一般情况、临床症状、髋关节正位片进行评价并记录。
采用SPSS 20.0软件进行数据统计分析。分别对各分组资料的年龄、体重指数进行t检验,对可能影响分型的因素,如ARCO分期和范围分型、坏死区位置等进行卡方分析,根据终止标准分别对各组进行生存分析,并进行log-rank检验,P<0.05为差异具有统计学意义。
2 结 果
根据术前髋关节正位X线片进行坏死区分析,其中A型26髋,B型17髋,C型16髋。各分型间年龄、性别间差异无统计学意义。坏死区不同分型组中患者的分期分析表明患者术前髋关节X线的坏死区分型与ARCO分期之间尚不能认为具有相关性,即各分型组坏死ARCO分级间差异无统计学意义(见表1)。
平均随访时间39个月(3~86个月),以全髋关节置换术为终止标准。所有患者经过术后的定期随访,有9髋最终因需髋关节置换而终止随访,剩余50髋随访到研究结束,平均(73.013±4.071)个月。髋关节置换中A型4髋,B型1髋,C型4髋。这三组资料进行K-M生存分析,A型组髋的平均生存时间为(65.310±5.803)个月,B型组髋的平均生存时间为(85.500±0.354)个月,C型组髋的平均生存时间(44.429±7.880)个月。对三组生存曲线进行log-rank检验,P=0.049,差异具有统计学意义。
以ARCO分期进展来作为终止标准,A型组有10髋,B型组有7髋,C型组有11髋分期发生进展。这三组资料进行K-M生存分析,A型组髋的平均生存时间为(49.151±6.919)个月,B型组髋的平均生存时间为(52.607±8.333)个月,C型组髋的平均生存时间(25.294±6.306)个月。对三组生存曲线进行log-rank检验,P=0.033,差异具有统计学意义。
根据上述数据,可认为坏死区的分型与患者髓芯减压术后的预后之间存在一定的相关性。
典型病例:a)42岁男性患者,髋部疼痛3个月,入院后诊断为ONFH,ARCO分期为Ⅱ期,坏死区信号与正常骨相似,分型为A型,行髓芯减压治疗,治疗前后影像学资料见图1~3;b)23岁男性患者,双髋疼痛1年入院,诊断为ONFH,ARCO分期为Ⅲ期,坏死区存在硬化改变,分型为B型,入院后行双侧髓芯减压治疗,治疗前后影像学资料见图4~5;c)54岁男性患者,右髋疼痛5个月入院,诊断为ONFH,ARCO分期为Ⅱ期,存在囊性改变,分型为C型,入院后行髓芯减压治疗,治疗前后影像学资料见图6~7。

图1 术前X线片示股骨头内信号稍异常,评价为ARCO Ⅱ期,分型为A 图2 入院时MRI的T1、T2加权像见双线征,坏死区内MRI表现与正常骨相似 图3 术后1年X线片示股骨头病变无明显恶化和好转
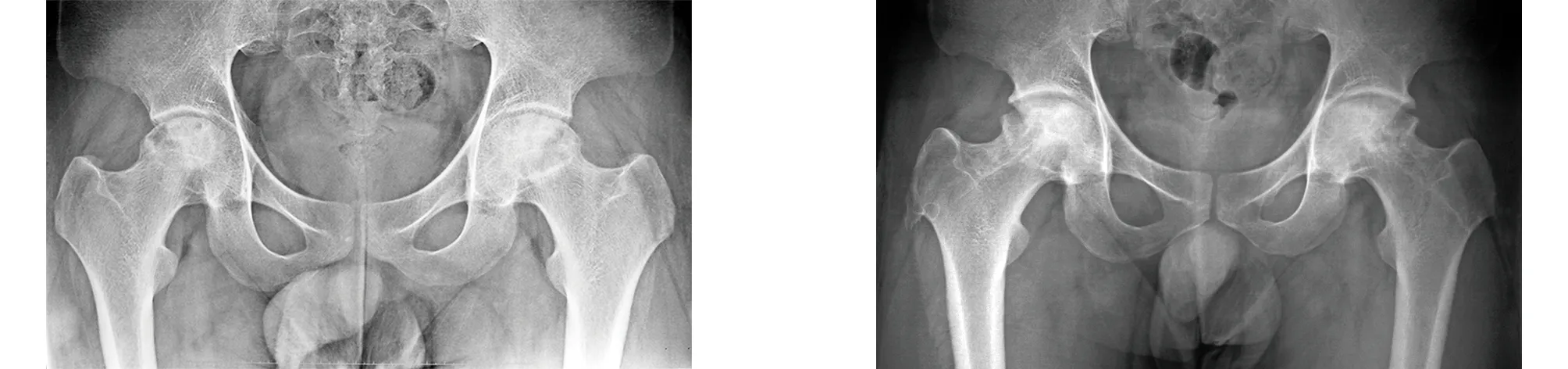
图4 术前X线片示股骨头有塌陷,评价为ARCO分期 Ⅲ期,分型为B 图5 术后4年X线片示股骨头轮廓无恶化,头内有成骨表现
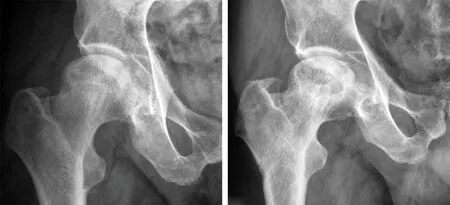
图6 术前X线片示股骨头内存在囊性改变,ARCO分期Ⅱ期,分型C 图7 术后3个月后疼痛,复查X线片示股骨头塌陷
3 讨 论
股骨头坏死疾病坏死事件发生后,组织修复过程是造成股骨头坏死疾病发病和进展的基础[5,12]。由于全身和局部因素的差异,患者间存在不同的修复方式,产生不同的预后,并会对治疗产生相应的影响[12-13]。
提高股骨头内坏死区的支撑能力是股骨头坏死治疗的目标之一。研究者试用了很多方法去提高股骨头内的支撑能力[10,18],但少有研究去研究不同患者是否会有不同的支撑能力,以及这种支撑力的差异是否会影响疾病的预后。
Steinberg曾发现股骨头坏死内存在囊性和硬化性两种X线表现方式[16],日本学者曾发现股骨头坏死区存在囊性、斑点状和硬化三种X线表现[13],但他们都未对这些不同表现方式对预后和治疗的影响进行相关研究。本研究根据他们的结果和我们的临床观察将股骨头无变化的改变加入分组,并将斑点状和硬化这两种有成骨表现的分为一组,更能全面反映股骨头改变。我们认为这些差异表现可能是修复过程差异造成的,并可能会产生不同的股骨头内支撑力和修复结果,因而会影响预后和治疗反应。本研究的结果验证了我们的猜想,不同的X线表现方式在经过髓芯减压治疗后,在疾病进展和全髋关节置换的2个终点上都存在显著性的差异,说明这些X线上的成骨差异确会影响股骨头坏死的保头治疗效果。
影响骨组织修复的因素有很多,但表现在局部的具体情况则是四种因素:细胞、因子、支架和力学环境[19]。全身因素更多影响的是细胞募集、炎性反应和因子释放,局部因素则会影响全部这四种因素,局部的血供状况影响细胞募集和因子释放,局部的炎性反应和范围会影响因子释放,局部骨组织的缺损状况影响支架状态,局部的应力影响力学环境[19-21]。在股骨头坏死发病中,坏死区的位置会影响股骨头内的应力状态,进而影响预后[19,22-24]。骨组织损伤后因子的释放存在时间和空间的限制,因而股骨头坏死的范围会影响其修复,进而影响其预后[13,20-23,25-26]。本研究发现的股骨头坏死后不同X线表现,可能是这些骨组织修复因素在股骨头坏死后共同作用的结果,符合文献中发现的股骨头坏死三种修复方式的假说(即限制性修复、破坏性修复和重建性修复的观察结果)[12-13],是股骨头坏死后的总体修复结果的反映。
本研究的缺点在于对坏死区的成骨特性分析缺少客观性,主要依据医生的主观分析,缺少量化指标,但这种成骨性的差异在临床上确实是可以明确看到的,目前国际上也缺乏相关的量化指标[13,16]。在今后的研究中,我们将进行相关的量化性研究。
通过本研究的结果分析,我们认为股骨头坏死的不同X线成骨表现对预后和治疗反应有明确的影响,在今后评价股骨头坏死治疗方法时要注重考虑患者本身的情况。
参考文献:
[1]Samy AM.Management of osteonecrosis of the femoral head:A novel technique[J].Indian J Orthop,2016,50(4):359-365.
[2]David S,Hungerford.Treatment of osteonecrosis of the femoral head[J].J Arthroplasty,2007,22(suppl 1):91-94.
[3]Shah SN,Kapoor CS,Jhaveri MR,et al.Analysis of outcome of avascular necrosis of femoral head treated by core decompression and bone grafting[J].J Clin Orthop Trauma,2015,6(3):160-166.
[4]Lieberman JR,Engstrom SM,Meneghini RM,et al.Which factors influence preservation of the osteonecrotic femoral head?[J].Clin Orthop Relat Res,2012,(470):525-534.
[5]Bassounas AEL,Karantanas AH,Fotiadis DI,et al.Femoral head osteonecrosis:Volumetric MRI assessment and outcome[J].Eur J Radiol,2007,63(1):10-15.
[6]Pierre Lafforgue.Pathophysiology and natural history of avascular necrosis of bone[J].Joint Bone Spine,2006,73(5):500-507.
[7]Takashi NishⅡ,Nobuhiko Sugano,Kenji Ohzono,et al.Progression and cessation of collapse in osteonecrosis of the femoral head[J].Clin Orthop Relat Res,2002(400):149-157.
[8]Byung-Woo Min,Kwang-Soon Song,Chul-Hyun Cho,et al.Untreated asymptomatic hips in patients with osteonecrosis of the femoral head[J].Clin Orthop Relat Res,2008(466):1087-1092.
[9]Kenji Ohzono,Masanobu Saito,Kunio Takaoka,et al.Natural history of nontraumatic avascular necrosis of the femoral head[J].J Bone Joint Surg(Br),1991,73(1):68-72.
[10]Malizos KN,Karantanas AH,Varitimidis SE,et al.Osteonecrosis of the femoral head:Etiology,imaging and treatment[J].Eur J Radiol.2007,63(1):16-28.
[11]Ng VY,Granger JF,Ellis TJ.Calcium phosphate cement to prevent collapse in avascular necrosis of the femoral head[J].Medical Hypotheses,2010,74(4):725-726.
[12]Hanns Plenk Jr,Martina Gstettner,Karl Grossschmidt,et al.Magnetic resonance imaging and histology of repair in femoral head osteonecrosis[J].Clin Orthop Relat Res,2001(386):42-53.
[13]Masaki Takao,Takashi NishⅡ,Takashi Sakai,et al.Repair in osteonecrosis of the femoral head:MR imaging features at long-term follow-up[J].Clin Rheumatol,2010,29(8):841-848.
[14]Sugano N,Kubo T,Takaoka K,et al.Diagnostic criteria for non-traumatic osteonecrosis of the femoral head[J].J Bone Joint Surg(Br),1999,81(4):590-595.
[15]Samuel J,Parsons,Niall Steele.Osteonecrosis of the femoral head:Part 1—Aetiology,pathogenesis,investigation,classification[J].Current Orthopaedics,2007,21(6):457-463.
[16]Steinberg ME,Hayken GD,Steinberg DR.A quantitative system for staging avascular necrosis[J].J Bone Joint Surg(Br),1995,77(1):34-41.
[17]Yang P,Bian C,Huang X,et al.Core decompression in combination with nano-hydroxyapatite/polyamide 66 rod for the treatment of osteonecrosis of the femoral head[J].Arch Orthop Trauma Surg,2014,134(1):103-112.
[18]Aarvold A,Smith JO,Tayton ER,et al.A tissue engineering strategy for the treatment of avascular necrosis of the femoral head[J].Surgeon,2013,11(6):319-325.
[19]Giannoudis PV,Einhorn TA,Marsh D.Fracture healing:The diamond concept[J].Injury,2007,38(S4):3-6.
[20]Dallas Burton Phemister.Repair of bone in the presence of aseptic necrosis resulting from fractures,transplantations,and vascular obstruction[J].Clin Orthop Relat Res,2008(466):1020-1033.
[21]Nick A Athanasou.Pathology of bone injury[J].Diagnostic histopathology,2009,15(9):437-443.
[22]Sen RK,Tripathy SK,Aggarwal S,et al.Early results of core decompression and autologous bone marrow mononuclear cells instillation in femoral head osteonecrosis[J].J Arthroplasty,2012,27(5):679-686.
[23]Doblare M,Garcia JM,Gomez MJ.Modelling bone tissue fracture and healing:a review[J].Engineering Fracture Mechanics,2004,71(13-14):1809-1840.
[24]Assouline-Dayan Y,Chang C,Greenspan A,et al.Pathogenesis and natural history of osteonecrosis[J].Semin Arthritis Rheum,2002,32(2):94-124.
[25]Geris L,Gerisch A,Sloten JV,et al.Angiogenesis in bone fracture healing:A bioregulatory model[J].J Theor Biol,2008,25(1):137-158.
[26]Dimitriou R1,Tsiridis E,Giannoudis PV.Current concepts of molecular aspects of bone healing[J].Injury,2005,36(12):1392-1404.
