卡托普利-地高辛缓速释双层片的初步药动学研究
2018-04-27马晓星
马晓星,徐 涛
(齐齐哈尔医学院 药学院, 黑龙江 齐齐哈尔 161006)
卡托普利(captopril,CAP)是血管紧张素转换酶抑制剂, 通过阻断血管紧张素I转变成具有高活性的血管紧张素Ⅱ,从而使血管紧张素Ⅱ的水平降低,起到扩张周围血管、减轻钠水储留、保钾保镁作用,减轻心脏后负荷,增加心脏排出量,营养心肌。地高辛(digoxin,DIG)是治疗心衰的正性肌力药,通过增加心肌细胞内Ca2+,增强心肌收缩力,兴奋迷走神经,减慢房室结的传导,减慢心率。文献报道,临床上使用卡托普利与地高辛联合治疗充血性心力衰竭,口服地高辛达后,加服卡托普利,地高辛可使心室容积及张力下降,不增加或降低总耗氧量,但地高辛不减轻前后负荷。而卡托普利能改善充血性心力衰竭患者的心脏功能,通过降低血浆血管紧张素Ⅱ和醛固酮水平而使心脏前后负荷减轻,二者联合用药比单用一种疗效更佳,作用加强,病程减短,是治疗心衰的首选药物[1-3]。卡托普利半衰期短,给药频繁,从而带来临床用药的不方便性。国外已有CAP缓释胶囊上市,国内上市的有卡托普利缓释片。地高辛起效慢,为提高地高辛在其安全范围内的释药速度,快速达到有效血药浓度,有报道将其制成分散片[4-5]。为此,根据临床用药特点及药物性质,本项目研制卡托普利-地高辛缓速释双层片,既能体现联合用药的优势,提高疗效,又能减少患者服药次数,提高其顺应性。
1 材料
1.1 药品与试剂
地高辛(武汉拉那白医药化工有限公司,批号:130405);卡托普利(武汉拉那白医药化工有限公司,批号:130513);卡托普利缓释片(上海凯宝药业股份有限公司,批号:111003);地高辛(上海信谊药厂有限公司生产,批号:20140206);甲醇(色谱纯,天津市福晨化学试剂厂);乙腈(色谱纯,天津市光复精细化工研究所)。
1.2 实验动物
10只家兔(雄性),体重平均 2.5 kg,购于辽宁医学院实验研究中心,动物实验许可证号:SYXK(辽)2014-0005。
1.3 仪器
集热式恒温加热磁力搅拌器(DF-101S,河南省于华仪器有限公司);真空干燥箱(DZF6050,上海博远实业有限公司);溶出度测定仪(RC-6,天津市光学仪器厂);单冲压片机(TDP,上海第一制药机械厂);高效液相色谱仪(D-1200,广州菲罗门科学仪器有限公司);台式高速离心机(TG22-WS,上海赵迪生物科技有限公司);超声清洗仪(KQ-250DE,昆山市超声仪器有限公司)
2 方法与结果
2.1 卡托普利-地高辛缓速释双层片的制备
根据国内外文献报道,临床观察显示[2-3,6]:口服地高辛,每日1次,加服卡托普利,每日3次,每次12.5mg,确定双层片剂量:每片含卡托普利37.5mg,地高辛0.25mg。
卡托普利缓释层处方:卡托普利3.75g,HPMC 14g,MCC 7.3g,硬脂酸镁0.2g,7%淀粉浆适量,制成100片。缓释层制备工艺:称取上述处方量原料药和辅料混匀,加淀粉浆制软材,过16目筛制粒,50℃干燥,18目筛整粒,加硬脂酸镁0.2g混匀。
地高辛速释层处方:载药颗粒9.6g,L-HPC4.5g,硬脂酸镁0.15g,制成100片。速释层制备工艺:称取地高辛0.3g,溶于400ml75%乙醇中,喷于100g空白颗粒,得载药颗粒,取载药颗粒10g与L-HPC、硬脂酸镁混匀。压制过程:先预压卡托普利缓释层,再填加速释层。
2.2 家兔体内初步药动学研究
2.2.1 色谱条件[7-8]
卡托普利:色谱柱:Agilent C18(250mm×4.6mm,5μm)。流动相:乙腈-1%醋酸(45:55),流速1.0ml·min-1。检测波长:257nm。柱温:38℃。
地高辛:Agilent C18(250mm×4.6mm,5μm)。流动相:甲醇-水( 60:40)。流速:1.0ml·min-1。检测波长:220nm。柱温:室温。
2.2.2 血浆样品的处理
卡托普利:取500ul血浆, 加30ul呋塞米,加50 ulNaOH (0.1mol·L-1)旋涡混合30s, 室温避光放置30min后, 加100μl1mol·L-1HCl溶液, 再加pH4.0缓冲液150μl混合15s, 加2.5ml萃取液(乙酸乙酯-苯=1:1), 旋涡2min,离心(2000r·min-1,10min),取有机相,40℃氮气吹干, 残渣用50μl流动相溶解后进样20μl。
地高辛:取血浆500μl,加呋塞米50μl,混合均匀,加1 mol·L-1硫酸溶液100μl,然后加提取液2ml(丙醇:氯仿=1:5),旋涡振荡5min,置离心机中,3000r·min-1离心,待分层后,吸取下清液,移至试管中;样品再加提取液2ml,重复萃取一次,合并萃取液,置37℃水浴氮气吹干,残渣用100μl流动相溶解,取20μl进样。
2.2.3 方法学研究
2.2.3.1 标准曲线的制备
卡托普利标准曲线:取空白血浆500 ul,加入30 μl浓度为6.25,12.5,25,50,100,200,400ug·ml-1的标准溶液,进行血样处理,以卡托普利浓度(C)为横坐标,卡托普利峰面积与内标物峰面积比值为纵坐标,加权最小二乘法(W=1/X2)进行回归,得回归方程A=0.00099C+0.00658(r=0.9990)。结果表明,血浆中卡托普利浓度在5~400ng·ml-1范围内线性良好。
地高辛标准曲线:取空白血浆500ul,加入10μl浓度为0.49,0.97,1.23,2.43,3.64,4.7,9.1ng·ml-1的标准溶液,进行血样处理,以地高辛浓度(C)为横坐标,地高辛峰面积与内标物峰面积比值为纵坐标,加权最小二乘法进行回归,得回归方程A=0.0462C-0.00556(r=0.9990)。结果表明,血浆中地高辛浓度在0.4~10ng·ml-1范围内线性良好。
2.2.3.2 方法专属性考察
对空白血浆、空白血浆加内标和对照品、给药后血浆进行专属性试验,结果见图2、图3,表明血浆中杂质不影响药物和内标物的测定。

图2 空白血浆(A),空白血浆加卡托普利和呋塞米(B),给药后含药血浆(C)的HPLC色谱图

图3 空白血浆(A),空白血浆加地高辛和呋塞米(B),给药后含药血浆(C)的HPLC色谱图
2.2.3.3 精密度试验
分别配制4,100,400ug/ml的卡托普利标准血样和0.5,2,10ng/ml的地高辛标准血样,每个浓度制备并测定5个样品,3d连续制备并测定3批。计算卡托普利批内及批间精密度RSD分别为0.71%,0.93%,0.35%和1.05%,1.14%,0.81%;地高辛批内及批间精密度RSD分别为1.18%,0.58%,0.39%和1.13%,0.99%,1.01%,符合测定要求。
2.2.3.4 回收率
分别配制4、100、400ug/ml卡托普利标准血样和0.5、2、10 ng/ml地高辛标准血样,每个浓度制备并测定5个样品,3d连续制备并测定3批。同时,另取空白血500μl,不加内标溶液,处理血样分析。考察样品及其内标的回收率。卡托普利3个浓度的回收率分别为93.72%,95.01%,94.76%;地高辛3个浓度的回收率分别为90.26%,95.19%,92.88%,符合测定要求。
2.2.3.5 样品稳定性
配制 4,100,400ug/ml卡托普利标准血样和0.5,2,10 ng/ml地高辛标准血样,分别室温放置1,3,5d,处理血样,进样测定。结果卡托普利和地高辛RSD均小于2%(n=3),表明血浆样品在上述条件下均稳定。
2.2.4 给药方案与血样采集
取10只家兔,体重平均2.5 kg,给药前禁食,4h后可进食,自由饮水。随机分成两组,每组5只,一组给卡托普利和地高辛市售片,一组给卡托普利-地高辛缓速释双层片。
给药后于20、45、60、120、240、360、480、600、720、1440、2160、2880min耳缘静脉取血2ml,置于含有肝素的离心管中。离心(3000r·min-1,8 min),取血浆于-20℃冰箱中保存待测。将待测血样按照“2.2.1”项下HPLC法计算血浆中地高辛及卡托普利含量,绘制血药浓度-时间曲线,见图4、图5,同时利用PKSolver 2.0软件计算出药动学参数,见表1、表2。

图4 卡托普利血药浓度-时间曲线图
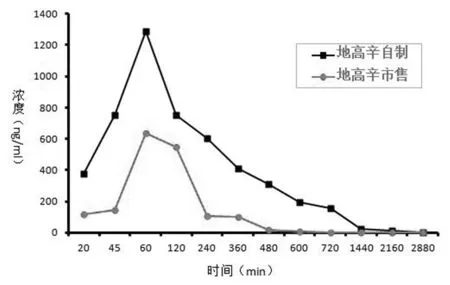
图5 地高辛血药浓度-时间曲线图
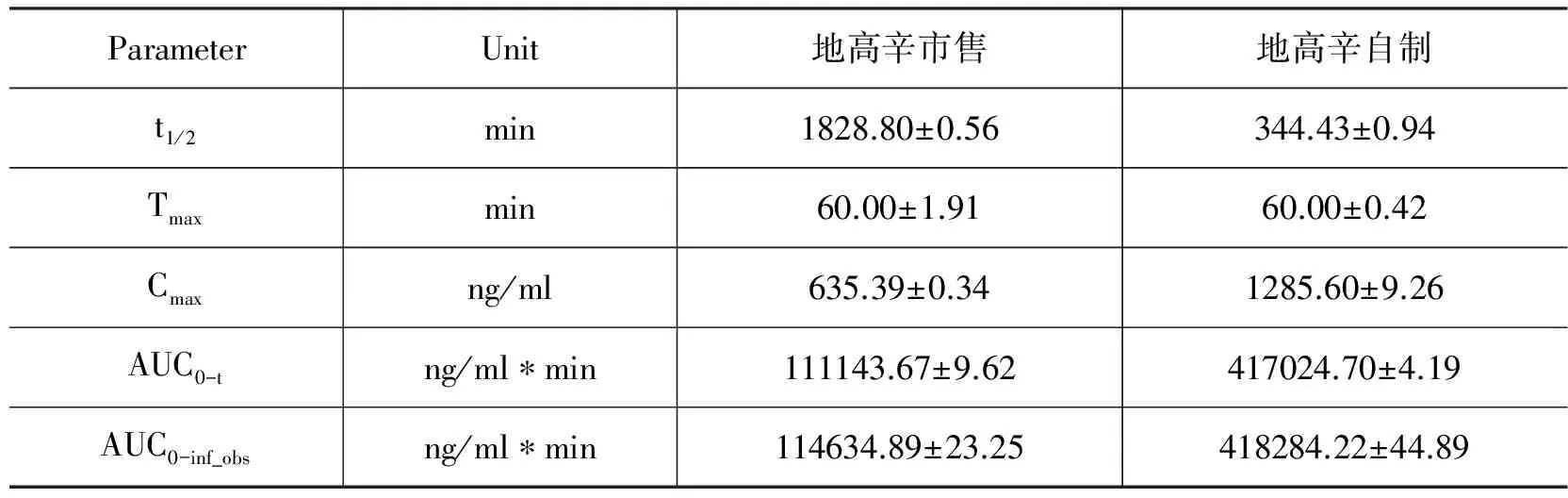
ParameterUnit地高辛市售地高辛自制t1/2min1828.80±0.56344.43±0.94Tmaxmin60.00±1.9160.00±0.42Cmaxng/ml635.39±0.341285.60±9.26AUC0-tng/ml∗min111143.67±9.62417024.70±4.19AUC0-inf_obsng/ml∗min114634.89±23.25418284.22±44.89

表2 自制制剂与市售制剂中卡托普利在家兔体内的部分药动学参数
结果显示,自制片中卡托普利和地高辛的AUC(0-∞)、Tmax、Cmax与市售片比较均有一定程度的增加;计算得相对生物利用度分别为(152.45±9.11) %和(375.21±13.11)% (相对生物利用度=AUC自制/AUC市售×100%);相对于市售片,自制片显著提高了药物口服生物利用度,二者具有一定的协同作用。
3 讨论
缓速释双层片的制备,采用湿法制粒压片制备卡托普利缓释层,释放度测定具有一定的缓释作用;空白颗粒法制备地高辛速释层,地高辛快速溶出;压制过程中,先预压卡托普利缓释层,再填加速释层,最后加入少量乳糖,制得的双层片完整,光泽度好,两层不宜裂开,且硬度符合要求。
本实验建立了HPLC法测定家兔血浆中地高辛和卡托普利浓度,方法学研究结果表明,该方法准确、可靠、简便,能够满足药动学研究要求。
通过家兔体内的药动学初步研究证实卡托普利-地高辛缓速释双层片中两种药物的AUC(0-∞)、Tmax、Cmax均呈现一定程度的增加,且卡托普利具有缓释作用;相对生物利用度与市售制剂比较也都有所提高,二者产生了一定的协同作用,这种协同作用的产生与临床上对于二者联合应用的文献报道相一致[9-11],因此,考虑复方制剂可适当减少用药剂量,具体应再进一步进行组方筛选,但产生这种协同作用的机制有待进一步研究,以更好地为临床合理用药提供理论依据。
参考文献:
[1] 刘兰,岳定员.地高辛和卡托普利联合用药探讨[J].中华现代医学与临床,2005,12(2):4-5.
[2] 刘秀花,王全智,徐丽萍.卡托普利与地高辛联合治疗心衰20例[J].新乡医学院学报,1994,11(1):78.
[3] 邹成红.卡托普利治疗心力衰竭55例临床观察[J].中外妇儿健康,2011,7(19):5.
[4] 毛东阳. 探讨地高辛分散片的研制与质量控制[J]. 现代医院,2008(3):61-63.
[5] 冯子群. 地高辛分散片的研制及质量控制[J]. 黑龙江科技信息,2014(19):22.
[6] Kirimli O, Kalkan S, Guneri S, et al.The effects of captopril on serum digoxin levels in patients with severe congestive heart failure[J].Int J Clin Pharmacol Ther 2001 Jul;39 (7):311-4.
[7] 王茂义,董亚琳,尤海生,等.RP-HPLC测定人血浆中卡托普利浓度及其药动学[J].中国药学杂志,2007(7):528-530.
[8] 阳波,李湘斌.RP-HPLC法测定人血清中地高辛浓度[J].中南医学科学杂志,2011(1):114-116.
[9] 万俊茹.卡托普利与地高辛联用治疗扩张型心肌病心衰的临床分析[J].中外医疗,2015(18):121-122.
[10] 巴拉提·吾马尔.卡托普利联合地高辛治疗扩张型心肌病致心力衰竭的临床观察[J].医疗装备,2016(4):53.
[11] 宋静华,高静,赵炳让.卡托普利对充血性心衰患者地高辛血药浓度的影响[J].天津医药,1997(3):145-146.
