多中心多学科团队疑难病例讨论(第4例)
2018-04-25张天楠,于仲勋,全美盈
1 病例报告
1.1 住院病史报告(儿科于仲勋)
女,10岁,因“间断发热4年,视力下降、脾大2年”于2018-08-23入住中国医学科学院北京协和医院(我院)儿科,至今。
现病史:2014年无明显诱因出现间断发热,最高体温38~39℃,无其他伴随症状,1~2个月发作1次,未特殊诊治。
2016年6月出现视力下降,左眼为著,就诊北京同仁医院,诊断“葡萄膜炎,眼底出血”,予口服甲泼尼龙、吗替麦考酚酯胶囊治疗,视力无明显改善。期间发现WBC减低(3.0~3.4×109·L-1)。
因“受凉后呕吐” 于2016-7-27至2016-8-10就诊于湘雅医院儿科。血常规:WBC 1.9×109·L-1,L 0.3×109·L-1,N 1.5×109·L-1,Hb 91 g·L-1,MCV 77.1 fL,MCH 23.9 pg,PLT 102×109·L-1。血生化:ALB 43.9 g·L-1,ALT 23 U·L-1,AST 18.6 U·L-1,尿素7.87 mmol·L-1,尿酸 453.3 μmol·L-1,CR 89.9 μmol·L-1,CK 38 U·L-1,CK-MB 29.6 U·L-1,铁蛋白 12.6 ng·mL-1。骨髓涂片:骨髓增生活跃,粒系53%,中晚幼及以上比例增高,红系37.5%,主要为中晚幼阶段,淋巴细胞7.5%,可见原、幼淋及个别幼单和部分退化细胞,全片巨核细胞及PLT分布可。感染:PCT 0.066 ng·mL-1,肺吸虫、血吸虫、旋毛虫、结核抗体、粪便寄生虫卵、TORCH、感染4项、肺炎支原体抗体等均(-)。免疫:CRP 1.33 mg·L-1,ESR 9 mm·h-1,C3、C4(-)。免疫球蛋白:IgG 7.04 g·L-1(降低),IgA、IgM在正常值范围。自身抗体谱:ANCA、抗心磷脂抗体、抗Sm抗体、抗SSA、抗SSB、ANA、抗ds-DNA抗体、抗Ro-52抗体、抗Scl-70抗体等均(-)。遗传:铜蓝蛋白 485 mg·L-1,乳酸 2 mmol·L-1,血、尿代谢病筛查正常。肿瘤:AFP、CEA、CA19-9、CA125、CA242、CA15-3、NSE等均(-)。腹部超声:肝脏、胆囊(-),门静脉主干内径10 mm,肠系膜上静脉内径5 mm,脾静脉内径12 mm,血流通畅,脾厚10 mm,脐下长38 mm,实质回声无明显异常,脾门区见17 mm×13 mm和12 mm×10 mm副脾声像。肝脏血管成像CTA+CTV:脾脏体积增大约9个肋单元,下缘达左侧盆腔内,实质内未见明显异常密度灶,增强后动脉期脾脏明显不均匀强化,CT值114~220 HU,门脉期强化均匀,CT值约157 HU,脾静脉增粗扩张,管径约1.4 cm,脾动脉稍增粗,肝静脉及其分支增粗,腹腔干、肝总动脉、肝固有动脉、腹主动脉、肠系膜上动脉、双肾动脉、门静脉主干及其分支、下腔静脉均显影好,未见明显狭窄、瘤样扩张及畸形血管团。电子胃镜:未见静脉曲张。胸部增强CT:未见明显异常,脾大。眼科:视力OD 0.4;OS 0.4。双眼视乳头边界不清,视网膜水肿,血管变细,见白鞘,黄斑部窥不清。建议手术脾切除,家长拒绝。
2016年8月就诊于北京同仁医院,停用吗替麦考酚酯胶囊,甲泼尼龙每周减半片,至减停。
2016-09-19至2016-10-13入住我院。入院查体:轻度贫血貌,腹稍膨隆,剑突下及右肋下可疑压痛,肝肋下、剑下未扪及;脾大,Ⅰ线15.5 cm,Ⅱ线14.5 cm,Ⅲ线 1.5 cm,质地中等。血常规:WBC (1.2~3.7)×109·L-1,Hb 98~120 g·L-1,PLT (71~129)×109·L-1。肝、肾功能正常。免疫球蛋白:IgG 4.61 g·L-1(降低),IgA 0.60 g·L-1(降低),IgM 0.42 g ·L-1。血清铁蛋白(Fer) 26 ng·mL-1(降低),尿常规、粪常规和凝血功能未见异常。免疫:体温正常时,CRP 9 mg·dL-1,ESR 7 mm·h-1;发热时,CRP 110 mg·dL-1,ESR 19 mm·h-1。TNF-α 28.5 pg·mL-1(升高),IL-6、IL-8、IL-10在正常值范围。抗可提取性核抗原(ENA)抗体、抗核抗体(ANA)3项、肝纤维化4项均(-)。TB细胞亚群:CD3+% 34%,CD19+4.8%,CD16+/56+8.9%,CD4+44.5%,CD8+35.4%(升高),CD4/CD8 1.26。感染:布氏杆菌凝集试验、G试验、抗莱姆抗体、EB病毒抗体、EBV-DNA、CMV-DNA、T-SPOT.TB、CMV-PP65、骨髓细菌涂片+培养+药敏、骨髓抗酸染色、尿培养、痰抗酸染色、痰细菌涂片+培养+药敏、杜氏利什曼原虫IgG抗体均(-)。针刺试验阴性。遗传:血氨、乳酸、β-葡萄糖苷酶、鞘磷脂酶在正常值范围。血涂片:RBC、WBC形态大致正常,PLT少见。骨髓涂片:增生活跃,粒∶红为2.3∶1,粒系中性分叶核粒细胞比例增高,部分中性粒细胞可见少许空泡变性,RBC大小不等,轻度中心淡染区扩大,淋巴及单核比例形态正常,PLT不少。腹部超声:肝剑下2.8 cm,肋下(-),回声均;脾厚4.7 cm,肋下6.6 cm,长径17.1 cm,脾门处见等脾回声,直径1.0 cm,双肾、胰腺、胆囊未见异常。门静脉彩色多普勒:门静脉主干内径1.0 cm,门静脉主干,左、右分支及矢状部管腔内血流通畅,充盈好,为入肝血流,最高流速59 cm·s-1。肠系膜上静脉、脾静脉内未见异常回声,血流通畅,充盈好。胰腺背侧脾静脉内径约0.9 cm。门静脉流速增高,脾静脉增宽。超声心动图:心脏结构及功能未见异常。全身DWI(2016-10-08,图1):实质内未见明显异常信号灶,中线居中;双侧颈部未见明显异常软组织影;双肺未见明显结节及实变影;肝脏稍饱满,呈獭尾肝;脾脏显著增大,右缘过中线,下极接近盆腔入口,ADC值约0.72;脾门区小结节影,信号与脾相近;胆、胰、双肾形态规则,信号均匀;膀胱充盈良好;幼女型子宫,双侧附件区未见明显异常信号。片中所见诸中轴及附肢骨质未见明显异常信号;双侧颌下、颈部、髂血管旁散在淋巴结,部分稍饱满,ADC值不低。印象:脾脏显著增大,伴副脾结节;肝脏稍饱满;双侧颌下、颈部、髂血管旁散在淋巴结,部分稍饱满,ADC值不低,炎性可能。眼科会诊:符合葡萄膜炎。综合考虑:患儿自身炎症性疾病可能性大,淋巴瘤不除外,建议行基因检测。基因检测(免疫panel)结果:MEFV基因c.1759+8c>t(p.E148Q)杂合突变,母源性;TMEM173基因c.5.4ddcc杂合突变,父源性;BIRC4(XIAP)基因c.*12>G 纯合突变(X染色体)。
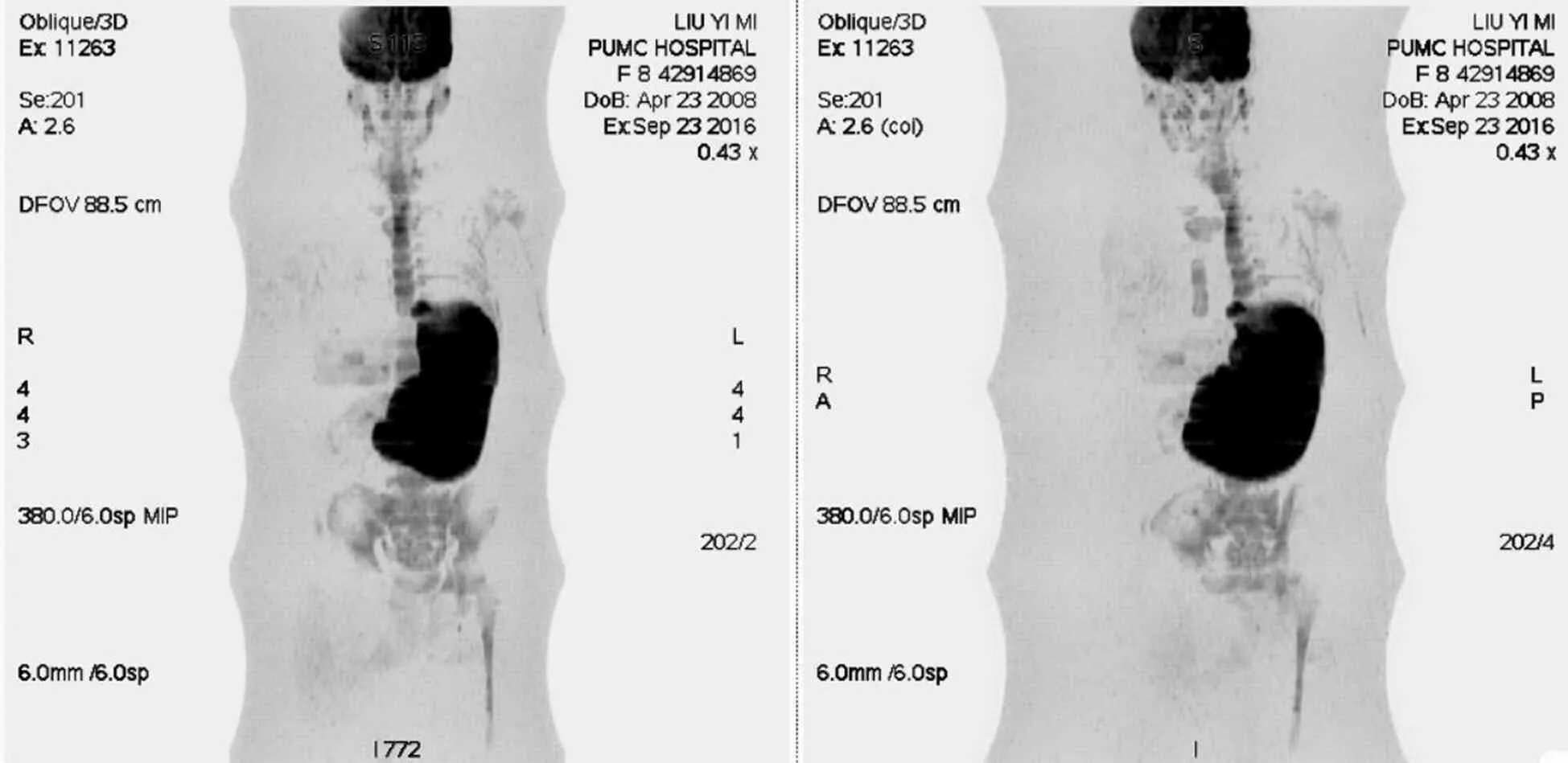
图1 患儿全身DWI
出院后规律服用泼尼松(10 mg, qd;2018-06-22减至7.5 mg, qd),期间眼科随诊考虑符合家族性地中海热(FMF)改变,予秋水仙碱治疗(0.25 μg,bid,2017-04-19至2017-06-20),患儿临床症状及血常规(WBC持续减低)无明显好转,停用。
2018-08-09于首都儿科研究所附属儿童医院行“脾切除术”。病理:脾切除标本1个,24 cm×14 cm×4 cm,脾下脾小结残存,脾窦广泛瘀血扩张,部分血管周围纤维组织增生显著,结合临床、形态及免疫组化结果,符合慢性瘀血性脾肿大。2018-08-11发热,最高体温38℃,伴咳嗽,咳少量白痰,次日热退。2018-08-21再次发热,最高体温 37.8℃,伴咳嗽,呕吐胃内容物6次,次日热退。为进一步诊治来我院。
患儿自发病以来,精神一般,食欲可,大小便无异常,近2年体重增长2 kg,脾切除术术前35 kg,术后33.5 kg。
既往史和个人史:患儿系G2P2,足月顺产,生长发育与同龄儿相当,现就读小学,成绩优秀。生后久居北京,偶回湖南居住。否认疫区、疫水接触史。按计划预防接种。
月经史:无。
家族史:母亲、姐姐、弟弟均体健。父亲43岁,2018年3月因“下肢无力疼痛”查ESR 94 mm·h-1, CRP 280 mg·L-1。2018年8月,心脏磁共振显示,心脏肥大,主动脉瓣增厚、关闭不全,左室增大,左室心尖段肌小梁增多,左、右室壁运动减低,LVEF 49%;肝酶升高;脂肪肝。否认家族中有类似疾病史,否认家族性精神病、肿瘤病、遗传性疾病病史。
体格检查:身高143 cm(P50),体重33.7 kg(P50),BSA 1.22 m2。T 36.8℃,P 100·min-1,R 21·min-1,BP 113/66 mmHg。面容、皮肤未见异常,手指及足趾偏长,心肺未见异常。腹正中见一纵向手术切口,自剑突下2 cm至耻骨联合上4 cm,长约12 cm,表面结痂,切口周边无红肿,无脓性分泌物。肝肋下、剑下未及。肠鸣音5·min-1。全腹无压痛、反跳痛。脊柱、关节、四肢、神经查体未见异常。
住院期间无发热,监测血常规:WBC (7.19~12.12)×109·L-1,Hb 99~125 g·L-1,PLT (933~1 190)×109·L-1。PLT增多考虑脾切除术后改变。网织红细胞 3.9%。外周血涂片:RBC、WBC形态大致正常,PLT增多。尿常规:pH 6.0,WBC 70·μL-1,蛋白微量,潜血(-);24 h尿蛋白定量0.13 g/24 h。粪常规未见异常。
免疫:ESR 6~19 mm·h-1,CRP 3~118 mg·L-1。炎症因子:TNF-α 87(参考上限8.1)pg·mL-1,IL-6 6.3(参考上限5.9)pg·mL-1。免疫球蛋白及补体:IgG 5.72 g·L-1,IgA 1.04 g·L-1,IgM 0.30 g·L-1;C3 1.308 g·L-1,C4 0.275 g·L-1。淋巴细胞亚群:T(85.2%)513·μL-1,T4(44.5%)268·μL-1,T8(35.4%)213·μL-1,B(4.8%)29·μL-1,NK(8.9%)54·μL-1,T4/T8 1.26。抗ENA抗体、ANA抗体、ANCA、抗磷脂抗体、肝纤维化4项均阴性。
影像学:头颅CT平扫示双上颌窦炎。胸部增强CT、超声心动图、泌尿系B超、下肢深静脉彩超未见明显异常。2018-09-03腹部增强CT+CTA:脾脏切除术后改变;脾窝内多发软组织结节,副脾结节代偿性增大可能;门静脉左支腔内充盈缺损,远段未见显影,考虑血栓形成可能;门静脉及其肝内右侧属支略增粗;腹膜后及肠系膜根部多发饱满淋巴结。血流功能显像示,在血流期,腹主动脉显影后2 s双肾显影,6~8 s显影欠清晰,双肾位置、大小、形态正常;在功能期,1 min双肾实质示踪剂浓聚达高峰,峰值较低,2 min双肾集合系统显影,4 min膀胱显影,观察至20 min,双肾实质内示踪剂已大部分排出,双肾盂见示踪剂残留,活动后显示大部分排出。肾小球滤过率估计值(eGFR)69.6 mL·min-1,右肾34.3 mL·min-1,左肾35.4 mL·min-1。双肾血流灌注及功能较差。
1.2 病例特点总结、讨论目的及问题(儿科全美盈) ①10岁,女,病程4年;②主要表现:反复发热,葡萄膜炎,脾大;③血三系轻度减低,符合脾亢;④发热时CRP升高;⑤目前未发现明确感染、肿瘤及先天遗传代谢性疾病的证据;⑥脾静脉迂曲增宽,肝静脉及门脉增宽,淤血性脾大,肝功能正常,肝纤维化4项正常,术后发现门静脉血栓;⑦GFR 69.6 mL·min-1,血流及灌注功能较差;⑧2016年免疫缺陷基因包检测MEFV未见明确致病突变;⑨父亲曾有ESR、CRP升高,心肌病变。
目前诊断:葡萄膜炎、发热、脾大原因待查,自身炎症性疾病可能,淋巴瘤不除外,X连锁凋亡抑制因子(XIAP)缺陷不除外;脾切除术后,继发PLT增多症可能性大;门静脉血栓。
原发病诊断尚不明确,从慢性发热及脾大切入,考虑慢性炎症,如SLE、幼年特发性关节炎(JIA)、Felty综合征,淀粉样变性,自身炎症性疾病;以及血管因素导致脾淤血,形成门静脉高压。①Felty综合征的支持点:脾大,血三系减低,发热,葡萄膜炎;不支持点:病史较长,目前无关节炎证据(65%~83%的Felty综合征患者有ANA、ANCA或抗组蛋白抗体阳性)。②淀粉样变性的支持点:脾大,肾功能异常,发热偶伴有胃肠道表现;不支持点:脾脏病理无提示,血清蛋白电泳及免疫固定蛋白电泳(-)。③FMF的支持点:反复发热,脾大,葡萄膜炎;不支持点:突变位点为杂合突变,来源于母亲,母亲体健; 曾试验性秋水仙碱治疗,因无效停用。④XIAP的支持点:发热,脾大,葡萄膜炎,BIRC4(XIAP) c.*12>G 纯合突变(X染色体);不支持点:无典型噬血表现,携带该突变的男性多为健康人群。⑤门静脉高压的支持点:肝脏血管成像CTA+CTV提示,脾静脉增宽,肝静脉及其分支增宽,门静脉增宽;不支持点:未见其余血管畸形,无肝硬化表现,心脏超声未见明显异常。
问题:①脾大,葡萄膜炎,发热原因未明,考虑自身免疫性或自身炎症性疾病可能性大,后续如何诊断及治疗;②是否存在门静脉高压及其与脾大的因果关系;③行全外显子基因检测及分析的必要性及意义。
2 多中心多学科讨论
2.1 北京大学第一医院儿科刘雪芹(摘录) 患儿主要临床表现为发热、巨脾和葡萄膜炎,病因主要考虑风湿病、血管炎、自身炎症性疾病和原发免疫缺陷病。风湿病:常见有发热、脾大伴葡萄膜炎的疾病为JIA,但患儿发热常持续1~3 d,可自行退热,发热间隔半月至1月,与JIA常见热型不符,且患儿无关节症状,暂不考虑JIA。血管炎:常表现为多系统受累且皮疹多见,患儿临床表现与之不符。自身炎症性疾病:FMF与患儿热型相符,MEFVp.E148Q基因突变;患儿目前尚无伴发浆膜炎和淀粉样变相关发现,肾功能轻度下降,可评估肾穿可能。原发免疫缺陷病:患儿IgG减低合并淋巴细胞及T、B细胞绝对计数下降,不能除外原发免疫缺陷病。X连锁淋巴组织增生性疾病(XLP):表现为发热、免疫球蛋白下降,BIRC4基因纯合突变,突变位点位于非编码区,XIAP不能除外,有待进一步鉴别。
2.2 华中科技大学同济医学院附属同济医院儿科方峰(摘录) 患儿巨脾合并门脉高压原因未明,结合目前影像学及相关检查结果,基本可除外肝性门脉高压及肝后性门脉高压可能。结合腹部B超及CT结果,考虑脾肾分流可能。查阅文献,脾肾分流导致脾脏瘀血,可引起脾大。但患儿门脉流速增加,此为不支持点,需警惕动脉门脉瘘可能。自身炎症性疾病和原发免疫缺陷病虽可解释发热、葡萄膜炎和脾大症状,但手术病理提示脾淤血,未发现淋巴细胞浸润等征象,同时,患儿以门静脉及脾静脉病变为主,而免疫性血管炎常累及动脉,故不支持自身免疫性疾病和原发免疫缺陷病的诊断。
2.3 上海交通大学医学院附属新华医院儿科何珂骏(摘录) 患儿Th1/Th2比例失衡,T细胞比例升高,粗略估算CD3+DNT细胞比例升高,需警惕免疫相关疾病,但免疫相关疾病常累及肾脏,目前肾脏表现不显著,可通过检测尿蛋白及尿微量蛋白评估肾脏有无受累,测定IgG亚类进一步评估免疫功能。此外,基因结果未能完全解释病情,可考虑体细胞突变可能。自身炎症性疾病不除外FMF可能,可行多重探针广谱分析(MLPA)进一步明确。
2.4 四川大学华西第二医院儿科陆晓茜(摘录) 查阅文献,有报道BIRC4突变可引起以葡萄膜炎等为特征的疾病,与患儿症状类似。为明确诊断,可通过流式细胞仪检测XLAP表达,明确突变意义。
2.5 北京大学第一医院眼科张文博(摘录) 患儿双眼视力下降,前房浅,眼压不高,玻璃体炎,视神经视网膜炎累及血管。病因考虑感染、非感染及伪装综合征。感染因素以单纯疱疹病毒、带状疱疹病毒、弓形虫、巨细胞病毒感染多见,但多次病原学及相关抗体检测无阳性发现,考虑感染可能性不大,可行房水及玻璃体病毒抗体检测或PCR检测。非感染常见白塞病、SLE和结节病,但均与患儿目前表现不符。此外,需警惕伪装综合征,该病常由累及中枢的淋巴瘤引起,可行颅脑MRI评估颅内有无病灶;眼内液IL-10升高及IL-10/IL-6>1,提示伪装综合征可能。
2.6 中南大学湘雅二医院儿科李晓燕(摘录) 患儿出生于湖南,为血吸虫病高发地区,慢性血吸虫感染可引起脾大、阻塞性门脉高压;且以往经验发现,少数慢性血吸虫感染患者可持续病原学检测阴性。需警惕慢性血吸虫感染可能,建议多次检测血吸虫抗原及抗体,以进一步除外。
2.7 复旦大学附属儿科医院孙金峤(摘录) 结合患儿发热、脾大、葡萄膜炎三大主要临床症状,考虑免疫失调疾病可能性大,可行T、B细胞精细亚群分类检测及淋巴细胞凋亡实验等,观察淋巴细胞功能有无改变。虽然检测到BIRC4基因纯合突变,但BIRC4突变引起的XLP-2型主要表现为淋巴增殖及EBV易感,淋巴细胞亚群检测可发现CD4/CD8比值倒置,患儿脾脏病理表现为脾淤血,无EBV感染证据,未发现CD4/CD8比值改变。同时,遗传模式不符,患儿父亲无明显XLP-2表现,考虑BIRC4突变起病可能性低,可行家系全外显子测序进一步除外。血管炎不能除外,可完善颅脑MRA及MRV进一步明确。
2.8 重庆医科大学附属儿童医院温贤浩(摘录) FMF的不支持点:无心脏病变,无关节症状、肾脏病变、皮疹等,秋水仙碱治疗无效。原发性免疫缺陷病:XIAP 缺陷症可以解释周期性发热、葡萄膜炎、脾大,检测到BIRC4(XIAP) 基因c.*12>G 纯合突变。但不能解释其父亲及弟弟不发病。有报道女性杂合突变可发病,原因可能是父源性X染色体非随机失活,并偏向带有致病基因的另1条X染色体。但基因测序检测出XIAP为双等位基因。可考虑完善XIAP蛋白表达水平及功能检测,细胞凋亡、NKT 细胞的检测,及X染色体失活(XCI)比值。
2.9 浙江大学医学院附属儿童医院沈和萍(摘录) XLP是一种以致死性EBV感染、B细胞和细胞毒性T细胞失控增生导致淋巴瘤高发、噬血细胞综合征和免疫缺陷为主要表现的X连锁隐性遗传性疾病。发病率为1/100万,XLP分为两型,XLP-1为编码SLAM相关蛋白(SAP)的基因SH2D1A突变所致, XLP-2为编码凋亡抑制蛋白的基因XIAP突变所致。XLP-1与XLP-2表现的差异:①XLP-1更易发生淋巴瘤,②XLP-2更易脾大,③ XLP-2较易发生结肠炎。XLP患者仅对EBV特别敏感,对其他疱疹病毒如单纯疱疹病毒、巨细胞病毒和6型疱疹病毒的免疫反应正常。可采用单克隆抗体分析SAP和XIAP蛋白,进一步分析SH2D1A或XIAP基因。
2.10 中山大学广州市妇女儿童医疗中心金颖康(摘录) XLP相关基因突变可以与其他自身炎症性疾病存在炎症通路的“交叉反应”,如可以降低NLRP3基因的活性,表现出与隐热蛋白相关周期综合征(CAPS)类似的临床表现,但患儿为女孩,XLP在自身炎症性疾病中的机制还需进一步探讨。综合考虑基因检测结果,需注意重叠综合征的可能,如自身炎症性疾病重叠,自身炎症性疾病与尚未出现的自身免疫性疾病、甚至少见的自身免疫性疾病早期重叠。
2.11 广州市妇女儿童医疗中心眼科项道满(摘录) 眼科专科检查提示病情持续、波折加重,眼科诊断:中后部葡萄膜炎。特点:慢性“葡萄膜炎”;未见免疫沉积物的结节样改变,葡萄膜炎常见的感染性及自身免疫性指标均阴性;CRP、TNF-α 等炎症指标升高。结合临床特征,提示自身炎症性疾病相关的视网膜血管炎,合并表位扩张或隐蔽抗原释放等机制继发的中间型葡萄膜炎。
3 自由发言
上海市儿童医院郝胜 患儿脾切术后,使用生物制剂有增加感染的风险,需权衡获益与风险。
广西医科大学贾文胜 患儿有免疫缺陷基础,不能完全除外感染,未做病理组织培养。
华中科技大学同济医院儿科方峰 基因型不能完全解释,但临床表现支持诊断XIAP,可以行XIAP蛋白表达水平检测,如结果提示表达偏低,则更加提示XIAP。
患儿病程4年肾血流图像提示灌注异常,目前监测肌酐尚在正常范围,不能除外肾脏慢性受累,建议继续监测肾脏相关标志物。
中山大学广州妇女儿童医疗中心金颖康 目前已报道的年龄最大的家族性噬血细胞综合征患者为1例69岁的西班牙女性,建议对患儿家系密切随访,XLP携带者可长期无临床表现。
4 讨论总结(全美盈医师)
原发病考虑自身炎症性疾病可能性大,XIAP可能;全外显子测序对明确诊断有很大提示意义。考虑患儿免疫缺陷基础,使用生物制剂治疗原发病带来的感染风险较大,目前暂不适宜使用生物制剂治疗。需密切随访该家系成员。
致谢:本病例诊疗过程中北京协和医院儿科多次组织多学科讨论,感谢给予极大支持的各位儿科专家(宋红梅、肖娟、邱正庆、李正红、王薇、马明圣、全美盈、简珊)、病理科专家(陈杰)、感染科专家(郭伏平)、眼科专家(睢瑞芳)。
本病例为儿科发展联盟秘书处组织的多中心多学科团队疑难病例讨论,感谢儿科发展联盟各成员其他医院的专家(以医院首字汉语拼音排序):
北京大学第一医院儿科(刘雪芹、张文博);重庆医科大学附属儿童医院(温贤浩);复旦大学附属儿科医院(孙金峤);华中科技大学同济医学院附属同济医院儿科(方峰);上海交通大学医学院附属新华医院儿科(何珂骏);四川大学华西第二医院儿科(陆晓茜);中国医科大学盛京医院眼科(杨宏伟);浙江大学医学院附属儿童医院血液肿瘤科(沈和萍);中南大学湘雅二医院儿科(李晓燕);中山大学广州市妇女儿童医疗中心呼吸科(金颖康)眼科(项道满)。
