败酱草抑制大肠癌HCT-8/5-FU细胞耐药的作用研究
2018-04-24刘望予娄云云汤锦周王建荣陈锦缎
周 庄 ,刘望予 ,娄云云 ,汤锦周 ,王建荣 ,陈锦缎
(1.福州市第二医院,福建 福州 350007;2.福建中医药大学中西医结合研究院,福建 福州 350122;3.福建中医药大学药学院,福建 福州 350122)
大肠癌发病率和死亡率均呈逐年上升趋势,每年新增病例高达120万,死亡病例也远超60万人[1-2]。 化疗是大肠癌晚期患者、转移性患者等不适合手术患者的主要治疗方式[3],5-氟尿嘧啶(5-FU)是大肠癌化疗的基础用药[4],广泛应用于大肠癌治疗。然而,耐药的产生和毒副作用的存在是影响其临床疗效并最终导致治疗失败的主要原因[5]。因此,抑制耐药性将有助于提高化疗药物疗效和降低化疗药物使用浓度,从而降低化疗导致的毒副作用。
大肠癌属中医“肠癖”“肠覃”范畴,以“湿热蕴毒下迫大肠、热伤肠络、毒邪成痈”为主要病机,“清热解毒、消痈散结”是其治法治则之一[6-7]。 败酱草属败酱科植物黄花败酱、白花败酱的干燥全草,具有清热解毒、祛瘀止痛、消痈排脓的功效,符合大肠癌“清热解毒、消痈散结”治法治则[8-9],已有研究报道,败酱草在临床中广泛应用于大肠癌等恶性肿瘤的治疗,且疗效确切[10]。基础研究也证实了败酱草具有显著抑制大肠癌细胞增殖、诱导细胞凋亡、抑制血管新生以及抑制炎症相关因子的作用[11-15]。然而,对大肠癌治疗药物5-FU耐药的影响尚未见报道,因此,本课题探讨了败酱草对5-FU耐药性的影响。
1 材料
1.1 细胞株和药物 人源性肠癌细胞株HCT-8和耐5-FU的HCT-8/5-FU细胞株均购于江苏南京凯基生物科技发展有限公司;败酱草全草购于福建中医药大学国医堂。
1.2 试剂 胎牛血清(FBS)、RPMI 1640空白培养基、含 EDTA(0.25%)的胰蛋白酶(美国 GBICO公司);PBS、青霉素-链霉素(美国 Hyclone公司);结晶紫、MTT(美国 Amresco公司);5-FU粉末、阿霉素(美国Sigma公司)。
1.3 仪器 细胞培养工作台(苏州净化设备公司);CO2培养箱(美国Thermo Fisher公司);离心机(德国Eppendorf公司);全自动酶标仪(美国Bio-Tek公司);荧光倒置显微镜系统(德国徕卡公司)。
2 方 法
2.1 药物配制 败酱草全草500 g溶入4 000 mL 80%乙醇中,加热回流提取2次,每次30 min,提取液过滤,滤液减压浓缩(50℃,0.01MPa)至相对密度1.05,喷雾干燥(进出口温度为 140℃/80℃)得干粉[16];称量适量提取物,用 50%DMSO 和 50%PBS溶解,配制成 250 mg/mL的储存溶液,经震荡和超声后,-20℃分装保存备用;使用前置室温恢复,用RPMI 1640完全培养基稀释成所需的浓度并过滤,并用 DMSO 补齐[16]。
2.2 5-FU溶液配制 采用DMSO溶解适量的5-FU粉末,并配制成1M的存储液,置于-20℃冰箱保存备用。使用时采用倍比稀释法将5-FU储存液用完全培养基配制成所需的使用浓度,用于细胞干预。
2.3 细胞培养 将细胞置于25 cm2的培养瓶中培养,待细胞覆盖率达80%~90%时,用含EDTA的胰酶消化(每瓶加入0.8 mL胰酶,消化2~3 min);待细胞消化下来后,加入2~3倍体积的新鲜完全培养基(完全培养基含10%FBS、100 U/mL青霉素和100 μg/mL 链霉素的 RPMI 1640 培养液)中和,将上述细胞悬液转移到15 mL的离心管中离心(1 000 转 /min,3~5 min);离心结束后,弃上清,并加入5 mL新鲜培养基,重悬、计数,用于后续的接种、传代。HCT-8细胞用RPMI 1640完全培养基培养,HCT-8/5-FU 用含 15 μg/mL RPMI 1640 完全培养基培养,实验前改用不含5-FU的RPMI 1640完全培养基培养。
2.4 倒置显微镜观察细胞生长 HCT-8和HCT-8/5-FU 分别按 2×105/mL接种于 6孔板中(2 mL/孔),置于培养箱中培养过夜,并给予不同浓度的5-FU 干预(0~200 μM)或败酱草干预(0~2 mg/mL)。药物干预24 h后通过倒置显微镜(×200)观察细胞生长。
2.5 MTT法检测细胞活力 取对数生长期的HCT-8/5-FU细胞及其亲本细胞HCT-8,分别接种于96孔板(100 μL /孔,0.8×105/mL);细胞置于培养箱中培养过夜后,分别加入终浓度为 0、50、100和200 μM 5-FU 溶液 (HCT-8/5-FU 细胞和 HCT-8细胞)或 0、0.5、1、2 mg/mL 败酱草溶液(HCT-8/5-FU细胞)干预24 h,每个剂量各3各复孔。实验结束后,弃上清液,每孔加入 MTT 溶液(100 μL/孔,0.5 mg/mL)并在培养箱中避光孵育4 h;孵育结束后,弃 MTT 溶液,并加入 DMSO(100 μL/孔)溶解,采用全自动酶标仪(波长为570 nm)测定OD值,并根据OD值计算细胞的活力。以对照组细胞活力为100%,实验组的细胞活力=实验组OD值/对照组OD值×100%。
2.6 荧光倒置显微镜观察阿霉素(ADM)蓄积情况取对数生长期HCT-8/5-FU细胞接种于6孔板(1×105/mL,2 mL/孔),细胞置于培养箱中培养过夜后,分别给予不同浓度的败酱草溶液(0~2 mg/mL)干预24 h。实验结束后,弃上清,PBS清洗3遍,加入适量的阿霉素染色溶液(5 μM,1 mL/孔),培养箱避光孵育后,用预冷的PBS清洗3遍,用荧光倒置显微镜观察拍照(×200)。
2.7 统计学方法 数据采用SPSS 20.0统计软件分析。计量资料属正态分布的以(x±s)表示,2组数据和多组数据分别采用独立样本t检验和多因素方差分析。
3 结 果
3.1 HCT-8/5-FU细胞株对5-FU具有耐药性验证 HCT-8和HCT-8/5-FU细胞分别经不同浓度5-FU(0、50、100、200 μmol/L)干预后,倒置显微镜观察发现HCT-8细胞数目逐渐减少,部分细胞出现皱缩、变圆和漂浮等现象,而HCT-8/5-FU细胞未见明显细胞形态和细胞数量改变,可见其具有一定的耐药性(图1A)。这一现象进一步通过MTT实验进行验证,MTT检测结果如图1B所示:HCT-8细胞经不同浓度5-FU干预后,细胞活力显著降低;而HCT-8/5-FU细胞在不同浓度5-FU干预后,细胞活力下降不明显;在相同浓度5-FU干预下,HCT-8的细胞活力显著低于HCT-8/5-FU细胞。进一步证实了HCT-8/5-FU细胞对5-FU具有一定的耐药性。
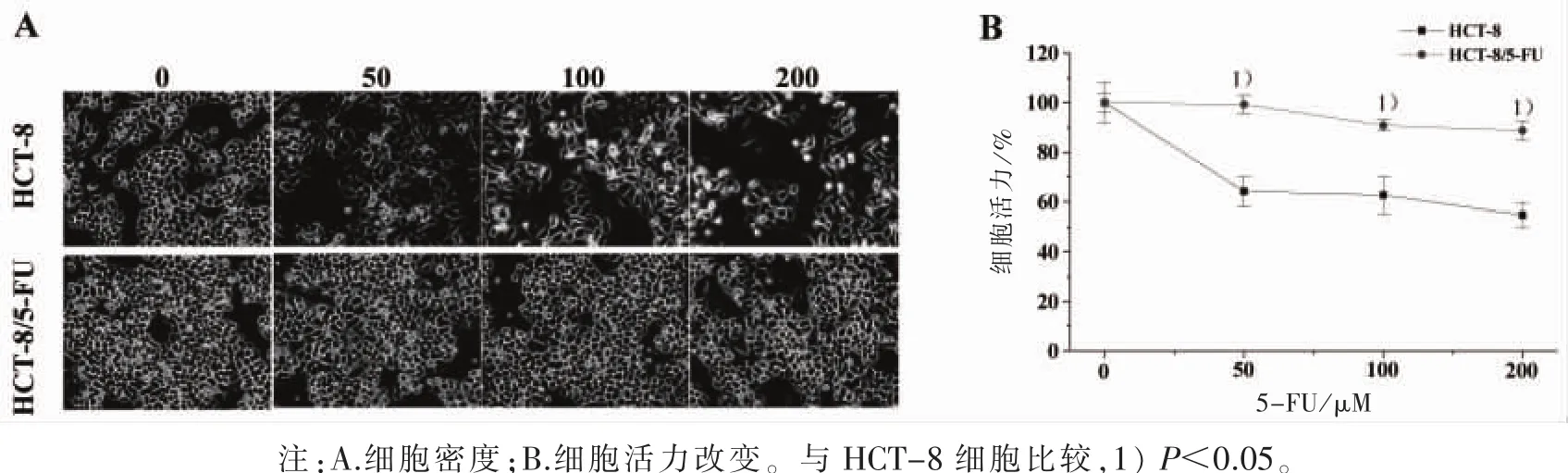
图1 HCT-8/5-FU细胞耐药性验证图(×200)
3.2 败酱草对HCT-8/5-FU细胞生长的影响 倒置显微镜的观察结果如图2所示:不同浓度败酱草(0.5~2 mg/mL)干预后,HCT-8/5-FU 细胞覆盖率明显降低,可见部分细胞变小、变圆,提示败酱草对HCT-8/5-FU细胞的生长有一定的抑制作用。
3.3 败酱草对HCT-8/5-FU细胞活力的影响 如图3所示:用不同浓度的败酱草溶液干预24 h,HCT-8/5-FU细胞株细胞活力明显降低,具有统计学差异(P<0.05);且浓度越高,细胞活力越低。实验结果进一步证实了败酱草对HCT-8/5-FU细胞生长的抑制作用。
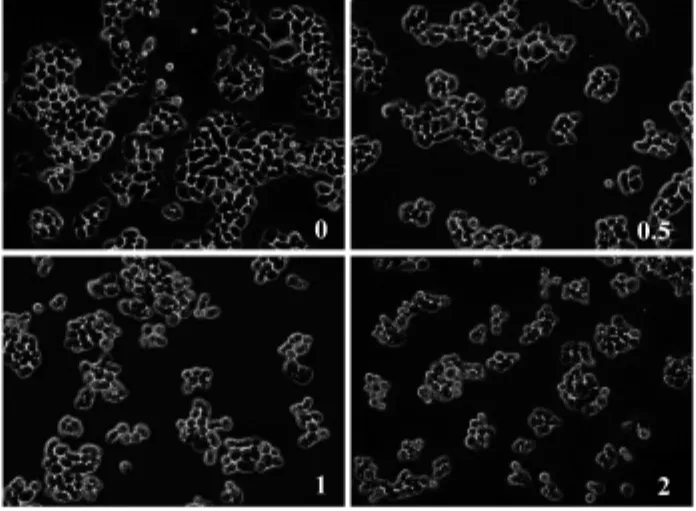
图2 败酱草对HCT-8/5-FU细胞形态的影响(×200)
3.4 败酱草溶液对HCT-8/5-FU细胞阿霉素蓄积的影响 阿霉素具有自带荧光的特性,阿霉素在细胞内的荧光强度可以反映其在细胞内的浓度从而反映细胞膜的外排功能。本研究采用阿霉素染色和倒置荧光显微镜观察不同浓度败酱草干预对阿霉素蓄积的影响。如图4所示:与对照组比较(荧光较弱),不同浓度败酱草溶液(0.5~2 mg/mL)干预后,可显著增加阿霉素(红色荧光)在HCT-8/5-FU细胞株细胞内的蓄积。结果提示败酱草具有抑制HCT-8/5-FU细胞膜药物外排的作用。
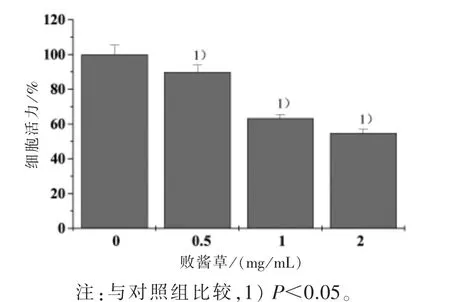
图3 败酱草对HCT-8/5-FU细胞活力的影响
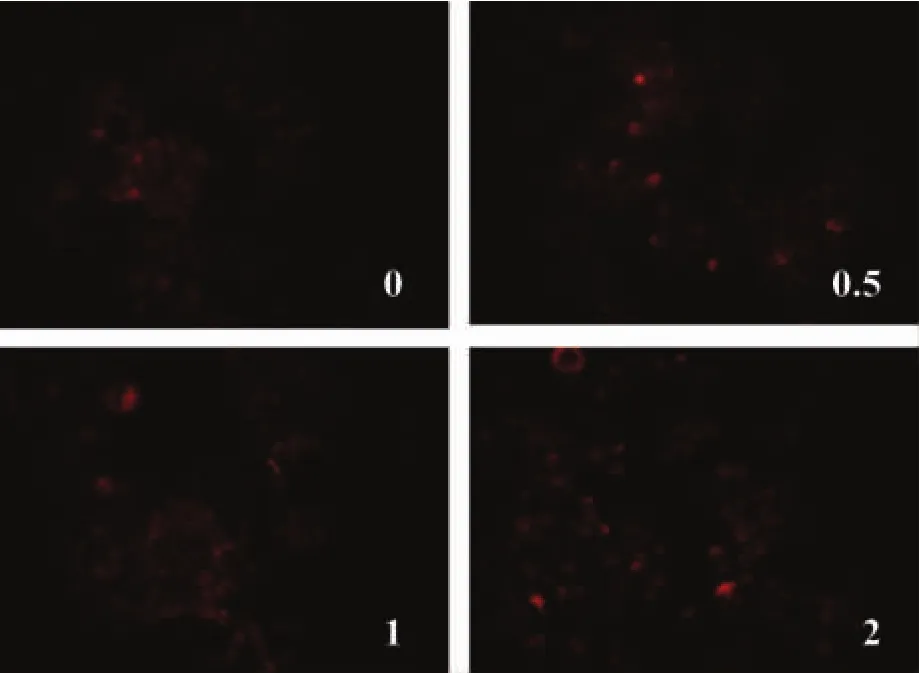
图4 败酱草对HCT-8/5-FU细胞阿霉素蓄积的影响(×200)
4 讨论
5-FU是大肠癌化疗基础用药,在体内会转化成氟尿嘧啶核苷酸,具有抑制DNA、RNA合成的作用[17],临床上广泛应用于消化系统肿瘤的治疗[4]。然而化疗过程产生耐药是影响化疗疗效和最终导致治疗失败的最主要原因。肿瘤化疗导致的耐药机制极其复杂,其中ABC家族蛋白高表达介导的细胞膜的外排功能异常增强和细胞凋亡增殖蛋白异常表达介导的凋亡抵抗是肿瘤细胞产生耐药功能的主要机制之一[18],因此,抑制肿瘤细胞生长和药物外排功能是抑制耐药的重要途径之一。
中药治疗恶性肿瘤的历史悠久,疗效可佳,而且相对化疗药物,具有毒副作用较小和作用靶点多等特点。基础研究已证实败酱草具有显著抑制大肠癌细胞增殖、诱导细胞凋亡和抑制血管新生的作用[10-12]。本研究进一步研究了败酱草具有显著抑制HCT-8/5-FU细胞的作用,同时也初步证实了败酱草干预能够抑制HCT-8/5-FU细胞的外排功能。可见,败酱草对大肠癌耐药具有一定的抑制作用。
大肠癌耐药的发生发展过程极为复杂,其发生机制与多条信号转导通路的异常调控密切相关,而败酱草治疗大肠癌具有多成分、多靶点的作用特点。本研究仅从细胞层面观察败酱草对于大肠癌耐药的影响,败酱草对于大肠癌耐药细胞的调控作用及复杂机制的研究仍有待进一步深入。
参考文献:
[1] JEMAL A,BRAY F,CENTER M M,et al.Global cancer statistics [J].CA Cancer J Clin,2011,61(2):69-90.
[2] BRENNER H,KLOOR M,POX C P.Colorectal cancer [J].Lancet,2014,383(9927):1490-1502.
[3] 徐珊,徐昌芬.肿瘤多药耐药性发生机制及中药逆转作用的研究进展[J].中国肿瘤生物治疗杂志,2006,13(6):404-411.
[4] CARRILLO E,NAVARRO S A,RAMIREZ A,et al.5-Fluorouracil derivatives:a patent review [J].International Society of Amyloidosis,2015,25(10):1-14.
[5] OHTSU A.Chemotherapy for metastatic gastric cancer:past,present,and future [J].Gastroenterol,2008,43(4):256-264.
[6] 陈叶,刘金涛,朱源,等.大肠癌中医辨证及治疗概况[J].中国肿瘤生物治疗杂志,2015,11(3):243-251.
[7] 杨静,刘洪斌,李东华.清热解毒方改善脓毒症大鼠脏器功能的比较[J].中国中西医结合外科杂志,2012,18(2):157-160.
[8] 赵栋,丁青,肖艺.败酱草的研究进展[J].中医药导报,2009,15(10):76-78.
[9] 王蒨.败酱草的研究进展[J].医学综述,2009,15(13):2021-2022.
[10]高学敏.中药学[M].7版.北京:中国中医药出版社,2002:140-142.
[11] CHEN L,LIU L,YE L,et al.Patrinia scabiosaefolia inhibits colorectal cancer growth through suppression of tumor angiogenesis [J].Oncol Rep,2013,30(3):1439-1443.
[12] LIU L,SHEN A,CHEN Y,et al.Patrinia scabiosaefolia induces mitochondrial-dependent apoptosis in a mouse model of colorectal cancer [J].Oncol Rep,2013,30(2):897-903.
[13] PENG J,CHEN Y,LIN J,et al.Patrinia scabiosaefolia extract suppresses proliferation and promotes apoptosis by inhibiting the STAT3 pathway in human multiple myeloma cells [J].Mol Med Rep,2011,4(2):313-318.
[14] ZHANG M,SUN G,SHEN A,et al.Patrinia scabiosaefolia inhibits the proliferation of colorectal cancer in vitro and in vivo via G1 /S cell cycle arrest [J].Oncol Rep,2015,32(2):856-860.
[15] LEE E J,KIM C,KIM J Y,et al.Inhibition of LPS-induced inflammatory biomarkers by ethyl acetate fraction of Patrinia scabiosaefolia through suppression of NF-κB activation in RAW 264.7 cells [J].Immunopharmacol Immunotoxicol,2012,34(2):282-291.
[16]黄炜,杨斌,陈阳,等.败酱草乙醇提取物对人结肠癌细胞Caco-2 凋亡与增殖的影响[J].福建中医药,2013,44(3):57-59.
[17] TOLBA M F,ABDEL-RAHMAN S Z.Pterostilbine,an active component of blueberries,sensitizes colon cancer cells to 5-fluorouracil cytotoxicity [J].Sci Rep,2015,16(5):15239.
[18] BROXTERMAN H J,GOTINK K J,VERHEUL H M.Understanding the causes of multidrug resistance in cancer:a comparison of doxorubicin and sunitinib [J].Drug Resist Updat,2009,12(5):114-126.
