索非布韦联合α-干扰素治疗慢性丙型肝炎患者疗效比较的Meta分析
2018-03-28焦方舟张海月张文斌王鲁文龚作炯
焦方舟,张海月,张文斌,王鲁文,龚作炯
慢性丙型肝炎(CHC)在全球范围流行,大约1.85亿人感染了丙型肝炎病毒(HCV),未经正规治疗的CHC患者将向肝纤维化、肝硬化和肝细胞癌进展[1]。传统的治疗方法是α-干扰素(IFN-α或PEG-IFN)联合利巴韦林(RBV)。随着口服直接抗病毒药(DAA)的研发和应用,治疗CHC患者有了革命性的进展,其中以索非布韦(sofosbuvir,SOF)为代表的DAA药在国外已成为主要的抗HCV药物。虽然大量临床研究证实SOF联合RBV治疗CHC可获得较高的持续病毒学应答率(SVR)[2-5],而SOF/PEG-IFN/RBV是否比SOF/RBV或PEG-IFN/RBV治疗有更好的治疗效果还有待证实。本研究旨在通过循证医学方法检索国内外应用SOF/PEG-IFN/RBV与SOF/RBV或PEG-IFN/RBV治疗CHC患者的临床研究,比较它们疗效的差异。
1 资料与方法
1.1 检索策略 应用计算机检索 PubMed、Cochrane Library、中国期刊全文数据库(CNKI)、中国生物医学文献数据库(CBM)、万方数据库和中文科技期刊全文数据库(VIP),检索时间截止至2017年3月。以“慢性丙型肝炎、索非布韦、聚乙二醇干扰素、利巴韦林 ”,“Chronichepatitis C、Sofosbuvir、Peginterferon alfa、Ribavirin”为检索词,并对纳入研究的参考文献进行二次检索。文献纳入标准:(1)随机对照试验或队列研究;(2)比较 SOF/PEG-IFN/RBV与 SOF/RBV或SOF/PEG-IFN/RBV与PEG-IFN/RBV治疗的疗效差异。疗效结局指标:快速病毒学应答(RVR)、SVR、不良发应。文献排除标准:(1)无对照组的文献;(2)重复发表的文献。
1.2 资料提取和文献质量评价 提取纳入文献的一般信息,包括第一作者、发表年份、研究对象感染HCV基因型、年龄、性别、具体干预措施、疗程、结局指标等。质量评价:由2名医生独立地采用Jadad评分量表[6]对纳入的研究进行质量评价。具体评估标准包括:(1)随机序列的产生(2分);(2)随机化隐藏(2分);(3)盲法(2分);(4)撤出和退出(1分),满分为7分,4~7分视为高质量文献。
1.3 统计学方法 应用Cochrane协作网提供的RevMan 5.2软件和Stata 12.0软件进行Meta分析。采用统计学I2检验各研究间的异质性。当异质性小(I2≤50%,P≥0.1)时,采用固定效应模型进行Meta分析;当研究间异质性较大(I2>50%,P<0.1)时,采用随机效应模型分析,根据其异质性可能的来源进行相应的亚组分析,并应用敏感性分析检验结果是否稳定,即依次剔除各个研究,观察P值是否发生改变。以Begg’漏斗图和Begg检验[7]进行发表偏倚的评估。
2 结果
2.1 纳入研究的一般情况 共检出相关文献111篇,去除非临床研究和重复文献后,纳入94篇。通过阅读文题和摘要,剔除不符合纳入标准文献后,最终纳入合格文献9篇[8-16],共827例患者(SOF/PEG-IFN/RBV组 444例,SOF/RBV组 269例,PEG-IFN/RBV组114例)被纳入本次研究。文献的质量评价结果表明,3篇研究≥4分,为高质量文献,而其他文献质量均<4分,为低质量研究。所纳入的各研究的基本资料和质量评分见表1,具体的干预措施见表2。
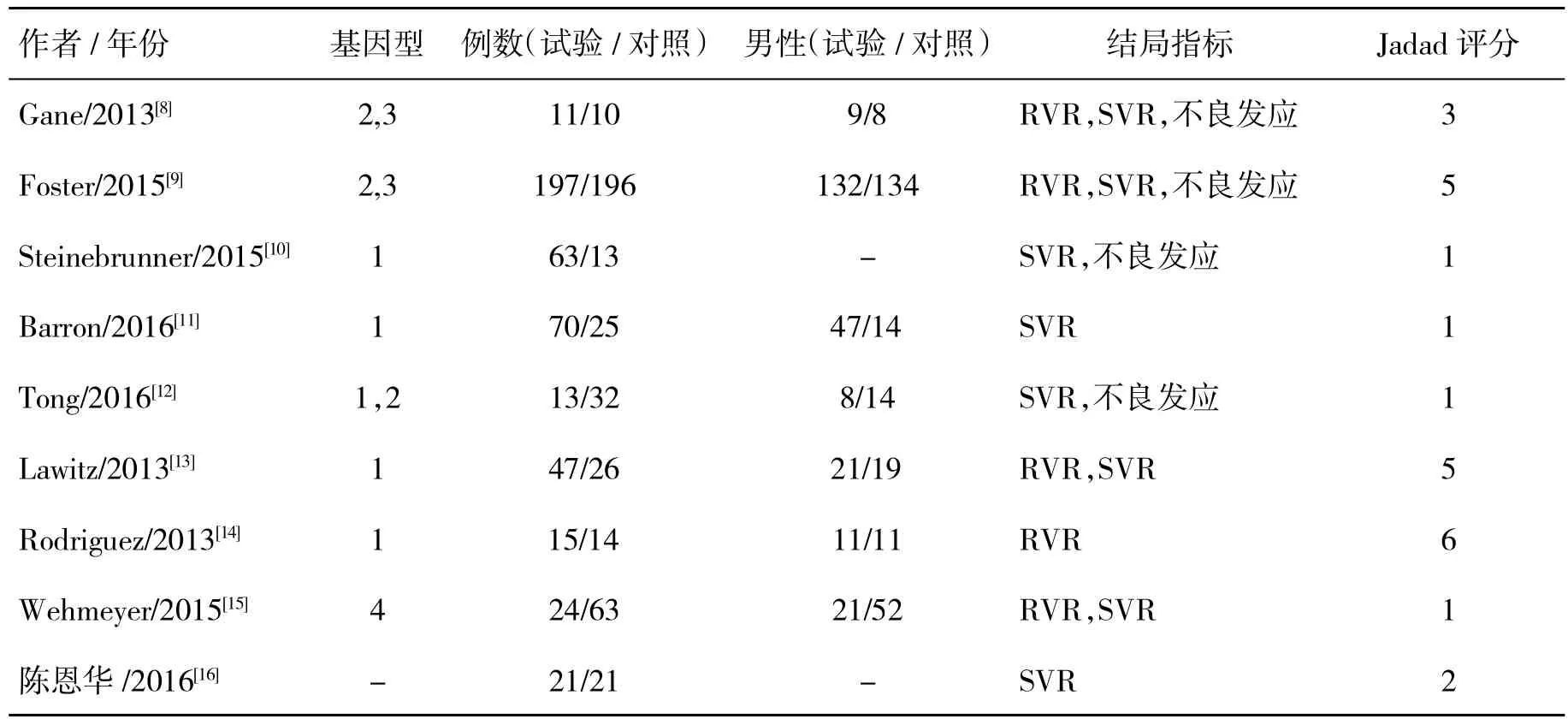
表1 纳入研究的基本资料和质量评分
2.2 RVR 3个研究[8-10]比较了SOF/PEG-IFN/RBV组与SOF/RBV组的RVR,3个研究[13-15]比较了SOF/PEG-IFN/RBV组与PEG-IFN/RBV组的RVR。异质性检验发现,各研究间存在异质性(P=0.13,I2=55%;P=0.006,I2=80%),采用随机效应模型处理,结果SOF/PEG-IFN/RBV组RVR与SOF/RBV组比为 86.7%对 71.7%(Z=3.08,P=0.002);与 PEGIFN/RBV组比为 91.7%对 32.3%(Z=2.76,P=0.006),表明SOF/PEG-IFN/RBV治疗获得的RVR更高(图1)。
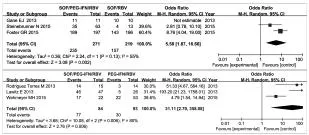
图1 SOF/PEG-IFN/RBV组与SOF/RBV组或PEG-IFN/RBV组RVR比较的Meta分析
2.3 SVR 5个研究[8-12]比较了SOF/PEG-IFN/RBV组与SOF/RBV组在治疗结束后12周时的SVR,3个研究[13,15-16]比较了SOF/PEG-IFN/RBV组与PEGIFN/RBV组在治疗结束后12周时的SVR。异质性检验发现,SOF/PEG-IFN/RBV组与SOF/RBV组之间存在异质性(P=0.06,I2=60%),采用随机效应模型处理,而 SOF/PEG-IFN/RBV组与 PEG-IFN/RBV组间研究无异质性(P=0.26,I2=26%),采用固定效应模型处理。结果SOF/PEG-IFN/RBV组与SOF/RBV组比SVR为89%对74.1%(Z=1.40,P=0.16),而与PEG-IFN/RBV组比为 85.7%对 44.2%(Z=5.35,P<0.00001), 表明 SOF/PEG-IFN/RBV 治 疗 与SOF/RBV治疗CHC患者SVR差异无统计学意义,而与PEG-IFN/RBV治疗比,SVR更高(图2)。

图2 SOF/PEG-IFN/RBV组与SOF/RBV组或PEG-IFN/RBV组SVR比较的Meta分析
2.4 不良反应发生率 本研究比较了SOF/PEG-IFN/RBV组与SOF/RBV组不良事件发生情况,包括头疼、疲劳、失眠、恶心、皮疹、头晕、肌痛、腹泻、易怒、瘙痒、食欲减退、关节痛、发热、贫血(HB<100 g/L)。Meta分析结果显示,SOF/PEG-IFN/RBV组头疼、疲劳、恶心、皮疹、肌痛、食欲减退、关节痛、发热、贫血(HB<100g/L)等的发生率均较SOF/RBV组高,差异具有统计学意义(P<0.05);SOF/PEG-IFN/RBV组头晕、肌痛、腹泻、易怒、瘙痒、失眠等不良事件发生率与SOF/RBV组比,差异无统计学意义(P>0.05,表3)。

表3 SOF/PEG-IFN/RBV组与SOF/RBV组不良反应发生率比较的Meta分析
2.5 发病偏倚 经Begg检验,P=0.734,Begg漏斗图基本对称,表明研究间存在发表偏倚的可能性非常小(图 3)。

图3 Begg漏斗图
A:SOF/PEG-IFN/RBV组与SOF/RBV组比较Meta分析的Begg漏斗图;B:SOF/PEG-IFN/RBV组与PEG-IFN/RBV组比较Meta分析的Begg漏斗图 两漏斗图提示纳入研究间无明显的发表偏倚
3 讨论
CHC是全球性公共卫生问题,传统的抗病毒(IFN-α或PEG-IFN联合RBV)治疗对于基因2型或3型患者的SVR是80%,对于基因型1型患者仅为40%~50%[17]。随着DAA药物的上市,给CHC患者的治疗带来了里程碑式的意义。DAA具有口服、疗程短、泛基因型、不良反应轻的特点,并可用于治疗丙型肝炎肝硬化、失代偿期肝病患者[18]。目前,美国肝病学会指南已把DAA药物作为治疗丙型肝炎的常规首选药物。对于基因3型等难治性慢性丙型肝炎患者,指南推荐SOF/PEG-IFN/RBV联合治疗[19]。已有研究对SOF/PEG-IFN/RBV与SOF/RBV治疗方案进行比较,发现SOF/PEG-IFN/RBV与SOF/RBV 治疗 CHC 患者均获得较高的 SVR[8,9,11,12]。因此,本研究通过循证医学方法对这些数据进行了比较分析,发现SOF/PEG-IFN/RBV与SOF/RBV治疗CHC患者的疗效差异和不良反应发生情况,并且比较了SOF/PEG-IFN/RBV与传统抗病毒治疗方案(PEG-IFN/RBV)的疗效差异。
本研究应用RevMan5.2软件进行Meta分析,结果显示,SOF/PEG-IFN/RBV组RVR显著高于SOF/RBV组或PEG-IFN/RBV组,SOF/PEG-IFN/RBV组SVR显著高于PEG-IFN/RBV组,但与SOF/RBV组比,无统计学差异。在不良反应方面,SOF/PEG-IFN/RBV组头疼、疲劳、恶心、皮疹、肌痛、食欲减退、关节痛、发热、贫血这些不良事件发生率均较SOF/RBV组高,且差异具有统计学意义。通过Stata12.0软件对研究进行发表偏倚评估,Begg检验结果以及漏斗图显示不存在发表偏倚。Liu X[20]行Meta分析发现对于初治的慢性丙型肝炎患者,应用SOF/PEG-IFN/RBV和SOF/RBV获得SVR分别为89%和72%,不良反应发生率分别为4%和3%,该Meta分析结果与本研究结果类似。
综上所述,基于索非布韦的抗病毒治疗CHC患者可获得较高的病毒学应答率,而且索非布韦联合干扰素和利巴韦林治疗相比索非布韦联合利巴韦林或聚乙二醇干扰素联合利巴韦林治疗慢性丙型肝炎可获得更高的快速病毒学应答率。
本系统评价尚存在以下局限性:(1)纳入的研究较少,中文研究较少,高质量的病例对照研究也较少;(2)各研究报道的结局指标不尽相同,且个别文章数据无法使用,使分析结果受到限制;(3)受研究设计的局限和样本量的限制,本研究结果的可靠性尚需大样本、高质量的研究予以证实。
[1]Kattakuzhy S,Levy R,Kottilil S.Sofosbuvir for treatment of chronic hepatitis C.Hepatol Int,2015,9(2):161-173.
[2]Abraham GM,SpoonerLM.Sofosbuvirin thetreatmentof chronic hepatitis c:new dog, new tricks.Clin Infect Dis,2014,59(3):411-415.
[3]Omata M,Nishiguchi S,Ueno Y,et al.Sofosbuvir plus ribavirin in Japanese patients with chronic genotype 2 HCV infection:an open-label,phase 3 trial.J Viral Hepat,2014,21(11):762-768.
[4]Shah SR,Chowdhury A,Mehta R,et al.Sofosbuvir plus ribavirin in treatment-naive patients with chronic hepatitis c virus genotype 1 or 3 infection in India.J Viral Hepat,2017,24(5):371-379.
[5]Kao JH,Chien RN,Chang TT,et al.A phase 3b studyof sofosbuvir plus ribavirin in Taiwanese patients with chronic genotype 2 hepatitis c virus infection.Liver Int,2016,36(8):1101-1107.
[6]霍晴,古赛.甘草酸二铵肠溶胶囊治疗脂肪性肝病疗效Meta分析. 实用肝脏病杂志,2015,18(4):371-374.
[7]Begg CB,Mazumdar M.Operating characteristics of a rank correlation test for publication bias.Biometrics,1994,50(4):1088-1018.
[8]Gane EJ,Stedman CA,Hyland RH,et al.Nucleotide polymerase inhibitor sofosbuvir plus ribavirin for hepatitis c.N Engl J Med,2013,368(1):34-44.
[9]Foster GR,Pianko S,Brown A,et al.Efficacy of sofosbuvir plus ribavirin with orwithoutpeginterferon-alfa in patientswith hepatitis C virus genotype 3 infection and treatment-experienced patients with cirrhosis and hepatitis C virus genotype 2 infection.Gastroenterology,2015,149(6):1462-1470.
[10]Steinebrunner N,Sprinzl MF,Zimmermann T,et al.Early virological response may predict treatment response in sofosbuvir-based combination therapy of chronic hepatitis C in a multi-center“real-life”cohort.BMC Gastroenterol,2015,15:97.
[11]Barron J,Xie Y,Wu SJ,et al.Treatment of chronic hepatitis C infection with sofosbuvir-based regimens in a commercially insured patient population.Am Health Drug Benefits,2016,9(6):327-335.
[12]Tong MJ,Chang PW,Huynh TT,et al.Adverse events associated with ribavirin in sofosbuvir-based therapies for patients with chronic hepatitis C:a community practice experience.J Dig Dis,2016,17(2):113-121.
[13]Lawitz E,Lalezari JP,Hassanein T,et al.Sofosbuvir in combination with peginterferon alfa-2a and ribavirin for non-cirrhotic,treatment-naive patients with genotypes 1,2,and 3 hepatitis C infection:a randomised,double-blind,phase 2 trial.Lancet Infect Dis,2013,13(5):401-408.
[14]Rodriguez-Torres M,LawitzE,KowdleyKV,etal.Sofosbuvir(GS-7977)plus peginterferon/ribavirin in treatment-naive patients with HCV genotype 1:a randomized,28-day,dose-ranging trial.J Hepatol,2013,58(4):663-668.
[15]Wehmeyer MH,Jordan S,Lüth S,et al.Efficacy and safety of sofosbuvir-based triple therapy in hepatitis C genotype 4 infection.Dig Liver Dis,2015,47(9):811-814.
[16]陈恩华.聚乙二醇干扰素利巴韦林单用及联合索非布韦治疗慢性丙型肝炎疗效观察. 母婴世界,2016,12(2):74.
[17]Zeuzem S,Berg T,Moeller B,et al.Expert opinion on the treatmentof patients with chronichepatitis C.JViralHepat,2009,16(2):75-90.
[18]窦晓光,丁洋.我国丙型肝炎防治新策略探讨.传染病信息,2016,29(2):71-72,100.
[19]AASLD/IDSA HCV GuidancePanel.HepatitisC guidance:AASLD-IDSA recommendations for testing,managing,and treating adults infected with hepatitis C virus.Hepatology,2015,62(3):932-954.
[20]Liu X,Wang Y,Zhang G,et al.Efficacy and safety of sofosbuvir-based therapy for the treatment of chronic hepatitis C in treatment-naive and treatment-experienced patients.Int J Antimicrob Agents,2014,44(2):145-151.