Ag修饰C掺杂TiO2薄膜的光电响应性能
2018-03-23落全伟李秀燕刘瑞萍范明明
落全伟,李秀燕,任 超,刘瑞萍,曹 铃,范明明
(太原理工大学 物理与光电工程学院,山西 晋中 030600)
自从1972年Fujishima和Honda发现光照TiO2电极分解水产生氢气这一现象以来,半导体光催化技术就成为催化领域的一大热点[1]。随着能源的日趋紧缺以及环境的日益恶化,寻找高效清洁的能源以及制备能改善环境的光催化材料成为科学研究者的努力方向之一。由于TiO2自身具有廉价、无毒、化学性质稳定等优点,所以它一直都是光催化方面的主要研究对象[2]。同时TiO2也存在着先天的缺点,比如:禁带宽度大(锐钛矿相为3.2 eV,金红石相为3.0 eV),使得它的光响应范围落在了紫外光区域,这一缺陷极大的限制了它在太阳光下的光电及光催化性能,因为太阳光中紫外光大概只有3%~5%[3]。因此,对TiO2的改性使得它的光响应范围落在可见光区域就成为科研的追求方向。常见的TiO2改性方法有:金属掺杂、非金属掺杂(比如:C,N,S,F等)、金属-非金属共掺杂、半导体复合、表面光敏化等手段[4]。研究表明,C掺杂对改善TiO2的可见光催化活性具有显著的效果[5-6]。HIROSHI IRIE et al[7]先在空气中氧化TiC原料36 h后再在氧气中淬火一段时间制备出了具有可见光活性的C掺杂TiO2光催化剂。DE-EN GU et al[8]将TiC和硝酸与乙醇的混合液在60 ℃环境下搅拌12 h制备了C掺杂TiO2催化剂。但常见的以TiC为原料制备C掺杂TiO2催化剂大多采用低温、耗时的方式来实现,生产周期长,不利于实际应用。此外,C掺杂TiO2虽然可以增加对可见光的响应,但同时也会提高光生电子-空穴的复合率。研究表明,在TiO2催化剂表面进行贵金属沉积能有效提高电子-空穴的分离率从而提高其光电性能及光催化活性。常用的沉积贵金属有Ag,Au,Rt,Rh,Ru等[9-10]。本研究采用高温,低时长热氧化TiC的方式制备了C掺杂TiO2薄膜,利用光还原沉积法[11-12]在C掺杂TiO2薄膜表面负载了Ag纳米颗粒,并对薄膜的光电响应性能进行了研究。
1 实验制备
1.1 TiC薄膜的制备
将1 g的TiC粉末(粒径为40 nm)加入100 mL的去离子水中,将其混合液在超声波振荡器中震荡1 h使其分散均匀。将纯Ti片(Ti纯度≥99.9%,尺寸为40 mm×10 mm×1 mm)先后用800#和1 000#的砂纸进行打磨,然后将打磨好的Ti片放入10 mL的酸洗液中进行酸洗,酸洗液V(HF)∶V(浓HNO3)∶V(去离子水)=1∶3∶6为实验室自制,酸洗时长5 min,将酸洗后的钛片分别顺次放入丙酮、乙醇、去离子中超声波清洗3 min.之后采用电泳沉积法制备TiC薄膜,其中电压为15 V,电泳时长为4 h.
1.2 C-TiO2薄膜及Ag-C-TiO2薄膜的制备
将制备好的TiC薄膜置于管式炉(OTF-1200X)中热氧化3 h使其生成C-TiO2薄膜。由于热氧化温度在550 ℃以下时TiC未能完全转变为C-TiO2,故只对热氧化温度在550~750 ℃范围内的样品进行研究,热氧化的温度分别设定为550,600,650,700,750 ℃.将制备好的C-TiO2薄膜浸入浓度分别为0.01,0.02,0.03,0.04,0.05 mol/L的AgNO3溶液中90 min,然后将其浸入浓度为0.1 mol/L的甲醇溶液中并在功率为300 W的氙光灯紫外光下(带通频率为350 nm)进行光还原90 min,使其生成Ag-C-TiO2薄膜。
1.3 样品结构及表面形貌的表征
采用丹东浩元仪器DX-2700型X射线衍射仪对薄膜的物相结构进行分析,使用铜靶,λ=0.154 18 nm;电压40 kV,电流40 mA;扫描范围20°~80°.样品的表面形貌和表面能谱分析(EDS)采用日本JEOL型扫描电子显微镜测试。
1.4 薄膜样品的光电性能测定
利用电化学工作站(CHI 660e,上海辰华仪器有限公司)采用三电极体系统测定Ag-C-TiO2和C-TiO2薄膜样品的瞬态光电流。其中,以薄膜样品作为工作电极,饱和甘汞电极作为参比电极,铂片作为辅助电极,电解液为0.5 mol/L的Na2SO4溶液,工作电极面积为1.2 cm2.以功率为300 W的氙光灯(PLS-SXE300C/CUV,北京泊菲莱科技有限公司)为光源,可见光使用的滤波片截止频率为420 nm,紫外光使用的滤波片带通频率为350 nm.
样品的荧光光谱采用英国爱丁堡生产的稳态/瞬态荧光光谱仪FLS980测试,激发波长为470 nm,扫描范围540~700 nm.
样品的紫外-可见光吸收光谱(UV-Vis)采用日本岛津公司生产的UV-2600型紫外-可见光谱仪测试,吸收波长范围300~800 nm.
2 结果与讨论
2.1 薄膜的相结构分析
图1为TiC经过热氧化后生成样品的XRD图谱,反映出经过不同温度热氧化生成的C-TiO2样品的相结构变化。图中2θ为25.4°、48.1°的衍射峰分别对应于锐钛矿相TiO2的(101)和(200)晶面;2θ为27.5°、36.1°分别对应于金红石相TiO2的(110)和(101)晶面。在550~650 ℃热氧化温度范围,生成的C-TiO2薄膜由锐钛矿相和金红石相的混晶构成,在700~750 ℃时完全转变为金红石相。相关文献认为,由锐钛矿相和金红石相组成的混合晶相的TiO2具有更高的光电性能及光催化活性[13-14],因此下面对550~650 ℃生成的C-TiO2的相结构进行进一步分析。
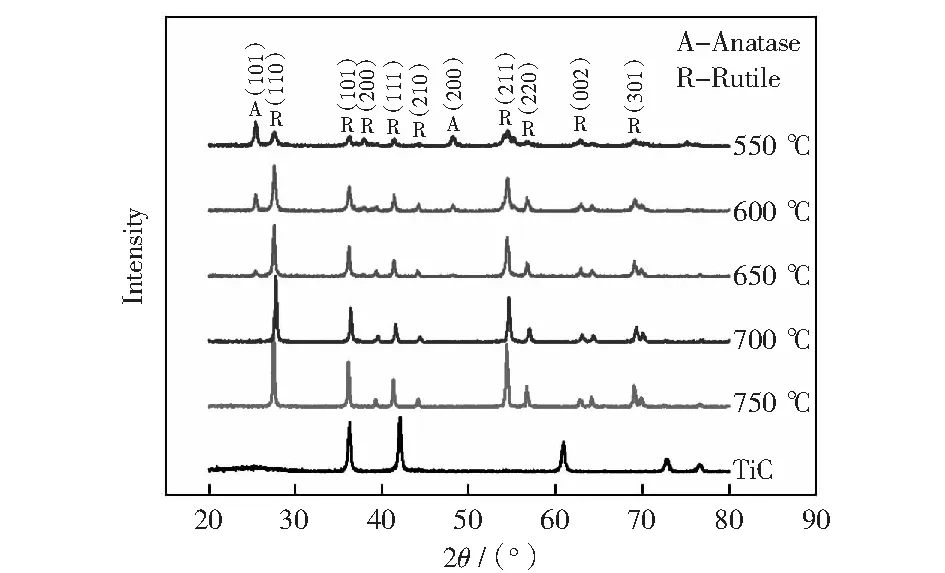
图1 TiC及不同温度下制备的C-TiO2样品的XRD谱Fig.1 XRD patterns of TiC and C-TiO2 formed at different temperature
根据Scherrer公式
可求得样品中锐钛矿相和金红石相C-TiO2的平均粒径。公式中:D为晶粒尺寸,nm;k为Scherrer常数,其值为0.89;λ为X射线波长,其值为0.154 18 nm;β为积分半高宽度,在计算过程中需转化为弧度,rad;θ为衍射角。
锐钛矿相和金红石相混合晶相的C-TiO2的平均粒径Davg可根据如下公式计算求得:
式中,DA代表锐钛矿相(Anatase)的平均粒径;DR代表金红石相(Rutile)的平均粒径;IA和IR分别代表锐钛矿相(101)晶面(2θ为25.4°)和金红石相(110)晶面(2θ为27.5°)对应的衍射峰强度。
混晶中锐钛矿相的百分比R可根据如下公式计算求得[15-20]
R=(1+0.8IA/IR) .
其中,IA和IR的含义同上式。混晶的晶相组成及晶粒尺寸见表1.随着热氧化温度的升高,C-TiO2的晶粒变大,且锐钛矿相向金红石相转变。650 ℃生成的C-TiO2(记作C-TiO2650)的平均晶粒大小约为28 nm,锐态矿相占比7%,其余为金红石相。
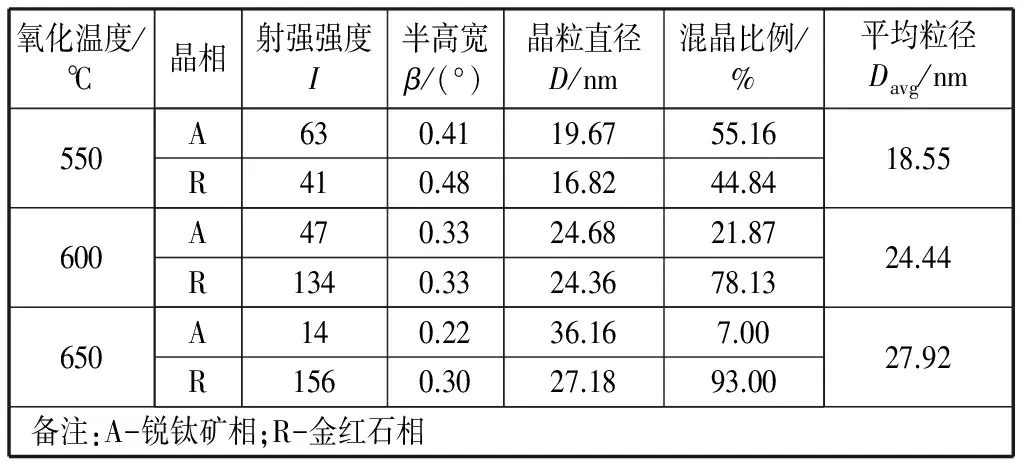
表1 C-TiO2的晶相组成及晶粒尺寸Table 1 Crystalline phase constituent and grain size of C-doped TiO2
2.2 薄膜的表面形貌及成分分析
图2(a)为TiC薄膜放大5 000倍时的表面形貌图,可以看出采用电泳沉积法在Ti片表面均匀地沉积上了TiC薄膜,表明所选取的电泳沉积TiC的工艺参数是合适的。图2(b)是C-TiO2650薄膜样品放大5 000倍的表面形貌图,经热氧化处理生成的C-TiO2薄膜较之前的TiC薄膜更为致密。图2(c)是负载Ag的C-TiO2650薄膜样品(记作Ag-C-TiO2650)的高倍表面形貌图,负载Ag时AgNO3溶液的浓度是0.03 mol/L;从图2(c)中可以清晰的看出Ag颗粒相对均匀地分布在C-TiO2薄膜表面。图2(d)是Ag-C-TiO2650薄膜表面各成分的原子百分比。

图2 薄膜样品的SEM与EDS表征Fig.2 SEM images and EDS analysis of the samples
2.3 薄膜的光电响应性能
图3(a)和3(b)是不同温度下制备的C-TiO2薄膜样品分别在可见光和紫外光下测试的瞬态光电流密度图。C-TiO2薄膜除了具有紫外光电响应性能,对可见光也有显著的响应,这是因为C元素的掺杂。此外,可以发现C-TiO2650样品对紫外光和可见光都表现出最佳的光电响应性能,其中可见光下C-TiO2的瞬态光电流密度约为28 μA/cm2,紫外光下C-TiO2的瞬态光电流密度约为50 μA/cm2.
为了进一步优化C-TiO2薄膜的性能,本实验通过配制浓度分别为0.01,0.02,0.03,0.04,0.05 mol/L的AgNO3溶液,利用光还原沉积法,在C-TiO2650样品表面负载了Ag纳米颗粒,以探究不同的Ag负载量对C-TiO2薄膜光电响应性能的影响规律。图3(c)和3(d)为不同的Ag-C-TiO2薄膜分别在可见光和紫外光下测试的瞬态光电流密度图。从图中可以看出,负载Ag可以显著改善C-TiO2薄膜对紫外和可见光的光电响应性能,而且AgNO3溶液的浓度会影响到所制备的Ag-C-TiO2薄膜样品的性能。在浓度为0.03 mol/L的AgNO3溶液中制备的Ag-C-TiO2薄膜样品具有最大的瞬态光电流密度。其在可见光下的最大瞬态光电流密度约为460 μA/cm2,是未负载Ag样品的16.4倍;在紫外光下该样品的最大瞬态光电流密度约为780 μA/cm2,是未负载Ag样品的15.6倍。
AgNO3浓度对Ag-C-TiO2薄膜瞬态光电流密度的影响说明,Ag的负载量对薄膜的光电响应性能有直接影响,过多或者过少的Ag负载量都不利于薄膜光电性能的提高。当Ag负载量过少时,C-TiO2在光的作用下产生的电子-空穴对不能及时地分离迁移到薄膜表面参与光电反应;当Ag负载量过多时,光生电子-空穴对反而会在Ag颗粒附近再次复合,过量的Ag颗粒充当了电子-空穴对的复合中心,从而影响了Ag-C-TiO2薄膜的光电响应性能[21-23]。此外,在测定Ag-C-TiO2薄膜样品的瞬态光电流密度时发现,薄膜样品对光的响应非常迅速,且在光持续照射下瞬态光电流密度相对稳定,衰减现象不太明显;这说明在C-TiO2薄膜表面负载贵金属Ag不仅能有效抑制电子-空穴对的复合,而且能提高载流子的迁移速率。
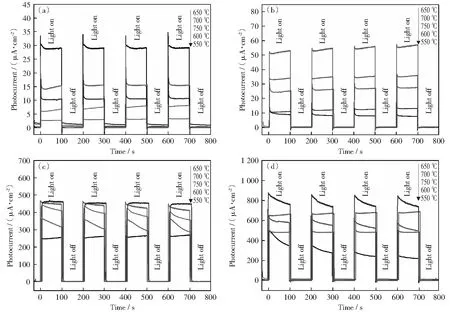
(a)、(b)为不同温度制备的C-TiO2薄膜分别对可见光和紫外光的响应;(c)、(d)为不同AgNO3浓度下制备的Ag-C-TiO2650薄膜分别对可见光和紫外光的响应图3 薄膜的瞬态光电流密度Fig.3 Transient photocurrent density of the film samples
2.4 薄膜的紫外-可见光吸收性能和荧光光谱分析
为了分析薄膜的光吸收性能,对常用的P25样品进行了对比研究。图4为P25和C-TiO2650的紫外-可见吸收光谱图,附图为样品的(αhv)2-hv关系图。通过对比图4中可知,C-TiO2650的吸收谱较P25发生红移,在可见光区C-TiO2650比P25有更强的吸收。根据Kubelka-Munk公式
α=A(hv-Eg)n/2/hv.
式中:α为吸收系数,hv是入射光光子的能量,A是和材料相关的常数,Eg为带隙,n的取值与半导体的带隙特性相关,直接带隙为1,间接带隙为4.由于TiO2为直接带隙,故此处n取值为1.计算拟合得到(αhv)2-hv关系图,然后采用曲线拐点外推法得到C-TiO2650的带隙值Eg为3.04 eV,而P25的带隙为3.25 eV[24-25].

图4 P25和C-TiO2650的紫外-可见吸收光谱,附图为样品的(αhv)2-hv关系图Fig.4 UV-vis absorption spectrum of P25 and C-TiO2650. The inset is (αhv)2-hv plot
图5是C-TiO2650与Ag-C-TiO2650样品的紫外-可见吸收光谱对比图。对比可以发现,负载Ag纳米颗粒的Ag-C-TiO2650样品在长波区域(λ>400 nm)的光吸收强度较C-TiO2650样品显著增强。这主要是由于Ag纳米颗粒的局域表面等离子共振(LSPR)造成的,当Ag纳米颗粒受到一定频率的光照后,其表面的电子受到激发和光波的电场耦合后产生共振,导致Ag纳米颗粒表面的电场增强,增加了金属Ag中电子的能量强度[26]。此外,Ag纳米颗粒与TiO2间的相互作用及Ag纳米颗粒大小分布等因素都会对光吸收特征产生影响[27-29]。

图5 C-TiO2650与Ag-C-TiO2650的紫外-可见吸收光谱Fig.5 UV-visible absorption spectrum of C-TiO2650 and Ag-C-TiO2650
利用FLS980荧光光谱仪对样品进行了荧光光谱测试,采用的激发波长为470 nm.图6为样品C-TiO2650和Ag-C-TiO2650的荧光光谱。荧光峰均为光生非平衡载流子电子-空穴对的复合所致。对比发现样品C-TiO2650的荧光峰的强度要远大于Ag-C-TiO2650,由此说明负载Ag能有效地抑制C-TiO2650光生电子-空穴对的复合,从而提高其光电响应性能。
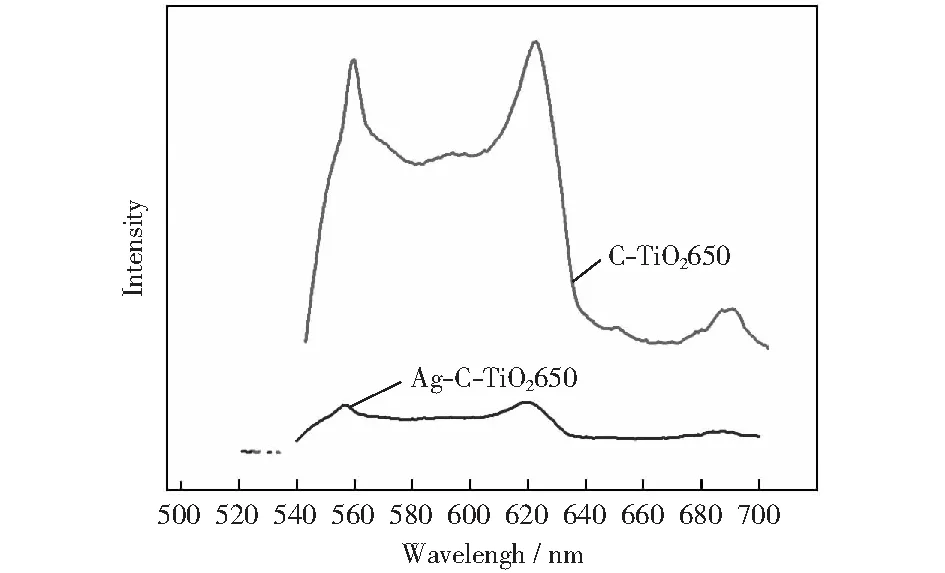
图6 样品Ag-C-TiO2650和C-TiO2650的荧光光谱Fig.6 Fluorescence spectrum of Ag-C-TiO2650 andC-TiO2650 samples
3 结论
1) 采用高温、低时长热氧化TiC的方法制备了C-TiO2薄膜。C-TiO2薄膜除了具有紫外光光电响应性能,对可见光也有显著的响应,其中C-TiO2650样品对紫外光和可见光都表现出最佳的性能。
2) 负载Ag可以显著改善C-TiO2薄膜对紫外和可见光的光电响应性能,而且AgNO3溶液的浓度会影响到所制备的Ag-C-TiO2薄膜样品的性能;在浓度为0.03 mol/L的AgNO3溶液中制备的Ag-C-TiO2薄膜样品具有最大的瞬态光电流密度。
3) C-TiO2薄膜在可见光区具有显著的光吸收,且负载Ag能有效地抑制C-TiO2薄膜光生电子-空穴对的复合,这些因素对提高薄膜的光电响应性能具有重要影响。
[1] FUJISHIMA A,HONDA K.Electrochemical photocatalysis of water at semiconductorelectrode[J].Nature,1972,238:5358.
[2] MACAK J M,TSUCHIYA H,SCHMUKI P.High-aspect-ratio TiO2nanotubes by anodization of titanium[J].Angew Chem Int Ed,2005,44(14):2100.
[3] ASAHI R,MORIKAWA T,OHWAKI T,et al.Visible-light photocatalysis in nitrogen-doped titanium oxides[J].Science,2001,293(5528):269-271.
[4] GARCIA C G,KLEVERLAAN C J,BIGNOZZI C A,et al.Time-resolved experiments in dye-sensitized solar cells using [(dcbH2)2Ru(ppy)2](ClO4)2as a nanocrystalline TiO2sensitizer[J].Journal of Photochemistry & Photobiology A Chemistry,2002,147(2):143-148.
[5] BAI A.Preparation and enhanced daylight-induced photo-catalytic activity of transparent C-doped TiO2thin films[J].Journal of Wuhan University of Technology-Mater Sci Ed,2010,25(5):738-742.
[6] ZHOU M,YU J.Preparation and enhanced daylight-induced photocatalytic activity of C,N,S-tridoped titanium dioxide powders[J].Journal of Hazardous Materials,2008,152(3):1229-1236.
[7] HIROSHI I,YUKA W,KAZUHITO H.Carbon-doped anatase TiO2powders as a visible-light sensitive photocatalyst[J].Chemistry Letters,2003,32(8):772-773.
[8] DE-EN G,YUN L, YANGB C,et al.Facile preparation of micro-mesoporous carbon-doped TiO2photocatalysts with anatase crystalline walls under template-free condition[J].Chemical Communications,2008,21(21):2453-2455.
[9] TRAN V H, GLUCHOWSKI P,LUKOWIAK A, et al.The influence of temperature, pressure and Ag doping on the physical properties of TiO2nanoceramics[J].Nanoscale,2016,8:19703-19713.
[10] XIA M,ZHANG Q,PAN P,et al.Enhanced surface photovoltaic properties of TiO2nanowiresdoped by Ag nanoparticles[J].Materials Letters,2015,160:544-546.
[11] DONG K, YU L,ZHANG Y, et al.Green synthesis of sulfur/graphene nanocomposite and photocatalytic performance[J].Science of Advanced Materials,2014,6(8):1828-1835.
[12] IHARA T,MIYOSHI M,IRIYAMA Y,et al.Visible-light-active titanium oxide photocatalyst realized by an oxygen-deficient structure and by nitrogen doping[J].Applied Catalysis B Environmental,2003,42(4):403-409.
[13] MCEVOY J G,CUI W,ZHANG Z.Degradative and disinfective properties of carbon-doped anatase-rutile TiO2,mixtures under visible light irradiation[J].Catalysis Today,2013,207(2):191-199.
[14] ZHANG L,MAN S T,TAN O K,et al.Facile fabrication and characterization of multi-type carbon-doped TiO2for visible light-activated photocatalytic mineralization of gaseous toluene[J].Journal of Materials Chemistry A,2013,1(14):4497-4507.
[15] SPURR R A,MYERS H.Quantitative analysis of anatase-rutile mixtures with an X-ray diffractometer[J].Analytical Chemistry,1957,29(5):760-762.
[16] LEWIS J P, WANG H.Second-generation photocatalytic materials: anion-doped TiO2[J].Journal of Physics Condensed Matter,2006,18(2):421-434.
[17] OHNO T,TSUBOTA T,NISHIJIMA K,et al.Degradation of methylene blue on carbonate species-doped TiO2photocatalysts under visible light[J].Chemistry Letters,2004,33(6):750-751.
[18] REN W,AI Z,JIA F,et al.Low temperature preparation and visible light photocatalyticactivity of mesoporous carbon-doped crystalline TiO2[J].Applied Catalysis B Environmental, 2007,69(3/4):138-144.
[19] PARAMASIVAM I,MACAK J M,SCHMUKI P.Photocatalytic activity of TiO2,nanotube layers loaded with Ag and Au nanoparticles[J].Electrochemistry Communications,2008,10(1):71-75.
[20] HSU S W,YANG T S,CHEN T K,et al.Ion-assisted electron-beam evaporation of carbon-doped titanium oxide films as visible-light photocatalyst[J].Thin Solid Films,2007,515(7/8):3521-3526.
[21] LIU J,CRITTENDEN J C,HAND D W,et al.Regeneration of adsorbents using heterogeneous photocatalytic oxidation[J].Journal of Environmental Engineering,1996,122(8):707-713.
[22] CHAKER H,CHÉRIF-AOUALI L,KHAOULANI S,et al.Photocatalytic degradation of methyl orange and real wastewater by silver doped mesoporous TiO2catalysts[J].Journal of Photochemistry & Photobiology A Chemistry,2015,318:142-149.
[23] MATHPAL M C,TRIPATHI A K,KUMAR P,et al.Polymorphic transformations and optical properties of graphene-based Ag-doped titania nanostructures[J].Physical Chemistry Chemical Physics,2014,16(43):23874.
[24] ZHOU N,POLAVARAPU L,GAO N,et al.TiO2coated Au/Ag nanorods with enhancedphotocatalytic activity under visible light irradiation[J].Nanoscale,2013,5(10):4236.
[25] PASCUAL J,CAMASSEL J,MATHIEU H.Fine-structure in the intrinsic absorption-edge of TiO2[J].Physical Review B,1978,18(10):5606-5614.
[26] KURIECHEN S K,MURUGESAN S.Carbon-doped titanium dioxide nanoparticles mediated photocatalytic degradation of azo dyes under visible light[J].Water,Air,& Soil Pollution,2013,224(9):1671.
[27] KIM K D,HAN D N,LEE J B,et al.Formation and characterization of Ag-deposited TiO2,nanoparticles by chemical reduction method[J].Scripta Materialia,2006,54(2):143-146.
[28] XIE K,LAN S,WANG C,et al.Photoelectrocatalytic properties of Ag nanoparticles loaded TiO2nanotube arrays prepared by pulse current deposition[J].Electrochimica Acta,2010,55(24):7211-7218.
[29] ZUO Q.Synthesis of Ag2@TiO2dimeric core-shell nanopaicles and non-resonance raman spectroscopy studies of TiO2-N719 interface[D].Xiamen:Xiamen University,2014.
