Ga-ZSM-5催化MTO生成初始烯烃反应机理研究
2018-03-23任瑞鹏
李 强,任瑞鹏
(太原理工大学 煤科学与技术教育部与山西省重点实验室,太原 030024)
乙烯和丙烯是现代化学工业的重要基础原料。目前,烯烃生产技术严重依赖石油,生产乙烯和丙烯的传统方法为轻油(石脑油、轻柴油)裂解工艺。由于石油资源的有限性和昂贵的价格,世界各国开始致力于非石油路线制乙烯和丙烯等低碳烯烃的技术开发。因此,以煤、天然气和生物气为原料制备甲醇进而生产乙烯和丙烯的替代路线,逐渐受到学术界和工业界的重视。Mobil公司于1976年在研究甲醇制汽油(methanol to gasoline, MTG)的过程中发现,烯烃是甲醇制备汽油的中间产物,通过控制反应条件可以高选择性地得到低碳烯烃,由此开始了对甲醇制烯烃(MTO)的研究[1]。而在各种不同类型的分子筛催化剂之中,ZSM-5由于其独特的孔结构,亲油疏水,热和水热稳定性高,拥有良好的催化活性和稳定性[2],不仅为择形催化提供了空间限制作用[3],而且为反应物和产物提供了丰富的进出通道,也为制备高选择性、高活性、抗积炭失活性能强的工业催化剂提供了晶体结构基础,因此它一直是催化甲醇制烯烃最主要的催化剂之一。
ZSM-5分子筛由于酸性太强、生成的烯烃选择性较低[4]、易积碳失活的缺点[5],需要对其进行合理的改性,因此,深入了解MTO催化反应机理显得尤为重要。然而,在MTO转化过程中,由于极其复杂的反应网络,尤其是产物分布的复杂性和反应中间体识别的困难性,使得对其反应机理的基础性研究非常具有挑战性[6-7]。尽管在过去的40年中进行了大量的实验和理论计算,MTO反应机理仍然是一个有争论的焦点[8-9]。MTO反应机理中的关键是C—C键如何从甲醇等Cl物种生成[10-11],到目前为止,已提出超过20种不同的反应机理。根据反应路线中所涉及到的中间体种类,可以将MTO反应机理分为直接反应机理和间接反应机理。其中,直接反应机理是指烯烃由C1物种直接耦合反应得到,反应中涉及到的C1物种可能包括氧鎓离子、碳正离子、卡宾和自由基等;间接反应机理(即烃池机理)是指甲醇首先和分子筛中已经存在的有机活性中心反应得到环状化合物中间体,然后通过消除反应得到乙烯和丙烯等烯烃产物。目前,越来越多的实验和理论结果表明,直接反应机理不大可能是MTO的反应机理[12-13],而烃池机理获得了越来越多的认可[10-14]。但是,烃池机理并不能合理地解释第一个C—C键及初始烯烃的生成。
先前的研究表明,Ga同晶替代ZSM-5分子筛的酸性低于Al同晶替代ZSM-5分子筛的酸性[15],可以减少烷基化反应中副产物的生成[16],提高目标产物的选择性。到目前为止,对分子筛上骨架镓酸中心的酸催化MTO反应机理的理论研究报道较少。因此,在本工作研究中,采用DFT研究方法,利用Ga同晶替代ZSM-5分子筛作为催化剂,对MTO反应过程中第一个C—C键及初始烯烃的生成做了全面系统的理论研究。此外,深入理解甲醇制烯烃反应机理,对开发高效催化剂、优化反应工艺以及提高烯烃选择性具有重要意义。
1 模型的选取和计算方法
1.1 模型的选取
ZSM-5分子筛的单个晶胞含有96个T位(正四面体中心),其中包含有12种独特的拓扑T位。其中位于竖直孔道和正弦孔道交叉处的T12位易被铝、镓替代[17-18]。此外,研究表明,周期性模型可以合理地描述空间限制作用和沸石框架的静电稳定作用,尤其是氧鎓离子和框架之间的相互作用[19-20]。因此,本工作中选取了周期性模型和T12位,如图1所示。
本工作中所使用的模型为全硅型ZSM-5分子筛(O192Si96)中一个Si原子被Ga原子取代后的模型,其中包含一个Brnsted酸位,优化后的晶格常数分别为:a=2.007 8 nm,b=2.007 8 nm,c=1.336 0 nm;α=β=γ=90°.

图1 Ga-ZSM-5周期性模型Fig.1 Ga-ZSM-5 modeled using the periodic model
1.2 计算方法
本文中的所有计算都是通过VASP(Vienna abinitio simulation package)[21]完成的。采用缀加投影波函数(PAW)方法来描述电子-离子的相互作用(electron-ion interactions)[22]1759,交换相关能采用广义梯度函数(GGA)PBE[22]1770进行计算,紧束缚芯电子采用PAW-GGA赝势进行描述。所有计算中平面波截断能(plane-wave basis cutoff energy)和布里渊区k点分别设置为400 eV和1×1×1.在结构优化和能量计算过程中,能量收敛标准为9.62×10-4kJ/mol,力收敛标准小于0.30 eV/nm,计算误差范围±0.01 eV,采用cNEB方法搜寻过渡态[23-24],通过振动频率分析得到唯一的虚频来确定过渡态。
对于吸附质A在催化剂分子筛表面的吸附能Eads,计算公式:
Eads=E(A/model)-E(A)-E(model) .
式中:E(A)、E(model)和E(A/model)分别表示自由态分子A、分子筛、A在分子筛中稳定吸附构型的能量。
对于反应A+B→C+D,计算反应能垒和反应热公式:
Ea=E(TS/model)-E[(A+B)/model] ,ΔE=E(C/model)+E(D/model)-E(A/model)-E(B/model) .
式中:E(x/model)(x=A,B,C,D)、E[(A+B)/model]和E(TS/model)分别表示单个物种与分子筛、反应物、过渡态的能量。
2 结果与讨论
2.1 二甲醚的生成
在甲醇转化的过程中,Brønsted酸催化甲醇脱水制二甲醚是MTO反应的第一步[1,25-26]。通过红外(IR)光谱和核磁共振(NMR)光谱可以直接观察到分子筛中酸性OH基团的存在[27-28]。在MTO反应过程中,甲醇转化存在两种不同的反应机理。第一种是分步机理,即二甲醚的生成是通过甲氧基中间体完成;第二种是协同机理,即两个甲醇分子直接反应生成二甲醚。
分步机理涉及两个不同的反应。首先是单个甲醇分子在Brønsted酸位上的吸附,其吸附能为-73.32 kJ/mol,这与文献[29-30]报道的-64.00~-83.00 kJ/mol相符。然后,吸附的甲醇分子经TS1-1与Brønsted酸反应脱水,生成的甲基基团紧附于沸石框架上的桥位氧原子上形成甲氧基,同时生成的水分子吸附于沸石催化剂表面。这个反应的活化能垒和反应热分别132.18,41.49 kJ/mol,通过振动频率分析得到的虚频为187.29 cm-1.吸附的水分子可以从催化剂表面脱附,脱附能为33.77 kJ/mol,而甲氧基可进一步与另外一个甲醇分子反应。随后另外一个甲醇分子经过甲氧基活化并反应,经TS1-2生成二甲醚分子,与此同时,Brønsted酸重新生成。这个甲醇分子在甲氧基上的吸附能为-25.08 kJ/mol,几乎是甲醇分子在Brønsted酸位上吸附能的三分之一,证实了其与甲氧基之间比较弱的相互作用。这个反应的活化能垒为138.93 kJ/mol,与先前研究报道[31-32]数据相符,该反应的反应热为-19.30 kJ/mol,通过振动频率分析得到的虚频为331.66 cm-1.
另一方面,协同机理涉及两个甲醇分子与Brønsted酸反应,经过TS1-3生成二甲醚和水;反应活化能垒为94.55 kJ/mol,反应热为80.08 kJ/mol,通过振动频率分析得到的虚频为284.04 cm-1.
综上所述,关于甲醇反应生成二甲醚的反应机理,协同机理比分步机理更占优势,因其活化能垒低于分步机理的活化能垒,此结论与先前研究报道[32-33]相符。以上所涉及反应的过渡态几何结构如图2所示。

图2 二甲醚生成过程中所涉及的过渡态几何结构(单位:nm)Fig.2 Optimized structures of the transition states in the formation of dimethyl ether
2.2 甲氧基的生成
研究甲醇在完全煅烧的SAPO-34上的吸附过程发现,甲氧基是第一个形成的中间体物种,其对水、甲醇和苯胺这些探针分子具有反应活性[1,25-26]。然而,先前的实验研究[34] 279表明,化学吸附形式的二甲醚不能够直接转化为甲氧基,大部分的二甲醚随着扩散和温度的升高而脱附,因为其吸附能低于甲醇的吸附能。在本工作研究中,二甲醚分子在Brønsted酸位的吸附能为-53.06 kJ/mol.
先前的理论研究[34] 280表明,甲氧基的生成是通过三甲基氧鎓离子(TMO)的分解来实现的,而TMO是通过两个二甲醚分子与Brønsted酸反应生成的。两个二甲醚分子与Brønsted酸反应,经过TS2-1,生成TMO和一分子甲醇。其活化能垒为68.50 kJ/mol,反应热-6.75 kJ/mol,通过振动频率分析得到的虚频为356.26 cm-1.生成的甲醇可以脱附,其脱附能为13.51 kJ/mol.随后,TMO经过TS2-2分解,生成甲氧基和二甲醚分子。该反应活化能垒为82.01 kJ/mol,反应热为26.05 kJ/mol,通过振动频率分析得到的虚频为145.00 cm-1.
与此形成鲜明对比的是,单个二甲醚分子与Brønsted酸通过TS2-3也可以生成甲氧基,其反应热为19.30 kJ/mol,活化能垒为235.41 kJ/mol,通过振动频率分析得到的虚频为337.67 cm-1.该反应能垒太高,与经过TMO分解而生成甲氧基的反应相比,可以认为此反应不可能发生。以上所涉及反应的过渡态几何结构如图3所示。
2.3 第一个C—C键的生成

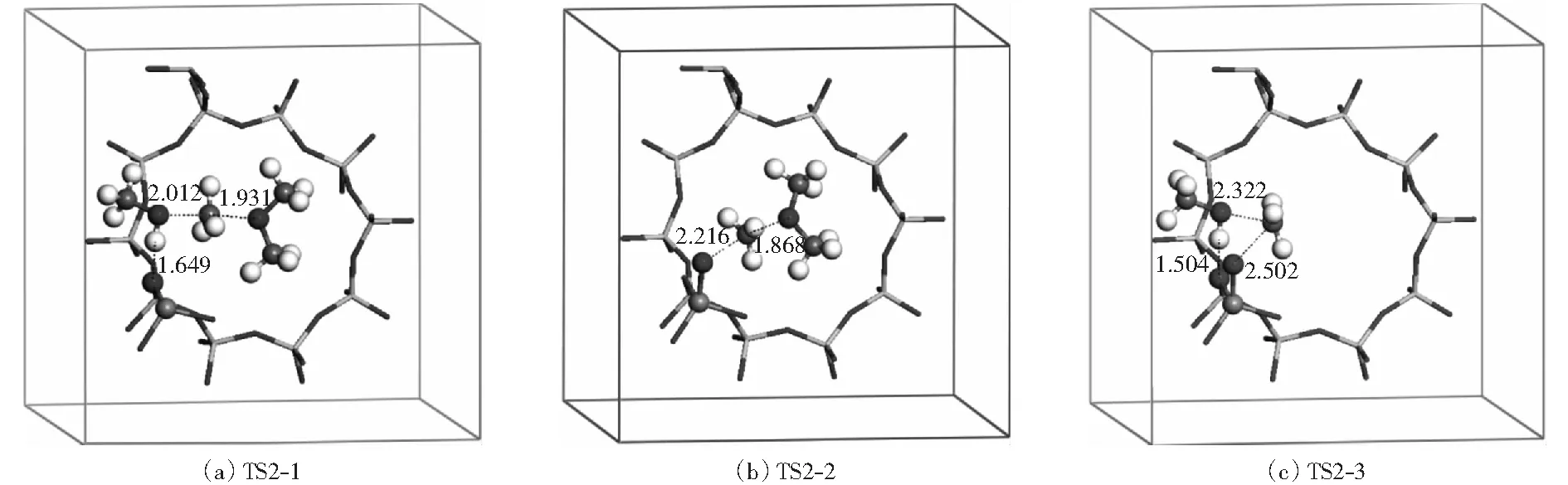
图3 甲氧基生成过程中所涉及的过渡态几何结构(单位:nm)Fig.3 Optimized structures of the transition states in the formation of methoxy species

1-ZOCH3+DME+DME(g);2-ZO-+CH3OCH2++CH4+DME(g);3-ZO-+CH3OCH2++DME+CH4(g);4-ZOH+CH3OCH2CH2OCH3+CH4(g)图4 第一个C—C键的生成的势能曲线Fig.4 Potential energy profile of the main route for the the formation of the first C—C bond
经过CH4的脱附与DME的吸附,并伴随有空间位置的调整,放出能量-118.67 kJ/mol,经过TS3-2生成1,2-二甲氧基乙烷,为第一个包含C—C键的物种,其活化能垒为108.06 kJ/mol,反应热为-153.40 kJ/mol,通过振动频率分析得到的虚频为1 007.40 cm-1.以上所涉及反应的过渡态几何结构如图5所示。
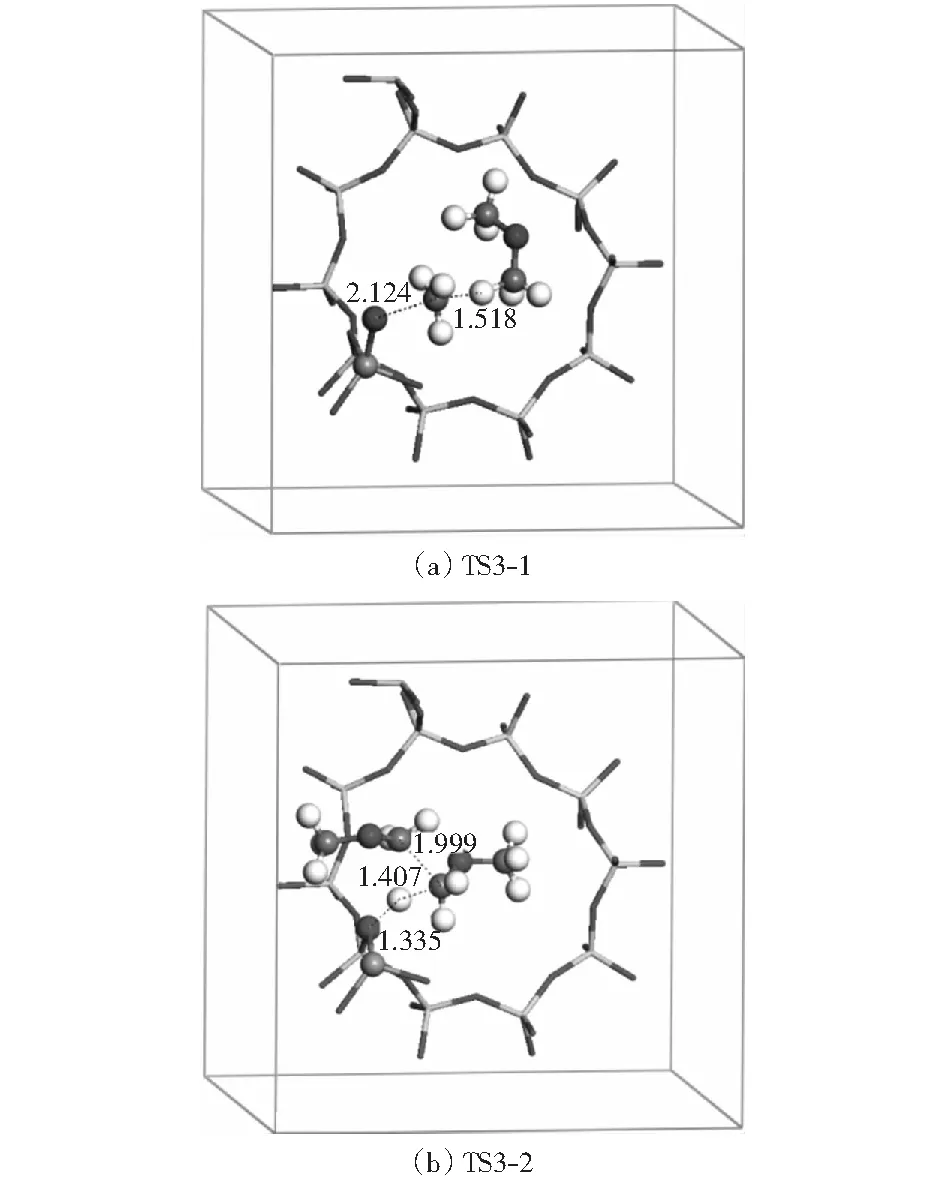
图5 第一个C—C键生成过程中所涉及的过渡态几何结构(单位:nm)Fig.5 Optimized structures of the transition states in the formation of the first C—C bond
2.4 初始烯烃的生成


1-ZOCH3+CH3OCH2CH2OCH3+3DME(g); 2-ZO-+CH3O+(CH3)CH2CH2OCH3+3DME(g); 3-ZOCH2CH2OCH3+DME+3DME(g); 4-ZO-+CH3OCH2++CH3CH2OCH3+3DME(g); 5-ZO-+CH3OCH2++DME+CH3CH2OCH3(g)+2DME(g); 6-ZOH+2DME+CH3OCH2CH2OCH3(g)+CH3CH2OCH3(g); 7-ZO-+TMO+CH3OH(g)+CH3OCH2CH2OCH3(g)+CH3CH2OCH3(g); 8-ZOCH3+CH3CH2OCH3+CH3OCH2CH2OCH3(g)+DME(g)+CH3OH(g); 9-ZO-+CH3O+(CH3)CH2CH3+CH3OCH2CH2OCH3(g)+DME(g)+CH3OH(g); 10-ZOCH2CH3+DME+CH3OCH2CH2OCH3(g)+DME(g)+CH3OH(g); 11-ZOCH2CH3+CH3OCH2CH2OCH3(g)+2DME(g)+CH3OH(g); 12-ZOH+CH2CH2+CH3OCH2CH2OCH3(g)+2DME(g)+CH3OH(g)图6 乙烯生成的势能曲线Fig.6 Potential energy profile of the main route for the formation of ethene

图7 乙烯生成过程中所涉及的过渡态几何结构(单位:nm)Fig.7 Optimized structures of the transition states in the formation of ethene
3 结论
本工作采用ZSM-5分子筛作为催化剂,构建周期性模型,以T12位为Ga的同晶取代活性位,在B3LYP/6-311G(d,p)水平上对所有中间体进行了优化。通过计算分析,得到了以下重要的结论:
1) 二甲醚的生成存在两种不同的反应机理。第一种是分步机理,即二甲醚的生成是通过甲氧基中间体完成的;第二种是协同机理,即两个甲醇分子在Brønsted酸催化下直接反应生成二甲醚。计算结果表明,协同机理比分步机理更有优势。
2) 两个二甲醚分子与Brønsted酸反应生成三甲基氧鎓离子(TMO),随后经过其分解产生甲氧基(CH3O-).

4) 1,2-二甲氧基乙烷经过一系列氧鎓离子和醚的生成及反应,最终生成了初始烯烃乙烯,随后诱导HCP机理的发生。
[1] STÖCKER M.Methanol-to-hydrocarbons:catalytic materials and their behavior[J].Microporous & Mesoporous Materials,1999,29(1/2):3-48.
[2] SEMELSBERGER T A,OTT K C,BORUP R L,et al.Generating hydrogen-rich fuel-cell feeds from dimethyl ether (DME) using Cu/Zn supported on various solid-acid substrates[J].Applied Catalysis A General,2006,309(2):210-223.
[3] HAN B,CHU Y Y,ZHENG A M,et al.Adsorption structure and energy of pyridine confined inside zeolite pores[J].Acta Physico-Chimica Sinica,2012,28(2):315-323.
[4] OLAH G A.Beyond oil and gas:the methanol economy[J].Angewandte Chemie International Edition,2005,44(18):2636-2639.
[5] LANGNER B E.Coke formation and deactivation of the catalyst in the reaction of propylene on calcined NaNH4-Y[J].Ind Eng Chem Process Des Dev,1981,20(2):326-331.
[6] ILIAS S,BHAN A.Mechanism of the catalytic conversion of methanol to hydrocarbons[J].ACS Catalysis,2013,3(1):18-31.
[7] KAREN H,JEROEN V D M,KRISTOF D W,et al.Unraveling the reaction mechanisms governing methanol-to-olefins catalysis by theory and experiment[J].Chem Phys Chem,2013,14(8):1526-1545.
[8] ERICHSEN M W,SVELLE S,OLSBYE U.H-SAPO-5 as methanol-to-olefins (MTO) model catalyst:towards elucidating the effects of acid strength[J].Journal of Catalysis,2013,298(2):94-101.
[9] WANG X,DAI W,WU G,et al.Verifying the dominant catalytic cycle of the methanol-to-hydrocarbon conversion over SAPO-41[J].Catalysis Science & Technology,2014,4(3):688-696.
[10] SVELLE S,OLSBYE U,JOENSEN F,et al.Conversion of methanol to alkenes over medium- and large-pore acidic zeolites:steric manipulation of the reaction intermediates governs the ethene/propene product selectivity[J].Journal of Physical Chemistry C,2007,111(49):151-157.
[11] HEREIJGERS B P C,BLEKEN F,NILSEN M H,et al.Product shape selectivity dominates the methanol-to-olefins (MTO) reaction over H-SAPO-34 catalysts[J].Journal of Catalysis,2009,264(1):77-87.
[12] CLARKE J K A,DARCY R,HEGARTY B F,et al.Free radicals in dimethyl ether on H-ZSM-5 zeolite:a novel dimension of heterogeneous catalysis[J].Journal of the Chemical Society Chemical Communications,1986,5(5):425-426.
[13] MARCUS D M,MCLACHLAN K A,WILDMAN M A,et al.Experimental evidence from H/D exchange studies for the failure of direct C—C coupling mechanisms in the methanol-to-olefin process catalyzed by HSAPO-34[J].Angewandte Chemie International Edition,2006,45(19):3133-3136.
[14] BJØRGEN M,SVELLE S,JOENSEN F,et al.Conversion of methanol to hydrocarbons over zeolite H-ZSM-5:on the origin of the olefinic species[J].Journal of Catalysis,2007,249(2):195-207.
[15] YUAN S P,WANG J G,LI Y W,et al.Siting of B, Al, Ga or Zn and bridging hydroxyl groups in mordenite:an ab initio study[J].Journal of Molecular Catalysis A Chemical,2001,175(1):131-138.
[16] 李永昕,何学艺,柳娜,等.HZSM-5分子筛催化苯与碳酸二乙酯烷基化合成乙苯[J].石油化工,2009,38(6):608-612.
LI Y X,HE X Y,LIU N,et al.Synthesis of ethylbenzene by alkylation of technology,2009,38(6):608-612.
[17] DEROUANE E G,FRIPIAT J G.Quantum mechanical calculations on molecular sieves:properties of the Si—O—T(T=Si,Al,B) bridge in zeolites[J].Journal of Physical Chemistry,1987,91(1):145-148.
[18] CHATTERJEE A,VETRIVEL R.Electronic and structural properties of aluminum in the ZSM-5 framework[J].Microporous Materials,1994,3(3):211-218.
[19] WANG S,WEI Z,CHEN Y,et al.Methanol to olefins over H-MCM-22 zeolite:theoretical study on the catalytic roles of various pores[J].ACS Catalysis,2015, 5(2):1131-1144.
[20] LIU J,LIU Z F,FENG G,et al.Dimerization of propene catalyzed by brønsted acid sites inside the main channel of zeolite SAPO-5:a computational study[J].Journal of Physical Chemistry C,2014,118(32):18496-18504.
[21] KRESSE G,FURTHMÜLLER J.Efficiency of ab-initio total energy calculations for metals and semiconductors using a plane-wave basis set[J].Computational Materials Science,1996,6(1):15-50.
[22] KRESSE G,JOUBERY D.From ultrasoft pseudopotentials to the projector augmented-wave method[J].Physical Review B Condensed Matter,1999,59(3):1758-1775.
[23] HENKELMAN G,UBERUAGE B R,JNSSON H.A climbing image nudged elastic band method for finding saddle points and minimum energy paths[J].Journal of Chemical Physics,2000, 113(22):9901-9904.
[25] WANG W,HUNGER M.Reactivity of surface alkoxy species on acidic zeolite catalysts[J].Chem Inform,2008,41(48):895-904.
[26] WANG W,JIANG Y,HUNGER M.Mechanistic investigations of the methanol-to-olefin (MTO) process on acidic zeolite catalysts by in situ solid-state NMR spectroscopy[J].Catalysis Today,2006,113(1/2):102-114.
[27] WANG W,BUCHHIOLZ A,SEILER M,et al.Evidence for an initiation of the methanol-to-olefin process by reactive surface methoxy groups on acidic zeolite catalysts[J].Journal of the American Chemical Society,2003,125(49):15260-15267.
[28] HUO H,PENG L,GAN Z,et al.Solid-state MAS NMR studies of Brønsted acid sites in zeolite H-Mordenite[J].Journal of the American Chemical Society,2012, 134(23):9708-9720.
[29] VETRIVEL R,CATLOW C R A,COLBOURN E A.Structure and dissociation mechanisms of methanol in ZSM-5 zeolite[J].Journal of Physical Chemistry,2002, 93(11):4594-4598.
[30] SHAH R,GALE J D,PAYNE M C.Methanol adsorption in zeolites:a first-principles study[J].Journal of Physical Chemistry,1996,100(28):11688-11697.
[31] TAJIMA N,TSUNEDA T,TOYAMA F,et al.A new mechanism for the first carbon-carbon bond formation in the MTG process:a theoretical study[J].Chem Inform,1998,29(48):8222-8229.
[32] LESTHAEGHE D,VAN S V,MARIN G B,et al.Understanding the failure of direct C—C coupling in the zeolite-catalyzed methanol-to-olefin process[J].Angewandte Chemie,2006,45(11):1714-1719.
[33] BLASZKOWSKI S R,SANTEN R A V.Theoretical study of the mechanism of surface methoxy and dimethyl ether formation from methanol catalyzed by zeolitic protons[J].Journal of Physical Chemistry B,1997,101(13):2292-2305.
[34] LI J,WEI Z,CHEN Y,et al.A route to form initial hydrocarbon pool species in methanol conversion to olefins over zeolites[J].Journal of Catalysis,2014,317(317):277-283.
[35] YAMAZAKI H,SHIMA H,IMAI H,et al.Direct production of propene from methoxy species and dimethyl ether over H-ZSM-5[J].Journal of Physical Chemistry C,2012,116(45):24091-24097.
