右美托咪定对颅脑损伤患者术后镇痛效果的影响
2018-03-20王庆辉姜万维
王庆辉,姜万维
(大连大学附属中山医院 麻醉二部,辽宁 大连 116001)
颅脑损伤手术患者常因术后心率、血压剧烈波动而躁动不安,加重继发性脑缺血缺氧,甚至危及患者生命[1]。临床上该类患者应适当给予镇静治疗,有助于减轻气管导管、机械通气等刺激所致应激反应,也可减少患者术后疼痛,避免发生意外[2]。故镇痛、镇静治疗已成为颅脑损伤患者治疗的重要组成部分,也是非常必要的治疗措施[3]。右美托咪定2009年6月在我国正式上市,已广泛应用于术后镇静镇痛治疗。本研究选择2016年1—12月大连大学附属中山医院收治的60例颅脑损伤患者,对其中30例给予静脉泵注右美托咪定治疗,以观察右美托咪定对该类患者术后血流动力学及镇痛镇静的影响。
1 资料与方法
1.1 一般资料
选择2016年1—12月大连大学附属中山医院收治的60例颅脑损伤患者,均为重症监护病房(ICU)收入的急性颅脑创伤患者,均经CT或MRI等影像学检查确诊,入院时间1~8 h;其中男34例,女26例;年龄21~57岁,平均(35.0±4.6)岁;体重51~89 kg,平均(58.1±6.8)kg;格拉斯哥(GCS)评分7~13分,收缩压(SBP)>100 mmHg,中心静脉压(CVP)>8 mmHg,心率(HR)>60次/min。将患者以随机数字表法分成对照组与观察组,两组的一般临床资料差异无统计学意义(P>0.05),具有可比性。见表1。本研究经我院医学伦理委员会批准且患者家属均签署相关知情同意书。
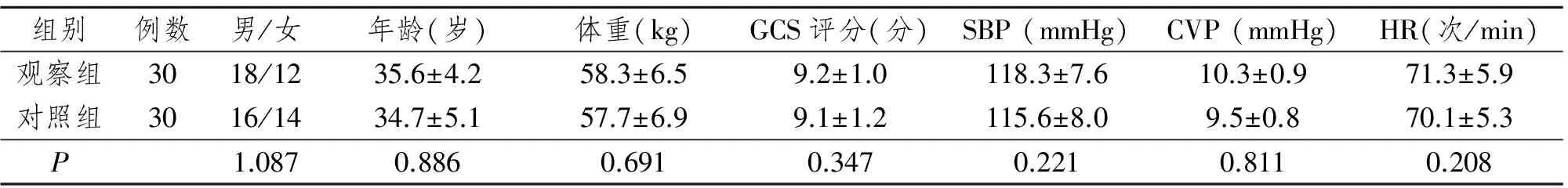
表1 两组一般资料比较
1.2 麻醉方法
入手术室后实施患者常规监护,连接脑电双频指数(BIS)监护仪并进行记录BIS。建立静脉通道给予乳酸钠林格注射液。对照组进行常规麻醉措施,观察组在对照组基础上,于麻醉诱导前静脉泵入右美托咪定1 μg/kg,10 min泵入预定剂量后改为0.5 μg/(kg·h)静脉持续泵入,直至术后24 h。诱导麻醉:面罩吸氧,对照组、观察组分别以5 ng/mL、4 ng/mL靶控输注瑞芬太尼(20 μg/mL),1 min后当瑞芬太尼达到预设的血药浓度,依次静脉注射咪达唑仑(0.1 mg/kg)、丙泊酚(2 mg/kg)、顺式阿曲库铵(0.2 mg/kg),同时去氮给氧3 min,再经口快速气管插管连接Drager麻醉机行机械通气,参数设定:潮气量8~10 mL/kg、氧流量2 L/min、呼吸频率12次/min、吸呼比1∶2、呼气末二氧化碳分压35~40 mmHg(1 mmHg=0.133kPa)。麻醉维持:靶控输注丙泊酚(2~3 ng/mL),术中依据BIS调整血药浓度维持BIS值40~60,同时间断静脉注射阿曲库铵(0.25 mg/kg)。术中如平均动脉压下降超过基础值30%时,静脉注射麻黄碱(6 mg);如平均动脉压上升超过基础值30%时,根据具体情况加大丙泊酚或(和)瑞芬太尼剂量;如心率<50次/min静脉注射阿托品(0.5 mg);如心率>100次/min时则静脉注射(0.5~1.0)mg/kg的艾司洛尔。手术结束前30 min停用阿曲库铵,缝皮结束时停用所有麻醉药;手术结束后待患者清醒拔除气管导管送回病房,术后均给予舒芬太尼进行静脉自控镇痛(PCIA),其中对照组给予舒芬太尼2 μg/kg和盐酸雷莫司琼0.3 mg,观察组给予舒芬太尼2 μg/kg、右美托咪定200 μg和盐酸雷莫司琼0.3 mg,以上两组药物均溶于生理盐水100 mL。PCIA的给药模式为负荷量+背景剂量+PCA模式,即首次负荷量1.5 mL,随后以1.5 mL/h匀速注入,镇痛不满意时,患者可自行按压PCA键给药,按压1次的药量为1.0 mL,锁定时间为15 min,每个患者使用镇痛泵持续镇痛24 h。
1.3 检测指标
(1)记录患者术后2 h(T1)、4 h(T2)、8 h(T3)、12 h(T4)、24 h(T5)5个时点的HR、MAP变化,记录各时刻RSS镇静评分,疼痛VAS评分和PCIA舒芬太尼的总用量;(2)记录两组术后患者PCIA的有效按压次数;(3)记录药物不良反应发生情况。
1.4 统计学方法
应用SPSS20.0软件进行数据统计分析,正态分布的计量资料以均数±标准差表示,组间比较采用t检验;计数资料以百分率表示,组间比较采用χ2检验;P<0.05为差异有统计学意义。
2 结 果
2.1 术后各时间点HR和MAP比较
观察组在T1-T4各时点的HR和MAP均明显低于对照组,差异均有统计学意义(P<0.05)。见表2。
表2两组患者术后各时点HR、MAP比较
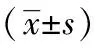
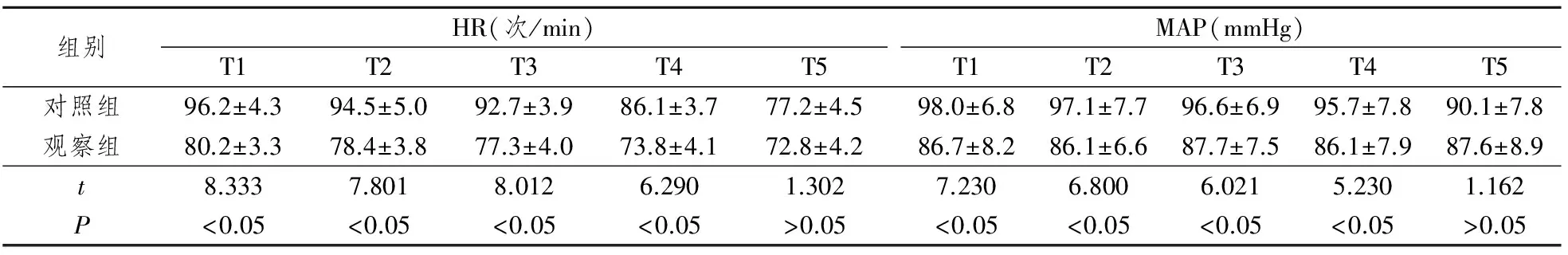
组别HR(次/min)T1T2T3T4T5MAP(mmHg)T1T2T3T4T5对照组96.2±4.394.5±5.092.7±3.986.1±3.777.2±4.598.0±6.897.1±7.796.6±6.995.7±7.890.1±7.8观察组80.2±3.378.4±3.877.3±4.073.8±4.172.8±4.286.7±8.286.1±6.687.7±7.586.1±7.987.6±8.9t8.3337.8018.0126.2901.3027.2306.8006.0215.2301.162P<0.05<0.05<0.05<0.05>0.05<0.05<0.05<0.05<0.05>0.05
2.2 术后VAS和RSS评分比较
观察组T1-T5各时点的VAS评分均明显低于对照组,差异均有统计学意义(P<0.05);在T1时刻,RSS镇静评分两组间差异有统计学意义(P<0.05)。见表3。
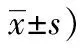
表3 两组患者各时点 VAS和RSS 评分比较
1)与对照组比较,P<0.05
2.3 两组术后PCIA有效按压次数比较
在T1、T2和T3时刻两组有效按压次数差异有统计学意义,P<0.05。见表4。
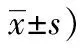
表4 两组术后PCIA有效按压次数比较
1)与对照组比较,P<0.05
2.4 两组术后PCIA舒芬太尼用量比较
观察组在T1、T2时累计舒芬太尼用量均明显少于对照组,差异有统计学意义(P<0.05)。T3、T4、T5(24 h总用量)时累计舒芬太尼用量与对照组无明显差异(P>0.05)。见表5。
表5两组术后PCIA舒芬太尼用量比较
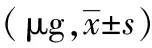
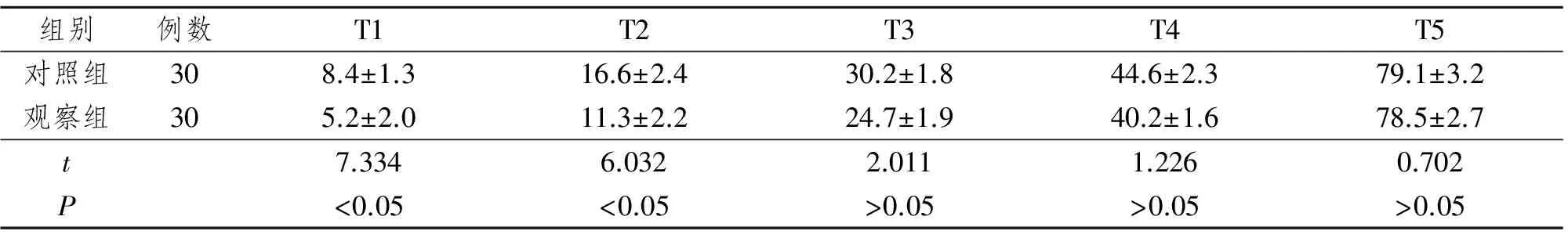
组别例数T1T2T3T4T5对照组308.4±1.316.6±2.430.2±1.844.6±2.379.1±3.2观察组305.2±2.011.3±2.224.7±1.940.2±1.678.5±2.7t7.3346.0322.0111.2260.702P<0.05<0.05>0.05>0.05>0.05
2.5 两组术后不良反应发生情况比较
观察组呕吐、恶心发生率明显少于对照组,差异有统计学意义(P<0.05)。见表6。

表6 两组术后不良反应发生情况比较
心动过缓为心率<60次/min
3 讨 论
右美托咪定是1999年美国食品药品管理局(FDA)批准用于成年人ICU短时间(<24 h)的镇静镇痛类药物。右美托咪定作为α2肾上腺素受体激动剂,其药理机制为直接作用于蓝斑区中的α2肾上腺素受体,抑制神经元放电,而使患者产生剂量依赖性的催眠作用或镇静的效应,具有无呼吸抑制的优势,同时其还具有止涎、利尿、抗寒战等作用,其镇痛作用后来才被发现[5-6]。
临床中多数患者在围术期因自身忧虑、恐惧等情绪及麻醉与手术所致的应激反应,会导致的交感神经兴奋,而出现心率增快、血压升高等症状。右美托咪定直接作用于蓝斑区中的α2肾上腺素受体,抑制机体内的去甲肾上腺激素释放以及抑制脊髓背角、小脑中去甲肾上腺素的作用而产生镇静作用[7];可有效抑制交感神经的过度兴奋,提高患者围术期血流动力学稳定性并防止心肌缺血,加之无呼吸抑制作用,尤其适合缺血性心脏病、高血压、高度紧张所致心动过速、ICU机械通气的镇静、神经功能定位的手术等[8-9]。另外有报道证实右美托咪定还可通过介入和导向机体内脊髓背角中α-2A、α-2C受体作用,而抑制脊髓中间神经元的超极化以及机体内伤害性感受器的活动而实现镇静作用[10]。右美托咪定所产生镇痛作用是因其抑制中枢系统与外周组织中的α2肾上腺素受体作用,与其他镇痛药联用可发挥很好的协同作用。本研究结果提示,观察组T1-T5各时点的VAS评分明显低于对照组,差异均有统计学意义(P<0.05),与文献报道结果相符。
有研究结果证实,α2肾上腺素受体激动剂能引发并维持自然非眼动睡眠,一定的剂量范围内机体唤醒功能仍存在,即右美托咪定对患者产生镇静效应具有可唤醒性,这是相比其他药物的优势[11]。右美托咪定还可降低机体中枢交感神经的活动,使机体内炎性细胞因子产生大大降低,在加强局麻药作用的同时可减少患者术后镇痛药物用量,其有效的抗炎作用可解释其镇痛效应[12-13]。除此之外右美托咪定还可降低围术期机体的应激反应导致神经内分泌反应,有效降低患者发生寒战症状,进而降低围术期可能导致患者发生心肌缺血风险[14-16]。Tsaousi 等[17]研究结果证实右美托咪定可减少阿片类镇痛药物用量。麻醉中同时应用瑞芬太尼、阿片类药物会导致患者出现剂量依赖性的呼吸抑制,而右美托咪定能有效降低瑞芬太尼用量,也降低呼吸抑制及痛觉超敏的概率[18]。本研究结果显示,对照组术后PCIA舒芬太尼在2 h、4 h时间点用量明显多于观察组,差异有统计学意义(P<0.05),与上述结果相符,说明联合应用右美托咪定也可以减少术后PCIA舒芬太尼的用量。术后患者存在的疼痛可导致恶心、呕吐等并发症,而恶心、呕吐可让患者存在不等程度的不适感,严重时可影响水和电解质的代谢、手术切口裂开、形成切口疝、误吸及吸入性肺炎,不利于手术患者术后的康复[19]。本研究两组患者术后总呕吐、恶心发生率较低,但观察组术后呕吐、恶心的发生率(0、6.7%)较对照组(30%、40%)更低,两组比较差异有统计学意义(P<0.05)。
低血压和心动过缓均为右美托咪定在临床应用中可能带来的负面效应,但绝大多数临床试验已证实,连续输注右美托咪定过程中,患者的心率、血压下降均不明显,都是在临床可控范围内,经一般性治疗即可恢复,患者心律不齐、小幅度血压变化也能在停药后逐渐恢复[20-21]。本研究结果也发现观察组患者T1-T4的HR、MAP要较对照组有所下降,但并没有发生心动过缓及镇静过度的情况,可见本研究中观察组应用小剂量右美托咪定能发挥较好的镇静作用、维持稳定的血流动力学,而没有发生过度镇静的现象。
综上所述,颅脑损伤患者围术期应用右美托咪定,在发挥有效镇痛镇静作用外可维持患者血流动力学的稳定,并降低术后舒芬太尼的使用量,同时还能降低呕吐、恶心发生率。但在临床应用中应警惕其可能出现的心动过缓、过度镇静等不良反应。
[1] 高进喜,王守森. 颅脑损伤预后早期预测模型的研究进展[J].中华神经外科杂志,2016,32(2):204-206.
[2] 闫诺,杨程. 目标导向液体治疗对颅脑损伤急诊开颅患者预后的影响[J]. 中华创伤杂志,2016,32(10):893-897.
[3] 牟林,乔鲁军,田勇刚,等. 右美托咪啶和脑电双频指数用于重症监护病房机械通气老年患者的镇静作用 [J]. 中国老年学杂志,2016,36(2):390-392.
[4] 吕云落,张媛,尹加林,等.右美托咪定复合小剂量氯胺酮在困难气道纤维支气管镜插管中镇静遗忘的效果[J].临床麻醉学杂志,2016,32(7):657-660.
[5] 高毅,冷玉芳,葛亮,等.腹腔注射右美托咪啶对神经病理性疼痛大鼠镇痛的实验研究[J].中国疼痛医学杂志,2015,21(8):575-580.
[6] 李建玉,杨秀环,董文芳,等.右美托咪定对瑞芬太尼持续输注下腹腔镜胆囊切除术患者机械痛觉阈值的影响[J]. 实用医学杂志,2015,31(21):3574-3577.
[7] Pajoumand M, Kufera JA, Bonds BW, et al. dexmedetomidine as an adjunct for sedation in patients with traumatic brain injury[J].J Trauma Acute Care Surg,2016,81(2):345-351.
[8] 王平,徐晖. 右美托咪定的药物相互作用[J].国际麻醉学与复苏杂志,2016,37(6):551-554.
[9] Ren X, Ma H, Zuo Z. dexmedetomidine Postconditioning Reduces Brain Injury after Brain Hypoxia-Ischemia in Neonatal Rats[J].J Neuroimmune Pharmacol, 2016,11(2):238-247.
[10] 王昆,李成文,卫宏图,等.右美托咪定混合舒芬太尼自控静脉镇痛对脊柱手术后患者睡眠质量的影响[J]. 中华麻醉学杂志,2015,35(10):1224-1227.
[11] 陈淼,韩雪萍,尚学栋,等. 右美托咪定对颈内动脉球囊闭塞试验患者术中唤醒试验质量的影响[J]. 中华麻醉学杂志,2017,37(5):601-605.
[12] Bishnoi V, Kumar B, Bhagat H, et al.Comparison of dexmedetomidine Versus Midazolam-Fentanyl Combination for Monitored Anesthesia Care During Burr-Hole Surgery for Chronic Subdural Hematoma[J].J Neurosurg Anesthesiol,2016,28(2):141-146.
[13] 王梅芳,濮建峰,黄迅.右美托咪定对老年胃癌根治术全麻诱导期及恢复期心血管反应的影响[J]. 实用临床医药杂志,2015,19(21):160-161.
[14] 于涛,黄英姿,郭凤梅,等.异丙酚和右美托咪定镇静对重症患者并发急性循环衰竭时容量反应性的影响[J].中华麻醉学杂志,2015,35(5):593-597.
[15] 马敏,李冬梅. 右美托咪定在临床应用中的研究进展[J]. 实用药物与临床,2016,19(5):644-647.
[16] Jiang L, Hu M, Lu Y, et al.The protective effects of dexmedetomidine on ischemic brain injury: A meta-analysis[J].J Clin Anesth,2017,40(1):25-32.
[17] Tsaousi GG, Lamperti M, Bilotta F. Role of dexmedetomidine for Sedation in Neurocritical Care Patients: A Qualitative Systematic Review and Meta-analysis of Current Evidence[J].Clin Neuropharmacol,2016,39(3):144-151.
[18] 艾春雨,江晓菁,马虹,等. 不同剂量右美托咪啶对非体外循环冠状动脉旁路移植术患者麻醉诱导期间血流动力学的影响[J]. 中国医师进修杂志,2016,39(2):105-108.
[19] 张继如,陈敏,王志强,等. 右美托咪定和七氟醚改善冠心病非心脏手术患者围术期心肌缺血的比较[J].临床麻醉学杂志,2017,33(3):273-276.
[20] 储靖,李宏,蔡春妹,等.右美托咪定与舒芬太尼鼻内给药用于儿童口腔科门诊手术镇静的临床观察[J]. 中山大学学报(医学科学版),2017,38(3):438-442.
[21] 陈鹏,王鹏,黄庆先.右美托咪定对非体外循环冠状动脉旁路移植术患者早期认知功能的影响[J].心肺血管病杂志,2017,36(1):40-42.
