Al2O3/CTS复合微球对Cr(VI)的吸附性能研究
2018-03-18张润虎宁门翠
张润虎,宁门翠,李 理
(1.昆明冶金高等专科学校 化工学院,云南,昆明 650033; 2.昆明冶金高等专科学校 环境工程学院,云南,昆明 650033)
含铬废水的来源广泛,若处理不当将污染环境。Cr的毒性与其存在的价态有关,Cr(VI)是Cr的最高价态,毒性强,比Cr(III)大 100倍,极易溶于水,通过食物链在生物体内富集,对人体危害极大。由于Cr(VI)具有毒性和致癌性,世界卫生组织(WHO)已将饮用水中总铬的最高允许含量设定为0.05 mg·L-1[1]。
目前,中国饮用水中Cr(VI)的允许浓度也为0.05 mg·L-1[2]。处理含Cr(VI)废水方法包括化学沉淀,吸附,离子交换,膜分离,反渗透,凝结/絮凝和溶剂萃取等[3-9]。在这些方法中,吸附是从废水中去除铬的常用方法之一。γ-氧化铝是一种多孔性、高分散度的固体材料,为微孔结构,比表面积大,具有良好的吸附性能、表面活性和优良的热稳定性等。CTS是自然界广泛存在的阳离子多糖,安全无毒,并可生物降解的链状大分子,含有大量的羟基、氨基,可借助氢键,也可借助盐键形成具有类似网状结构的笼形分子,进而对金属离子产生螯合作用,因此能有效地吸附或捕集溶液中的金属离子。已发表的研究资料中,多是单独使用氧化铝或CTS对废水的吸附研究,而以γ-氧化铝为载体,负载天然有机高分子CTS基材料的复合微球未见报道,无机-有机复合微球的制备可以有效的利用可再生资源,并提高吸附容量。本文制备Al2O3/CTS复合微球吸附材料,研究其对模拟废水中Cr(VI)的吸附作用和影响因素性,可以为生产废水中Cr(VI)的去除提供新的方法和理论指导,具有重要的科学意义和社会意义。
1 实验部分
1.1 仪器与试剂
离心机 L-500,湖南湘仪公司;数显型顶置式搅拌器 RW-20,IKA公司;电热恒温鼓风干燥箱,DHG-9246A型,厦门精艺兴业设备有限公司;紫外可见分光光度计,岛津UV-160A。
冰醋酸,99.5% 西陇化工股份有限公司;氢氧化钠,AR 上海国药集团化学试剂有限公司;CTS 脱乙酰度 ≥85% 济南海得贝海洋生物工程有限公司;重铬酸钾 AR 西陇化工股份有限公司;γ-氧化铝 ≥92% 淄博杰众新材料有限公司。
1.2 复合微球的制备
配制质量分数为2%的冰醋酸溶液。将CTS和氧化铝溶于醋酸溶中静止过夜。向溶胀后的CTS中加入适量PEG 2000(制孔剂),搅拌至产生大量均匀小气泡。将CTS缓慢倒入到装有液体石蜡的烧杯中,搅拌使其成均匀小球,加入适量Span 80(乳化剂)乳化,然后加入适量甲醛(保护氨基)交联。加入适量1∶1的乙醇和NaOH的混合液,使其破乳,静置分成,洗涤后得到甲醛保护CTS微球。将微球置于三口烧瓶中,加入NaOH碱化(活化6位羟基)后,加入适量环氧氯丙烷(预交联提高球机械强度),抽滤,洗涤得到甲醛保护的环氧交联CTS微球。
脱甲醛保护:将微球在稀HCl溶液中反应6 h,抽滤,热水边洗边用NaOH调至中性,45 ℃真空干燥得Al2O3/CTS微球。
1.3 吸附实验
吸附实验方法:量取50 mL 某浓度的含Cr(VI)水样于250 mL 锥形瓶中,向其中加入Al2O3/CTS微球若干克,在振荡器上以120 r ·min-1速率振荡,定时取样过滤,测定滤液中Cr(VI)的含量。
吸附量公式(1)计算:
(1)
式中:qe为平衡吸附量(mg·g-1),C0为吸附前溶液中Cr(VI)初始浓度(mg·g-1),Ce为平衡浓度(mg·L-1),V为含Cr(VI)溶液体积(L),m为吸附剂的质量(g)。
2 结果与讨论
2.1 接触时间的影响
从图1中的曲线可以直观的看出Al2O3/CTS复合微球吸附Cr(VI)的吸附率随时间的变化趋势。在吸附前10min,CTS/Al2O3微球吸附Cr(VI)的吸附率急剧增长,10min时吸附率为90.1%。15min后到40minAl2O3/CTS复合微球吸附Cr(VI)的吸附率缓慢增加,增加的幅度很小,当吸附时间达到40min后,Al2O3/CTS复合微球对Cr(VI)的吸附达到平衡,吸附率为95.4%。因此Al2O3/CTS复合微球对Cr(VI)吸附的最宜吸附时间为10min,平衡吸附时间为40min。
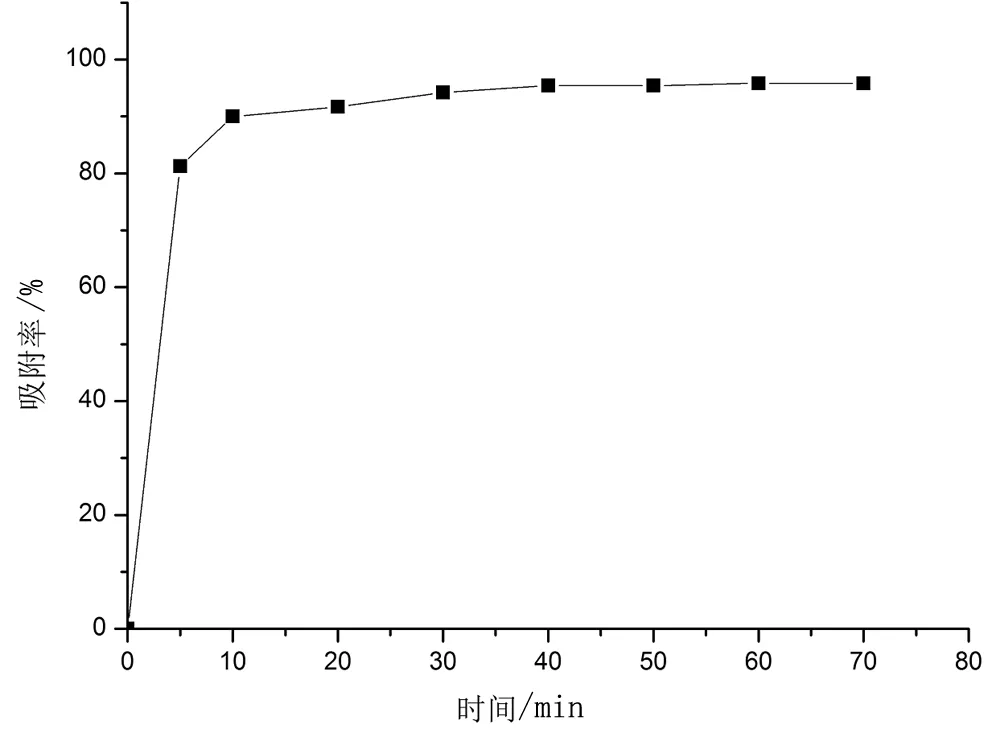
图1 时间对吸附Cr(VI)效果的影响
2.2 pH值的影响
酸度既影响吸附剂的表面性质,也影响吸附质的组成,是吸附过程的重要因素。如图2所示,不同的pH值对Cr(VI)的吸附性能有明显的影响,吸附过程明显依赖着pH值。可以看出,当pH值<5时,吸附率随pH值的增大而增大,而当pH值大于5.0时,吸附率明显随着pH值的增大而减小,在pH值=5.0时出现一个顶峰。故Al2O3/CTS复合微球吸附Cr(VI)的最佳pH值为5.0。
当pH值较小时,酸性较强,羧甲基CTS中的羧基的离解受到了抑制,使溶液中阴离子减小,而此时-NH2也以氨根离子形式存在,所以导致羧甲基CTS对金属的吸附络合能力大大减弱。随着pH值的增大,羧基和游离氨基的含量增加,与金属络合能力提高,吸附容量增大。当pH值增大7.0,随着pH值的增大,溶液中的氢氧根离子增多,与Cr(VI)发生反应生成沉淀,降低了溶液中Cr(VI)浓度。
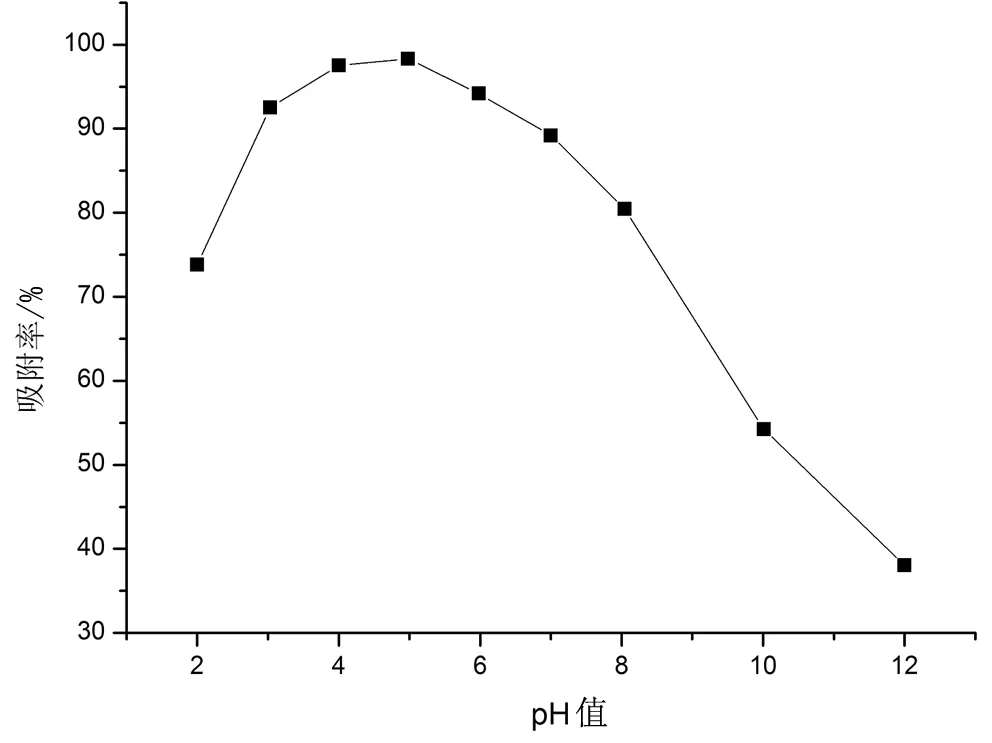
图2 pH值对Al2O3 / CTS吸附Cr (VI)离子效果的影响
2.3 吸附剂加入量的影响
如图3所示,当吸附剂用量小于0.05g时,Cr(VI)的吸附率随着吸附剂用量的增加,在吸附剂用量<0.02g时,吸附率随吸附剂用量的增加而急剧增大,因吸附剂用量的增加使得吸附剂的表面积增加,从而能够提供更多的吸附位。吸附剂用量在0.02g到0.05g时,吸附剂对Cr(VI)的吸附率缓慢增加,而在吸附剂用量大于0.05g是,吸附率不在随吸附剂的增加而增大,而是基本保持在一个定值,则吸附达到平衡,如再增加吸附剂的用量,吸附率不会再增加。故Al2O3/CTS复合微球对Cr(VI)吸附的最适用量为0.05g。

图3 吸附剂用量对吸附Cr(VI)的影响
2.4 Al2O3/CTS吸附Cr(VI)的等温线
实验方法,采用分批平衡技术,用移液管移取50mL不同浓度的Cr(VI)溶液于锥形瓶中,分别加入0.075gAl2O3/CTS复合微球,然后将锥形瓶放入振荡器中,在室温25± 1 ℃下,中速振荡达吸附平衡,然后取出离心取样,用分光光度计测定各样品的吸光度,计算出吸附后溶液中的Cr(VI)的浓度。


图4 Al2O3/CTS吸附Cr(VI)的Langmuir吸附等温线
根据图4确定的实验温度下Q0及b数值,具体Q0与b值表1。
同样为了进一步验证Al2O3/CTS复合微球吸附Cr(VI)的吸附情况,采用无量纲平衡参数RL的表达式来表征Langmuir吸附等温的基本特性:
式中, Co(mg·L-1)为吸附质的最大初始浓度;b(L·mg-1)为Langmuir吸附平衡常数。通过计算,Al2O3/CTS复合微球吸附Cr(VI)的RL值介于0~1之间,表明制备的Al2O3/CTS复合微球吸附Cr(VI)具有非常很好的吸附作用。
Freundlich等温方程也是一种经典的热力学吸附模型[12],它描述一定温度、平衡状态下,溶液中金属离子的浓度(Ce)与被吸附的金属量(qe)的关系,这一方程也广泛被应用于废水处理中。Freundlich型(F型)吸附等温式是基于吸附质在多相表面上的吸附建立的经验吸附平衡模式。其线性方程式为:
用吸附实验数据与Freundlich等温方程进行线性拟合分析,其结果如图5。
与Langmuir等温方程相比,Freundlich等温方程的拟合程度较好,在实验温度条件下,Freundlich相关系数大于Langmuir等温方程拟合的相关系数。Freundlich常数1/n值介于0.1~0.5之间,表明Al2O3/CTS复合微球对Cr(VI)具有很好的吸附性能。

图5 Al2O3/CTS吸附Cr(VI)的Freundlich吸附等温线

表1 Langmuir 和 Freundlich等温模型参数
2.5 Al2O3/CTS微球对Cr(VI)的热力学数据
Al2O3/CTS复合微球吸附Cr(VI)的热力学函数ΔG0、ΔH0、ΔS0可通过式(3)、(4)和(5)确定[13]。
(3)
(4)
△G°=△H°-T△S°
(5)
式中Kc是平衡常数,CAe和Ce(单位均为mg·L-1)是平衡时溶质在吸附剂中的和溶液中的浓度。R是理想气体常数(8.314J/(K·mol)),T(K)是绝对温度。
以lnKc ~1/T 作图可得到一条直线。焓变ΔH°和熵变ΔS°的值可以通过直线的斜率和截距求得,lnKc ~1/T直线图如图6所示。
Al2O3/CTS复合微球吸附Cr(VI)的热力学参数见表2。从表2中的结果可以看出,不同温度下吸附反应的ΔG均小于零,说明该吸附过程是自发进行的;而且随着温度的升高,其数值下降。吸附过程的焓变(ΔH)大于零,表明该过程是吸热的。熵变(ΔS)大于零,说明Al2O3/CTS复合微球吸附Cr(VI)过程中混乱度增加。


表2 不同温度下Al2O3/CTS对Cr(VI)的吸附热力学参数
3 结论
Al2O3/CTS复合微球吸附Cr(VI)的吸附量为41.67mg·g-1,吸附时间40min即可认为达到吸附平衡。在pH值为5左右时,Al2O3/CTS复合微球对Cr(VI)的去除效果较好。吸附过程中,ΔGO值在-3.89 kJ·mol-1到-1.05kJ mol-1之间,ΔH° =26.67 kJ·mol-1,ΔS =94.61.81kJ-1·mol-1,说明Al2O3/CTS复合微球吸附水中Cr(VI)为自发、吸热、熵增过程,高温有利于吸附。
