1-烯丙基-3-丁基咪唑氯离子液体的合成研究
2018-03-18张玲玲刘雁红
张玲玲,马 瑞,刘雁红,*
(1. 天津科技大学新农村发展研究院,天津 300457;2. 天津科技大学食品工程与生物技术学院,天津 300457)
离子液体是接近室温或室温呈液态的熔盐体系,也称室温熔盐[1]。它一般由含氮、磷的有机阳离子和无机阴离子组成。离子液体兼具离子态和液态双重特性,具有零蒸汽压、高热稳定性、宽的液态温度范围、导电率高、溶解性好、可设计性等许多独特性质,可循环利用,是一种有机绿色溶剂[2-3]。离子液体的应用十分广泛,在电化学中主要应用于电池中电解质,金属镀层,太阳帆板等;在生物方面主要应用于生物质处理,药物释放,杀菌剂等;在有机合成反应中,离子液体主要作为溶剂或催化剂[4];在溶剂和催化剂上多用于合成、催化反应、微波化学;在材料合成中,作为溶剂和模板剂应用于纳米金属材料和分子筛的制备中[5];近年来,离子液体作为一种绿色溶剂,逐渐在生物大分子中有了广泛应用,广泛用于萃取分离蛋白质[6]、作为毛细管壁的动态涂层分离酸性以及碱性蛋白质[7-8]等。离子液体阴阳离子种类繁多,其合成方法主要有直接法[9]、间接法[10]、微波合成法[11]、超声波辅助合成法[12]、电化学合成法[13]等各种方法。直接法与其他方法相比较而言,合成步骤少,产物提纯操作方便,副产物含量与种类少,可以合成种类非常多的离子液体,所以本文选用直接法合成1-烯丙基-3-丁基咪唑氯离子液体。
1 材料与方法
1.1 材料与试剂
烯丙基氯(分析纯)、N-丁基咪唑(分析纯):百灵威科技有限公司;二氯甲烷(分析纯):天津市化学试剂研究所;氘水(分析纯):天津康科德科技有限公司;溴化钾(光谱纯):天津港东化学试剂厂。
1.2 仪器与设备
集热式磁力加热搅拌器(JR-2):天津欧诺仪器仪表有限公司;集热式磁力加热搅拌器(DF-Ⅱ):山东鄄城嘉德仪器厂;傅立叶变换红外光谱仪(Tensor 2型):德国布鲁克仪器公司;核磁共振光谱分析仪(AVANCE Ⅲ 400MHz):德国布鲁克仪器公司。
1.3 1-烯丙基-3-丁基咪唑氯离子液体的制备方法
1.3.1 实验原理
采用直接法合成1-烯丙基-3-丁基咪唑氯离子液体,其反应式如下:
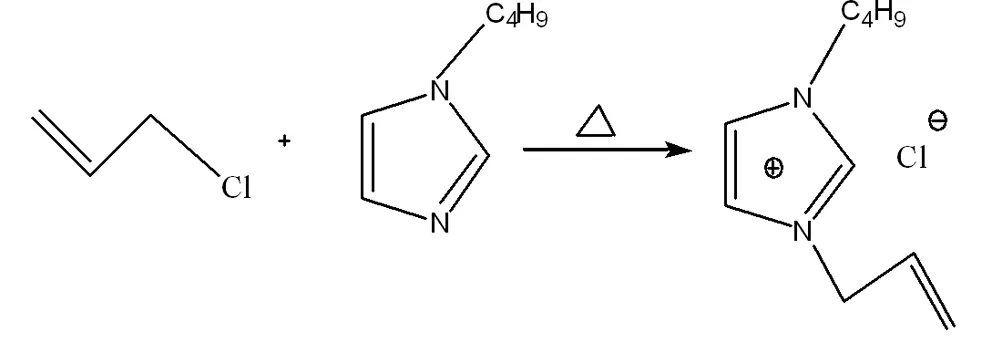
图1 1-烯丙基-3-丁基咪唑氯离子液体合成的反应式
1.3.2 实验方法
按一定比例称取N-丁基咪唑和烯丙基氯,先将N-丁基咪唑加入三口圆底烧瓶中,冰水浴下把烯丙基氯滴加到圆底烧瓶中,保持反应稳定,不发生剧烈反应,液体无白沫产生,瓶中无白烟产生,滴完后加热回流,磁力搅拌数小时,随着反应时间的延长溶液颜色逐渐变深,由浅黄色变成黄色,粘度也随之增大,直至反应完全后停止,旋蒸除去过量的烯丙基氯,得到深黄色液体,干燥,称重,计算收率。
1.4 1-烯丙基-3-丁基咪唑氯离子液体的表征
1.4.1 离子液体的傅里叶红外光谱测定
准确称量0.15 mg 样品与150 mg 干燥的溴化钾,充分研磨至细末贴壁。使用压片机将混合粉末压制成圆形薄片,用红外光谱仪做全波段扫描(4000~500 cm-1),扫描次数为16次,分辨率为4,以空白样品为采集背景。
1.4.2 离子液体的核磁共振分析
由四甲基硅烷作内标物,氘代作溶剂,核磁共振波谱测定后,分析图中的吸收峰,分析分子中氢原子的种类和数量,然后确定离子液体的结构。
2 结果与分析
2.1 1-烯丙基-3-丁基咪唑氯离子液体制备的实验
通过查阅参考文献[14],本文从反应物烯丙基氯和N-丁基咪唑物质的量比、反应时间、反应温度进行单因素实验来合成1-烯丙基-3-丁基咪唑氯离子液体,计算相应离子液体的收率情况。
2.1.1 单因素实验
2.1.1.1 反应物物质的量比对离子液体收率的影响
固定反应温度 50 ℃,反应时间 11 h,改变烯丙基氯和N-丁基咪唑的物质的量比,考察两者配比对1-烯丙基-3-丁基咪唑氯离子液体收率的影响,结果见图2。

图2 烯丙基氯和N-丁基咪唑物质的量比对离子液体收率的影响
从图2可以看出,在n(烯丙基氯)∶n(N-丁基咪唑)= 1.3∶1前,随着反应物比例的增加,收率呈较快上升趋势,但在n(烯丙基氯)∶n(N-丁基咪唑)= 1.3∶1后,上升趋势不明显,且有轻微下降趋势,而在物质的量比为1.3∶1处合成离子液体收率达到最大值93.77 %,推测可能是物质的量比为1.3 ∶1时已充分反应,后烯丙基氯过量对实验结果影响不大。故选择二者的物质的量比为1.3∶1。
2.1.1.2 反应时间对离子液体收率的影响固定反应物物质的量比n(烯丙基氯)∶n(N-丁基咪唑)= 1.3∶1,反应温度 50 ℃,改变反应时间,考察反应时间对1-烯丙基-3-丁基咪唑氯离子液体收率的影响,结果见图3。

图3 反应时间对离子液体收率的影响
从图3可知,随着反应时间的增加,1-烯丙基-3-丁基咪唑氯的收率逐步增加,在反应时间为3 h 时,其收率达到最高点为93.76 %,随着时间的增加,产物颜色逐渐变深但收率变化不大,即在3 h 时反应已基本完全,因此选择反应时间为3 h 比较适宜。
2.1.1.3 反应温度对离子液体收率的影响
固定反应物物质的量比n(烯丙基氯)∶n(N-丁基咪唑)= 1.3∶1,反应时间 3 h,改变反应温度,考察反应温度对1-烯丙基-3-丁基咪唑氯离子液体收率的影响,结果见图4。

从图4可知,产物收率随着反应温度的增加而逐步增加,特别是在反应温度为50 ℃ 之前,产物收率增加趋势较大,在50 ℃ 收率达到最大为93.77 %,50 ℃ 后随着反应温度的增加,增长速度趋于平缓,甚至有上下波动趋势,推测可能有副反应发生从而影响收率,因此反应温度选择50 ℃较适宜。
2.1.2 1-烯丙基-3-丁基咪唑氯离子液体制备的正交实验
基于单因素实验结果,制定因素水平表1,进行正交实验,从而得到离子液体的最佳制备条件。
选择烯丙基氯和N-丁基咪唑的物质的量比、反应温度、反应时间进行三因素三水平的正交实验,实验结果如表2所示。

表1 因素水平表

表2 三因素三水平正交实验表
由表2的极差R可知,三个单因素对离子液体收率的影响大小依次为:反应时间>反应温度>n(烯丙基氯)∶n(N-丁基咪唑)。收率最高的为3号实验组A1B3C3,工艺条件为n(烯丙基氯)∶n(N-丁基咪唑)=1.3∶1、反应温度50 ℃,反应时间3 h,收率为93.77 %。
2.1.3 最优工艺条件下制备离子液体的验证实验
在最优工艺条件下进行验证实验,结果见表3。

表3 验证实验
由表3可知,最优工艺条件下1-烯丙基-3-丁基咪唑氯离子液体的收率可稳定在93.64 %左右。
2.2 1-烯丙基-3-丁基咪唑氯离子液体的结构表征
2.2.1 离子液体的傅里叶红外光谱分析

从图5可知,3000 cm-1附近的特征吸收峰为多种饱和与不饱和的C-H伸缩振动峰,1562 cm-1是阳离子咪唑环的特征吸收峰。1645 cm-1和1464 cm-1分别与烯丙基上的C=C伸缩振动峰和=CH2对应的C-H弯曲振动峰。1165 cm-1处是咪唑环中的C-H弯曲振动峰,在990 cm-1和920 cm-1左右对应的是烯丙基中的-CH=CH2的C-H面外弯曲振动峰。因此996 cm- 1处属于-CH=CH2的C-H面外弯曲振动峰,947 cm-1是-CH=CH2的C-H面内摇摆振动峰。另外在3400 cm-1处有水分杂质的信号,可能是由于1-烯丙基-3-丁基咪唑氯具有强烈的吸潮性。从图中分析可知该产品与1-烯丙基-3-丁基咪唑氯离子液体的结构相符。
2.2.2 1-烯丙基-3-丁基咪唑氯离子液体的核磁共振分析
由图6可以看出,该产物共有17个H,与1-烯丙基-3-丁基咪唑氯中H的个数相符。其中,1H NMR(400MHz,D2O)δ:0.8 - 0.9(t,3H,1-H),1.2~- 1.3(m,2H,2-H),1.8~1.9(m,2H,3-H),4.2(t,2H,4-H),4.7~ 4.9(m,2H,7-H),5.3~5.5(m,2H,9-H),6.0(m,1H,8-H),7.5~7.6(d,2H,5-H),8.8~8.9(s,1H,6-H),由以上分析可推断出1-烯丙基-3-丁基咪唑氯的结构如图7所示,与事实相符,故产物1-烯丙基-3-丁基咪唑氯合成取得成功。


图7 1-烯丙基-3-丁基咪唑氯的分子结构
3 结论
采用直接法合成离子液体1-烯丙基-3-丁基咪唑氯,考察了反应时间、反应温度及n(烯丙基氯)∶n(N-丁基咪唑)对1-烯丙基-3-丁基咪唑氯收率的影响,并以正交实验来确定其最佳工艺条件为:反应时间为3 h,反应温度为50 ℃,n(烯丙基氯)∶n(N-丁基咪唑)=1.3∶1,且在最佳工艺条件下进行验证实验,收率可稳定在93.77 %左右。从产品红外谱图和核磁谱图分析可知,实验得到的产品与预期结果的结构相符。该离子液体的研究意义在于其既可作为溶剂,可通过单一或复合的形式溶解纤维素,可循环利用,干净环保,还可以作为功能单体用于聚合物的合成,用于吸附蛋白操作中[15],具有很大的应用前景。
