改良的DPPH与ABTS自由基法评价不同葡萄籽油抗氧化能力
2018-03-10梁红敏任继波李彦奎高德艳胡文效
梁红敏 任继波 李彦奎 高德艳 胡文效
(山东省葡萄研究院,山东省葡萄栽培与精深加工工程技术研究中心,济南 250100)
葡萄籽是葡萄酒、葡萄果汁饮料生产中产生的资源性副产物,葡萄籽含油量为14%~17%[1]。葡萄籽油是葡萄籽经过进一步加工得到的一种植物性油脂,含有较高含量的不饱和脂肪酸,主要以亚油酸为主,亚油酸具有能够降低和调节低密度脂蛋白胆固醇水平的作用,葡萄籽油中还含有多酚、维生素类等有益微量物质,使得葡萄籽油具有一定的抗氧化活性[2-4]。
葡萄籽油的抗氧化能力是评价葡萄籽油品质的一个重要指标。目前多数抗氧化能力评价方法都是在水溶液、缓冲溶液或者乙醇体系中进行[5]。1,1-二苯基-2-三硝基苯肼(1,1-diphenyl-2-picryhydrazyl,DPPH)法和2,2’-联氮双-(3-乙基苯并噻唑林-6-磺酸)二胺盐[2,2’-azinobis(3-ethylbenzothiazoline-6-sulfonicacid)ammoniumsalt,ABTS]法作为广泛应用的清除自由基能力的体外抗氧化检测方法,在测定样品的抗氧化活性时,一般也是在水/乙醇体系中进行,不能将脂溶性成分充分溶解。有些研究采用有机溶剂将活性成分提取出来再进行抗氧化活性检测,操作复杂,误差较大[6-7]。乙酸乙酯是DPPH法测定植物油清除自由基能力时常用的溶解全油和非极性部分的溶剂[8-9],但有研究发现由于乙酸乙酯的低黏性以及对极性物质的溶解度较低,不是植物油很好的溶剂[10-12]。Dionysios等[13]研究了不同溶剂对DPPH与ABTS自由基法测定植物油抗氧化能力的影响,结果表明对于DPPH和ABTS自由基法分别采用异丙醇和正丁醇作为植物油非极性部分的溶剂效果最好。
葡萄籽油的分离方法主要有物理压榨法、有机溶剂提取法和超临界CO2萃取法等,由于不同方法提取的原理不同,提取葡萄籽油的抗氧化性能和品质会有差异。本研究采用DPPH与ABTS甲醇体系、DPPH异丙醇与ABTS正丁醇体系对超临界CO2萃取法、溶剂提取法、冷榨法与热榨法4种不同方法提取的葡萄籽毛油及精炼油的体外抗氧化能力进行测定,研究不同提取方法对葡萄籽油抗氧化能力的影响,并对葡萄籽油极性部分中多酚含量与抗氧化能力的相关性进行研究,进一步为葡萄籽油的提取和开发利用提供依据。
1 材料与方法
1.1 材料与试剂
公酿一号葡萄籽:日照太阳城葡萄酒庄园(2015)。
1,1-二苯基-2-三硝基苯肼(1,1-diphenyl-2-picryhydrazyl,DPPH)、2,2’-联氮双-(3-乙基苯并噻唑林-6-磺酸)二胺盐(2,2’-azinobis(3-ethylbenzothiazoline-6-sulfonicacid)ammoniumsalt,ABTS)、Fe3+-三吡啶三吖嗪(2,4,6-Tri(2-pyridyl)-1,3,5-triazine,TPTZ)、6-羟基-2,5,7,8-四甲基苯并二氢吡喃-2-羧酸(6-hydroxy-2,5,7,8-tetramethylchroman-2-carboxylicacid,Trolox)、没食子酸(Gallicacid,GAE)标准品、福林酚试剂:Sigma公司;甲醇、异丙醇、正丁醇:国药集团试剂有限公司。
1.2 仪器与设备
TQ-150S型索氏提取器:上海启前电子科技有限公司;HA221-40-02超临界CO2萃取设备:南通华安有限公司;QYZ-500型液压压榨机:泰安良君益友机械有限公司;UV5200紫外可见分光光度计:上海元析仪器有限公司;DGG-9140B型电热恒温鼓风干燥箱:上海森信实验仪器有限公司;TDL-5型高速离心机:上海安亭科学仪器厂;WK-500B高速粉碎机:青州精诚机械有限公司;RE-52AA旋转蒸发仪:上海亚荣生化仪器厂。
1.3 方法
1.3.1 不同提取方法制备葡萄籽油样品
超临界CO2萃取葡萄籽油工艺:取400g葡萄籽粉(物料粉碎度60目)至于1L萃取釜中,设置萃取温度45 ℃、萃取压力30MPa,萃取时间60min,收集分离釜中萃取物,去水得到葡萄籽油,称重,得率为16.2%。
溶剂提取法提取葡萄籽油工艺:称取100g葡萄籽粉(物料粉碎度60目),置于索氏提取器中,烧瓶中加入一定量的石油醚(60~90 ℃),放入恒温水浴锅中提取2h后,取出并蒸干提取液,得到葡萄籽油粗品,冷却,称重,毛油得率为16.8%。
低温压榨法提取葡萄籽油工艺:取40kg葡萄籽粉(物料粉碎度60目),设置压力40MPa、时间60min、榨膛温度50 ℃,经过沉淀过滤后得葡萄籽油,得率为7.5%。
热榨法提取葡萄籽油工艺:取40kg葡萄籽粉(物料粉碎度60目),压榨压力40MPa,压榨时间60min,蒸料时间40min、物料粉碎度60目、榨膛温度50 ℃。在最佳工艺条件下,葡萄籽油出油率为12.2%。
溶剂法与热榨法制备的葡萄籽油毛油需要经过精炼。精炼工艺:取粗油,测定酸价,放入烧杯中,毛油加热至65 ℃加磷酸(1%),加水(3%)脱胶,加入NaOH脱酸,自然沉降4h,碱炼油加热到80~85 ℃,60r/min下加8%水进行水洗,在抽真空条件下(-0.08MPa),脱水后加活性白土(中性)1%~3%脱色,过滤、脱臭得到精制葡萄籽油。
1.3.2 抗氧化能力测定葡萄籽油样品制备
参考Dionysios等[13]的方法制备样品。
极性部分的制备:称取2.0g葡萄籽油样品,加入3mL甲醇,漩涡振荡5min,5 000r/min离心5min,取上层清液,重复萃取3次,合并上清液定容至10mL。冰箱保存备用。
非极性部分的制备:称取萃取后残余的脂溶性部分,分别用正丁醇、异丙醇溶解。
葡萄籽油全油样品的制备:将葡萄籽油分别用正丁醇、异丙醇溶解,配制成至一定浓度的样品溶液。
1.3.3 极性部分抗氧化能力测定
1.3.3.1DPPH自由基清除能力
参考Espín等[14]方法,称取0.039 4gDPPH,用甲醇定容至100mL,再用甲醇稀释,配制成浓度为1×10-4mmol/L的DPPH溶液。取2mL稀释的极性部分样品与2mLDPPH溶液反应,避光反应2h,以甲醇溶剂做空白对照,测量其在波长517nm处的吸光度(Ai)。取2mL甲醇与2mLDPPH反应,避光反应2h,517nm处测吸光度值(A0),按照公式计算自由基清除率。

以Trolox(水溶性维生素E类)为标准物质,以Trolox浓度对清除率作标准曲线,计算样品对Trolox的等值抗氧化活性,结果用μmolTrolox/100g油表示。DPPH甲醇体系标准曲线线性方程为y=2.384 1x-1.580 3,R2=0.999 6。
1.3.3.2ABTS自由基清除能力
参考Marfil等[15]方法配制ABTS反应液。使用时将其稀释至吸光值为0.7±0.02,取6mL稀释液与200μL一定浓度的样品混合,反应30min,测734nm下吸光值(Ai),取200μL甲醇与6.0稀释液反应,避光反应30min,734nm处测吸光度值(A0),按照公式计算自由基清除率。

以Trolox(水溶性维生素E类)为标准物质,以Trolox浓度对清除率作标准曲线,计算样品对Trolox的等值抗氧化活性,结果用μmolTrolox/100g油表示。ABTS甲醇体系标准曲线线性方程为y=0.171 4x-0.07,R2=0.999 1。
1.3.4 非极性部分样品与全油样品抗氧化能力测定
1.3.4.1DPPH自由基清除能力
参考Dionysios等[13]的方法用异丙醇溶液配制DPPH自由基反应液,对脂溶性部分和全油样品DPPH自由基清除能力进行检测,测试方法同1.2.3.1所述。
以Trolox(水溶性维生素E类)为标准物质,以Trolox浓度对清除率作DPPH异丙醇体系标准曲线。计算样品对Trolox的等值抗氧化活性,结果用μmolTrolox/100g油表示。DPPH异丙醇体系标准曲线线性方程为y=2.386 8x+4.382 6,R2=0.999。
1.3.4.2ABTS自由基清除能力
参考Dionysios等[13]的方法用正丁醇溶液配制ABTS自由基反应液,对脂溶性部分和全油样品ABTS自由基清除能力进行检测,测试方法同1.2.3.2所述。
以Trolox(水溶性维生素E类)为标准物质,以Trolox浓度对清除率作ABTS正丁醇体系标准曲线。计算样品对Trolox的等值抗氧化活性,结果用μmolTrolox/100g油表示。ABTS正丁醇体系标准曲线线性方程为y=0.170 8x+1.072,R2=0.999 8。
1.3.5 葡萄籽油总酚含量测定
参考王华等[16]的方法,以没食子酸为标准品,绘制标准曲线。分别对4种不同方法提取的葡萄籽油采用1.3.2葡萄籽油极性部分制备方法进行处理,再按照制作标准曲线的方法进行操作,结果以没食子酸当量表示(μgGAE/g)。没食子酸标准曲线线性方程为y=0.015x-0.002,R2=0.999 4。
1.3.6 数据处理
实验结果为平行实验的平均值。使用Excel软件处理数据,作图。采用SPSS19.0数据处理软件。采用Duncan方法进行方差分析,不同字母表示显著性差异(P<0.05,n=3),置信水平95%(P=0.05)。具有相同字母表示两者无显著差异(P>0.05),字母顺序按均值大小排列。采用Pearson双变量进行相关性分析。
2 结果与分析
2.1不同方法提取葡萄籽油毛油及精练油极性部分抗氧化能力
2.1.1 极性部分DPPH自由基清除能力
采用DPPH甲醇体系评价葡萄籽油极性部分对DPPH自由基的清除能力,甲醇能够将葡萄籽油中的极性成分溶解,不同葡萄籽油极性部分对DPPH自由基的清除能力如图1所示。

图1 不同葡萄籽油极性部分对DPPH自由基的清除能力注:1溶剂法(毛油),2溶剂法(精炼油),3热榨法(毛油),4热榨法(精炼油),5低温压榨油,6超临界CO2萃取油。余同。
由图1可以看出,这6种不同葡萄籽油极性部分对DPPH自由基的清除能力大小为:热榨毛油>低温压榨油>热榨精炼油>溶剂法毛油>溶剂法精炼油>超临界CO2萃取油。各不同葡萄籽油的清除能力具有显著性差异。热榨毛油的清除能力最强,溶剂法毛油也有一定的清除能力,但是这2种毛油经过精炼后清除能力显著降低,表明精练过程显著影响葡萄籽油的抗氧化能力。超临界CO2萃取油的清除能力较弱,可能是因为CO2是非极性物质的溶解剂,对葡萄籽中多酚、甾醇等极性抗氧化成分的溶解性较小[17-18],因此导致葡萄籽油中极性部分的DPPH自由基清除能力较弱。
2.1.2 极性部分ABTS自由基清除能力
采用ABTS甲醇体系评价不同葡萄籽油极性部分对ABTS自由基的清除能力结果如图2所示。

图2 不同葡萄籽油极性部分对ABTS自由基的清除能力
由图2可以看出,这6种不同葡萄籽油极性部分对ABTS的清除能力大小为:热榨毛油>低温压榨油>热榨精炼油>溶剂法毛油>溶剂法精炼油=超临界CO2萃取油。溶剂法精炼油与超临界CO2萃取油的ABTS自由基的清除能力无显著差异,但其他不同葡萄籽油的清除能力具有显著性差异,结合极性部分对DPPH自由基的清除能力,结果表明,与溶剂法精炼油、热榨法精炼油、超临界CO2萃取油相比,低温压榨法提取葡萄籽油极性部分的抗氧化能力最强。
2.2不同方法提取葡萄籽油毛油及精练油极性部分抗氧化能力
2.2.1 非极性部分DPPH自由基清除能力
采用DPPH异丙醇体系评价葡萄籽油非极性部分对DPPH自由基的清除能力,异丙醇能够将葡萄籽油中的脂溶性部分溶解,不同葡萄籽油非极性部分对DPPH自由基的清除能力如图3所示。

图3 不同葡萄籽油非极性部分对DPPH自由基的清除能力
由图3可以看出,这6种不同葡萄籽油非极性部分对DPPH自由基的清除能力大小为:超临界CO2萃取油=溶剂法毛油>热榨毛油=低温压榨油>溶剂法精炼油>热榨精炼油。溶剂法毛油与超临界CO2萃取油非极性部分DPPH自由基的清除能力无显著差异,热榨毛油与低温压榨油非极性部分DPPH自由基的清除能力无显著差异,超临界CO2萃取油非极性部分DPPH自由基的清除能力最强,可能是因为超临界CO2萃取温度较低,且减少了与空气接触,而热榨法与溶剂法提取油脂在精炼过程中不断与空气接触,温度也较高,造成油脂中非极性抗氧化成分如维生素E等的损失。
2.2.2 非极性部分ABTS自由基清除能力
采用ABTS正丁醇体系评价葡萄籽油非极性部分对ABTS自由基的清除能力,不同葡萄籽油非极性部分对ABTS自由基的清除能力如图4所示。
由图4可以看出,这6种不同葡萄籽油非极性部分对ABTS的清除能力大小为:超临界CO2萃取油>溶剂法毛油=热榨毛油>低温压榨油>溶剂法精炼油>热榨精炼油。溶剂法毛油与热榨法毛油的ABTS自由基的清除能力无显著差异,其他不同葡萄籽油的清除能力差异显著。结合非极性部分对DPPH自由基的清除能力,结果表明,与溶剂法精炼油、热榨法精炼油、低温压榨油相比,超临界CO2萃取葡萄籽油非极性部分的抗氧化能力最强。
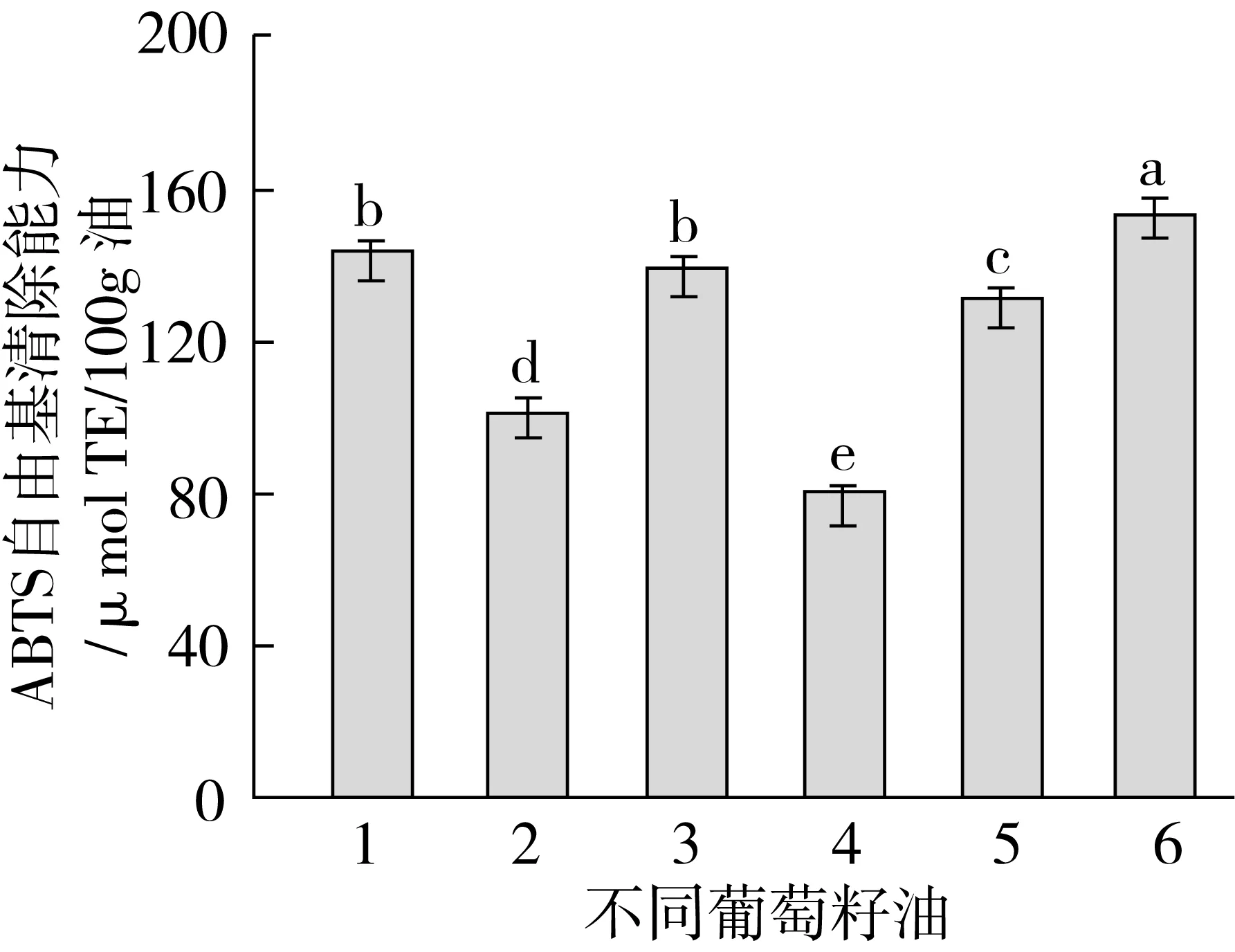
图4 不同葡萄籽油非极性部分对ABTS自由基的清除能力
2.3不同方法提取葡萄籽油毛油及精练油全油抗氧化能力
2.3.1 全油DPPH自由基清除能力
采用DPPH异丙醇体系评价葡萄籽油全油对DPPH自由基的清除能力,异丙醇能够将葡萄籽油全部溶解,不同葡萄籽油全油对DPPH自由基的清除能力如图5所示。
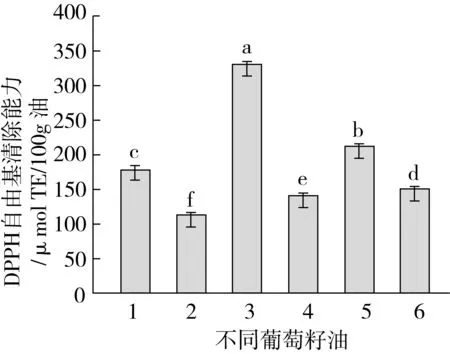
图5 不同葡萄籽油全油对DPPH自由基的清除能力
由图5可以看出,这6种不同葡萄籽油全油对DPPH自由基的清除能力大小为:热榨毛油>低温压榨油>溶剂法毛油>超临界CO2萃取油>热榨精炼油>溶剂法精炼油。不同葡萄籽油的清除能力具有显著性差异。热榨毛油与溶剂法提取毛油的DPPH自由基的清除能力最强,但是经过精炼,清除能力明显降低,低温压榨油与超临界CO2萃取油在提取过程中保持较低的温度,不需要精炼,保留了较高的抗氧化能力。
2.3.2 全油ABTS自由基清除能力
采用ABTS正丁醇体系评价不同葡萄籽油全油对ABTS自由基的清除能力,结果如图6所示。
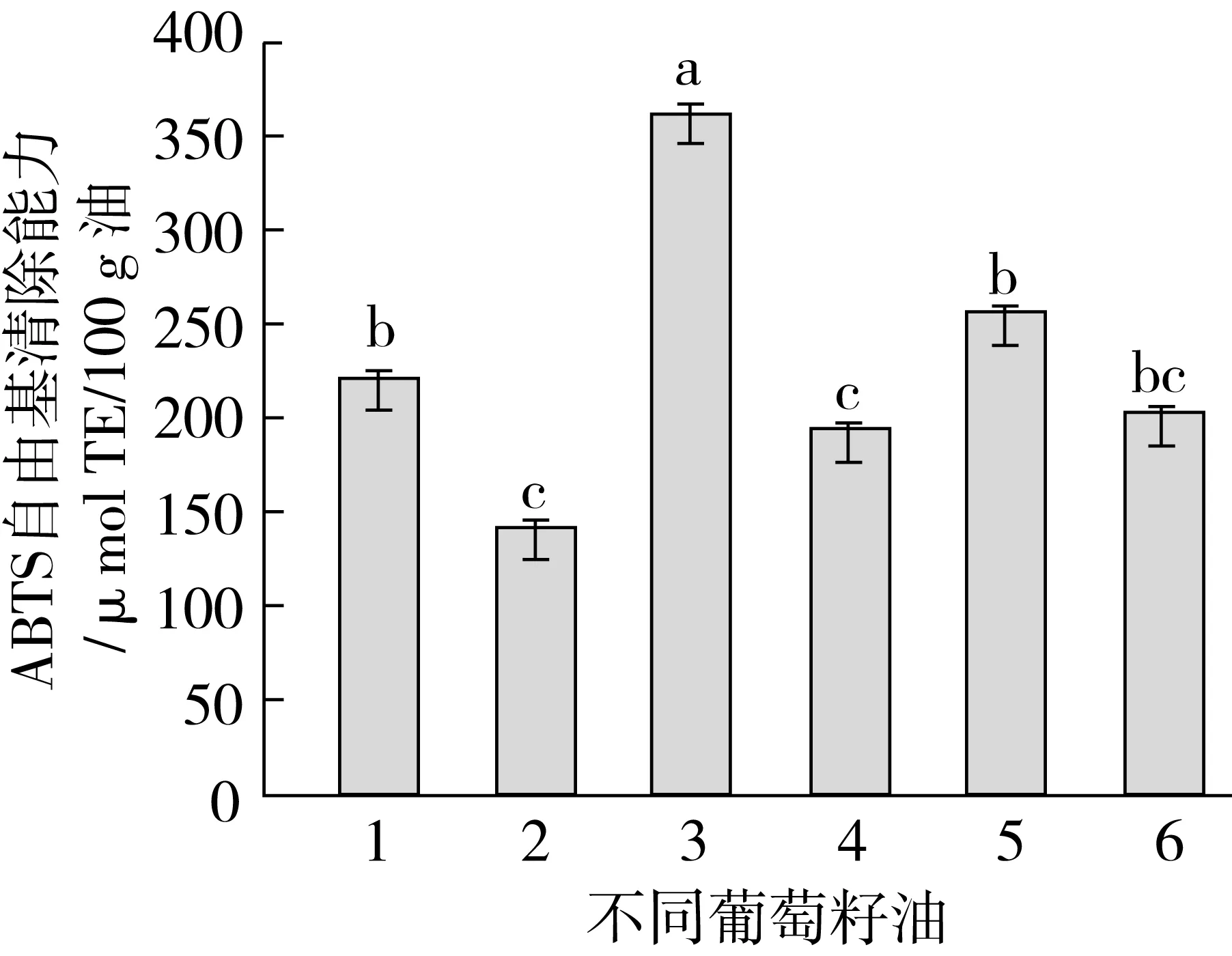
图6 不同葡萄籽油全油对ABTS自由基的清除能力
由图6可以看出,这6种不同葡萄籽油全油对ABTS的清除能力大小为:热榨毛油>低温压榨油>超临界CO2萃取油>溶剂法毛油>热榨精炼油>溶剂法精炼油。低温压榨油与超临界CO2萃取油的ABTS自由基的清除能力无显著差异,溶剂法精炼油与热榨法精炼油的ABTS自由基的清除能力无显著差异,其他不同葡萄籽油的清除能力差异显著。结合全油对DPPH自由基的清除能力,结果表明,在溶剂法精炼油、热榨法精炼油、低温压榨油、超临界CO2萃取油中,低温压榨油最好,其次是超临界CO2萃取油。
2.4 葡萄籽油总酚含量与抗氧化能力的相关性
不同葡萄籽油中多酚含量及与极性部分自由基清除能力之间相关性分析见表1。

表1 不同葡萄籽油中多酚含量及与极性部分自由基清除能力之间相关性分析
注:**表示在P<0.01水平上显著相关。
由表1可以看出,这6种不同葡萄籽油总酚含量大小为:热榨毛油>低温压榨油>溶剂法毛油>热榨精炼油>超临界CO2萃取油>溶剂法精炼油。溶剂法毛油与热榨法精炼油的总酚含量无显著差异,溶剂法精炼油与超临界CO2萃取油的总酚含量无显著差异,其他不同葡萄籽油的总酚差异显著,热榨毛油与溶剂法毛油的总酚含量经过精炼后显著减少,在溶剂法精炼油、热榨法精炼油、低温压榨油、超临界CO2萃取油中,低温压榨油多酚含量最高,为101.3μgGAE/g,溶剂法精炼油的多酚含量最低,为11.57μgGAE/g,这与其他研究者的研究结果有差距[19-21],可能与葡萄品种、提取方法和精练过程不同有关。各不同葡萄籽油总酚含量与极性部分DPPH和ABTS自由基的清除能力具有显著的正相关性,相关系数分别为0.985、0.969,表明葡萄籽油中多酚含量可能是葡萄籽油极性部分发挥抗氧化作用的主要成分。
3 结论
采用DPPH与ABTS甲醇体系评价不同方法提取葡萄籽油极性部分的抗氧化能力,DPPH异丙醇与ABTS正丁醇体系评价非极性部分与全油的抗氧化能力,结果表明不同葡萄籽油全油的抗氧能力较高,略高于极性部分和非极性部分的抗氧化能力,表明在DPPH异丙醇、ABTS正丁醇体系中,葡萄籽油极性抗氧化成分也充分发挥了清除自由基的能力,这也证明了DPPH异丙醇和ABTS正丁醇体系能够用于评价葡萄籽油体外抗氧化能力;在溶剂法精炼油、热榨法精炼油、低温压榨油、超临界CO2萃取油中,低温压榨法提取葡萄籽油极性部分清除DPPH与ABTS自由基的能力最强,超临界CO2萃取油非极性部分与低温压榨法提取葡萄籽油全油的DPPH与ABTS自由基清除能力最强,热榨毛油与溶剂法提取毛油在经过精炼后抗氧化能力显著降低;低温压榨油的多酚含量较高,各不同葡萄籽油总酚含量与极性部分DPPH和ABTS自由基的清除能力具有显著的正相关性。
[1]CALABRESEG.Tablegrapenutritionalvalue[J].Bulll’OIV,2003(1):124-133
[2]孙来华.葡萄籽功能成分及其应用[J].食品研究与开发,2011,32(7):184-187
SUNLH.Applicationofgrapeseedanditsfunctionalcomposition[J].FoodResearchandDevelopment,2011,32(7):184-187
[3]张静,袁毅,刘利军.葡萄籽油的提取及精炼工艺优化[J].食品科学,2011,3(10):40-43
ZHANGJ,YUANY,LIULJ.Processoptimizationforextractionandrefiningofgrapeseedoil[J].FoodScience,2011,3(10):40-43
[4]邹磊.酿酒后葡萄籽综合利用的研究进展[J].中国酿造,2012,21(2):16-18
ZOUL.Comprehensiveutilizationofgrapeseedafterwinebrewing[J].ChinaBrewing,2012,21(2):16-18
[5]文镜,刘璇,赵建.荧光法及化学发光法在保健食品抗氧化体外实验中的应用[J].中国酿造,2009(11):130-133
WENJ,LIUX,ZHAOJ.Applicationoffluorescenceandchemiluminescenceindeterminationofanti-oxidationcapabilityofhealthfoodinvitroexperiments[J].ChinaBrewing,2009(11):130-133
[6]周晴芬,徐洲,魏岚,等.4种油茶籽油中多酚类物质的抗氧化活性比较研究[J].中国油脂,2014,39(1):35-38
ZHOUQF,XUZ,WEIL,etal.Comparisonofantioxidantactivitiesofpolyphenolsinfourkindsofoil-teacamelliaseedoils[J].ChinaOilsandFats,2014,39(1):35-38
[7]FRANCOMN,GALEANO-DAZT,LPEZ,etal.Phenoliccompoundsandantioxidantcapacityofvirginoliveoil[J].FoodChemistry,2014,163:289-298
[8]ARRANZS,CERTR,PÉREZ-JIMÉNEZJ,etal.Comparisonbetweenfreeradicalscavengingcapacityandoxidativestabilityofnutoils[J].FoodChemistry,2008,110(4):985-990
[9]刘慧敏.不同植物油微量成分与抗氧化能力的相关性研究[D].无锡:江南大学,2015
LIUHM.Studyontheminorcomponentsindifferentvegetableoilsandtheirrelationwithantioxidantcapacity[D].Wuxi:JiangnanUniversity,2015
[10]PREVCT,EGATINN,POKLARUN,etal.DPPHassayofvegetableoilsandmodelantioxidantsinproticandaproticsolvents[J].Talanta,2013,109:13-19
[11]PÉREZ-JIMÉNEZJ,ARRANZS,TABERNEROM,etal.Updatedmethodologytodetermineantioxidantcapacityinplantfoods,oilsandbeverages:Extraction,measurementandexpressionofresults[J].FoodResearchInternational,2008,41(3):274-285
[12]DAWIDOWICZAL,WIANOWSKAD,OLSZOWYM.OnpracticalproblemsinestimationofantioxidantactivityofcompoundsbyDPPHmethod(Problemsinestimationofantioxidantactivity)[J].FoodChemistry,2012,131(3):1037-1043
[13]DIONYSIOSC,CristodouleasC,FotakisA,etal.ModifiedDPPHandABTSassaystoassesstheantioxidantprofileofuntreatedoils[J].FoodAnalyticalMethods,2015,8:1294-1302
[14]ESPNJC,SOLER-RIVASC,WICHERSHJ.Characterizationofthetotalfreeradicalscavengercapacityofvegetableoilsandoilfractionsusing2,2-diphenyl-1-picrylhydrazylradical[J].JournalofAgriculturalandFoodChemistry,2000,48(3):648-656
[15]MARFILR,GIMÉNEZR,MARTNEZO,etal.Determinationofpolyphenols,tocopherols,andantioxidantcapacityinvirginarganoil(Arganiaspinosa,Skeels)[J].EuropeanJournalofLipidScienceandTechnology,2011,113(7):886-893
[16]王华.葡萄与葡萄酒实验技术操作规范[M].西安地图出版社,1999
[17]李淑芬,吴希文,侯彩霞,等.超临界流体技术幵发应用现状和前景展望[J].现代化工,2007,27(2):1-7
LISF,WUXW,HOUCX,etal.Supercriticalfluidtechnologyandapplication[J].ModernChemicalIndustry,2007,27(2):1-7
[18]蒋志国.超临界CO2萃取葡萄籽油及萃取物中多酚类物质的研究[D].沈阳:沈阳农业大学,2003
JIANGZG.Studyontheminorcomponentsindifferentvegetableoilsandtheirrelationwithantioxidantcapacity[D].Shenyang:ShenyangAgriculturalUniversity,2003
[19]BAILS,STUEBIGERG,KRISTS,etal.Characterisationofvariousgrapeseedoilsbyvolatilecompounds,triacylglycerolcomposition,totalphenolsandantioxidantcapacity[J].FoodChemistry,2008,108(3):1122-1132
[20]LUTTERODTH,SLAVINM,WHENTM,etal.Fattyacidcomposition,oxidativestability,antioxidantandantiproliferativepropertiesofselectedcold-pressedgrapeseedoilsandflours[J].FoodChemistry,2011,128(2):391-399
[21]DEMIRTASI,PELVANE,ÖZDEMIRIS,etal.LipidcharacteristicsandphenolicsofnativegrapeseedoilsgrowninTurkey[J].EuropeanJournalofLipidScienceandTechnology,2013,115:641-647.
