次氯酸钠对剑水蚤灭活动力学及紫外强化灭活
2018-03-02何盼盼聂小保蒋昌波唐韵子隆院男长沙理工大学水利工程学院湖南长沙410114水沙科学与水灾害防治湖南省重点实验室湖南长沙410114
何盼盼,聂小保*,蒋昌波,唐韵子,隆院男,徐 超 (1.长沙理工大学水利工程学院,湖南 长沙410114;2.水沙科学与水灾害防治湖南省重点实验室,湖南 长沙 410114)
剑水蚤是水源水体中常见的桡足类浮游动物.当水体发生富营养化时,剑水蚤可大量孳生并随原水进入自来水厂[1].由于剑水蚤体型较小,且迁移运动能力强,一旦进入水厂,以“混凝-沉淀-过滤”为代表的常规净水工艺难以对其实现有效拦截,剑水蚤将在供水管网中出现,引发供水水生生物和微生物风险[2-4].近年来,在我国屡有自来水中剑水蚤检出报道[5-7].
自来水厂常采用积极的强化混凝、强化过滤等策略来提高对剑水蚤的拦截率,但效果有限.Van Lieverloo等[8]对荷兰34个自来水厂的调研表明,即便采用强化策略,出水厂中剑水蚤的平均检出密度仍高达1.39ind./m3;优化混凝沉淀和过滤操作条件下,剑水蚤拦截去除率也仅有56.7%[9];Adam等[10]认为过滤对剑水蚤去除效果有限的主要原因在于,反冲洗过程中滤层存在难以流化的死区.因此,作为自来水厂最后一道工艺操作,消毒单元对剑水蚤的灭活就显得格外重要.
次氯酸钠/液氯是自来水厂常用消毒剂,具有灭活效率高、灭活效果稳定,操作简单等突出优势,因而也是自来水厂灭活剑水蚤等水生生物的首选消毒剂[11].研究者就NaClO对灭活水生生物开展了大量研究工作,内容涉及灭活动力学[12]、水质条件对灭活效果影响[13],以及操作条件优化[14]等.已有研究采用的CT值一般在70mg⋅min/L以下,虽然与自来水厂实际消毒操作条件接近,但考虑到剑水蚤对NaClO耐受性较强,将灭活CT值控制在70mg⋅min/L以内,可能无法对灭活动力学过程做出完整描述.此外,已有研究采用的剑水蚤种属、底质和灭活条件等不尽相同,导致结论也不尽相同.有研究[13]认为弱酸环境较弱碱环境,更有利于NaClO对剑水蚤的灭活;也有研究[11]表明pH值基本不会影响NaClO对剑水蚤的灭活效果.
同时,研究者普遍认为,NaClO灭活剑水蚤会增加自来水厂出厂水消毒副产物风险[13-14].紫外协同氧化剂消毒是常用的消毒副产物风险控制技术之一,经紫外预处理后,氧化消毒所需剂量大幅降低,有利于消毒副产物风险控制[15-16].USEPA(美国环保署)也把紫外协同氧化作为自来水厂贾地鞭毛虫和隐孢子虫灭活的推荐技术[17].作者前期研究表明[12],当紫外剂量为40mJ/cm2时,紫外预处理可将NaClO对蠕虫类水生生物的灭活反应活化能由8754J/mol降至7219J/mol[12].目前,尚未见关于紫外协同氧化灭活剑水蚤的相关报道.
本文拟将NaClO灭活剑水蚤的CT值范围适当增大,在此条件下,对灭活动力学过程进行系统分析,同时重点考察底质pH值和浊度对灭活作用的影响.此外,还探讨了NaClO灭活水蚤过程中,紫外协同氧化策略的可行性,旨在为自来水厂剑水蚤的高效灭活提供理论和技术依据.
1 材料与方法
1.1 实验材料
剑水蚤采自长沙市某自来水厂活性炭滤池反冲洗水,经鉴定剑水蚤为温中剑水蚤(Mesocyclops thermocyclopoides).从活性炭滤池反冲洗水中挑取具卵袋的剑水蚤,转移至8L自制培养箱.剑水蚤繁殖培养采用某校园内富营养化湖水,总磷约0.6mg/L,COD约10mg/L.培养箱温度控制在25℃,每天曝气4h,光照8h.每次实验时,从培养箱中取适量水置于10.5cm培养皿,用直径2mm的吸管挑取个体大小接近(约1mm),跳动活跃的成虫至所需数量,经蒸馏水清洗后备用.
NaClO溶液为分析纯,有效氯8%,采用0.1mol/L的磷酸盐缓冲溶液稀释配制成所需浓度的灭活溶液.
pH值调整通过滴加1mol/L的HCl或NaOH溶液来实现;浊度通过投加高岭土来控制;实验用水均为蒸馏水.
1.2 实验方法及装置
NaClO灭活实验在10.5cm培养皿中进行.pH值和浊度调整好的NaClO溶液,首先进行浓度测定,作为灭活初始浓度.在每个培养皿中加入60mL已知浓度灭活剂,每个培养皿中投放30个剑水蚤,并开始计时.每间隔一定时间对剑水蚤进行观测,通过剑水蚤的触角是否抖动来判别其是否存活,并将死亡的剑水蚤挑出,记录下存活数N.灭活完毕后,测定溶液NaClO浓度,作为灭活剂的最终浓度,NaClO浓度的变化按线性过程考虑.
紫外预处理在自制准平行紫外照射装置(如图1)中进行.紫外照射采用UV-C波段,波长253.7nm.紫外照射剂量20~200mJ/cm2.紫外照射完毕后,将剑水蚤全部转移至其它培养皿进行NaClO灭活,灭活操作同前.
除灭活动力学实验外,其余实验每组均重复3次.
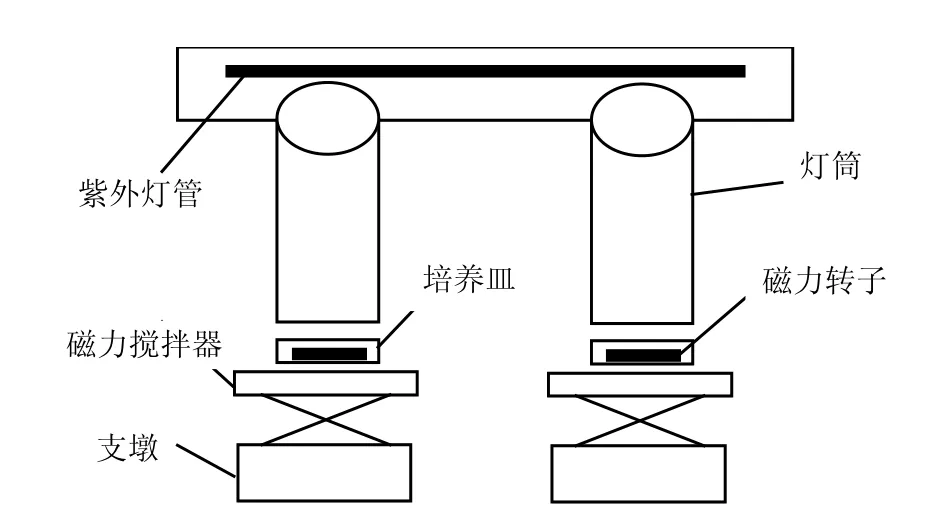
图1 紫外照射装置Fig.1 The ultraviolet radiation device
具体实验方案及灭活实验条件如表1所示.

表1 实验方案和灭活实验条件Table 1 Summary of tests and inactivation experimental conditions
1.3 指标测试和数据分析方法
NaClO浓度采用哈希DR900型便携式测定仪测定;pH值采用雷磁PHS-3C型酸度计测定;浊度采用WGZ-500B型浊度仪测定;紫外照射强度采用UV512C型紫外照度计测定.
灭活效果采用剑水蚤的对数存活率来评价.对数存活率以ln(N/N0)计,其中,N0是灭活反应初始阶段的剑水蚤的数目,N为灭活反应进行一定时间段之后,水样中存活剑水蚤数目.
采用Origin 9.0软件对灭活反应动力学实验数据进行线性拟合和分析.
2 结果与讨论
2.1 次氯酸钠对剑水蚤的灭活动力学过程
图2给出了不同初始浓度条件下,NaClO对剑水蚤的灭活动力学过程.当初始浓度为3~5mg/L时,相同CT值条件下,剑水蚤的灭活效率比较接近,灭活动力学过程符合迟滞型的两阶段准一级动力学过程[18]:
式中:k1和k2分别为准一级动力学过程第1和第2阶段的直线斜率;ln(N1/N0)和ln(N2/N0)分别为第1和第2阶段的直线在纵轴上的截距;CTlag为迟滞期对应的CT值;(N/N0)c为控制组剑水蚤的存活率;CT12为第1阶段和第2阶段分界处对应的CT值.当初始浓度为2mg/L时,呈现类似的灭活动力学过程,只是迟滞期变为慢速的准一级动力学过程,相应整个灭活过程演变为三阶段准一级动力学过程.
研究表明[18-21],NaClO灭活细菌和病毒,在一定条件下也呈两阶段准一级灭活动力学特征,且第一阶段灭活反应速率常数k1往往大于第二阶段反应速率常数k2.本研究中NaClO灭活剑水蚤为迟滞型两阶段准一级动力学过程,并且k1要小于k2.迟滞期的存在与剑水蚤体表甲壳有关,NaClO要灭活剑水蚤首先必须渗透体表甲壳,而体表甲壳对剑水蚤的保护能力,要远强于细胞壁对细菌或病毒衣壳对病毒的保护能力[13],因此CT值需达到一定水平后方能产生灭活效果.迟滞期现象在对贾地鞭毛虫[22]、隐孢子虫[18]和蠕虫类水生生物[12]的氧化灭活研究中也有报道.本研究中当NaClO初始浓度为3~5mg/L时,CTlag为80mg⋅min/L左右.至于k1小于k2,可能与剑水蚤体内抗氧化系统相关.水蚤体内含有丰富的过氧化氢酶(CAT)、超氧化物歧化酶(SOD)和金属硫蛋白(MT)等[23],由上述物质组成的抗氧化系统,有助于增强剑水蚤对NaClO的耐受性,当CT值超过CT12后,抗氧化系统被破坏,故灭活速率常数开始增加.而细菌、病毒等微生物不具备完整的抗氧化系统,部分敏感菌随CT值的增加可能变为抗性菌[20],因此在NaClO灭活过程中k1大于k2.
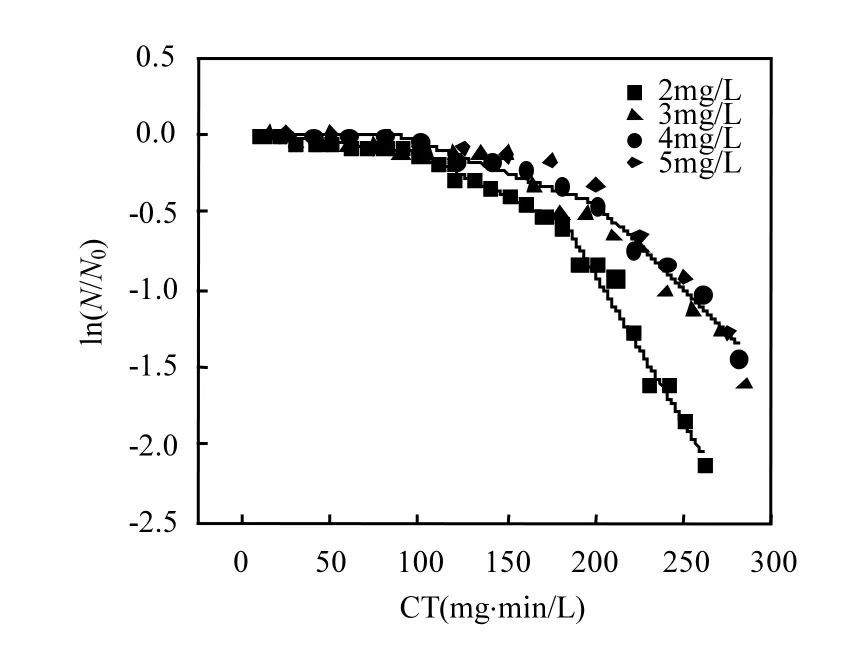
图2 不同初始浓度下NaClO对剑水蚤的灭活动力学过程Fig.2 The inactivation kinetics of Cyclops by NaClO under different initial concentrations
需指出的是,初始NaClO浓度为2mg/L时迟滞期消失,并且相同CT值的灭活率也要高于3~5mg/L时.实验中观察到,初始NaClO浓度为2mg/L时,剑水蚤在NaClO胁迫下立刻做大幅度快速跃动;初始NaClO浓度高于2mg/L后,则未见剑水蚤明显跃动.De Beer等[24]认为生物体表面与NaClO溶液之间存在固液边界层,NaClO向生物体内的渗透首先必须经过边界层;Perry和Chilton[25]的研究表明,NaClO的渗透通量与边界层厚度的平方呈反比.因此在低浓度情况下,剑水蚤的大幅度快速跃动有效降低了边界层厚度,NaClO向剑水蚤体内的渗透得到加强,故灭活效率要高于3~5mg/L时.
图3给出了不同温度下,NaClO对剑水蚤的灭活动力学过程.为便于灭活反应活化能的计算,采用迟滞型一阶段准一级灭活动力学模型对图3数据进行拟合,得到5℃、20℃和25℃时的灭活反应速率常数分别为0.01219、0.01328和0.0136,说明温度的提高有助于剑水蚤灭活效率的提升.图3同时表明,温度提升可大幅缩短迟滞期,这是因为温度提升可以促进NaClO向剑水蚤体内的渗透.

图3 不同温度下NaClO对剑水蚤的灭活动力学过程Fig.3 The inactivation kinetics of Cyclops by NaClOunder different temperatures
图4给出了NaClO灭活剑水蚤的反应速率常数Arrhenius图,拟合计算结果表明,实验条件下NaClO对剑水蚤的灭活反应活化能为3774J/mol.Fernando[22]和Corona-Vasquez等[18]分别采用NaClO对贾地鞭毛虫和隐孢子虫进行灭活,得到各自的灭活反应活化能分别为45788J/mol和68980J/mol;Churn等[26]研究表明NaClO对细小病毒H-1的灭活反应活化能为2400J/mol;作者前期研究发现[12],NaClO对饮用水中蠕虫类水生生物的灭活反应活化能为8754J/mol,从灭活反应活化能看,剑水蚤较贾地鞭毛虫、隐孢子虫和蠕虫类水生生物而言,更难于被NaClO灭活,但耐受性要强于细小病毒H-1.当然,由于上述研究采用的底质和灭活条件各不相同,该结论还有待进一步证实.

图4 NaClO灭活剑水蚤的反应速率常数Arrhenius曲线Fig.4 Arrhenius plot of rate constants for the inactivation of Cyclops by NaClO
2.2 pH值对剑水蚤灭活效果的影响
不同pH值条件下NaClO对剑水蚤的灭活动力学过程见图5.为便于计算比较,采用迟滞型一阶段准一级灭活动力学模型对图中数据进行拟合.经计算,pH值为6、7和8时的灭活反应速率常数分别为0.0093、0.0214和0.0203,说明在灭活期内,中性条件下灭活效率最高,碱性条件次之,酸性条件最低.对比相同CT值下的灭活率可以发现,中性条件灭活率要高于酸性和碱性;当CT值小于70mg⋅min/L时,酸性条件灭活率要高于碱性,超过70mg⋅min/L后则碱性要高于酸性.
pH值决定了NaClO溶液中HOCl和ClO-物质的量之比,因而是决定其消毒灭活效率的重要因素之一[27].研究表明[28],HOCl对微生物的灭活效率是ClO-的80倍左右,酸性环境被认为更利于NaClO对细菌、病毒等微生物的消毒灭活.但需要指出的是,上述结论可能只适合于消毒灭活接触时间较短的情况,即灭活CT值较小的范围,这是因为HOCl和ClO-在水中的化学稳定性差异较大.ClO-化学稳定性较好,而HOCl的化学稳定性取决于水溶液的pH值(表2)[27],pH值越高,HClO在水中的化学稳定性越好.

图5 不同pH值下NaClO对剑水蚤的灭活动力学过程Fig.5 The inactivation kinetics of Cyclops by NaClO under different pH

表2 HOCl在不同pH下衰减至1/10所需时间[27]Table 2 HOCl in different pH decay time required for 1/10[27]
综合考虑NaClO溶液pH值,以及HOCl和ClO-的灭活效率、化学稳定性可知,当灭活所要求的CT值较小(即灭活接触时间较短)时,pH值(以6、7和8为例)对NaClO溶液灭活效率的影响,以改变溶液中HOCl和ClO-物质的量之比为主,HOCl和ClO-的化学稳定性可以不予考虑,酸性条件下HOCl含量更高,因此灭活效率更高.饮用水的NaClO消毒所采用的CT值一般都比较小,故酸性条件下的消毒灭活效果更好.随着灭活时间的延长,pH值对NaClO溶液灭活效率的影响则以改变HOCl和ClO-的化学稳定性为主.假设灭活接触时间为60min,HOCl的灭活效率为1,根据表2可知pH值为6、7和8时,各自的灭活效率比大致为1:8:2.5,中性条件下灭活效率最高,碱性次之,酸性最差,这与本实验得到的结论较为一致.作者前期研究证实[12],在蠕虫类水生生物的NaClO灭活中,也是碱性条件下灭活效率要高于酸性条件.崔福义等[13]采用氯气灭活剑水蚤,氯气投加量2mg/L,灭活时间30min,当pH值小于6.5时灭活率达100%,而pH值为8时灭活率仅为50%.苏洪涛[11]的研究则表明,pH值在6.8~8范围内,有效氯浓度为2mg/L时,氯对剑水蚤的灭活效果几乎不受pH值影响.关于pH值对NaClO灭活剑水蚤的影响,相关研究者的研究结论不尽相同,可能正是由于各自所采用的灭活CT值存在较大差异所引起.
2.3 浊度对剑水蚤灭活效果的影响
为便于计算比较,采用两阶段准一级灭活动力学模型对图6中数据进行拟合.经计算,浊度为0.2、2和8时的灭活反应速率常数分别为0.0219、0.0196和0.0109,说明浊度物质的存在有助于提高剑水蚤对NaClO的耐受性.对比相同CT值下的灭活率可以发现,浊度越低,灭活率越高.由图6还可知,浊度的增加会导致慢速灭活的第一阶段延长,浊度为0.2、2和8时CT12分别为30、70和80mg⋅min/L.

图6不同浊度下NaClO对剑水蚤的灭活动力学过程Fig.6 The inactivation kinetics of Cyclops by NaClO under different turbidity
浊度物质对NaClO灭活细菌和病毒等微生物效果的抑制作用,在很多研究中已经得到证实[29-30],其抑制作用主要是因为很多微生物都是以粘附在浊度物质表面的形式存在于水中.本研究中,浊度物质的颗粒粒径要远小于剑水蚤,因此浊度物质对灭活效率的削弱,可能是由于浊度物质吸附在剑水蚤体表,从而阻碍了NaClO向剑水蚤体内的渗透过程.此外,液相主体中的浊度物质,也会迟滞NaClO从液相主体向剑水蚤体表边界层的传质过程,这也会对灭活效果造成一定影响.
2.4 紫外照射对NaClO灭活剑水蚤的影响

图7 紫外照射下NaClO对剑水蚤的灭活动力学过程Fig.7 The inactivation kinetics of Cyclops by NaClO following UV irradiation pre-treatment under different pH
实验中,当紫外照射剂量为20~200mJ/cm2时,单独紫外照射均未见有剑水蚤死亡现象,说明单独紫外照射对剑水蚤不具灭活效果.固定紫外照射剂量为40mJ/cm2,不同pH值条件下,紫外照射对剑水蚤灭活动力学过程的影响见图7.图7表明,紫外照射对NaClO灭活效果具有明显的强化作用.首先,经紫外照射后,灭活动力学曲线的迟滞期明显缩短(图7(a))或消失(图7(b)和7(c));其次紫外照射提高了灭活反应速率常数,pH值为6、7和8时,单独NaClO灭活的灭活反应速率常数分别为0.0093、0.02185和0.0206,经紫外照射预处理后,各自分别提高至0.0105、0.02673和0.0286.
在饮用水消毒中,紫外照射与NaClO联用对细菌和病毒等微生物具有协同效应,紫外照射可以起到强化NaClO灭活效果和减小药剂使用量的作用[31-32].本研究证实,对于剑水蚤的NaClO灭活,紫外照射同样可以起到强化作用.与细菌和病毒等微生物不同,剑水蚤等微型水生生物具有较坚硬的体壁,体壁中的脂质层对紫外照射的抵御能力非常强[33],因此单独紫外照射无法实现灭活.但紫外照射将对脂质层起到破坏作用,这有助于NaClO向剑水蚤体内的渗透,NaClO可以迅速透过剑水蚤体壁,因此灭活迟滞期消失或缩短,同时灭活反应速率常数增加.但紫外照射对剑水蚤脂质层的破坏作用如何,破坏程度是否与紫外照射剂量相关,这些都还有待进一步研究.
3 结论
3.1 NaClO对剑水蚤的灭活动力学过程符合迟滞型两阶段准一级动力学过程;灭活反应活化能为3774J/mol,说明剑水蚤对NaClO的耐受性一般要高于细菌和病毒,但低于贾地鞭毛虫、隐孢子虫和蠕虫类水生生物.
3.2 pH值对NaClO溶液灭活剑水蚤的影响,主要通过改变溶液中HOCl和ClO-物质的量之比,以及HOCl和ClO-的化学稳定性来实现.当灭活CT值超出一定水平后,中性条件下NaClO对剑水蚤的灭活效率最高,碱性次之,酸性最差.
3.3 浊度物质会迟滞NaClO从液相主体向剑水蚤体表边界层的传质过程,被剑水蚤体表吸附后也会阻碍NaClO向剑水蚤体内的渗透过程,因此对NaClO的灭活效果有削弱作用.
3.4 单独紫外照射无法实现对剑水蚤的灭活,但可以强化NaClO对剑水蚤的灭活效果.经紫外照射后,剑水蚤灭活迟滞期消失或缩短,同时灭活反应速率常数增加.
[1] 邢 宏.水处理工艺中剑水蚤的防治及水质生物评价 [J]. 净水技术, 2004,23(6):16-17.
[2] Ferreira L, Du Preez H H. Investigation into occurrence of aquatic invertebrates throughout drinking water purification plants [J]. Water Science & Technology: Water Supply, 2012,12(2):250-257.
[3] Wang Q, You W, Li X W, et al. Seasonal changes in the invertebrate community of granular activated carbon filters and control technologies [J]. Water Research, 2014,51(6):216-227.
[4] Francoise B, Benoit B, Yolanda D, et al. Role of predation by zooplankton in transport and fate of protozoan (oo)cysts in granular activated carbon filtration [J]. Water Research, 2010,44(4):1072-1081.
[5] 林 涛,曹 钰,陈 卫.饮用水处理中剑水蚤携带细菌的研究[J]. 华中科技大学学报(自然科学版), 2013,41(4):128-132.
[6] 赵志伟,崔福义,林 涛,等.二氧化氯对剑水蚤类浮游动物的灭活与去除 [J]. 环境科学, 2007,28(8):1759-1762.
[7] 孙兴滨,倪慧珊,宋弼尧.饮用水消毒过程中剑水蚤对生物稳定性的影响及变化规律 [J]. 净水技术, 2016,35(2):43-46.
[8] van Lieverloo J H M, Hoogenboezem W, Veenendaal G, et al.Variability of invertebrate abundance in drinking water distribution systems in the Netherlands in relation to biostability and sediment volumes [J]. Water Research, 2012,46(16):4918-4932.
[9] 刘冬梅,崔福义,吴雅琴,等.预氧化协同常规水处理工艺去除剑水蚤 [J]. 供水技术, 2007,1(1):32-34.
[10] Adam K, Heath R G M, Steynberg M C. Invertebrates as biomonitors of sand-filter efficiency [J]. Water SA, 1998,24(1):43-48.
[11] 苏洪涛.供水生产中水蚤类浮游生物控制技术研究 [D]. 长沙:湖南大学, 2007.
[12] Nie X B, Li Z H, Long Y N, et al. Chlorine inactivation ofTubifex tubifexin drinking water and the synergistic effect of sequential inactivation with UV irradiation and chlorine [J]. Chemosphere,2017,177(6):7-14.
[13] 崔福义,林 涛,刘冬梅,等.氧化剂对剑水蚤类浮游动物的灭活效能及影响 [J]. 哈尔滨工业大学学报, 2004,36(2):143-146.
[14] 刘冬梅,崔福义,吴雅琴,等.预氧化协同常规水处理工艺去除剑水蚤 [J]. 供水技术, 2007,1(1):32-34.
[15] Wang X J, Hu X X, Wang H B, et al. Synergistic effect of the sequential use of UV irradiation and chlorine to disinfect reclaimed water [J]. Water Research, 2013,46(4):1225-1232.
[16] Dykstra T S, O’Leary K C, Chauret C, et al. Impact of UV disinfection on biological stability in distribution systems [J].Journal of Environmental Engineering and Science, 2007,6:147-155.
[17] USEPA, Ultraviolet disinfection guidance manual. EPA 815-D-03-007, 2003.
[18] Corona-Vasquez B, Samuelson A, Rennecker J L, et al.Inactivation ofCryptosporidium parvumoocysts with ozone and free chlorine [J]. Water Research, 2002,36:4053-4063.
[19] 陈雨乔,段晓笛,陆品品,等.给水管网中耐氯性细菌的灭活特性研究 [J]. 环境科学, 2012,33(1):104-109.
[20] 张 云.三种含氯消毒剂灭活饮用水中病毒的效果及其表观动力学研究 [D]. 上海:复旦大学, 2011.
[21] Zhang B, Luo YG, Zhou B, et al. A novel microfluidic mixer-based approach for determining inactivation kinetics of Escherichia coli O157: H7 in chlorine solutions [J]. Food Microbiology, 2015,49:152-160.
[22] Fernando W J N. Theoretical considerations and modeling of chemical inactivation of microorganisms: Inactivation of Giardia Cysts by free chlorine [J]. Journal of Theoretical Biology, 2009,259:297-303.
[23] 汤保华.三种新型杀菌剂对水生蚤类动物影响的初步研究 [D].乌鲁木齐:新疆农业大学, 2005.
[24] De Beer D, Srinivasan R, Stewart P S. Direct measurement of chlorine penetration into biofilms during disinfection [J]. Applied and Environmental Microbiology, 1994,60:4339-4344.
[25] Perry R H, Chilton C H. Chemical engineers’ handbook [M]. 5th ed. McGraw-Hill, New York, 1973.
[26] Churn C C, Boardman G D, Bates R C. The inactivation kinetics of H-1parvovirus by chlorine [J]. Water Research, 1984,18:195-203.
[27] Granum P E, Magnussen J. The effect of pH on hypochlorite as disinfectant [J]. International Journal of Food Microbiology,1987,4:183-186.
[28] Bremer P J, Monk I, Butler R. Inactivation ofListeria monocytogenes/Flavobacteriumspp. biofilms using chlorine:impact of substrate, pH, time and concentration [J]. Letters in Applied Microbiology, 2002,35:321-325.
[29] Winward G P, Avery L M, Stephenson T, et al. Chlorine disinfection of grey water for reuse: Effect of organics and particles [J]. Water Research, 2008,42:483-491
[30] Berman D, Rice E W, Hoff J C. Inactivation of particleassociated coliforms by chlorine and monochloramine [J].Applied and Environmental Mirobiology,1988,54:507-512
[31] Lyon B A, Cory R M, Weinberg H S. Changes in dissolved organic matter fluorescence and disinfection byproduct formation from UV and subsequent chlorination/chloramination [J]. Journal Hazardous Materials, 2014,264:411-419.
[32] Shang C, Cheung L M, Liu W. MS2coliphage inactivation with UV irradiation and free chlorine/monochloramine [J].Environmental Engineering Science, 2007,24:1321-1332.
[33] Valacchi G, Weber S U, Luu C, et al. Ozone potentiates vitamin E depletion by ultraviolet radiation in the murine stratum corneum[J]. Febs Letters, 2000,466:165-168.
