Ru/改性蛭石制备及催化马来酸酯加氢性能研究
2018-02-20韩燕絮徐天晓
王 磊 ,韩燕絮 ,徐天晓 ,刘 浪 *
(1.新疆大学 化学化工学院,新疆 乌鲁木齐 830046;2.新疆大学 应用化学研究所 能源材料化学教育部重点实验室,新疆 乌鲁木齐 830046)
丁二酸二甲酯(DMS)作为重要的有机化工原料及中间体,主要用于医药、食品工业等,也是合成生物可降解塑料聚丁二酸丁二醇酯(PBS)的重要原料之一,其合成工艺主要包括以丁二酸和甲醇为原料的酯化法[1]及马来酸二甲酯为原料的催化加氢法[2-3]。与酯化法相比,催化加氢法工艺流程简单,所得产品纯度高,但通常需要在较高温度或较高压力下进行。针对该问题,本课题组开展绿色马来酸酯催化加氢工艺研究工作。实验结果显示,采用吸附-沉淀法制备Ru/Al2O3催化剂在70℃、1.0MPa条件下,可高效地实现马来酸二甲酯加氢合成DMS,原因是在催化剂制备过程中高效地去除了其中残留的氯,同时活性组分在催化剂载体上保持较高分散度[4]。但是研究发现催化剂Ru/Al2O3热稳定性差,经再次氧化-还原处理后出现严重烧结,催化活性急剧降低。
载体对催化剂的活性与稳定性具有非常重要的影响。蛭石是一种天然粘土矿物,属于2∶1型层状硅酸盐结构,具有较好的阳离子交换能力,而且结构层具有胀缩性,层间距会随着层间物质类型和状态的变化而变化,这种特殊结构的材料为嵌入纳米级金属颗粒提供了较为理想的环境,是一种理想的催化剂载体[5]。代斌等[6]采用碳改性膨胀蛭石为载体制备HgCl2催化剂用于乙炔的氢氯化反应,乙炔的转化率达到97.3%,氯乙烯的选择性为100%。侯震山等[7]以改性蛭石为载体制备了高度分散的Ni催化剂用于甲烷与二氧化碳的重整反应,其催化活性、稳定性优于催化剂Ni/Al2O3,原因是在高温条件下改性蛭石的层间结构依然保持稳定,其层间限域作用可以有效稳定活性组分Ni。蛭石独特的层间限域作用及高稳定性对改善蛭石基复合材料的催化性能具有重要作用。
在文献调研与实验室前期研究工作基础上,本文利用蛭石层间距的可调变特性,通过对蛭石原矿进行改性,获得有机柱撑蛭石。以有机柱撑蛭石为载体,RuCl3·xH2O为活性组分前驱体,Na2CO3为沉淀剂,采用吸附-沉淀法制备出负载型Ru催化剂,结合TPO-TPR技术及XRD、BET表征手段,以马来酸二甲酯加氢合成DMS为探针反应,考察Ru/m-V的催化性能及氧化还原稳定性,并与采用相同方法制备的Ru/Al2O3进行比较。
1 实验部分
1.1 试剂与仪器
Al2O3,600℃焙烧;蛭石,采自新疆尉犁且干布拉克蛭石矿;硝酸、无水碳酸钠、十六烷基三甲基溴化铵、硝酸银、马来酸二甲酯、无水甲醇、盐酸,分析纯;RuCl3·xH2O,w(Ru)=37%;氢气、氮气、氧气,φ=99.999%。
精密电子天平,上海精密仪器仪表有限公司;DF-101S集热式恒温加热磁力搅拌器,郑州长城科工贸有限公司;SHB-III循环水式多用真空泵,郑州长城科工贸有限公司;101型电热鼓风干燥箱,北京市永光明医疗仪器有限公司;200 mL高压反应釜,南通博润石油科技有限公司;FINETEC-3010程序升温吸附仪,浙江泛泰仪器有限公司,德国布鲁克AXS有限公司的D8-ADVANCE型X射线衍射仪;美国Quantachrome公司的ASIQM0002-6自动物理吸附仪;美国FEI公司Tecnai G2 F20场发射透射电子显微镜。
1.2 催化剂制备
1.2.1 有机改性蛭石(m-V)制备
将5g蛭石原矿粉体分散于50mL的0.1mol/L硝酸溶液中,95℃搅拌4h后抽滤、洗涤至滤液呈中性为止,滤饼60℃干燥4h后研磨得酸化蛭石粉体;然后,将酸化蛭石粉体与1.5moL/L的Na2CO3溶液混合,制成质量分数为15%的蛭石矿浆。100℃搅拌4h后抽滤,洗涤至滤液呈中性为止。滤饼80℃干燥4h后研磨得到酸化钠化蛭石样品。最后,将其按1g∶16mL的比例分散于蒸馏水中,搅拌10min后加入一定计量的十六烷基三甲基溴化铵 (C16TAB)溶液。60℃搅拌2h,静置2h后抽滤,洗涤滤饼至无Br-为止(用0.1mol/L AgNO3检测滤液)。滤饼80℃干燥至恒重,研磨筛分,得到有机改性蛭石样品,记为m-V。
1.2.2 Ru/m-V催化剂制备
分别以Al2O3和有机改性蛭石(m-V)为载体制备负载型Ru基催化剂,具体操作步骤如下:称取2g m-V(或Al2O3)样品加入到50mL蒸馏水中,充分搅拌分散1 h,然后将计量的Ru盐溶液加入到上述悬浮液中,30℃搅拌3h,加入0.1mol/L Na2CO3溶液调节pH至9~10,继续恒温搅拌3 h,静置过夜,抽滤,洗涤至滤液呈中性,经0.1mol/L AgNO3检测无沉淀生成。最后,120℃恒温干燥,得催化剂Ru/m-V-fresh(或Ru/Al2O3-fresh)。新制Ru基催化剂经不同预处理过程并命名,具体如表1所示。
1.3 催化性能评价
将100.0mg催化剂、5.0g马来酸二甲酯和45mL甲醇依次加入到高压反应釜中,密封后先用氮气吹扫釜内空气,然后充H2至1.0MPa,温度达到70℃后,启动搅拌器。反应过程中,维持压力、温度及转速恒定,由气体质量流量计记录反应过程中的瞬时耗氢量与累计耗氢量。待反应结束后,使反应釜冷却至室温后卸压、对反应后混合物进行分析。马来酸二甲酯转化率的计算公式为:

2 结果与讨论
2.1 催化剂及改性蛭石XRD表征

图1 蛭石原矿(A)及有机柱撑蛭石(B)的XRD谱图
图1为原矿蛭石与改性蛭石XRD谱图。图1A中,2θ在 5.96°和30.16°的衍射峰为蛭石的特征衍射峰。蛭石作为一种天然的层状黏土矿物,其特殊的结构层具有可调变性,层间距会随着进入层间物质的类型和状态的变化而变化。经酸化-柱撑后蛭石的XRD谱图如图1B所示。经有机改性后,(001)的特征衍射峰移至2.42°,根据布拉格公式可以计算出柱撑蛭石的层间距为4.09nm。以上结果说明,经改性后蛭石仍保留完整的层状结构,由于有机阳离子的插入,其层间距增大。

图2 Ru催化剂XRD谱图
负载型催化剂XRD结果如图2所示。由图可知,在焙烧-还原处理后的催化剂Ru/m-V-O、Ru/Al2O3-O、Ru/m-V-N、Ru/Al2O3-N均出现了金属Ru的特征衍射峰,但直接还原活化后的催化剂上未检测到金属Ru的特征衍射峰,这说明直接还原活化催化剂上活性组分的粒径较小或者是以无定型状态存在的,而焙烧后在此活化的催化剂其结晶度较高。比较Ru/Al2O3-N-Ru/m-V-N还可以发现,采用蛭石为载体的催化剂经氮气焙烧再还原后的Ru/m-VN上未见活性组分Ru的特征衍射峰,催化剂Ru/Al2O3-N在2θ为44.01°处出现金属Ru特征衍射峰。在空气中焙烧-还原催化剂上也可以观测到Ru/Al2O3-O上金属Ru的衍射峰峰形尖锐而Ru/m-V-O上金属Ru的衍射峰较为宽化。这说明活性组分在蛭石载体上的热稳定性优于在Al2O3上的稳定性。
催化剂Ru/Al2O3-O4H上,2θ在44.01°处为金属Ru的特征衍射峰(PDF No.06-0663),峰形尖锐。与Ru/Al2O3-O4H相比,Ru/m-V-O4H上金属Ru特征衍射峰宽化弥散。以上结果说明,以有机蛭石为载体的Ru催化剂氧化还原稳定性高于催化剂Ru/Al2O3。
2.2 载体N2物理吸附-脱附分析
载体Al2O3和m-V的N2吸附-脱附曲线如图3所示。由图3可知,载体Al2O3和m-V均为典型的IV型吸附-脱附等温线,具有介孔材料的特征但孔径分布不均一。由表2数据可以看出,载体Al2O3与m-V孔结构存在显著差异,平均孔径分别为9.62nm和4.23nm。其中,样品m-V在相对压力接近1.0处存在垂直尾翼,说明载体有机蛭石中除介孔外还存在大孔。

图3 不同载体材料的吸附-脱附曲线
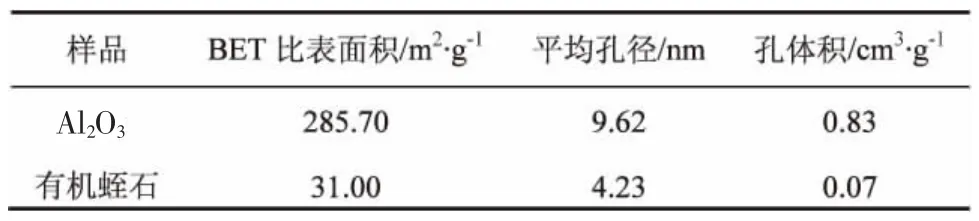
表2 Ru催化剂的比表面积、孔径及孔体积分析结果
2.3 催化剂H2-TPR表征
催化剂H2-TPR结果如图4所示。Ru/m-V-fresh仅在100℃有一个还原峰,峰形尖锐,对称性好,对应Ru(OH)x的还原[4]。而Ru/Al2O3--fresh还原温区较宽并且还原温度低于Ru/m-V-fresh。经焙烧处理后的催化剂上所对应的还原峰为RuOx的还原峰。采用空气处理的Ru/m-V的还原温度在129℃,高于经过相同过程处理的Ru/Al2O3的还原温度。以上结果说明Ru物种在不同载体上的分布状态各异,其与蛭石的相互作用高于Al2O3。氮气气氛焙烧后Ru/m-V还原温度在68℃。对于样品Ru/Al2O3,氮气气氛焙烧后所得氧化物在50~150℃范围内连续出现还原峰,低温时还原峰强度低,高温时还原峰强度高。上述结果可能是由于Ru(OH)3在氮气气氛中发生歧化反应生成RuOx和Ru导致的[8]。结合XRD的结果分析,由于Ru(OH)3与蛭石载体作用较强,且分布状态均一,焙烧过程中生成的RuOx与Ru均不会发生明显聚集,易于还原。Ru/Al2O3在氮气气氛焙烧后,由于与载体的作用较弱发生聚集同时分布状态不均一,因此还原峰温度向高温移动。XRD的结果也显示,Ru/Al2O3经氮气焙烧还原后,结晶程度增大。
为考察Ru催化剂的氧化还原稳定性,将直接还原活化催化剂再次氧化后进行程序升温还原。二者与新鲜催化剂相比,还原温度均向高温移动。催化剂Ru/m-V-O4H的还原温度在110℃,略高于Ru/Al2O3-O4H的还原温度。结合XRD分析结果可知,以蛭石为载体的催化剂的氧化还原稳定性优于Ru/Al2O3,原因是层状粘土的特殊结构提高了其与活性组分的相互作用,这也是导致还原温度升高的原因。
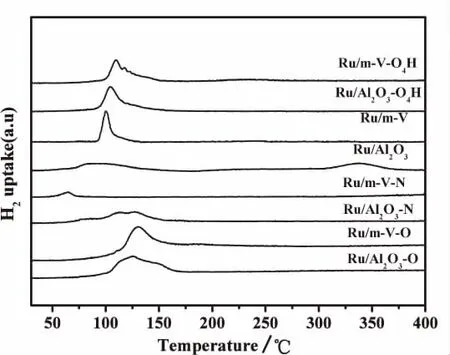
图4 不同气氛焙烧后Ru催化剂的H2-TPR谱图
2.4 催化剂活性评价
在排除内扩散和外扩散的影响,反应温度70℃,氢气压力 1.0MPa,搅拌速率600r/min下,以马来酸二甲酯为底物,甲醇为溶剂,考察了不同过程处理后催化剂的加氢活性,结果如图5所示。其中反应后分析测试显示,所有催化剂上DMS的选择性均达到了99%以上,因此可以用耗氢量定量计算DMM的转化率。
在催化剂Ru/m-V和Ru/Al2O3上,DMM的转化率在10min时均达到40%。在40min时,Ru/m-V上DMM转化率达到100%。催化剂Ru/Al2O3上DMM达到100%转化率所需时间为22min。由图可知,在反应初期 (10min内),以上两个催化剂上DMM单位时间内的转化率相同,随着反应进行,催化剂Ru/Al2O3的活性变化不大,但Ru/m-V的活性逐渐降低。结合催化剂的组织结构分析,由于Al2O3的平均孔径大于m-V,随着反应物浓度的降低,在Ru/m-V上的传质的阻力大于Ru/Al2O3,导致催化剂活性降低。

图5 Ru催化剂上马来酸二甲酯加氢活性
由XRD可知,由于焙烧后活性组分分散度降低,相同载体上经过焙烧还原后的催化剂活性低于直接还原活化催化剂的活性。由XRD及H2-TPR分析结果可知,改性蛭石载体与活性组分作用强于Al2O3,采用焙烧处理后Ru/m-V的分散性优于Ru/Al2O3。催化剂活性评价结果也显示:采用相同处理过程所获得Ru/m-V的活性高于Ru/Al2O3,与催化剂表征结果一致,进一步证实Ru/m-V催化剂的稳定性优于Ru/Al2O3。
直接还原后的催化剂经再次氧化还原,用于马来酸二甲酯加氢反应,其转化率-时间曲线结果如图5B所示。由图可知,蛭石负载Ru催化剂上单位时间内DMM的转化率高于Ru/Al2O3,。Ru/m-V上达到30%转化率所需时间为18min,低于Ru/Al2O3催化剂25min。以上结果进一步证实了Ru/m-V催化剂的氧化还原稳定性优于Ru/Al2O3,原因是Ru/m-V催化剂上活性组分的分散程度优于Ru/Al2O3。
3 结论
原矿蛭石经结构修饰和有机柱撑改性后,其层状结构完整且层间距增大到4.09nm,该特性为负载金属颗粒提供理想的空间环境。催化剂活性评价结果显示,在相同条件下,Ru/m-V催化剂的活性高于Ru/Al2O3。直接还原活化所得催化剂的催化活性高于焙烧还原所得催化剂,原因是经过焙烧后活性组分在载体上聚集,分散度降低。Ru/m-V直接还原活化催化剂的氧化还原稳定性优于Ru/Al2O3。结合H2-TPR,XRD,氮气物理吸-附脱附的表征结果可以得出,以有机柱撑蛭石为载体的催化剂,由于蛭石特殊层间结构,增强了活性组分与载体的相互作用,改善了其热稳定性,提高了氧化还原稳定性。该研究可为改善催化剂稳定性提供一条新的路径。
