燃烧法制备Zr、Sm双助剂Ni/γ-Al2O3甲烷化催化剂
2018-02-20胡天益马宏方钱炜鑫张海涛应卫勇
胡天益,马宏方,钱炜鑫,张海涛,应卫勇
(华东理工大学化工学院大型工业反应器工程教育部工程中心,化学工程联合国家重点实验室,上海 200237)
随着世界范围内环保意识的提高,提高化石燃料的利用效率日益突出。由于我国富煤、贫油、少气的能源结构,发展将煤转变成清洁能源的技术显得尤为重要,而天然气高热值、无污染的优点恰恰符合我国的能源转变战略,随着城镇化的发展,天然气需求的增速远远大于其产量的增速[1]。煤制天然气不仅可以减少直接燃烧煤所带来的污染,还能缓解我国天然气供应不足的压力[2]。
合成气甲烷化技术是在1902年由Sabatier和Senderens首次发现,利用Ni催化剂催化CO和H2反应生成CH4[3]。此后,甲烷化得到了世界各国学者们的广泛关注。在已知的甲烷化催化剂中,钌基催化剂表现出最高的催化活性,但钌属于稀有金属,其成本较高,所以商业化的可能性不高[4]。镍基催化剂在甲烷化反应表现出较好的催化活性,而且价格适中,因此在甲烷化反应的研究中得到了普遍的应用[5,6]。
ZrO2因为具有氧化还原性和酸碱性而被广泛的应用于催化领域[10],ZrO2的引入可以提高活性组分分散度,减小晶粒尺寸,改变载体和活性组分之间的相互作用,从而提高催化剂的催化活性和选择性等[11]。Luo等[12]在Ni基催化剂中引入Sm元素能够有效提高CO甲烷化的催化活性和热稳定性等;盛茵等[13]在Ni基催化剂中添加Sm2O3能提高活性组分的分散度以及抑制Ni晶粒的增长。本文利用溶液燃烧法制备添加Zr、Sm单助剂以及Zr、Sm双助剂的Ni/γ-Al2O3甲烷化催化剂,考察了Zr、Sm对CO甲烷化的催化活性,并用 BET、XRD、TEM、H2-TPR、CO-TPD对催化剂进行表征。
1 实验部分
1.1 催化剂的制备
催化剂中Ni的质量分数为30%,采用溶液燃烧法制备。将一定量的 Ni(NO3)2·6H2O,Al(NO3)3·9H2O溶解在200mL的二乙二醇中,制备5份,在其中一份中加入一定量的Sm(NO3)3·6H2O,使得助剂Sm在催化剂中质量分数为2%,在另外四份中加入一定量的 Sm(NO3)3·6H2O 和 Zr(NO3)4·5H2O,使得 Zr在催化剂中的质量分数为2%,Sm质量分数依次为0%,2%,4%,6%。在70℃的条件下持续搅拌2h至前驱体全部溶解,然后转移到马弗炉中从70℃升到700℃,升温速率为2℃ /min,溶液达到700℃后恒温6h,之后自然冷却到室温,取出催化剂研磨后使用。只含单助剂的催化剂记为Ni-2Zr和Ni-2Sm,含双助剂的催化剂记为Ni-xZrySm(x、y分别为Zr和Sm的质量分数)。
1.2 催化剂表征
1.2.1 N2低温吸附
催化剂低温吸附是在美国Micromeritics公司的ASAP2020低温吸附仪上测定的。将样品装入测试管后,在350℃下预处理4h除去水蒸气等杂质。比表面积由Brunauer-Emmet-Teller(BET)在相对压力(p/p0)为0.1~0.3之间计算得出,孔容和平均孔径则利用Barrett-Joyner-Halenda方法计算得出。
1.2.2 XRD
样品晶相分析采用日本Rigaku公司的D/Max 2550 X射线衍射仪。采用CuKα射线,扫描电压为40kV,电流为 100mA,扫描角范围为 10~80°,步长为 0.02°。
1.2.3 H2-TPR和CO-TPD
H2-TPR及CO-TPD采用美国Micromeritics公司的AutoChemII 2920化学吸附仪测定。H2-TPR测定步骤:称取0.1g样品放入U型石英管中,在氩气的气氛下加热至350℃并维持1h,然后自然冷却至室温,切换j(H2)=10%的H2/Ar混合气,以10℃/min的升温速率加热至1000℃,通过TCD测量H2含量变化。
3.1 小米的功效与作用 小米又名白粱粟、粢米、粟谷、硬粟、籼粟、谷子、寒粟、黄粟和稞子等,为禾本科植物粱或粟的种仁,我国南北各地均有栽培。小米的营养价值很高,含有丰富不饱和脂肪酸、大量的维生素E、铁和磷等微量元素。中医认为,小米味甘咸,有清热解毒,健脾除湿,和胃安眠等功效,还具有和中益胃,滋阴养血的作用,小米表面的小米黄色素具有抑制金黄色葡萄球菌和铜绿假单胞菌作用。
CO-TPD测定步骤:将0.2g的样品在600℃下用H2还原2h,待样品冷却至室温后切换至CO进行吸附1h,然后切换为Ar吹扫1h出去物理吸附的CO,之后在Ar气氛围下以 10℃/min的速率升温至600℃,通过TCD测量CO含量。
1.2.4 TEM
TEM采用JEOL JEM-2100型透射电镜。将样品加入无水乙醇中,利用超声振荡30min使样品在乙醇中均匀分散,取样滴加在铜网上,经过红外干燥再进行观察。仪器的操作电压为200kV。
1.3 催化剂活性考评
催化剂考评在固定床反应器中进行,反应管尺寸为 14×2×500mm。称取 60~80 目催化剂 0.5g,在反应管上下两端对称填入不同粒度的石英砂,使得催化剂的装填位置处于恒温区。通入氮气以2℃/min的升温速率将催化剂加热至700℃,切换氢气还原催化剂2h,接着切换氮气将催化剂冷却至反应所需温度,待温度稳定后,切换至合成气(j:CO 17.4%,CO28.8%,H267.6%,N26.2%),催化剂的低温活性在220~320℃的温度范围内测定,反应压力为2MPa,反应空速为 12000 mL·g-1·h-1。
2 结果与讨论
2.1 N2低温吸附
对催化剂进行N2低温吸附表征,结果如表1所示,从表1可以看出,相比于单助剂催化剂,双助剂催化剂的比表面积、孔容、孔径都有所下降,并且随着助剂含量的增加而逐渐减小,这可能是催化剂表面上的Zr物种和Sm物种导致的比表面积减小,同时有可能有一部分助剂物种堵塞孔道而导致孔容孔径的下降。

表1 催化剂物理结构性质Table 1 Physical structure and property of catalysts
2.2 XRD
图1是催化剂的XRD图谱,NiO的衍射峰位于37.3°、43.2°、62.9°和 75.3°,NiAl2O4尖晶石的峰位于19.1°、31.4°、 37.2°、 45.2°、 59.7°和 65.8°,NiAl2O4尖晶石对甲烷化反应没有催化活性,且在较高温度下也难以被还原[14]。图1中并没有出现Zr或Sm物种的特征衍射峰,说明Zr和Sm含量较低且可能高度分散在催化剂表面从而无法被XRD检测出相应衍射峰。
从图1中可以看出,相比于单助剂催化剂,双助剂催化剂 Ni-2Zr2Sm 在 45.2°和 65.8°处的 NiAl2O4尖晶石衍射峰明显减小,说明Zr、Sm双助剂的添加可以削弱Ni与载体之间的相互作用,从而减少NiAl2O4尖晶石的产生,而随着双助剂中Sm含量的增加,NiAl2O4尖晶石衍射峰进一步减少。

图1 Ni-2Zr、Ni-2Sm、Ni-2Zr2Sm、Ni-2Zr4Sm、Ni-2Zr6Sm催化剂XRD图谱Fig.1 XRD patterns of catalysts:Ni-2Zr,Ni-2Sm,Ni-2Zr2Sm,Ni-2Zr4Sm,Ni-2Zr6Sm
2.3 TEM
对还原后的催化剂进行TEM表征,结果如图2所示,Ni颗粒平均粒径列于表1。从图2中可以看出,五个催化剂中没有出现Ni团聚的现象,且Ni颗粒均匀地分散在催化剂表面。Ni-2Zr、Ni-2Sm、Ni-2Zr2Sm、Ni-2Zr4Sm、Ni-2Zr6Sm的平均粒径分别为16.0nm、15.2nm、12.8nm、12.5nm、11.7nm, 与单助剂催化剂相比,双助剂催化剂具有更小的Ni颗粒平均粒径,说明双助剂能更有效地抑制Ni颗粒的聚集。

图2 Ni-2Zr、Ni-2Sm、Ni-2Zr2Sm、Ni-2Zr4Sm、Ni-2Zr6Sm催化剂TEM图Fig.2 TEM images of catalysts:Ni-2Zr,Ni-2Sm,Ni-2Zr2Sm,Ni-2Zr4Sm,Ni-2Zr6Sm
2.4 H2-TPR
NiO物种一般被分为三种类型:α-NiO、β-NiO和γ-NiO[15-18]。α-NiO对应H2-TPR中低温还原峰(<500℃),与Al2O3相互作用较弱,在高温下还原所得Ni颗粒容易团聚;β-NiO对应中温还原峰 (500~800℃),与载体相互作用较强,在高温下还原所得Ni颗粒尺寸较小,且分散性较好;γ-NiO对应高温还原峰 (>800℃),与载体的相互作用强,也就是NiAl2O4尖晶石结构,在高温下也较难还原。H2-TPR表征结果如图3所示,从图3中可以看出,五个催化剂均没有出现明显的α-NiO对应的低温还原峰,可能是由于剧烈的燃烧过程,导致NiO与载体之间较强的相互作用。相比于单助剂催化剂,当添加Zr、Sm双助剂后,NiO的还原峰均朝着低温方向移动,说明Zr、Sm双助剂的添加能削弱NiO与载体之间的相互作用,抑制NiAl2O4尖晶石的生成。Ni-2Zr2Sm催化剂中β-NiO含量最多,而低温催化活性的Ni主要来自于β-NiO的还原。

图3 Ni-2Zr、Ni-2Sm、Ni-2Zr2Sm、Ni-2Zr4Sm、Ni-2Zr6Sm催化剂H2-TPR图谱Fig.3 H 2-TPR profiles of catalysts:Ni-2Zr,Ni-2Sm,Ni-2Zr2Sm,Ni-2Zr4Sm,Ni-2Zr6Sm
2.5 CO-TPD

图4 Ni-2Zr、Ni-2Sm、Ni-2Zr2Sm、Ni-2Zr4Sm、Ni-2Zr6Sm催化剂CO-TPD图谱Fig.4 CO-TPD profiles of catalysts:Ni-2Zr,Ni-2Sm,Ni-2Zr2Sm,Ni-2Zr4Sm,Ni-2Zr6Sm
催化剂的CO-TPD图谱如图4所示。160℃处的脱附峰为催化剂表面弱吸附的CO[19],在300℃以上的脱附峰为参与甲烷化反应的CO[20]。双助剂催化剂的CO脱附峰温度比单助剂催化剂更高,说明双助剂催化剂拥有更强的CO吸附能力,且其300℃以上的脱附峰面积均比单助剂催化剂大,说明双助剂催化剂有更多的CO吸附活性位,而这可能是因为双助剂催化剂的Ni颗粒粒径更小。随着Sm助剂含量的增加,催化剂的CO吸附性能并没有明显改变。
2.6 催化剂活性考察

图5 Ni-2Zr、Ni-2Sm、Ni-2Zr2Sm、Ni-2Zr4Sm、Ni-2Zr6Sm催化剂上CO转化率Fig.5 CO conversion over catalysts:Ni-2Zr,Ni-2Sm,Ni-2Zr2Sm,Ni-2Zr4Sm,Ni-2Zr6Sm
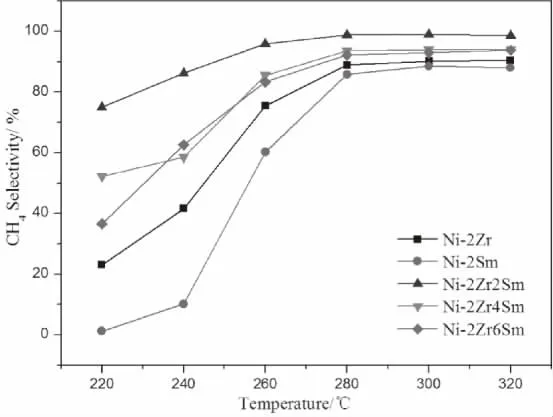
图6 Ni-2Zr、Ni-2Sm、Ni-2Zr2Sm、Ni-2Zr4Sm、Ni-2Zr6Sm催化剂上CH4选择性Fig.6 CH 4 selectivity over catalysts:Ni-2Zr,Ni-2Sm,Ni-2Zr2Sm,Ni-2Zr4Sm,Ni-2Zr6Sm
图5 和图6分别为催化剂上CO转化率和CH4选择性随温度变化曲线。从图5、6中可以看出,随着温度的升高,CO转化率和CH4选择性均逐渐升高,同一温度下,双助剂催化剂的CO转化率和CH4选择性均高于单助剂催化剂,可能是因为双助剂催化剂高温还原后得到Ni颗粒粒径更小,有更多的活性位。在双助剂催化剂中,Ni-2Zr2Sm在同一温度下有着更高的CO转化率和CH4选择性,可能是其含有更多的β-NiO。
2.7 高温稳定性考评
Ni-2Zr2Sm催化剂的低温活性最好,对Ni-2Zr2Sm、Ni-2Zr和Ni-2Sm高温稳定性进行测试,考察单、双助剂催化剂的高温稳定性差异,结果如图7所示。从图7可以看出,在经过50h的高温稳定性测试后,三个催化剂均没有失活,表现出良好的高温稳定性,可能是因为燃烧法制备的催化剂中Al2O3将Ni颗粒阻隔,抑制了Ni颗粒的团聚烧结[6]。Ni-2Zr2Sm在高温稳定性测试中表现出最好的催化活性,CO转化率约为92.5%,Ni-2Zr和Ni-2Sm的CO转化率分别约为89.2%和85.2%。

图7 Ni-2Zr、Ni-2Sm、Ni-2Zr2Sm高温稳定性测试Fig.7 Stability test of catalysts:Ni-2Zr,Ni-2Sm,Ni-2Zr2Sm
3 结论
采用燃烧法制备了Ni/γ-Al2O3催化剂,考察了Zr、Sm单助剂和双助剂对甲烷化催化活性的影响,利用氮气低温吸附、XRD、TEM、H2-TPR和CO-TPD对催化剂进行了表征。Zr、Sm双助剂催化剂相比于单助剂催化剂能更有效地抑制NiAl2O4尖晶石的产生,含有更多的β-NiO,在高温下还原能得到粒径较小的Ni颗粒,从而提供更多的活性位,提高了CO甲烷化催化性能;Ni-2Zr2Sm具有最好的低温活性和较好的高温稳定性。
