卵巢甲状腺肿的影像学表现与误诊分析
2018-02-20丁维磊
吴 琛 路 莉 张 敏 丁维磊 徐 凯
卵巢甲状腺肿(struma ovarii, SO)是一种起源于生殖细胞的成熟性畸胎瘤,是单胚层畸胎瘤最常见的类型,由全部或大部分甲状腺组织构成[1]。目前国内外关于此瘤的影像学表现的报道少见。本文回顾经手术病理证实的8例卵巢甲状腺肿病例,总结其影像表现,并分析误诊的原因,以期提高对SO的认识。
方 法
1.病例资料
搜集我院2011~2017年经手术病理证实的8例卵巢甲状腺肿病的患者资料。年龄34~66岁,平均(53.3±11.5)岁。5例患者因体检B超发现就诊,1例以腹胀就诊,1例以下腹痛就诊,1例因阴道不规则出血就诊。所有患者术前均行肿瘤指标检查,仅2例患者CA125升高并伴有中等量腹水,术前腹水病理检查未发现恶性肿瘤细胞。8例患者主诉及临床查体均无明显甲亢症状及体征,均无甲状腺癌病史。
2.检查方法
本组共8例SO,所有患者均行超声检查,同时其中有2例行CT检查,1例行MRI检查。
超声检查采用Siemens 2000彩色多普勒超声诊断仪,经腹部探头频率4MHz,经阴道探头频率8MHz。常规超声检查病变部位、大小、边界、回声特点及血供情况。
盆腔CT检查采用GE Lightspeed 16层螺旋CT扫描机,扫描参数:管电压120kV,管电流420~500mA,层厚及层间距均为5mm。增强扫描用高压注射器经肘静脉注入对比剂碘海醇(300mgI/ml)80 ~ 100ml, 注 射 速 率 为 3ml/s, 注 入 后20~30秒、60~70秒行动脉期和静脉期扫描。
盆腔MRI检查采用GE Signa 3.0T MR系统,MRI平扫行FSE序列矢状位T1WI,矢状位T2WI及T2WI压脂序列,轴位T2压脂序列。平扫参数:矢状位 T1WI:TR440ms,TE7.7ms,层厚 5mm,层间距 1mm。T2WI:TR4000ms,TE136.6ms;矢状位T2WI层厚5mm,层间距1mm;轴位T2WI层厚6mm,层间距2mm。MRI增强对比剂采用Gd-DTPA,剂量0.1mmol/kg经肘静脉以2ml/s流速高压注入。行轴位、矢状位、冠状位肝脏容积快速三维成像(liver acquisition with volume acceleration,LAVA)扫描。
3.图像分析
所有图像由1名放射科主治医师和1名主任医师采用盲法进行分析。观察内容包括肿块部位、大小、形态、有无分隔、有无实性成分、内部的密度/信号及强化程度、有无钙化,是否合并腹腔积液。
结 果
1.超声表现
8例SO均位于单侧卵巢,右侧4例,左侧4例。肿瘤最长径约4.2~9.8cm。1例超声检查为类圆形的强回声的实性肿块,边界尚清,探及丰富的血流信号,盆腔探及中等量积液。7例超声检查为囊实性肿块,表现为以囊性为主的混合性回声,形态不规则,实性部分均表现为稍高回声,其中仅4例实性成分探及呈点状或细条状的血流信号(图1);2例病灶中探及钙化灶;3例囊腔中探及多个囊壁间隔,并有血流信号;1例有大量腹水。
2.CT 表现
2例行盆腔CT检查者病灶均为囊实性肿块,在囊壁或实性成分中出现弧形状或点状钙化。1例行CT平扫及增强检查者,平扫时病灶内不同密度的囊腔,其中一高密度囊腔,CT值约63HU,增强后CT值无明显变化;实性成分平扫CT值84HU,增强后动脉期CT值为160HU,静脉期CT值为113HU(图2),呈明显强化;盆腔中可见大量积液。1例仅行CT增强患者实性成分动脉期CT值125HU,静脉期CT值约98HU。
3.MRI表现
1例行盆腔MRI检查,肿瘤内示多发大小不等囊性病变,囊腔内信号多变,部分呈T1W稍低信号、T2W极低信号,部分呈T1W稍低信号、T2W高信号。实性成分T1W及T2W均呈等信号。增强后实性成分及囊壁明显强化,呈“花边样”,囊性成分无强化(图1)。
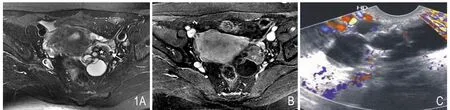
图1 女,51岁,左侧SO。A.为轴位T2压脂序列,B.为轴位LAVA增强序列。左侧附件区囊实性肿块,可见多发大小不等的囊性灶,实性成分(*)增强后实性成分及囊腔分隔明显强化,可见“花边征”。实性成分之间的部分囊腔(白箭)表现为T2WI极低信号的特性。C.为彩色多普勒超声,可见实性成分及囊壁间隔有血流信号。
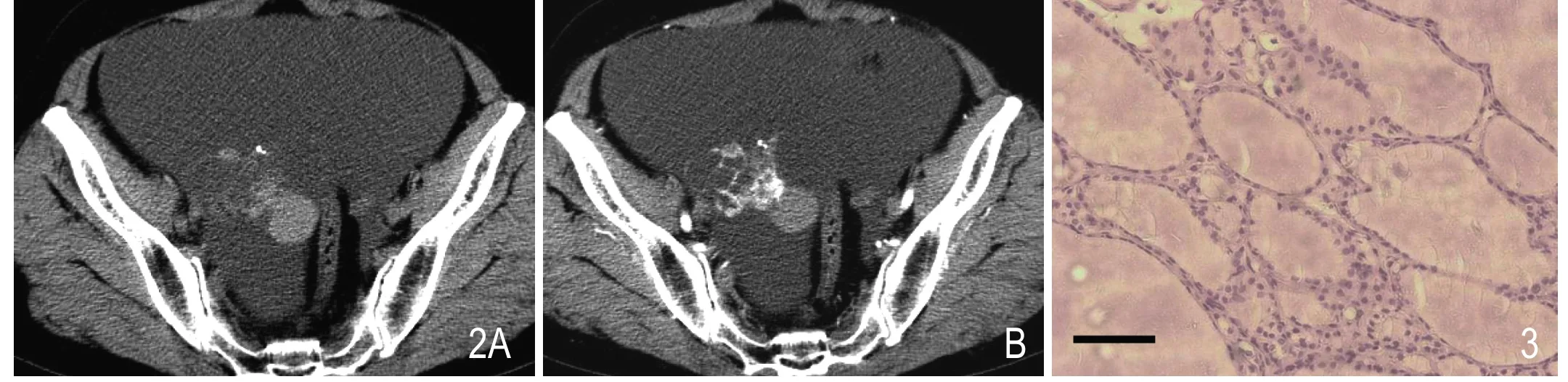
图2 女,62岁,右侧SO。A.平扫显示右侧附件区囊实性肿块,病灶内见高密度囊腔,囊腔内见线样分隔。实性成分内点状钙化。大量盆腔积液。B.增强检查囊性成分未强化,分隔及实性成分明显强化。图3 为SO的病理特征(HE染色,×200,Bar=100μm),镜下可见大小不等的甲状腺滤泡,滤泡被覆单层扁平细胞,滤泡内充满红染的胶质。
4.手术及病理表现
8位患者术中所见肿瘤与邻近组织无黏连,肿块包膜完整,表面光滑,部分呈分叶状。2例腹腔抽出淡黄色腹水。肿块最大径约4~9.8cm。8例肿瘤切面可见大小不一的囊腔,部分囊腔内含胶冻样物质,囊壁光滑,囊壁薄,厚约1~3mm。7例以囊性成分为主,仅1例以实性成分为主。有2例可见钙化灶。
镜下肿瘤为正常或增生性甲状腺组织,可见大小不等的滤泡组织,滤泡壁被覆单层柱状上皮或扁平上皮,滤泡腔可见嗜伊红染色的胶质。
病理结果:4例为卵巢甲状腺肿,3例为卵巢甲状腺肿合并对侧囊性畸胎瘤,1例为卵巢甲状腺肿合并黏液性囊腺瘤。
讨 论
1.SO 的临床
SO发病率较低,约占成熟性畸胎瘤的2.7%[2],临床较罕见,且患者多无特异性临床表现,故术前诊断较为困难。而且SO大多数是良性的,只有少部分(约0.3%~5%)出现恶性转化为卵巢恶性甲状腺肿,如甲状腺滤泡癌和乳头状癌,占卵巢肿瘤0.01%,畸胎瘤的0.3%。SO发病高峰期为50~60岁左右,极少发生在青春期[3]。SO多发生在单侧卵巢,瘤体一般较大,但最大径多<10cm。约15%~25%患者有颈部甲状腺肿大,5%~15%患者有甲状腺机能亢进症,手术后甲亢症状可迅速消退[4]。本组中因术前均未诊断为SO,故未行甲状腺功能的辅助检查。有文献报道约17%的SO患者有腹水或假Meigs征(即在出现腹水的同时伴有胸腔积液),甚至伴有血清CA125增高,但CA125的增高程度及胸腹腔积液的出现与肿瘤为恶性并无相关性[4-7]。本组中有2例SO出现腹水伴血清CA125异常升高,最高达1162U/ml。
SO的治疗为手术切除,术后通常不需要其他后续治疗,良性SO复发率极低,但对于合并腹水且肿瘤标志物较高的患者,应定期进行CA125检测及盆腔超声检查。本组8位患者均手术切除,术后病理均证实为良性SO,未进行其他后续治疗,随访复查未出现肿瘤复发。
2.SO的影像学表现与病理基础
根据2014年WHO肿瘤分类标准中,SO归为单胚层成熟性畸胎瘤,SO可出现与正常甲状腺上皮相同的组织学和病理学改变,如结节性甲状腺肿、甲状腺腺瘤、桥本甲状腺炎等改变;也可伴发囊性成熟性畸胎瘤、囊腺瘤、囊腺癌及类癌等[4],本组中有3例伴发对侧囊性畸胎瘤,1例合并黏液性囊腺瘤。
根据SO的病理特点,综合本组研究及相关文献,总结SO的特征:SO通常为单侧卵巢发病,肿块一般较大,形态可规则或不规则,边界清楚;多为囊实性肿块,囊性为主多见,实性为主少见。囊性部分为多房囊腔,可因囊腔中含有不同浓缩程度的甲状腺球蛋白及甲状腺激素等物质,因此在超声、CT及MRI检查时囊腔内回声、密度及信号不同,会出现特征性的征象。相较于水而言,超声表现为较高回声[8],CT平扫时这些囊腔密度较高[7,9],而在MRI上这些囊腔表现T2W极低信号[7],增强后此类囊腔无强化。SO的实性成分、囊壁及分隔中含有甲状腺组织,具有吸收碘和分泌甲状腺激素的特性,因此超声表现为囊内出现高回声或中等回声结节伴血流信号[8,10],CT密度较高,MRI表现为T1WI上相对邻近的肌肉组织为等信号、T2WI上等或稍高信号,增强后肿瘤的实性成分和间隔明显强化,有时实性部分围绕在囊腔周围,呈分叶状改变,表现为“花边样”强化[9]。本文中病例数较少,仅部分病例表现出与上述相符的明显的超声特征。文献中[2,8-9]提到SO实性成分、囊壁及房间隔钙化常见,但本组研究中钙化检出率较低,笔者认为可能与本组中超声对细小钙化检查的局限性有关。
3.误诊分析
本组研究中:2例出现假Meigs综合征及CA125升高恶性表现,超声或CT检查提示富血供肿块,术前误诊为卵巢恶性肿瘤。回顾分析影像图像后,此2例肿块体积较大,但是边界清楚,周围组织器官受压,腹腔内及腹膜后无肿大淋巴结,没有恶性肿瘤的侵袭性和转移表现。术后病理显示病灶中实性的甲状腺组织较多,因此图像上提示丰富血流。5例误诊为畸胎瘤,此5例仅行超声检查,均表现为囊实性肿块,回声混杂,未进一步行CT或者MRI检查,检查结果受操作者的经验水平及被检查者的自身因素影响,而且少见的SO容易忽视。术后病理显示囊性成分为主,囊腔较多,囊液清亮或呈胶冻样,因此回声复杂,对诊断有一定的干扰。1例行超声及MRI检查后误诊为囊腺瘤,此例肿块含甲状腺胶质的囊腔体积小数量少,且位于实性成分之间,而此囊腔在T1WI上呈等低信号,T2WI上呈低信号,增强后无强化,易误认为肿瘤内的陈旧性出血。术后病理亦证实了实性成分中可见小囊腔含胶冻样物质。
针对无特殊临床症状的附件区占位性病变,SO要与以下几种疾病鉴别。囊腺瘤及囊腺癌:以囊性成分为主,实性成分少见。浆液性囊腺瘤:多为单房,囊腔内回声、密度或信号均匀。粘液性囊腺瘤:为多房,囊腔大小不等,囊液回声、密度或信号不同,囊壁均匀增厚。当囊壁不规则增厚,囊腔内出现壁结节,肿块为囊实性且边界不清,提示为囊腺癌。卵巢巧克力囊肿:多好发于育龄期女性,临床常有痛经史,大囊周边伴小囊为其主要特征。脓肿:常表现出典型的临床症状如疼痛、发热、白细胞升高等,抗炎治疗后好转。异位妊娠:患者有停经史,结合妊娠试验,当伴有出血时,行后穹窿穿刺可以帮助诊断。囊性畸胎瘤:CT可较好显示其内含有皮脂样物质、脂肪、毛发,及牙齿和骨组织;通过MRI扫描多方位、同层面不同序列的仔细比对,亦可发现含少量脂肪的畸胎瘤,而减少误诊或漏诊[11]。
除此之外,由于SO的病理特点,以及SO有一定的概率与畸胎瘤、囊腺瘤及类癌等伴发的特性,单一的影像学检查方法,无法准确诊断SO。所以联合多种影像检查方法可以更全面地对疾病的诊断及鉴别诊断。曾有报道123I或131I可积聚在SO的甲状腺组织中,因此,测定血清中甲状腺球蛋白、123I或131I扫描成像有助于SO的诊断[12]。
综上所述,SO特征为单侧附件的囊实性肿块,边界清楚,以多房囊性为主;实性成分及囊壁、间隔超声显示血流信号,CT或MRI增强表现为明显强化,以MRI增强的“花环样”强化为特异表现;囊腔内成分复杂,当超声提示稍高回声的囊腔,CT平扫出现高密度囊腔, MRI出现T2W极低信号的囊腔,且增强后无明显强化,应考虑SO的可能。但单一的影像检查方法,误诊率很大,结合超声及CT和(或)MRI检查可以提高诊断率。当行123I或131I扫描成像时,在甲状腺无核素异常浓聚时情况下,显像剂聚集在盆腔时,应当考虑到SO的可能。若出现胸腹水及CA125升高的恶性表现,SO在术前诊断中极易忽略,确诊要结合病理检查。
