TGR5多种配体抑制高脂饮食小鼠肥胖及高血糖的效果对比研究
2018-02-02陈小松闫柳陈瑛等
陈小松+闫柳+陈瑛等


[摘要]目的:本研究通过建立肥胖小鼠动物模型,分析比较胆汁酸膜受体TGR5多种配体的减肥及降糖效果,以筛选出TGR5最佳配体。方法:选取6周龄C57BL/6野生型小鼠,随机分为2组,分别用NF、HF喂养10周后,NF组小鼠采用NF继续喂养10周;将HF组小鼠分为7组,分别用HF、HF+OA(H)、HF+OA(L)、HF+CDCA、HF+CA、HF+DCA、HA+LCA喂养10周。共喂养20周后进行糖耐量实验、测定血清胰岛素水平并取肝脏脂肪组织做病理学观察,RT-PCR法检测脂肪酸合成与脂肪代谢相关基因表达情况。喂养过程中每周监测小鼠体重。结果:TGR5多种配体可激活TGR5调节肥胖小鼠体内糖脂代谢,降低小鼠体重、提高小鼠糖耐量水平,激活脂肪酸合成及氧化相关基因的表达,其中以OA(H)、CDCA和cA作用较为显著。结论:OA(H)、CDCA和CA可有效降低体重、提高糖耐量水平、降低血清胰岛素水平、缓解肝脏脂质沉积及调节脂肪代谢相关基因的表达。
[关键词]TGR5配体;褐色脂肪;肥胖;糖脂代谢
[中图分类号]R589.2 [文献标志码]A [文章编号]1008-6455(2017)07-0032-05
肥胖已成为当代重大公共卫生问题之一,并可增加高血压、冠心病和糖尿病等的发病风险。肥胖,即为白色脂肪组织(white adipose,WAT)的积累,于能量摄入大于能量消耗时发生。减肥和增加体力活动被认为是治疗肥胖最有效的方法,但是在许多情况下,这些生活方式的改变并不能长期坚持。另外,许多减肥药也因其不良副作用而退出市场,因此,开发新的安全有效的减肥药物成为治疗肥胖不可或缺的手段。
TGR5是首个被鉴定的胆汁酸膜G蛋白偶联受体,在糖类及能量代谢中均发挥着重要作用。TGR5高表达于褐色脂肪组织(brown adipose tissue,BAT)线粒体,在调节糖代谢中起着重要作用。前期研究发现,激活TGR5能够消耗能量达到减肥的效果,那么天然或半合成的TGR5的配体就很有可能开发为减肥药物。齐墩果酸(oleanolic acid,OA)是TGR5的天然植物配体,可使高脂饮食的动物体重下降,而且已被证实这种作用是通过激活TGR5实现的。除了OA外,初级胆汁酸胆酸(cholic acid,CA)和鹅去氧胆酸(chenodeoxycholic acid,CDCA),次级胆汁酸脱氧胆酸(deoxycholie acid,DCA)和石胆酸(lithocholic acid,LCA),亦是TGR5天然配體,均可作为信号分子参与能量代谢。胆汁酸-TGR5-cAMP-D2-T3-UCP信号通路在调节能量平衡和降低体重方面有着重要的作用。在本次研究中,笔者采用高脂饮食诱导形成后天肥胖小鼠模型,评估胆汁酸不同配体降低高脂肪饮食引起的肥胖和改善葡萄糖耐量的能力,以筛选出TGR5最佳配体,为抗肥胖药的发展提供理论基础。
1材料和方法
1.1实验动物:选取6周龄C57BL/6野生型小鼠,体重15~20g,饲养于福建医科大学实验动物中心,随机分为实验组和对照组。所有动物均按照实验动物护理和使用指南予以对待,所有实验均获得福建医科大学附属协和医院伦理委员会的批准并依据委员会指导方针进行。
1.2试剂:OA、CDCA、DCA、LCA、CA,均购自Sigma(St.Louis,MO,USA);苏木精伊红和血清胰岛素检测试剂盒购自罗氏应用科学(Indianapolis,IN,USA);其他试剂均购自Sigma。
1.3营养性肥胖动物模型的建立:所有小鼠置于25℃环境中,12h光照/12h黑暗交替。实验组小鼠饲喂高脂饲料(碳水化合物40%,蛋白质13%,脂肪40%,其他7%),即高脂(high fat diet,HF)组;对照组饲喂普通饲料(碳水化合物60%,蛋白质22%,脂肪10%,其他8%),为正常饮食(normal food diet,NF)组。动物自由摄食和饮水。
1.4药物干预:小鼠肥胖模型成功建立后,盯组小鼠随机分为七组(n≥5),一组采用单纯盯持续饲养,其余各组高脂饲料中加入不同干预药物:OA(H):100mg/kg,OA(L):80mg/kg,CDCA:5g/kg,DCA:2g/kg,LCA:1g/kg,CA:5g/kg,持续10周,每周监测小鼠体重。
1.5葡萄糖耐量实验与血清胰岛素水平检测:喂养结束后,小鼠饥饿16h,然后给予腹腔内注射葡萄糖(2g/kg),并以微型血糖仪(中国宁波kingkerry医疗器械有限公司)监测从0~120min时的血糖变化;血清胰岛素水平使用ELISA试剂盒测量,全血在4℃离心机中以2000g离心10min获得血清。
1.6免疫组织化学染色:喂养周期结束后,所有小鼠以CO2气体实施安乐死。从每只小鼠右叶肝脏取一定量肝脏组织,固定在PBS溶解的4%福尔马林溶液中,以制备石蜡切片或冰冻切片,用苏木精伊红染色;分离各组小鼠WAT及BAT进行油红O染色。
1.7 RT PCR检测脂肪酸合成与脂肪代谢相关基因表达情况:从组织样本中以TRI试剂(Molecular Research Center,Cincinnati,OH,USA)提取总RNA,用goloney鼠白血病病毒逆转录酶(Invitrogen,San Diego,CA,USA)从总RNA合成第一链cDNA。以小鼠管家基因β-actin为内参基因对mRNA进行标准化定量,使用Applied Biosystems 7300实时PCR系统(Applied Biosystems,Foster City,CA,USA)采用实时荧光定量PCR法对WAT和BAT中氧化相关因子如解偶联蛋白2(uncoupling protein 2,UCP2)、2型碘甲腺氨酸脱碘酶(2-iodothyronine deiodinase,D2)及环腺苷酸(cyclic adenosine monophosphate,cAMP)基因表达水平进行检测。特定上游(F)和下游引物(R)序列如表1所示。endprint
1.8统计学分析:相关数据采用(x±s)表示,双边t检验进行组间比较。P<0.05认为差异具有统计学意义。
2结果
2.1体重测量结果:所有小鼠共喂养20周,每周监测小鼠体重,具体测量数据如图1A;喂养周期结束后,将小鼠体重进行组间比较,结果表明,与其他组喂饲高脂饲料的小鼠相比,飼料中加入OA(H)、CDCA或CA后,这些小鼠虽饲喂高脂饮食,但体重和NF组小鼠无明显差异,与HF组相比,小鼠体重明显降低(P<0.05),见图1B。
2.2葡萄糖耐量实验及血清胰岛素水平检测结果:喂养周期结束后,小鼠空腹16h,给予腹腔注射葡萄糖(2g/kg),采用微型血糖仪测量0~120min的血糖水平,结果表明,与HF组小鼠相比,在高脂饲料中加入OA(H)、CDCA或cA以后,小鼠血糖水平明显下降(P<0.05),与正常饮食组小鼠血糖水平相当,结果见图1C~D;小鼠实施安乐死后,用ELISA法测定血清胰岛素水平(图1E),结果显示,CDCA组、CA组小鼠的血清胰岛素水平明显低于盯组小鼠(P<0.05)。
2.3 HE染色结果:如图2A所示,与正常饮食相比,高脂饮食能够促进脂质颗粒的聚积,如高分辨率图像上黑色箭头所示,这种现象在饲料中加入OA(H)、CA,尤其是CDCA后被逆转;OA(H)、CDCA、CA组的肝脏重量与正常饮食组小鼠无异,明显小于HF组小鼠(P<0.05),见图2B。
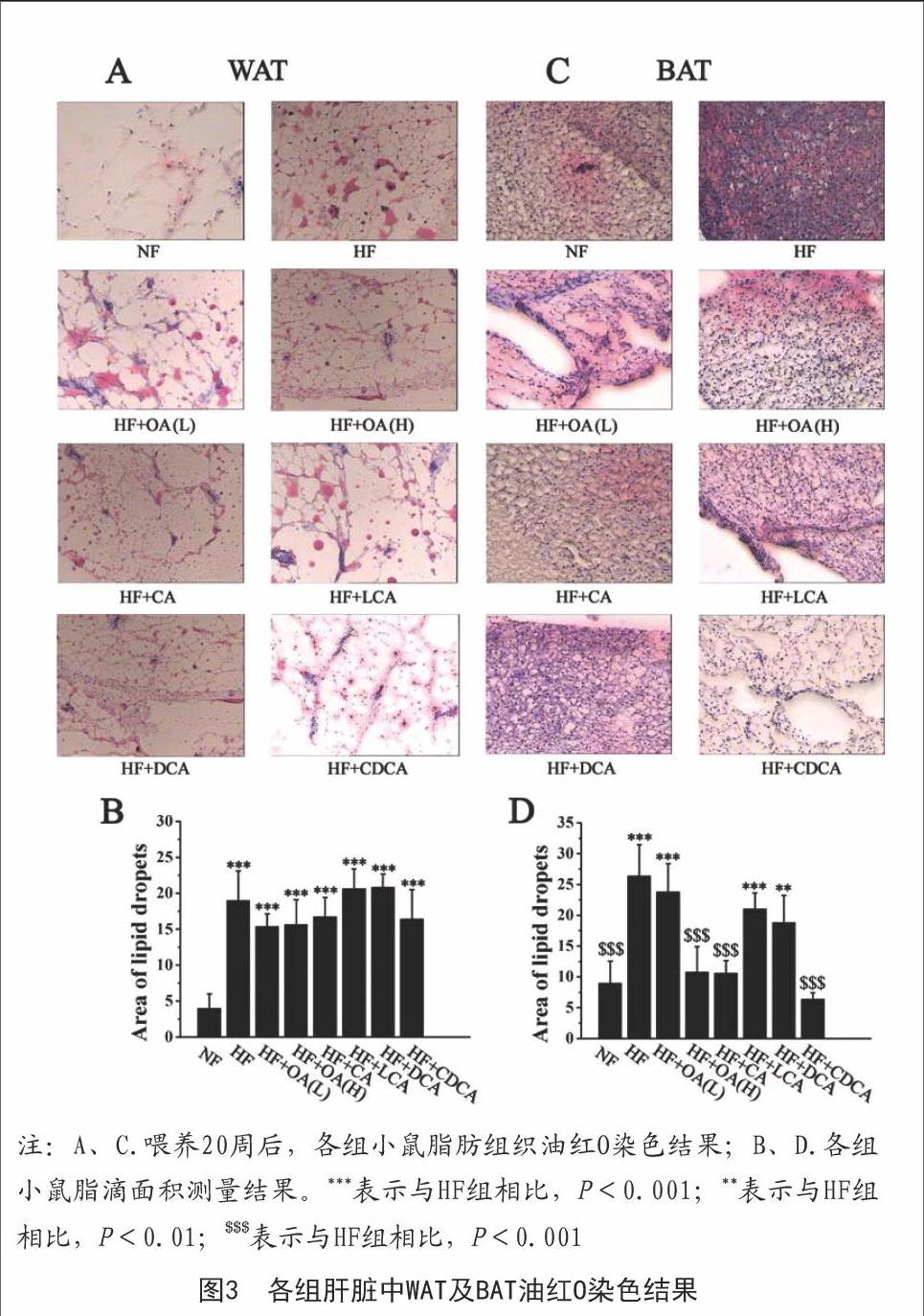
2.4油红O染色结果:各组肝脏脂肪组织病理切片情况详见图3A,脂肪含量检测结果见图3B,结果表明,OA(H)、CDCA组中的WAT与单纯HF组小鼠相比,脂肪聚积并无明显差异;OA(H)、CDCA、CA组中的BAT明显少于HF组小鼠体内的脂肪聚积。
2.5脂肪酸合成与脂肪代谢相关基因表达测定结果:对WAT而言,各组中的cAMP、UCP2及D2值无明显差异;而BAT中测量结果显示,OA(H)、CDCA及CA组中cAMP、UCP2及D2值均明显高于HF组(P<0.05),见图4。
3讨论
哺乳动物的脂肪组织主要包括WAT及相对少量的BAT。WAT是能量储存的主要部位,可分泌多种细胞因子和激素,调节能量代谢和胰岛素抵抗。BAT对成人能量代谢的影响于2009年才被发现,其包含许多小脂滴和较多数量的线粒体数目。BAT表达解偶联蛋白(uncoupling protein,UCP),UCP能够解偶联ATP合成呼吸链的活性,通过产热作用消耗能量。1983年,在Rothwell和Stock的一项人体试验研究中发现,仅50g BAT在完全激活后每天可增加人体20%的能量消耗。利用BAT对抗肥胖已成为一种潜在的治疗措施,而且越来越多的证据表明,BAT募集或BAT移植可以有效地降低体重,提高能量代谢。
TGR5是调节胆汁酸信号通路的新型膜受体,在之前的研究中发现,TGR5可以调节糖和能量代谢,因此可将其作为治疗肥胖的药物靶点。胆汁酸是肝脏中类固醇氧化产生的类固醇分子家族,具有溶解脂肪、促进消化吸收的作用,也可引起细胞内甲状腺激素激活促进能量消耗。胆汁酸通过激活cAMP调节受体TGR5,从而下调ATP合成,cAMP水平升高可激活PKA磷酸化CREB转录因子,进而通过与启动子上的CREs结合反式激活其靶基因,如D2的Dio2基因。在BAT中,D2的表达促进局部甲状腺激素的生产,转而增加能量消耗。WAT和BAT中其他参与能量消耗的基因在胆汁酸与受体结合后也被上调,这与前人研究报道结果一致。脂肪酸合成和氧化相关基因mRNA表达水平,在BAT增加,在WAT并无增加,说明BAT中TGR5的激活使这些基因mRNA表达水平的升高,引起能量的消耗及代谢的加速,并可通过抑制脂肪沉积导致体重下降,与单纯高脂饲料喂饲的小鼠相比,OA(H)、CDCA及CA组小鼠体重明显减少。此外,HE染色和油红O染色病理观察发现TGR5配体OA(H)、CDCA和CA具有显著抑制高脂饮食后肝脏脂质沉积和脂肪聚积的作用。
有研究认为TGR5不同的配体可能引发不同下游通路和基因表达谱,从而导致特定的结果产生。研究发现,在没有其他炎症刺激,如LPS存在的条件下,以配体激活TGR5,可引起IL-1β和TNF-α表达上调,而且这种效应不依赖于PKA的激活。在这种情况下,细胞因子的产生是通过激活JNK介导,进而上调miR-26a表达。这些结果表明,TGR5介导其生物学功能通过至少两个不同的下游信号通路。
TGR 5激活的另一个效应是促进胰高血糖素样肽(glucagon-like peptide-1,GLP1)的分泌。GLP-1是肠促胰素家族的一员,可促进餐后肠内分泌细胞分泌促胰岛素,其主要作用是调节胰岛素分泌。在本次研究中发现,与单纯高脂饲料喂饲的小鼠相比,OA(H)、CDCA和CA组小鼠的血清胰岛素水平明显低于HF组小鼠,表明这些配体能够移抑制高脂饮食引起的高胰岛素血症的发生。除了调节胰岛素水平,TGR5激活也被证明能减少喂食高脂饲料小鼠的血糖水平。本研究中,与HF组小鼠相比,OA(H)、CDCA及CA组小鼠血糖水平显著降低,提示TGR5天然配体能够使血糖水平下调。这些结果表明,OA(H)、CDCA和CA激活TGR5能够提高葡萄糖耐量,进一步证实了其潜在的治疗代谢紊乱的作用。
如今,选筛出高效安全的TGR5配体用于药物的研发迫在眉睫,许多研究也开始关注FXR的生理作用,FXR也是一种胆汁酸受体,激活后可用于治疗代谢紊乱。然而,临床前研究发现,FXR激活剂存在内在毒性,并能改变一些基因表达谱,这进一步提示了充分研究胆汁酸激活信号网络的必要性,以便筛选出最佳胆汁酸配体,为发展安全有效的药物疗法提供理论支持。
4结论
TGR5的激活可有效调节能量代谢,本研究通过建立后天肥胖小鼠模型,筛选了一些减肥效果较理想的TGR5配体,其中OA(H)、CDCA和CA可有效降低体重。CDCA和CA的干预能够显著降低胰岛素水平,提示这些配体可作为抗肥胖药,OA在高剂量下也能起到减肥作用,所以,对OA(H)、CDCA和CA的优化可用于开发抗肥胖药物。endprint
