LC—MS研究白芷中香豆素成分对多烯紫杉醇药代动力学的影响
2018-01-29管咏梅朱卫丰管雪静廖正根赵国巍董伟梁新丽
管咏梅+朱卫丰+管雪静+廖正根+赵国巍+董伟+梁新丽
[摘要] 建立测定大鼠血浆中多烯紫杉醇LC-MS方法,并分别研究白芷中3个香豆素成分(欧前胡素、异欧前胡素及氧化前胡素)对多烯紫杉醇药代动力学的影响。以紫杉醇为内标,血浆样品经甲醇沉淀蛋白,LC-MS测定,方法经特异性、线性范围、准确度、精密度、稳定性等确证适合用于血浆中多烯紫杉醇的测定。试验采用每组6只大鼠,分别口服灌胃给予多烯紫杉醇(50 mg·kg-1)组、氧化前胡素(8 mg·kg-1)配伍多烯紫杉醇(50 mg·kg-1)组;欧前胡素(15 mg·kg-1)配伍多烯紫杉醇(50 mg·kg-1)组、异欧前胡素(15 mg·kg-1)配伍多烯紫杉醇(50 mg·kg-1)组。LC-MS测定给药后血浆中多烯紫杉醇浓度,绘制血药浓度-时间曲线,并用DAS 2.0软件计算相关药代动力学参数。结果显示多烯紫杉醇与3个香豆素成分配伍前后其药代动力学参数有了明显的变化。血药浓度-时间曲线下面积(AUC)显著性增加,药峰浓度(Cmax)显著提高。表明白芷香豆素类化合物能促进多烯紫杉醇的口服生物利用度,三者对多烯紫杉醇口服生物利用度的影响作用氧化前胡素最强、异欧前胡素次之、欧前胡素最弱。
[关键词] 多烯紫杉醇; 欧前胡素; 异欧前胡素; 氧化前胡素; 药代动力学
[Abstract] The study was aimed to establish a liquid chromatography-tandem mass spectrometric method for the determination of the docetaxel concentration in rat plasma, and study the effect of coumarin constituents (imperatorin, isoimperatorin and oxypeucedanin) in Angelica dahurica on pharmacokinetics of docetaxel.Plasma was precipitated with acetonitrile and determined by LC-MS method with Paclitaxel as an internal standard. The specificity, linearity, range, accuracy, precision and stability of the method were suitable for the determination of docetaxel in plasma.Six sprague-dawley rats in each group received intragastric administration of docetaxel (50 mg·kg-1), oxypeucedanin (8 mg·kg-1) combined with docetaxel (50 mg·kg-1), imperatorin (15 mg·kg-1) combined with docetaxel (50 mg·kg-1), and isoimperatorin(15 mg·kg-1) combined with docetaxel (50 mg·kg-1).Their drug plasma concentration was determined by LC-MS with Paclitaxel as an internal standard to draw plasma concentration-time curve, and the phamacokinetic parameters were calculated by DAS 2.0. The results showed that the phamacokinetic parameters of docetaxel all had notable changes when combined with imperatorin, isoimperatorin, and oxypeucedanin, respectively. The phamacokinetic parameters AUC and Cmax were significantly increased, indicating that coumarin constituents in Angelica dahurica could promote the oral bioavailability of docetaxel, and their effects were in the following order: oxypeucedanin>isoimperatorin>imperatorin.
[Key words] docetaxel; imperatorin; isoimperatorin; oxypeucedanin; phamacokinetic
白芷為我国大宗常用中药材品种之一,其收载于2015年版《中国药典》一部[1],具有祛风散寒、燥湿排脓、止痛等功效[2],其活性组份主要为白芷香豆素和挥发油,前期研究结果表明白芷香豆素可促进配伍对药活性成分如葛根素、黄苓苷等的肠道转运[3-4],同时发现白芷香豆素有规律的促进P-gp介导的药物的肠道转运,而且对P-gp的表达具有一定的抑制作用[5]。进一步采用体外Caco-2细胞模型考察了白芷中香豆素单一成分对P-gp介导药物肠道转运的影响[6],研究结果表明白芷中欧前胡素、异欧前胡素及氧化前胡素可促进此类药物的肠道转运。P-gp是一种重要的药物转运蛋白,与药物结合后,在其核苷酸结合位点上结合ATP,ATP水解后所释放的能量使药物泵出细胞外,导致药物浓度下降,进而影响药物吸收[7-8]。在肿瘤细胞中P-gp一般表达较高,其可降低细胞内的药物浓度,导致肿瘤的多药耐药的发生。许多临床一线广泛使用的药物均能引起肿瘤的多药耐药作用,如长春花生物碱类、紫衫烷类、多柔比星等。多烯紫杉醇是紫杉烷类的抗肿瘤药物,是现有药物中治疗转移乳腺癌和非小细胞癌最有效的单剂化疗药物。但其水溶性低[9]、口服生物利用度低[10],进因而阻碍了其在口服制剂的应用。因此本文在此前研究基础上,建立血浆中多烯紫杉醇LC-MS测定方法,进一步研究白芷香豆素中欧前胡素、异欧前胡素和氧化前胡素对多烯紫杉醇药代动力学的影响。endprint
1 材料
1.1 药品与试剂
多烯紫杉醇(西安昊轩生物科技有限公司,批号DXZSC-141229);氧化前胡素对照品(上海融禾医药科技发展有限公司,批号100420);欧前胡素对照品(中国食品药品检定研究院,批号110826-200712);异欧前胡素对照品(中国食品药品检定研究院,批号110827-200407)。
1.2 仪器
AB 4500 QTRAP液质联用仪(美国AB公司);XW-80A涡旋混合器(上海青浦沪西仪器厂);3-18K型高速冷冻离心机(德国Sigma公司);微量移液枪(美国Thermo公司)。
1.3 动物
SD大鼠,雄性,体质量180~200 g,湖南斯莱克景达实验动物有限公司提供,许可证号SCXK(湘)2011-0003。
2 方法
2.1 大鼠血浆中多烯紫杉醇LC-MS/MS分析方法的建立
2.1.1 多烯紫杉醇色谱条件 色谱柱Agilent ZORBAXExtend-C18(2.1 mm×100 mm,3.5 μm),流动相A为乙腈,B为0.1%乙酸,梯度洗脱:0~1 min,30%~52% A;1~3 min,52% A;3~3.1 min,52%~70% A;3.1~5 min,70% A。柱温25 ℃,体积流量为0.4 mL·min-1,进样量为10 μL。
2.1.2 质谱条件 ESI离子源;正离子模式;多反应检测方式(MRM);测定多烯紫杉醇检测离子为 m/z 802.4→527.2,紫杉醇检测离子为 m/z 854.2→569.2;气帘气压35 psi (1 pis=6.895 kPa);喷雾电压5 500 V;去簇电压:多烯紫杉醇50 V,紫杉醇100 V;碰撞能量15 V;雾化器45 psi,平衡器45 psi。
2.1.3 血浆样品的处理 室温下水浴融化血浆,混匀,精密吸取100 μL,置于1.5 mL Eppendorf管中,依次加入20 μL空白甲醇,20 μL内标溶液,涡旋60 s,加入360 μL甲醇,涡旋3 min,16 000 r·min-1离心10 min,吸取上清液,按照2.1.2项质谱条件进样检测。
2.1.4 多烯紫杉醇儲备液与紫杉醇储备液的配制 精密称取定量的多烯紫杉醇对照品,甲醇超声溶解定容到25 mL量瓶,作为储备液。采用倍数稀释法,分别得到质量浓度0.025 5,0.051 0,0.255,0.510,2.55,5.10,10.2 mg·L-1的系列工作液。精密称取一定量的紫杉醇对照品,甲醇超声溶解定容至25 mL。临用时取出适量稀释至质量浓度为200 μg·L-1。
2.1.5 特异性 取大鼠空白血浆100 μL,按2.1.3项下方法操作,大鼠空白血浆不加内标(紫杉醇)样本、空白血浆加入内标样本、空白血浆加入多烯紫杉醇样本、给药后大鼠血浆加入内标(紫杉醇)样本,并记录相应的色谱图。
2.1.6 标准系列样品和质控样品的制备 精密移取SD大鼠空白血浆100 μL于1.5 mL离心管中,依次加入20 μL系列工作溶液,20 μL内标溶液,涡旋60 s,加入360 μL甲醇,涡旋3 min,16 000 r·min-1离心10 min,吸取上清液,备用。即得质量浓度为1.02,2.04,10.2,20.4,102,204,408 μg·L-1的标准系列样品和1.02(LLOQ),2.04(QCL),20.4(QCM),204 μg·L-1(QCH)系列质控样品。
2.1.7 标准曲线及线性范围 取大鼠标准血浆系列样品,采用2.1.1项LC-MS/MS条件进样。以多烯紫杉醇的加入浓度C为横坐标,以待测物As与内标Ai的峰面积比值(f=As/Ai)为纵坐标进行权重回归(权重系数为1/C2).
2.1.8 最低定量限与精密度和准确度 取多烯紫杉醇血浆质控系列样品(LLOQ,QCL,QCM,QCH)每种质量浓度5份,按2.1.3项下操作,连续测定3 d,以随行标准曲线计算最低定量限与质控样品的浓度,将同一浓度3 d共18个样品的实测浓度进行单因素方差分析,计算日内、日间精密度(RSD)和准确度(RE)。
2.1.9 提取回收率 取多烯紫杉醇血浆质控系列样品(QCL,QCM,QCH)每种质量浓度6份,按2.1.3项下操作,用其进样得到的峰面积除以未经提取处理的低、中、高3种相应质量浓度的多烯紫杉醇质控工作液及内标工作液后进样得到的峰面积,计算血浆中多烯紫杉醇的提取回收率。
2.1.10 稳定性 考察多烯紫杉醇低、中、高3个质量控制浓度的血浆样品在室温放置6 h,-20 ℃下放置7 d以及-20 ℃下反复冻融3次的稳定性。
2.2 白芷香豆素对多烯紫杉醇在大鼠体内药代动力学的影响
2.2.1 药代动力学给药方案 雄性SD大鼠随机分成6组,实验分3 d完成,每次实验前至少12 h禁食不禁水。分别灌胃给予50 mg·kg-1多烯紫杉醇、多烯紫杉醇(50 mg·kg-1)配伍氧化前胡素(8 mg·kg-1);50 mg·kg-1多烯紫杉醇、多烯紫杉醇(50 mg·kg-1)配伍欧前胡素(15 mg·kg-1);50 mg·kg-1多烯紫杉醇、多烯紫杉醇(50 mg·kg-1) 配伍异欧前胡素(15 mg·kg-1)。分别于给药后0.083,0.166,0.25,0.5,1,1.5,2,4,6,8,10,12 h眼眶静脉丛取血0.5 mL,并置于1.5 mL肝素抗凝管中,4 000 r·min-1离心10 min,精密吸取上清液至1.5 mL EP管中,立即储存于-20 ℃冰箱,备用。
2.2.2 数据处理 实验数据采用DAS 2.0药代动力学软件处理,非房室方法计算药代动力学参数。主要药代动力学参数是由平均血药浓度数据计算得到,Cmax和AUC的方差由软件自带的稀疏数据计算方法得到。endprint
3 结果
3.1 大鼠血浆中多烯紫杉醇LC-MS方法学考察
3.1.1 特异性 多烯紫杉醇及内标的峰形良好,保留时间分别为 2.85,3.19 min,大鼠空白血浆中的内源性物质不干扰测定,见图1。
3.1.2 标准曲线与线性范围 多烯紫杉醇在大鼠血浆中标准曲线方程为y=0.005 46x+0.013 4,R2=0.993 3,线性范围2.040~408.0 μg·L-1。
3.1.3 最低定量限与精密度和准确度 多烯紫杉醇日内精密度RSD为4.1%~8.3%,日间精密度RSD为5.9%~10%,RSD均小于15%,重复性好,符合要求。准确度91.20%~97.80%。最低定量限(LLOQ)为1.02 μg·L-1(S/N>10),表明该方法灵敏度高,可用于多烯紫杉醇的微量分析。
3.1.4 回收率 多烯紫杉醇方法回收率为80.10%~92.90%,RSD为2.9%~9.4%,小于15%;内标的提取回收率83.50%~96.70%,RSD为5.2%。
3.1.5 样品稳定性 多烯紫杉醇低、中、高3个浓度样品室温放置6 h后相对偏差RE为-10%~-1.7%,RSD≤8.9%。-20 ℃放置7 d后相对偏差RE为-7.3%~-2.6%,RSD≤9.3%。冻融3次后相对偏差RE为-0.40%~5.0%,RSD≤8.8%。表明多烯紫杉醇血浆样品在上述条件下稳定。
3.2 白芷香豆素对多烯紫杉醇在大鼠体内药代动力学的影响
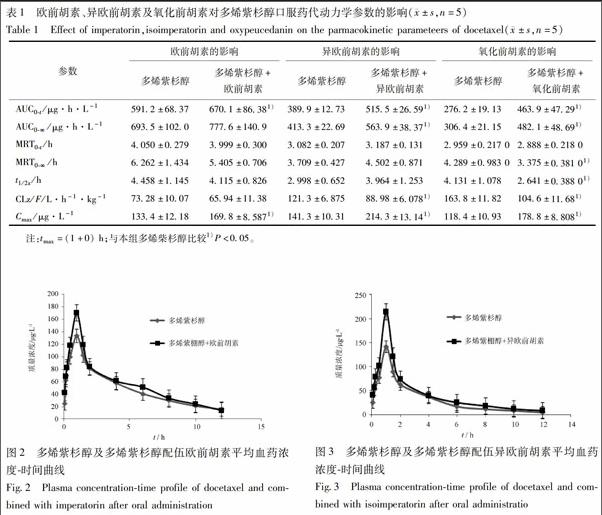
多烯紫杉醇及多烯紫杉醇分别配伍欧前胡素、异欧前胡素及氧化前胡素后的大鼠体内药代动力学参数见表1,血药浓度-时间曲线见图2~4。结果提示多烯紫杉醇配伍欧前胡素后AUC,Cmax及药时曲线下面积均有所提高;多烯紫杉醇配伍异欧前胡素后AUC,Cmax及药时曲线下面积显著提高,其中AUC,Cmax分别为配伍前的1.3,1.5倍;多烯紫杉醇配伍氧化前胡素后AUC,Cmax及药时曲线下面积显著提高,其中AUC,Cmax分别为配伍前的1.7,1.5倍。
4 讨论
目前许多药物和活性成分因P-gp外排而使其口服生物利用度差,使得该类药物难以开发成有效的口服制剂,甚至难以成药,如具有较强药理活性的柔比星、紫杉醇、长春新碱、芍药苷等[11-12]。前期实验结果表明白芷中欧前胡素、异欧前胡素及氧化前胡素对多烯紫杉醇的吸收促进作用。但上述研究是在体外细胞模型开展,本实验基于体外细胞模型结果的可信度,采用体内药代动力学分别验证该3种成分对多烯紫杉醇体内过程的影响,结果证实白芷中香豆素对多烯紫杉醇P-gp介导的药物有显著促进作用。
实验结果表明,多烯紫杉醇单独给药和分别配伍白芷中欧前胡素、异欧前胡素及氧化前胡素后,药代动力学行为有明显差异,差异主要表现在联合给药后的AUC,Cmax等参数上,联合给药后AUC,Cmax均较单独给药组显著提高,欧前胡素、异欧前胡素对多烯紫杉醇t1/2无显著影响,而氧化前胡素配伍多烯紫衫醇后t1/2下降,表明3种成分增加多烯紫杉醇生物利用度的原因与对消除率影响无关,可能是三者对介导多烯紫杉醇在体内外排作用的P-gp具有影响,或三者抑制了P-gp蛋白表达或其他原因导至其外排功能受到抑制,从而增加了多烯紫杉醇口服生物利用度。
[参考文献]
[1] 中国药典.一部[S]. 2015.
[2] 张富强, 聂红, 韦艺, 等. 白芷的化学与药理研究进展[J]. 南京中医药大学学报, 2002, 18(3): 190.
[3] 祝婧云,梁新丽,王光发,等. 白芷提取物对黄芩活性成分黄芩苷的吸收促进作用研究[J].药学学报,2011,46(2):232.
[4] 梁新丽,赵国巍,罗云,等. 外翻肠囊法研究白芷有效组份对配伍“对药”有效成分肠吸收的影响[J]. 中国实验方剂学杂志,2013,19(17):193.
[5] Liang X L, Zhang J, Zhao G W, et al.Mechanisms of improvement of intestinal transport of baicalin and puerarin by extracts of Radix Angelicae Dauricae[J]. Phytoth Res,2015,20:220.
[6] 管雪静,余世平,廖正根,等. 白芷中10种呋喃型香豆素对长春新碱肠道转运的影响[J]. 中草药, 2015, 46(14):2117.
[7] Gottesm M M, Tito F, Bates S E. Multidrug resistance in cancer: roleof ATP-dependent transporters[J].Nat Review Cancer,2002,1:48.
[8] Hait W N, Yang J M. Clinical management of recurrent breast cancer: development of multidrug resistance (MDR) and strategies to circumvent it[J]. Semin Oncol, 2005,32(6 Suppl 7):S1.
[9] Song S S, Chen F,Qi H, et al. Multifunctional tumor-targeting nano-carriers haled on hyaluronic acid-mediated and pH-sensitive proper-ties for efficient delivery of docetaxel[J].Pharm Res, 2014, 31(4):1032.
[10] Kim D W, Ramasamy T, Choi J Y, et al. The influence of bile salt onthe chemotherapeutic response of docetaxel-loaded thermosensitiveb nanomicelles [J].lnt J Nanomed, 2014, 9:3815.
[11] 潘啟超, 田晖. 多种中药单体逆转肿瘤多药耐药性[J].科学通讯,1995(40):1901.
[12] 李建华,秦风绮,杨佩满.蝙蝠葛碱逆转K562/ADM细胞多耐药性的研究[J].大连医科大学学报,2002,24(2):94.
[责任编辑 张燕]endprint
