连续卡洛法生产法尼基丙酮工艺研究
2018-01-12曹小明张展翅
曹小明 张展翅
(浙江浙邦制药有限公司,浙江 绍兴 312369)
Carroll重排,也叫Carroll反应,卡罗尔反应,卡洛反应。最早的描述出现在1940年[1~3],是有机合成中的一类重要反应,在医药、香料合成、化工合成领域应用非常广泛,例如合成甲基庚烯酮[4]、香叶基丙酮[5,6]、假性紫罗兰酮[7]和法尼基丙酮[8]等。Carroll反应的发生意味着烯丙醇或炔丙醇与乙酰乙酸乙酯或双烯酮反应之后,碳链增长,是Claisen重排反应的一种变异反应。
其反应通式如下:
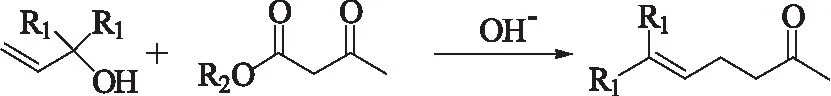
图1Carroll反应的反应通式
Fig1Carrollreactionreactionformula
通过对Carroll反应的研究发现,反应整个过程经历以下三个步骤[9]:①新的不饱和醇包括烯丙醇或炔丙醇,与乙酰乙酸乙酯或双烯酮反应生成不饱和醇乙酰乙酸酯;②这样的β-酮酯经负离子促进的Claisen重排反应后生成β-酮酸;③接着自动脱羧生成γ,δ-不饱和酮。
法尼基丙酮,化学名称为6,10,14-三甲基-5,9,13-十五碳三烯-2-酮,是金合欢基丙酮的同分异构体,以其为原料,可以合成异植物醇、进而进一步合成维生素E[10],市场需求量巨大,因此对法尼基丙酮的合成研究就具有非常重要的意义。
法尼基丙酮主要是以橙花叔醇为原料,在催化剂的作用下,经过Carroll反应一步合成而得。US2660608[11]提示了由四氢橙花叔醇和双烯酮制备金合欢基丙酮。
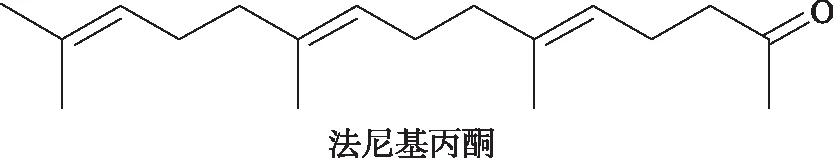
图2 法尼基丙酮和金合欢基丙酮的化学式Fig 2 The chemical formula of farnesylacetone and farnesylacetone
US2795617[12]利用烷醇铝,尤其是Al(O-CH(CH3)2)3的异丙醇铝,用量为醇用量的0.8-2.5%时,即能达到催化反应的目的。
许青青和姜华以橙花叔醇和乙酰乙酸甲酯为原料,异丙醇铝为催化剂,采用改良的Carroll反应,制得法尼基丙酮。最佳实验条件为:反应温度170 ℃,橙花叔醇、乙酰乙酸甲酯与催化剂异丙醇铝的摩尔比为1:1.11:0.02,保温温度为178~180 ℃,保温时间为2.5 h,收率可达99.0%。
朱为福[13]采用改良的Carroll反应,以3,7,11-三甲基-1,6,10-十二碳三烯-3-醇(橙花叔醇,C15H26O)和乙酰乙酸甲酯(C5H8O3)为原料,对金合欢基丙酮(6,10,14-三甲基-5,9,13-十五碳三烯-2-酮)的合成进行了放大试验研究。探索了反应条件对产品收率的影响。结果表明,反应最佳工艺条件为:n(C5H8O3)∶n(C15H26O)=1.1∶1、反应温度为170 ℃、反应时间4.5~5 h,在该优化条件下,产品收率99.0%;反应后再经中和、水洗、减压蒸馏,精制后产品纯度 大于96.3%,总收率为84.6%。用IR和MS确认了产品结构。工艺具有操作简便、生产时间短、能耗低、产品收率高等优点,具有较高的工业应用价值。
张峻松等人[14]以芳樟醇为原料,经过两步carroll反应后,得到金合欢基丙酮,总收率达50.9%。Carroll反应条件,醇与乙酰乙酸乙酯的摩尔比为1∶1.1,反应温度和保温温度控制分别为在160-165 ℃和165-170 ℃,保温时间2h,Carroll反应单步收率分别为93.9%和88.9%。
姚晓明[15]在合成吉法酯时,第一步合成法尼基丙酮,采用橙花叔醇为原料,以异丙醇铝为催化剂,滴加乙酰乙酸乙酯时,温度控制在170 ℃,温度变化要求不超过5 ℃,反应时间2h,178-180℃回收乙酰乙酸乙酯。
周武春等人[16]以香叶基芳樟醇为原料,加入香叶基芳樟醇摩尔比1.2-1.6的乙酰乙酸烷基酯,加入香叶基芳樟醇摩尔用量的0.5-10%有机铝催化剂,以酮类溶液为溶剂,在最高不超过160℃的温度下发生Carroll反应,低真空快速转移生成的低级醇和二氧化碳,转化率可达95%,产品收率超过66%。
陈海荣[17]以橙花叔醇为原料,与乙酰乙酸甲酯,异丙醇铝共同反应,甲醇为溶剂,100 ℃下经carroll反应制得法尼基丙酮。
浙江巨化基团公司制药厂[18]采用改良的carroll反应,以3,7,11-三甲基-1,6,10-十二碳三烯-3-醇(橙花叔醇)和乙酰乙酸甲酯为原料,异丙醇铝为催化剂,合成金合欢基丙酮进行了放大实验。反应釜控制温度在170℃,控制滴加乙酸乙酯2h,温差控制不超过2℃。回收甲醇后,升温至178-180℃,回收乙酸乙酰甲酯套用,保温反应2-3h,金合欢基丙酮的收率可达96.8%,质量分数为88.8%。具有较高工业应用价值。
李冬梅等人[19]研究了香叶基丙酮合成反应过程中馏出物的主要化学组成及其特征。结果表明,反应馏出物中除含正常的乙醇以外,还有未来得及反应而被夹带出来的原料乙酰乙酸乙酯和芳樟醇,其次还含有少量分解产物乙酸乙酯和乙酸、脱水产物月桂烯、异构产物香叶醇和橙花醇等成分,同时含有较多的来源于原料的杂质成分。实验室和工业规模条件下,对于本合成反应的控制存在明显的不同,小试验较易于控制两种反应原料的馏出,而在大生产调试生产时则更易于控制产物香叶基丙酮被夹带。
韩国SK公司公开了一种除去用异丙醇铝做催化剂经由carroll反应得到不饱和酮过程中残留催化剂的方法[20],此方法可以持续消除设备中大规模的异丙醇铝残留,采用选择性吸附剂附着在二氧化硅树脂上,消除效果可以达到1×10-6以下。
目前Carroll反应大多为间歇釜式反应操作,本文以法尼基丙酮生产为重点研究和说明。生产基本流程为将定量的催化剂、部分脚料(富含催化剂)及橙花叔醇投入釜中,加热升温至150-180℃时开始滴加乙酰乙酸甲酯,滴加完毕保温一段时间后,拉真空若干时间,取样检测,冷却放料。
能耗方面,整个反应过程需要消耗大量的蒸汽和冷却水。加上釜体每次冷却后下次重新投料时需要重新加热升温,也造成部分能耗的浪费。
安全环保方面,反应为间歇操作,由于生产气体CO2排放不均匀,导致收集的气柜经常异常波动,如反应过快还可能出现冒顶的现象,产生大量废气造成环境污染,也存在很大的安全隐患。
质量方面,其每台釜配套的贮槽多,人工操作多,同时会出现批次与批次之间的质量不稳定等情况,难以达到精准控制的要求。
操作上,间歇操作劳动强度大,员工数量也较多,人工成本较高。频繁的开关设备对设备的损坏率较高,频繁的卸料出料也存在一误操作等。
最关键的收率方面,间歇反应目前原料烯醇的摩尔收率在88%,酰化剂乙酰乙酸甲酯的摩尔收率在84%,均不是很高。
基于以上的研究结论,发现carroll反应过程中,根据不同的反应原料,即不同的不饱和醇类型,全程采用同样的温度来进行整个反应过程。另一反应原料采用取代或不取代的乙酰乙酸烷基酯。催化剂多采用有机铝进行催化。
本论文重点在于对反应工艺流程的探讨,以橙花叔醇和乙酰乙酸甲酯为原料,异丙醇铝为催化剂,通过釜式串联的方式分为三段五釜连续进行,分釜控温的方式,改变传统工艺中间歇式反应在一个反应釜中控制温度的弊端,使各步反应充分彻底的进行。通过小试研究对工艺的可行性和稳定性进行探讨,得出最佳工艺参数,使得橙花叔醇的选择性和产物的收率大大高于传统控温的选择性和收率。
1实验部分
1.1 实验仪器及试剂
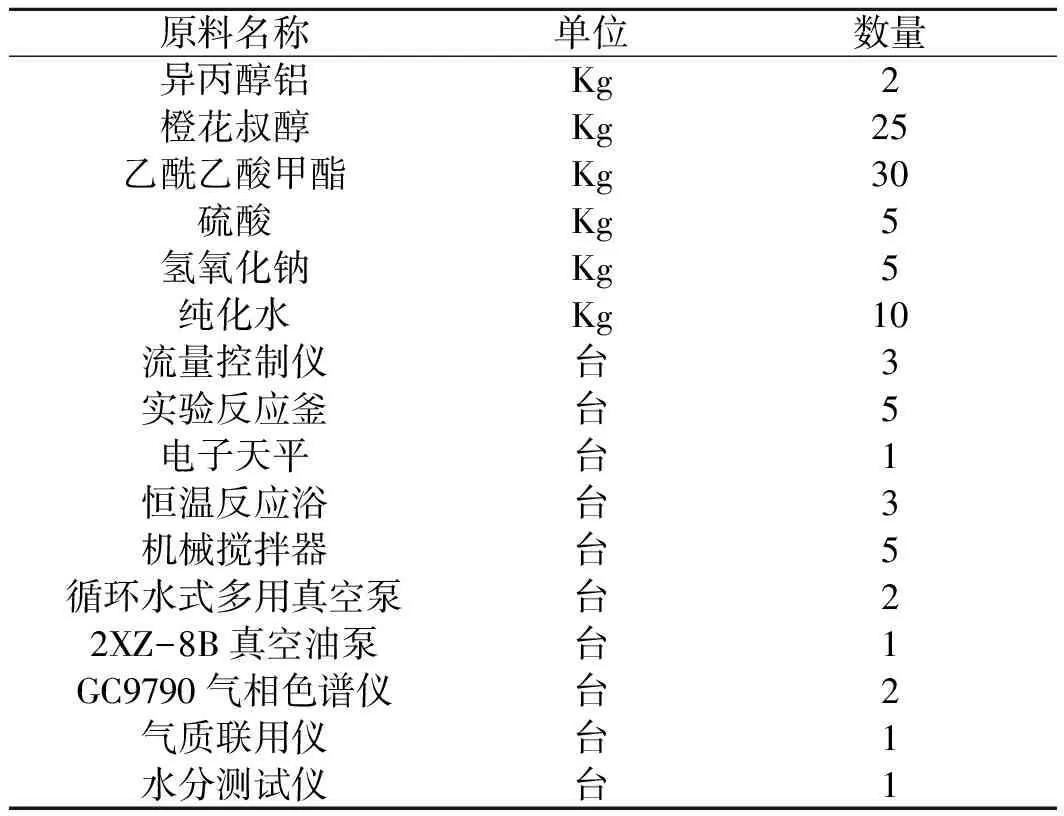
表1 实验仪器及试剂Table 1 experimental instruments and reagents
1.2 实验主要原料及产品
主要原料:橙花叔醇、乙酰乙酸甲酯、异丙醇铝
产品:法尼基丙酮
2实验过程
2.1 间歇Carroll反应工艺合成法尼基丙酮考察
Carroll反应中,使用的催化剂多为乙酰丙酮或乙酰乙酸酯的铝络合物。乙酰乙酸酯与叔乙烯基甲醇或炔丙醇在进行卡罗尔反应的情况下,一般使用甲基酯或乙基酯作为乙酰乙酸烷基酯,在不饱和醇的乙酸乙酰化中释放出低沸点的醇,如甲醇或乙醇,再与脱羧时形成的二氧化碳气体一起在反应时被蒸馏排出。
本研究主要考察新的生产工艺,即分釜控温的工艺对反应所产生的影响,再加上原料的价格优势,因此采用乙酰乙酸甲酯作为反应原料之一,与异丙醇铝形成乙酰乙酸铝络合物作为反应催化剂。
将原料按照橙花叔醇和酰化剂乙酰乙酸甲酯及催化剂异丙醇铝按照1∶1.2∶0.02的比例备料,先将橙花叔醇和催化剂投入反应釜,升温至150~180 ℃,开始滴加酰化剂二乙甲酯,滴加2 h,滴加完毕,保温反应5 h,然后减压至-100 pa将未反应完的原料橙花叔醇和酰化剂回收套用,合格产物法尼基丙酮进入下一步工序。

图3 carroll重排制备法尼基丙酮的合成路线Fig 3 synthesis route of Carroll rearrangement in preparation of farnesylacetone
2.2 连续Carroll反应工艺合成法尼基丙酮考察
法尼基丙酮,简称FA,接下来的内容将以橙花叔醇为原料合成法尼基丙酮为例讲述carroll反应连续化的改进工艺。
通过对反应过程的研究,我们发现此反应需要经过三个步骤:
①酯交换:催化剂异丙醇铝与Carroll剂乙酰乙酸类化合物进行酯交换,生成乙酰乙酸-R-酯;
②重排:上步合成的酯类重排,生成R-酮酸;
③脱羧:R-酮酸经过脱羧反应生成成品R-酮,同时有气体二氧化碳放出。

图4 carroll重排反应机理Fig 4 mechanism of Carroll rearrangement reaction
在这三步中,初期酯交换所需的温度不高,后温度逐渐升高到脱羧过程。针对这个过程中的温度及反应进程的差异,新技术将几个反应置于不同的反应釜中,设计了三段五釜的反应模式,进行分釜控温分段滴加,使得原料充分混合,收率更高。

图5 carroll反应连续化工艺流程图Fig 5 flow chart of Carroll reaction process
Carroll反应连续化工艺合成的过程及原理如下:
a、反应A釜,酯交换:
先将反应釜内备一部分上批法尼基丙酮反应液粗品(首次需间歇反应备一部分作为底料),升温,将原料橙花叔醇和酰化剂二乙甲酯及催化剂有机铝盐按照一定的比例滴加进入常压反应A釜,进行酯交换反应,控制酯交换反应温度和停留时间;
b、反应B釜,重排反应:
反应A釜产物通过釜溢流口缓慢进入反应B釜进行酯重排反应,控制重排反应温度,保证一定的停留时间;
c、反应C釜,脱羧反应:
反应B釜产物通过釜溢流口缓慢进入反应C釜进行脱羧反应,控制脱羧反应温度和停留时间。部分副产物甲醇及CO2通过塔顶冷凝器分别进入受槽和气柜回收处理;
d、保温D釜,保温反应:
反应C釜物料经过釜溢流口进入保温D釜继续反应,控制温度和停留时间;
e、减压E釜,原料回收:
保温D釜物料经过釜底出料,从减压E釜中间溢流口进入,控制温度、真空度和停留时间,将未反应完的原料R-醇和酰化剂回收套用至反应A釜,合格产物R-酮从釜底出料,进入下一步工序。
3结果分析与讨论
在橙花叔醇合成法尼基丙酮的反应过程中,不外加其他溶剂,而是以反应原料本身橙花叔醇和乙酰乙酸甲酯为反应溶剂,因此在接下来的因素研究中不考虑溶剂对产品收率的影响,重点研究其他变量因素,如,原料配比、催化剂投料量、温度、压力、保温时间、脚料套用等。具体见以下分析内容:
3.1 原料配比的影响
按照实施例的工艺步骤,对上述反应路线中其余工艺参数不变,只改变原料橙花叔醇与乙酰乙酸甲酯的摩尔配比,考察温度对最终产品收率的影响,结果见表2。
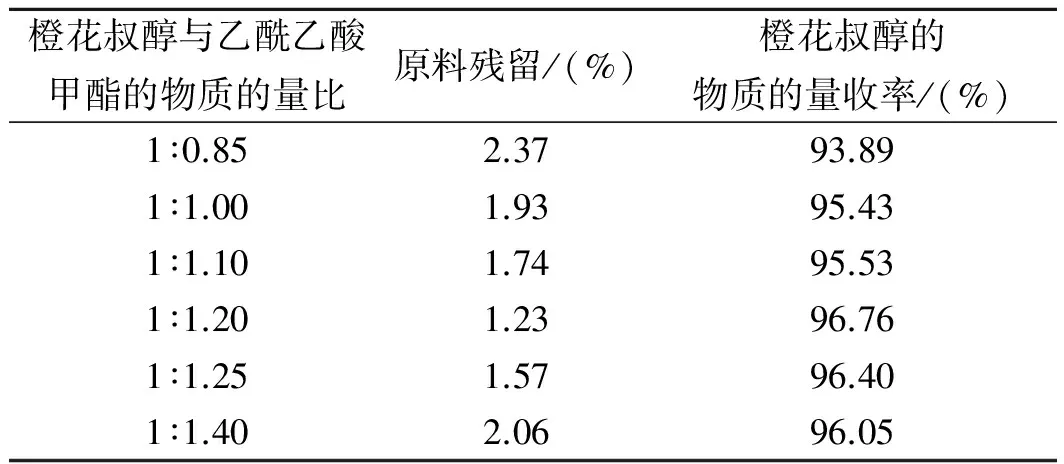
表2 橙花叔醇与乙酰乙酸甲酯不同比例时的收率变化Table 2 nerolidol and methyl acetoacetate yield changes at different ratios
从表2中可以看出,增加原料橙花叔醇与乙酰乙酸甲酯的物质的量比有利于收率提高,乙酰乙酸甲酯稍微过量有利橙花叔醇更完全的转变,但橙花叔醇与乙酰乙酸甲酯的物质的量比超过1∶1.20之后,对收率的提升作用表现的不明显,为了更既有利于工业生产的放大,节约成本,综合考虑,橙花叔醇与乙酰乙酸甲酯的物质的量比以1∶1.20为佳。
3.2 催化剂投料量对反应的影响
按照实施例的工艺步骤,对上述反应路线中其余工艺参数不变,只改变催化剂投料量,以橙花叔醇与异丙醇铝的摩尔比为变量,进行试验,试验结果见表3。
从表3中可以看出,法尼基丙酮的收率随着催化剂投料量的增加而增大,当橙花叔醇与异丙醇铝的物质的量比提升至1∶0.020之后,催化剂用量投料量的继续增加对终产物法尼基丙酮的收率提升影响较小,本着成本节约的原则,橙花叔醇与异丙醇铝的物质的量比为1∶0.020比较适宜。

表3 催化剂投料量对橙花叔醇的收率Table 3 the yield of the catalyst in the amount of the catalyst
3.3 反应A釜中温度的影响
按照实施例的工艺步骤,对上述反应路线中其余工艺参数不变,只改变反应A釜温度,进行试验,试验结果如下:

表4 反应A釜不同温度条件下反应的收率Table 4 Yield of reaction A reactor under different temperature conditions
温度对酯交换反应的转化率影响较大,温度低转化率低,同时酯交换速率低,反应时间延长。在其他条件恒定的情况下,对反应温度进行了试验,由试验结果可看出,温度在96-101℃之间达到最优,低于此温度反应不完全,高于此值时原料会挥发,都不利于反应的进行。
在由乙酰乙酸-R-酯重排生成至R-酮酸,温度不同,重排产物不同,在催化剂的作用下,乙酰乙酸-R-酯发生重排,生成R-酮酸。从表5可以看出,合理的温度范围应该定在120~128 ℃之间。
3.4 反应B釜中温度的影响
按照实施例的工艺步骤,对上述反应路线中其余工艺参数不变,只改变反应B釜温度,进行试验,试验结果如下:

表5 反应B釜不同温度的影响Table 5 Effects of different temperature on reaction B
3.5 反应C釜中温度的影响
按照实施例的工艺步骤,对上述反应路线中其余工艺参数不变,只改变反应C釜的温度,进行试验,试验结果如下:

表6 反应C釜温度对反应收率的影响Table 6 Effect of temperature on reaction yield of C
酮酸脱水时,温度对其影响很大,不同温度下的产物会有所不同。反应温度高,使得羧基与碳之间的键更容易断裂,脱羧反应较易发生,温度太低,则有可能形成酸酐。在此次温度优化试验中,得出此时将温度保持在155-170℃之间更为合理。
3.6 保温D釜保温时间对反应的影响
按照实施例的工艺步骤,对上述反应路线中其余工艺参数不变,只改变保温D釜的保温时间,进行试验,试验结果如下:
保温时间也是影响最终收率的重要因素之一,保温时间过短,反应还没有充分地进行;保温时间过长,则副产物的生成会增多。由上表可见,保温时间越长,原料残留越少,但这并不意味着反应产物的含量一定高。反应时间太长,反应中副产物产生的概率就越大,有效反应反而不足,优选保温时间在2~3 h。

表7 保温D釜保温时间对反应的影响Table 7 Effect of heat preservation time on reaction of thermal insulation D
3.7 减压E釜真空度对最终产物收率的影响
按照实施例的工艺步骤,对上述反应路线中其余工艺参数不变,只改变减压E釜的真空度,进行试验,试验结果如下:

表8 减压E釜真空度对最终产物收率的影响Table 8 Effect of vacuum E vacuum on the yield of final product
减压条件有助于将未反应原料和反应前份等R-OH从釜中分离出,以免影响后续反应的进行,生成非目标化合物,影响后续反应收率,给分离造成困难。从表8可以看出,真空度过小,反应前份残留严重,会对后续反应及分离造成困扰;真空度过大,部分产品会被拉走,使得产品收率得不到保证。从以上数据分析得出,减压反应釜的最适宜压力条件为-8 kPa~-12kPa。
4连续与间歇工艺对比考察
考虑到催化剂异丙醇铝的易吸潮变质的特性,本文中也采用全新催化剂进行对比试验。课题实验过程中分别进行了全新催化剂与套用脚料补加催化剂两种方案的实验,每种方案进行多釜串联连续反应与小试间歇反应对比,实验测试结果如下表所示:
为了进一步考察carroll反应连续新工艺与传统间歇工艺的区别,而尽量减少其他因素的干扰,现使用全新的催化剂和套用脚料的方式分别进行小试实验。从上述结果上看:
1)从图谱和杂质峰看,反应生成杂质明显减少了,产物法尼基丙酮主含量平均提升了4.95%。间歇时全新投料主含量为89.02%,套用脚料投料主含量为90.8%;连续化反应时全新投料主含量为94.65%,套用脚料投料主含量为95.07%。

表9 连续新工艺与传统间歇工艺对比Table 9 Comparison of continuous new technology and traditional batch process
2)主含量的提升,导致原料橙花叔醇和酰化剂乙酰乙酸甲酯的收率均得到了提高。全新投料时,橙花叔醇收率由间歇的88.26%提升至95.47%,乙酰乙酸甲酯收率由间歇的84.42%提升至94.05%;套用脚料投料时,橙花叔醇收率由间歇的88.56%提升至96.04%,乙酰乙酸甲酯收率由间歇的84.72%提升至94.43%。
3)从上述数据看,套用脚料之后,收率得到了进一步的提高。分析认为是脚中的一部分反应液和催化剂重新参与进酯交换过程中,继续后续反应,也说明了脚料套用在生产放大中有应用的可能。
在小试过程中,橙花叔醇与乙酰乙酸甲酯及异丙醇铝的投料物质的量比为1∶1.20∶0.020,反应A釜反应温度控制在96~101 ℃之间最优,反应B釜温度控制在120~128 ℃之间最优,反应C釜温度控制在155~170 ℃之间最优,保温D釜保温过程最佳控制时间控制在2~3 h最优,最后阶段减压E釜真空度控制在-8~-12 kPa最优。
同时,从脚料套用的数据上来看,套用之后的收率要高于不套用脚料的数据,为大生产放大提供了理论依据。
总之Carroll反应分釜控温的连续生产工艺要好于传统生产的间歇式生产工艺。
5结 论
连续Carroll生产法尼基丙酮控制过程较间歇过程收率提高比较明显。全新投料时,橙花叔醇收率由间歇的88.26%提升至95.47%,乙酰乙酸甲酯收率由间歇的84.42%提升至94.05%;套用脚料投料时,橙花叔醇收率由间歇的88.56%提升至96.04%,乙酰乙酸甲酯收率由间歇的84.72%提升至94.43%。
连续Carroll实施后,操作过程大大简化,可以减少现场操作人员;可以大幅度的降低生产的能耗;同时连续化操作也大大增强了工艺的稳定性,安全风险相应的也有所降低。
通过多釜串联连续Carroll反应小试的研究,为将来工业连续化大生产奠定了坚实的基础,同时可以实现该反应的精确控制,达到提升收率,节约能耗和提高劳动生产率,下降生产成本,同时也可推广至甲基庚烯酮、香叶基丙酮等Carroll反应的实施过程中。
[1] Carroll, M F, Addition of α,β-unsaturated alcohols to the active methylene group. Part I. The action of ethyl acetoacetate on linalool and geraniol[J]. J. Chem. Soc. 1940, 704~706.
[2] Carroll, M F, Addition of α,β-unsaturated alcohols to the active methylene group. PartⅡ. The action of ethyl acetoacetate on cinnamyl alcohol and phenylvinycarbinol[J]. J. Chem. Soc. 1940, 1 266~1 268.
[3] Carroll, M F, Addition of α,β-unsaturated alcohols to the active methylene group. Part Ⅲ. Scope and mrchanism of the reaction[J]. J. Chem. Soc. 1941, 507~511.
[4] CARSTEN, O; MANFRED, S; HEINZ, E; et, al. Continuous preparation of unsaturated ketones[J], US6329554 (B1), 2001.12.11.
[5] Tsuji, J, Allylic, allylic carnonates efficient allylating agents of carbonucleophiles in palladium-catalyzed reaction under neutural condition[J]. J. Org. Chem., 1985,107, 5 225~5 228.
[6] Tsuji, J. New synthetic reactions catalyzed by palladium complexes[J]. Pure & Appl. Chem., 1986,58(6), 869~878.
[7] 黄伟.假性紫罗兰酮合成新工艺[J].上海化工,2008,12,13~15.
[8] 许青青,姜华.合成法尼基丙酮的优化实验条件[J].化学试剂,2006,28(1),59~60.
[9] Kimel, W; Cope, A C, The rearrangement of allyl-type esters of β-keto acids[J]. J. Am. Chem. Soc. 1943, 65, 1 992.
[10] ANTHONY, H J Preparation of tocopherols[P]. US6262279 (B1),2001,07,17.
[11] W Kimel, H Park N J, et,al. Branched chain octadecenone and preparation thereof[P]. US2660608 (A) , 1953.11.24.
[12] W Kimel, H Park, et,al. Preparation of ketones[P]. US2795617 (A), 1957.06.11.
[13] 朱为福,许青青,姜华.金合欢基丙酮的合成放大试验[J].化工生产与技术,2010,17(1),33~35.
[14] 张峻松,贾春晓,毛多斌 等.金合欢基丙酮的合成与表征[J].化学世界,2004,2,86~88.
[15] 姚晓明,崔波,李国清 等.吉法酯合成工艺的研究[J].黑龙江医药科学,2010,36(3),26~28.
[16] 周武春,袁端锋,严强.一种合成替普瑞酮的方法[P].CN201010578339.1,2010.12.08.
[17] 陈海荣,胡宗琳.替普瑞酮合成工艺的改进[J].中国医药工业杂志,2004,35(8),449~450.
[18] 朱为福,许青青,姜华.金合欢基丙酮的合成放大实验[J].化工生产与技术,2010, 17(1),33~37.
[19] 李冬梅,赵振东,孙震 等.香叶基丙酮合成反应流出物组成及形成机理探讨[J].林产化工通讯,2003, 37(6), 8~11.
[20] H Y JUNG, J S KIM and S J LEE, Method for eliminating catalyst residues from unsaturated ketones produced through carroll’s reaction using ai-isopropoxide catalyst[J]. KR20020027812 (A), 2002. 04.15.
