GO/TiO2复合催化剂的制备及其光催化降解甲基橙
2018-01-12许文涛邵真真曹腾飞
许文涛 于 岩,2 盛 瑞 邵真真 曹腾飞
(1.齐齐哈尔大学材料科学与工程学院,黑龙江 齐齐哈尔 161006;2.黑龙江省高校精细化工重点实验室,黑龙江 齐齐哈尔 161006)
近年来,随着工业化进程的加快及污水排放量日益增多,严峻的环境问题越来越引起人们的关注。在众多污水处理方法中,光催化技术以其室温反应和可直接利用光源来驱动反应等优点,被认为是最有应用价值的污水处理方法[1,2]。目前,光催化剂种类很多,其中,TiO2因具有价格低廉、化学稳定性好、无毒且抗光腐蚀等特点,已成为光催化领域中研究较为广泛的材料之一[3~5].然而,TiO2的主要缺点为量子产率低,其光谱响应范围仅限在紫外区(通常<380nm) ,一定程度上限制了其光催化的活性[6]。为了解决这些问题,人们开始尝试通过改变合成方法,掺杂以及复合活性物质等措施来改善其某些表面特性,以期利用形貌的优化与组分间的协同作用来增强 TiO2等材料本身的活性[7]。氧化石墨烯(GO)含有多种官能团,具有许多优异的性能,因其碳层上富含羟基、羧基等官能团,具有反应活性点,能与许多无机非金属氧化物、金属纳米颗粒复合得到性能优异的复合材料。
目前,氧化石墨烯的制备方法已较成熟,但TiO2/氧化石墨烯复合材料的研究才刚刚开始。本文采用改进Hummer法制备出氧化石墨,再用溶胶-凝胶法制备了具有较高光催化活性的复载材料TiO2/GO,通过选择可溶性有机染料甲基橙模拟染料废液,对所制备的光催化剂进行了光催化活性研究, 获得了较为满意的结果。
1实验部分
1.1 试剂及仪器
甲基橙(MO)为市售分析纯(λmax=463 nm),异丙氧基钛(TTIP,98%)购于德国ABCR化学试剂公司,鳞片石墨购于青岛阎鑫石墨制品有限公司,K2S2O8购于天津凯通化学试剂有限公司,其他化学试剂均为市售分析纯,全部实验用水均为二次蒸馏水。
样品的FTIR由美国尼高利公司生产的傅里叶变换红外光谱仪测定,XRD谱采用德国Bruker-AXS(D8) X射线衍射仪进行分析,SEM和TEM分析采用Hitach公司的S-4700扫描电镜和H-7650透射电子显微镜,UV-Vis由北京普析通用公司生产的TU-1901型紫外-可见分光光度计测定。
光催化实验装置由圆柱形双层硬质玻璃冷凝套管和光强稳定的125 W高压Hg灯构成。反应时,通入自来水进行冷却,溶液距光源约10 cm,整个反应装制置于暗箱中。
1.2 实验方法
1.2.1GO的制备
采用改良的Hummers方法制备GO:依次向烧杯中加一定量过硫酸钾、五氧化二磷浓硫酸和天然鳞片石墨,80 ℃保持6 h。用去离子水洗涤至滤液呈中性,制得预氧化石墨。在冰水浴下,向预氧化石墨和浓硫酸混合液中,加入高锰酸钾、去离子水、30%的双氧水和盐酸。静置,将下层溶液放透析袋中。透析至水溶液呈中性,50 ℃的真空干燥箱中烘干备用。
1.2.2催化剂GO/TiO2的制备及表征
在制备GO/TiO2复合材料时,GO的加入量分别为0.7%,1.4%和2.1%(GO以干基计)。称取 GO溶于无水乙醇中,超声30min,制得GO分散液,在强烈搅拌下,加入盐酸,不同量的异丙氧基钛,搅拌3h, 80度陈化24 h,将反应液冷却至室温,过滤,洗涤至溶液呈中性,将得到的粉末研磨,保温焙烧4 h后,随炉冷却,得到复合粉体样品.将所得GO/TiO2复合物粉体用XRD、SEM、TEM进行了初步表征。
1.2.3光催化实验
将10 mg催化剂分散在新配的浓度为10 mg/L的90 mLMO溶液中, 形成的悬浮液,超声10 min,避光搅拌30 min,使催化剂在反应液中分散均匀且达到吸附-脱附平衡。开始加光并计时,每间隔一定时间取样(3 mL),并离心分离,所获上层清液通过紫外可见分光光度计在波长为463nm处测量其吸光度值, 跟踪测定MO吸光度值的变化。
2结果与讨论
2.1 XRD测试
如图1所示为制得的复合光催化剂及氧化石墨烯的XRD 谱图。从图1(a)中可看出,在2θ=10.5°处出现了氧化石墨烯的特征衍射峰,证明天然石墨经处理后被氧化得较为彻底,成功制得了氧化石墨烯。图1(b)为TiO2/氧化石墨烯复合材料(2.1% GO/TiO2)的 XRD 谱图。由图 1(b) 可知,所合成复合材料中出现了锐钛矿TiO2的衍射峰,衍射峰主要位于衍射角2θ 为 25. 4°, 38. 1°, 48.2°,54.3° 和55.4°(JCPDS 21-1272)处,与TiO2锐钛矿晶型基本一致[8]。同时,氧化石墨烯的特征衍射峰基本消失,这一结果说明,氧化石墨经较长时间超声后其结构被彻底剥离,形成单片层氧化石墨烯结构,而氧化石墨烯碳层上存在的带负电荷的含氧基团为复合提供了活性位点,使得锐钛矿型TiO2成功负载于GO碳层上。另外,根据Scherrer公式,利用衍射峰计算得到合成产物的晶粒平均粒径为 14 nm。
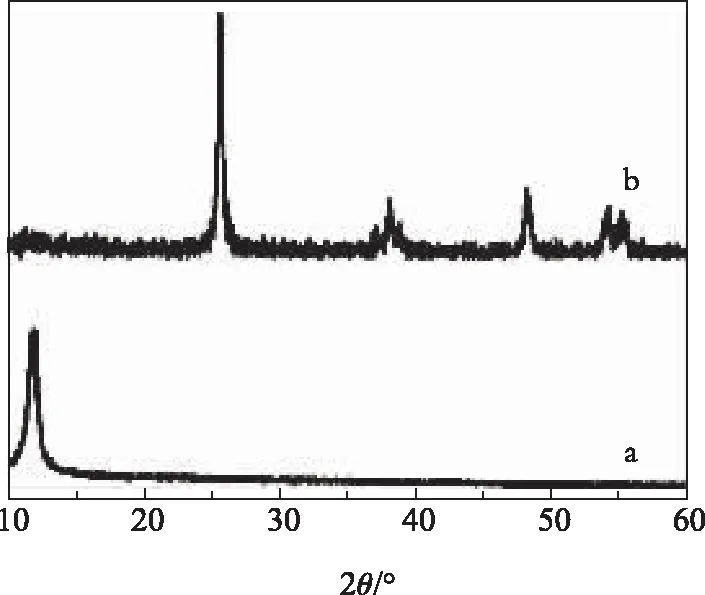
(a)GO;(b)TiO2/GO图1 GO和TiO2/GO的X射线衍射图谱Fig.1 XRD patterns of GO and TiO2/GO
2.2 TEM测试
在XRD分析的基础上,采用TEM分析技术对GO及复合材料GO/TiO2的形貌及复合情况进行研究,结果见图2和图3。从图2 GO的TEM照片中可以看出GO呈片状结构,与之相对比的是,从图3 GO/TiO2的TEM 照片中可以看出在GO的碳层上负载着纳米级TiO2球形颗粒,粒径在14 nm左右,与XRD结果一致。TEM分析结果也进一步证实GO与TiO2成功复合。

图2 GO的TEM谱Fig.2 TEM image of GO

图3 TiO2/GO的TEM谱Fig.3 TEM image of TiO2/GO
2.3 SEM测试
为了考察GO及复合材料TiO2/GO的形貌, 我们对GO和复合材料TiO2/GO进行了扫描电镜测试,结果如图4所示。由照片可见,所制得的氧化石墨烯具有较大的比表面积。复合材料TiO2/GO是由大量二氧化钛的粒子在氧化石墨烯表面附着生长形成致密的膜层。由于氧化石墨烯上含有许多含氧官能团,为其与TiO2紧密连接提供了连接点。

(a) GO;(b) TiO2/GO图4 GO和TiO2/GO的SEM谱Fig.4 SEM image of GO and TiO2/GO
2.4 光催化性能
为考察在紫外光条件下不同催化剂对MO的降解情况,分别进行了紫外直接光解、TiO2和具有不同比例复合材料TiO2/GO的光催化实验,相关结果如5所示。可以看出,不同催化剂使 MO降解的效率不同。其中,经120 min的紫外光照射后,TiO2和直接光解对甲基橙的降解率分别32.0%和5.3%,复合材料GO/TiO2的活性分别为29.3%、49.6%、92.8%,均高于单体和直接光解数据,这是由于TiO2在紫外区有较强吸收,其与GO复合后,二者间的协同作用可进一步提高催化剂降解MO的效率。将不同比例催化剂的实验结果比较可知,在紫外光催化条件下,MO随着光照时间的增加被逐渐降解,且在质量百分数为2.1% GO/TiO2复合材料的紫外光催化降解效率最高。
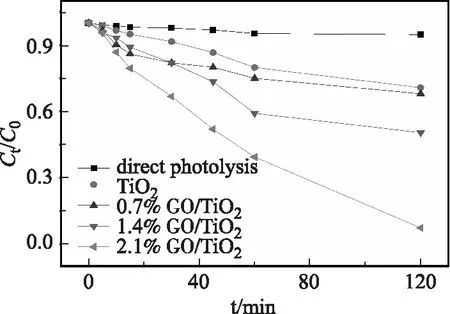
图5 不同催化剂紫外光催化MO降解图Fig.5 Profiles of photocatalytic degradation of MOunder UV light irradiation with different photocatalysts
3结 论
本文通过原位溶胶凝胶法制备了系列GO/TiO2复合材料, GO/TiO2有下列特征:(1)制备的复合催化剂主晶相为锐钛矿型TiO2;(2)GO表面富集的TiO2颗粒尺寸14 nm左右;(3)随着GO含量的增加,GO/TiO2复合材料的降解率增加,在120 min内,当GO加入量为2.1%时,GO/TiO2复合催化剂光催化降解率高达92.7%。
[1] Fujishima A,Rao T N,Tryk D A.Titanium dioxide photocatalysis[J].J Photoch Photobio C,2000,1(1):1-21.
[2] 李晓平,徐宝璐,刘国范 等.纳米TiO2光催化降解水中有机污染物的研究与发[J].功能材料,1999,30(3):242-248.
[3] Chen S Q,Lv G X.The photocatalytic and thermal catalytic reduction of CO2with H2over Pt /TiO2catalysts[J].J Mol Catal,2014,28(5):436-449.
[4] Liang K,Tay B K,Kupreeva O V.,et al.Fabrication of double-walled titania nanotubesand their photocatalytic activity[J].ACS Sustain Chem Eng,2014,2(4):991-995.
[5] Chen P, Khetan A,Yang F., et al.Experimental and theoretical understanding of nitrogen-doping induced strong metal?support interactions in Pd/TiO2catalysts for nitrobenzene hydrogenation[J].ACS Catal,2017,7(1):1 197-1 206.
[6] Kensei F, Yasutaka K, Yuki S.,et al. Fabrication of photocatalytic paper using TiO2nanoparticles confined in hollow silica capsules[J].Langmuir, 2017,33(1):288-295.
[7] Qiu B,Xing M Y,Zhang J L.Mesoporous TiO2nanocrystals grown in situ on graphene aerogels for high photocatalysis and lithium-ion batteries[J].J Am Chem Soc,2014,136(16):5 852-5 855.
[8] Matsumura M,Furukawa S,Saho Y, et al. Cadmium sulfide photocatalyzed hydrogen productlon from aqueous solutions of sulfite: effect of crystal structure and preparation method of the catalyst[J].J Phys Chem,1985,89(8) :1 327-1 329.
