双侧颈内静脉置管引流用于全胸腔镜不停搏再次三尖瓣手术的经验
2018-01-06黄宏前曾庆诗
黄宏前,曾庆诗
[1.广东省人民医院珠海医院,广东珠海519040;2.广东省心血管病研究所广东省人民医院(广东省医学科学院),广州510100]
双侧颈内静脉置管引流用于全胸腔镜不停搏再次三尖瓣手术的经验
黄宏前1,曾庆诗2
[1.广东省人民医院珠海医院,广东珠海519040;2.广东省心血管病研究所广东省人民医院(广东省医学科学院),广州510100]
目的总结双侧颈内静脉置管引流用于全胸腔镜不停搏再次三尖瓣手术的经验。方法回顾性分析自2014年3月至2017年3月于广东省人民医院行全胸腔镜不停搏再次三尖瓣手术患者43例的临床资料。全组患者采用静吸复合麻醉,通过双侧颈内静脉和股静脉置管进行静脉引流,股动脉置管进行全身灌注。转流中鼻咽温维持33℃~35℃、平均动脉压50~90 mm Hg(1 mmHg=0.133 kPa)。结果43例患者术中静脉引流效果好,手术视野清晰。未发现与双侧颈内穿刺置管相关的并发症,术后穿刺口愈合良好。结论保证充足的静脉引流维持术野清晰是全胸腔镜下不停搏再次三尖瓣手术的关键;双侧颈内静脉置管引流安全可行。
心脏外科手术;全胸腔镜;颈内静脉引流;不停搏;再次心脏手术
近年来,随着心脏瓣膜手术量的增加,需再次心脏瓣膜手术的患者也越来越多。再次心脏手术死亡和并发症的发生率高,一直都是外科需要攻破的难题。因胸腔黏连严重,传统开胸直视下分离心脏风险大,手术时间长。左心瓣膜手术后发生严重三尖瓣反流的患者,多存在不同程度的右心功能不全。全胸腔镜下,心脏在缓慢搏动中进行心脏手术可能更有利于患者术后恢复,但这就对手术、麻醉、体外医生提出了新的要求。心内操作期间需充足的静脉引流保证术野清晰。我们对43例全胸腔镜不停搏再次三尖瓣手术经验总结如下。
1 资料和方法
1.1 一般资料
选择2014年9月至2017年3月在广东省人民医院行全胸腔镜不停搏再次三尖瓣手术的患者43例为研究对象。患者的美国麻醉师协会(ASA)分级Ⅱ~Ⅲ级。男14例,女29例,年龄(55.42±10.47)岁,体质量(59.86±10.12)kg。主动脉瓣和二尖瓣置换术后16例、二尖瓣置换术后20例、主动脉瓣置换术后2例、二尖瓣置换和三尖瓣整形后4例、二尖瓣和三尖瓣置换后1例。胸片心胸比0.72±0.08。心电图示心房颤动31例、心肌缺血34例。超声心动图:极重度三尖瓣反流17例、重度三尖瓣反流21例,中度三尖瓣反流4例、三尖瓣置换后瓣膜梗阻1例。三尖瓣反流面积(18.74±11.61)cm2,右心房内径(75.08±19.25)mm,右心室内径(59.64±8.02)mm,左心房内径(52.87±14.02)mm,左心室内径(45.64±7.39)mm。左心室射血分数63.69%±7.81%,肺动脉压力(41.67±7.36)mmHg(1 mmHg=0.133 kPa)。
1.2 麻醉方法
术前用抗胆碱药戊乙奎醚减少分泌物使气道干燥,全部采用静吸复合麻醉。入手术室后,首先建立脉搏血氧饱和度、心电图和桡动脉有创血压监测。然后开始麻醉诱导,丙泊酚1.0~2.0 mg/kg、芬太尼 5~8 μg/kg、顺式阿曲库铵 0.2 mg/kg,全部进行双腔支气管插管。之后分别经皮双侧颈内静脉穿刺置入股动脉管(康心16~18 Fr)用于体外循环上腔静脉引流,再经左侧颈内静脉穿刺置入7.5 Fr三腔中心静脉管用于输液给药,经右侧颈内静脉穿刺置入鞘管(Edwards8.5Fr)用于放置漂浮导管。其他监测包括中心静脉压、肺动脉压、呼气末二氧化碳分压、尿量、经食管超声心动图等。麻醉维持使用微量泵注瑞芬太尼0.2~0.4 μg(/kg·min)、丙泊酚2~4 mg(/kg·h)、顺式阿曲库铵2~3 μg(/kg·min)和吸入七氟醚(0.5~1.5 MAC)。术中根据手术进程间断左侧单肺通气。开始体外循环后,在右心房切开前5 min左、右静脉注射美托洛尔或艾司洛尔控制心率在20~40次/min,同时辅以静脉注射胺碘酮减弱心肌张力和抑制室性心律失常。在缝合完右心房后行经食道超声检查三尖瓣膜手术效果。
1.3 体外循环方法
体外循环需经外周插管建立,以避免管道对术野的遮挡。如上述,上腔静脉引流由麻醉医生经皮双侧颈内静脉穿刺置入股动脉管建立,然后通过两根长约20 cm的3/8管把两根股动脉管的远心端连接到一个10 cm×10 cm×10 cm的Y型接头上,最后汇成一个通路连接到体外储血罐,如图1和图2所示。全身肝素化后再由外科医生行切开股静脉和股动脉置管,分别用于下腔静脉引流和全身灌注。体外循环中辅用负压辅助静脉引流技术(VAVD),负压控制在-20~-50 mmHg。术中只进行并行循环,不阻断主动脉和上、下腔静脉,保持心脏搏动。开始体外循环后即开始降温,术中鼻咽温温度维持在33°~35°,平均动脉压50~90 mmHg,流量60~80 mL/kg。心内操作即将完成时开始复温,缝合完右心房,复温满意后逐渐减流量终止体外循环。
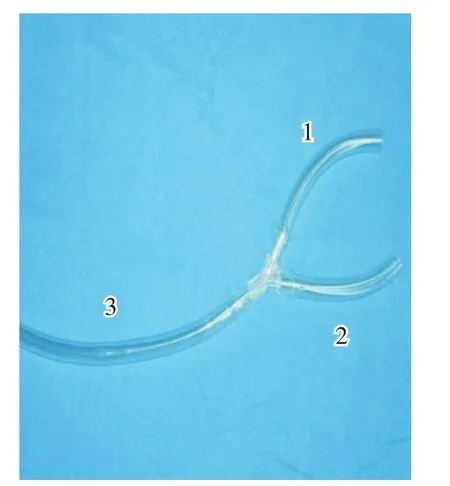
图1 上腔静脉引流通路图(1、2连接于双侧颈内静脉插管;3连接于储血罐)
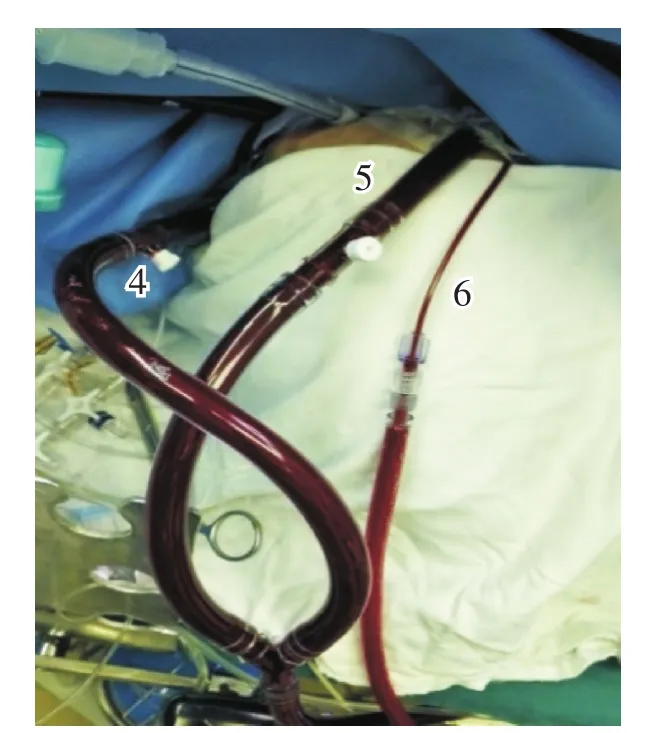
图2 加用鞘管通道辅助引流(4、5为双侧颈内静脉引流;6为鞘管引流)
1.4 统计学分析
采用SPSS 22.0软件进行统计分析。计量资料采用()、M(P25~P75)表示,计数资料采用百分比描述。
2 结果
全组患者麻醉诱导平稳,颈内静脉置管顺利。行三尖瓣置换术21例、三尖瓣成形术22例。转流中静脉引流效果好,手术视野清晰,如图3所示。手术时间为(165.25±40.16)min、体外循环时间为(113.82.4±60.50)min。术后 24 h胸液量260.96(20~1 020)mL、术后机械通气时间(19.86±13.5)h,重 症 监 护 室 滞 留 时 间 76.64(20.06~401.29)h。全组无1例发生颈内静脉穿刺意外,术后穿刺口愈合良好。全组术后院内死亡4例(9.3%),主要死因都是右心功能不全,严重低心排血量综合征,期间发生多器官功能障碍综合征(MODS),最终死亡,其余患者术后发生严重并发症5例(11.6%),其中1例发生严重消化道出血,2例发生肺不张呼吸衰竭,都经积极救治后好转,另2例发生脑梗死而遗留神经系统不良症状。
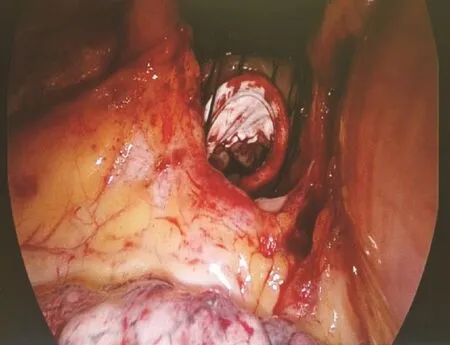
图3 转流中静脉引流效果好,手术视野清晰图像
3 讨论
心脏手术后重度三尖瓣关闭不全严重影响患者的生活质量及长期预后,需行再次三尖瓣手术治疗。此类患者病情复杂,围术期病死率高,国内、外都有报道[1-2]。探讨一种能减少心肌损伤、手术创伤和手术并发症的方法,可能有利于此类患者恢复。
全胸腔镜下心脏手术创伤小、术后疼痛反应轻、恢复快,在临床上应用越来越多[3-4]。有较多研究在不停搏下进行开胸直视心脏手术,减少了心肌缺血、缺氧损伤和避免再灌注损伤,获得较好的心肌保护,明显降低术后病死率[5-7]。本研究全组患者均在胸腔镜不停搏下进行心脏手术,术中不阻断主动脉和上、下腔静脉,有效避免缺血再灌注过程和高钾心停搏液对心肌的损伤,也减少了分离主动脉和上、下腔静脉带来的创伤。心脏始终在并行循环的缓慢搏动中进行手术,心内操作完成后就无需像传统停搏手术那样,需要较长的后并行循环时间。待缝合完右心房,调整好心率血压后即可减流量停止体外循环,相对缩短了手术时间。
不停搏下进行胸腔镜心脏手术对外科医生的操作技能提出了较高的要求。手术中需要充足的静脉引流来保证术野清晰,以利于手术操作。若引流不充分势必会导致血液流入右心房,导致视野模糊。同样的静脉置管引流方法,对于阻断上、下腔静脉与不阻断上、下腔静脉两种情况,引流结果往往存在较大差异。在阻断上、下腔静脉后,静脉血只能回流至储血罐这一个地方,由于引流管管径较小(16~18 Fr),需同时辅用负压辅助静脉引流技术(-20~-50 mmHg)技术,才可获得满意的静脉引流效果。而在不阻断上、下腔静脉时,静脉血就即可回流至储血罐,也可直接回流入心脏。此时采用以上同样的静脉引流方法,常常不能充分引流静脉保证术野清晰。因此,我们采取了再加用一条置管引流上腔静脉,即同时行双侧颈内静脉和股静脉置管,且辅用负压辅助静脉引流技术的静脉引流方法。
但双侧颈内静脉置管是否会填堵静脉腔,导致置管以上部位静脉血回流障碍,引起颅内压增高,增加脑水肿、脑出血、脑血栓形成等风险。吕发勤等[8]对正常成人的颈内静脉内径进行测量,结果右侧为(11.79±5.62)mm,左侧为(10.62±6.45)mm。吸气相内径增大,呼气相内径缩小,40~60岁组呼气相内径为(10.50±1.89)mm,随年龄增长颈内静脉内径有逐渐增宽趋势。而16 Fr管外径约6.0 mm、18 Fr管外径约7.0 mm。对比来看,不容易造成阻塞,同时颈内静脉与颈外静脉、颈前静脉等之间也存在较多侧支吻合,术中也未观察到有静脉血回流障碍征象。颈内静脉引流管大小选择,我们的经验是小于80 kg者选双侧16 Fr,大于80 kg者选右侧 18Fr,左侧 16Fr。张茂等[9]对正常成人的颈内静脉截面积进行测量,认为优势静脉以右侧为主。所以若术前未行颈内静脉超声检查者,选择右侧置入较粗的18Fr管则较为合适。穿刺位置为甲状软骨水平,置管深度需根据患者颈部长短确定,右侧置管尖端需到达左、右无名静脉交汇点以下,左侧置管尖端需达左侧颈内静脉与左锁骨下静脉交汇点以下。置入过深不仅不能增加引流,反而增加穿破静脉的风险。若置入过深管道开口贴近右心房时,在右心房切开后,就会有大量气体伴随着血液引流,反而会削弱引流效果。但有极少数患者行双侧两条颈内静脉管仍不满意引流上腔静脉。在排除负压不足后,可选择加用鞘管通道辅助引流,如图2所示。术中有时会发生上腔静脉引流管进气,可能的原因是负压过大或流量低静脉回流少。及时减小负压和(或)把右侧颈内引流静脉管夹毕改成鞘管引流多可改善。心脏在搏动中手术,术中右心室的血液会通过三尖瓣口反流回右心房,所以还需通过胸腔镜孔向右心房放置一条第三吸引管用于排空反流的血液。采用以上方法,我们取得了满意的引流效果,如图3所示。
总之,保证充足的静脉引流维持术野清晰是全胸腔镜下不停搏再次三尖瓣手术的关键;双侧颈内静脉置管引流安全可行。
[1]AKINS C W,BUCKLEY M J,DAGGETT W M,et al.Risk of reoperative valve replacement for failed mitral and aortic bioprostheses[J].Ann Thorac Surg,1998,65(6):1545-1542.
[2]李明文,陈林,肖颖彬.再次心脏瓣膜手术285例临床分析[J].心肺血管病杂志,2014,33(3):386-389.
[3]SEEBURGER J,BORGER M A,FALK V,et al.Minimal invasive mitral valve repair for mitral regurgitation:results of 1339 consecutive patients[J].Eur J Cardiothorac Surg,2008,34(4):760-765.
[4]LARS G S,FERNANDO A A,DELOS M C,et al.Minimally invasive versus conventional mitral valve surgery:apropensitymatched comparison[J].J Thorac Cardiovasc Surg,2010,139(4):926-932.
[5]SUDIP G,RAJWINDER S J,PHILIP W,et al.Beating heart mitral surgery in patients with poor left ventricular function[J].J Heart Valve Dis,2004,13(4):622-627.
[6]林辉,何巍,彭青云,等.心脏不停跳心内直视手术的临床研究(附1106例报告)[J].中华胸心血管外科杂志,2001,17(3):129-131.
[7]MASROOR S,DANCE G,ANGELI S J.Beating heart videoassisted mitralvalve surgery:a useful technique for high-risk patients[J].J Card Surg,2009,24(3):312-314.
[8]吕发勤,段云友,王文正,等.常成人颈内静脉的二维超声检测[J].中华超声影像学杂志,2004,13(3):236-237.
[9]张茂,杨俭新,刘志海,等.严重创伤患者颈内静脉截面积及呼吸变异与中心静脉压的关系[J].中华超声影像学杂志,2007,16(2):123-127.
Bilateral internal jugular vein catheter drainage for totally thoracoscopic beating tricuspid valve reoperation
HUANG Hong-qian1,ZENG Qing-shi2
(1.Guangdong General Hospital Zhuhai Hospital,Zhuhai,Guangdong 519040,China;2.Guangdong Cardiovascular Institute,Guangdong General Hospital,Guangdong Academy of Medical Sciences,Guangzhou 510080,China)
ObjectivesTo summarize the experiences of bilateral internal jugular vein catheter drainage for totally thoracoscopic beating tricuspid valve reoperation.MethodsFrom Septenber 2014 to March 2017,43 patients underwent totally thoracoscopic beating tricuspid valve reoperation in Guangdong General Hospital were selected.All the patients
intravenous inhalation anesthesia.Venous drainage was performed by bilateral internal jugular vein and femoral vein catheterization.Systemic perfusion was performed through femoral artery catheterization.Nasopharyngeal temperature maintained 33℃-35℃and mean arterial pressure maintained 50~90 mmHg(1 mmHg=0.133 kPa)during cardiopulmonary bypass.ResultsOf the 43 patients,venous drainage was good and surgical field of vision was clear during the operation.No complications associated with bilateral internal jugular puncture were found,and the puncture wound healed well after the operation.ConclusionsThe key of totally thoracoscopic beating tricuspid valve reoperation is ensuring adequate venous drainage to keep the operation field clear.Bilateral internal jugular vein catheter drainage is safe and feasible.
cardiac surgical procedures;totally thoracoscopic cardiac operation;internal jugular venous drainage;beating heart;cardiac reoperation
R654.2
A
1007-9688(2017)06-0704-04
10.3969/j.issn.1007-9688.2017.06.15
黄宏前(1989-),男,住院医师,研究方向为心脏手术麻醉
曾庆诗,E-mail:1963088488@qq.com
2017-03-24)
